芩术痛经巴布剂中黄芩苷和黄芩素及汉黄芩素的离体小鼠经皮渗透行为*
2019-08-07黄文涛肖柳程璐张耕杨全伟
黄文涛,肖柳,程璐,张耕,杨全伟
(1.武汉市第一医院药学部,武汉 430022;2.武汉市中医医院肿瘤科,武汉 430022)
2011年的流行病学调查中发现:60%的妇女中有重度原发痛经,其中51%的痛经妇女日常生活受到影响,17%的重度痛经患者因痛经而缺工或缺课,因此近年来医学界对痛经的治疗和研究较为关注。芩术痛经巴布剂可以很好地抑制子宫平滑肌痉挛,降低子宫平滑肌过度兴奋性,对原发性痛经具有良好的治疗效果。鉴于巴布剂具有基质载药量大,皮肤相容性好、药物释放平稳,药效持久,贴敷无过敏性及刺激性的特点,将其开发为贴敷舒适,不良反应少、经济方便的巴布剂[1-2]。为了考察该制剂的透皮率,笔者通过超临界提取技术,得超临界黄芩、白术混合提取物,制备成巴布剂,以制剂中主药黄芩中主要成分为研究对象,以黄芩苷、黄芩素、汉黄芩素的含量为考察指标,研究芩术痛经巴布剂的透皮性能,从而为临床用药提供依据。
1 仪器与试剂
1.1仪器 高效液相色谱仪:Waters e2695型色谱仪,紫外检测器:Waters 2489;岛津LC-16型色谱仪,SPD-16,紫外检测器:依利特色谱柱Extend C18分析柱(4.6 mm×200 mm,5 μm);艾柯超纯水机(EXCEED 型,成都艾柯水处理有限公司);电子天平:德国Sartorius ME215S(Max210 g,d=0.01 mg);RYJ-6A型药物透皮扩散实验仪(上海黄海药检仪器厂)。
1.2试剂 黄芩苷对照品(批号:110715-200212,纯度为100%),黄芩素对照品(批号:111545-200604,纯度为98.5%),汉黄芩素对照品(批号:111514-200403,纯度为98.5%),购于中国食品药品检定研究院;芩术痛经巴布剂自制(批号:171220);乙腈(色谱纯,美国Tedia Company);乙醇、甲醇(分析纯,国药集团化学试剂有限公司);磷酸(分析纯,国药集团化学试剂有限公司);水为纯化水。
1.3实验动物 SPF级雌性小鼠,体质量(20±5) g,由湖北省疾病控制中心动物实验室提供,合格证号:4200695787,实验动物许可证号:SCXK(鄂)2008-0030。
2 方法与结果
2.1色谱条件 色谱柱:岛津柱Wonda Sil C18分析柱(4.6 mm×200 mm,5 μm);流动相:乙腈-0.1%磷酸水(25:75);柱温30 ℃;流速1.0 mL·min-1;进样20 μL;检测波长280 nm。
2.2对照品溶液的制备
2.2.1混合对照品溶液的制备 精密量取黄芩苷、黄芩素、汉黄芩素对照品12.41,11.25,11.03 mg,分别置于50 mL量瓶中,加甲醇定容,摇匀,分别得黄芩苷、黄芩素、汉黄芩素对照品溶液。精密吸取上述对照品溶液各10 mL,置于50 mL量瓶中,加甲醇定容,摇匀,即得混合对照品储备液。
2.2.2缺黄芩苷混合对照品溶液的制备 精密吸取上述黄芩素、汉黄芩素对照品溶液各1 mL,置于5 mL量瓶中,加甲醇定容,摇匀,即得缺黄芩苷混合对照品。
2.2.3缺黄芩素混合对照品溶液的制备 精密吸取上述黄芩苷、汉黄芩素对照品溶液各1 mL,置于5 mL量瓶中,加甲醇定容,摇匀,即得缺黄芩素混合对照品。
2.2.4缺汉黄芩素混合对照品溶液的制备 精密吸上述黄芩苷、黄芩素对照品溶液各1 mL,置于5 mL量瓶中,加甲醇定容,摇匀,即得缺汉黄芩素混合对照品。
2.3供试品溶液的制备 称取比例的黄芩、白术药材,在优选的萃取压力为35 MPa,萃取温度为30 ℃,采用超临界二氧化碳萃取,所得萃取物溶于去离子水中,混合均匀作为步骤①;向步骤①中加入亚硫酸氢钠、乙二胺四乙酸、柠檬酸、卡波姆,混合均匀作为步骤②;取聚丙烯酸钠NP700溶于丙三醇中作为步骤③;取高岭土、甘羟铝、山梨醇、二氧化钛,混合均匀作为步骤④;将步骤④制备的组合物加入步骤③的组合物中,混合均匀作为步骤⑤;将步骤⑤制备的组合物加入到步骤②制备的组合物中,放置熟化,涂布于背衬层无纺布上,加盖防粘层聚乙烯薄膜,避光通风处自然晾干,即为自制的芩术痛经巴布剂。取自制的芩术痛经巴布剂(批号:171220),除去盖衬,称取该制剂约1.5 g(含黄芩生药量0.40 g),精密称定,置于50 mL锥形瓶中,精密加入70%乙醇50 mL,称质量,超声处理(140 W,频率42 kHz)30 min,静置放冷后再称定质量,用70%乙醇补充质量,滤过,取续滤液作为供试品溶液。
2.4缺黄芩的巴布剂制备 取白术药材,按上述“2.3”项制备方法,作为阴性供试品。
2.5专属性考察 取黄芩苷、黄芩素、汉黄芩素混合对照品、缺黄芩苷、缺黄芩素、缺汉黄芩素混合对照品、芩术痛经巴布剂样品及白术超临界提取物供试品作为阴性样品,分别进样20 μL,分别记录色谱图,见图1。对照品溶液和供试品溶液的特征峰在保留时间上分别对应一致,分离度良好,阴性溶液在特征峰处无干扰,表明此方法的专属性好。
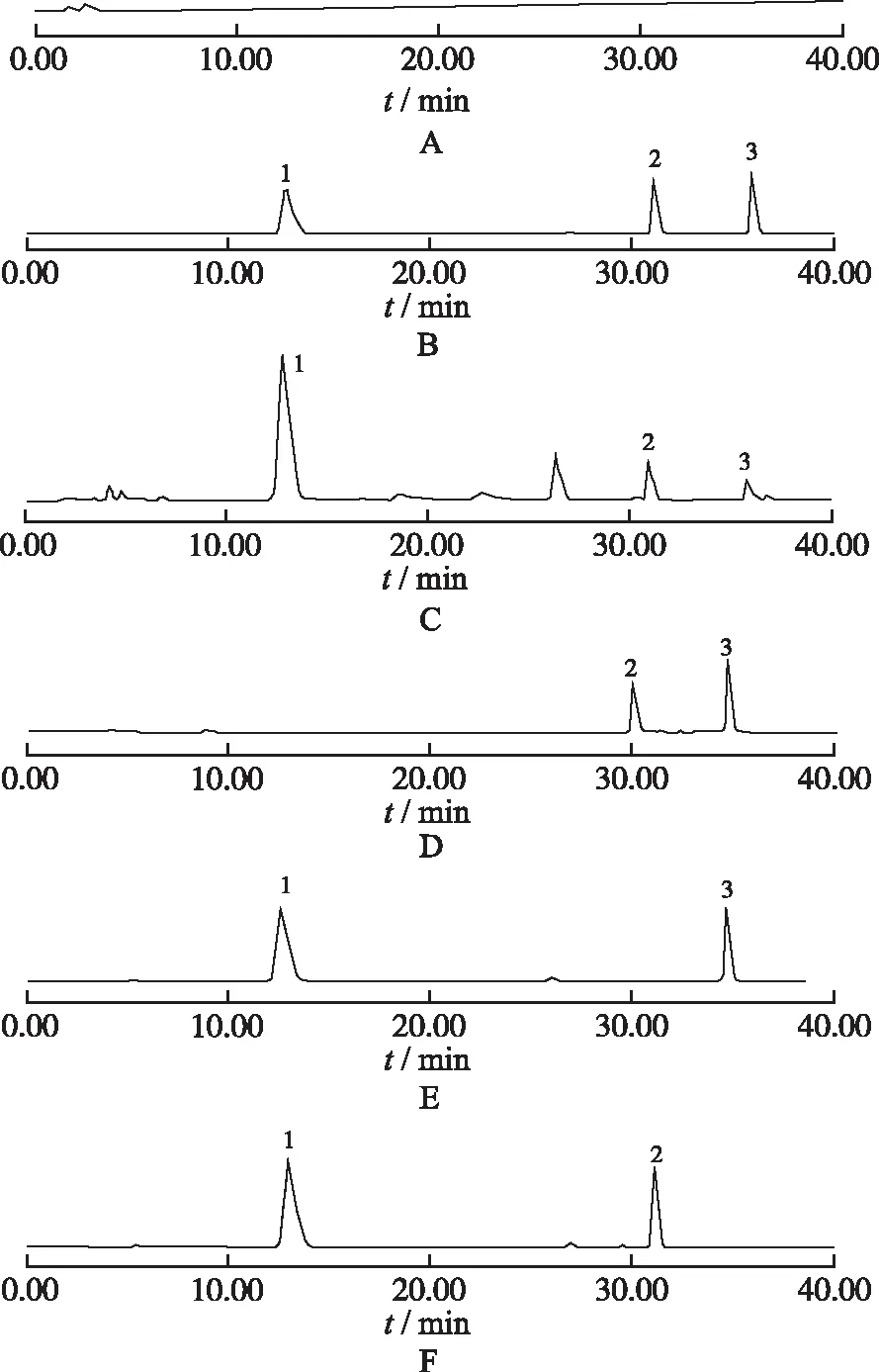
A.阴性供试品;B.混合对照品;C.供试品;D.缺黄芩苷阴性对照品;E.缺黄芩素阴性对照品;F.缺汉黄芩素阴性对照品;1.黄芩苷;2.黄芩素;3.汉黄芩素
图1 芩术痛经巴布剂HPLC色谱图
A.negative sample;B.mixed references;C.sample;D.reference without baicalin;E.reference without baicalein;F.reference without wogonin;1.baicalin;2.baicalein;3.wogonin
Fig.1HPLCchromatogramofQinshudysmenorrheaPapua
2.6线性关系考察 分别精密吸取上述混合对照品储备液1,2,4,6,8,10 mL,分别置于20 mL量瓶中,加甲醇溶解并稀释至刻度,摇匀,按“2.1”项下色谱条件,分别进样20 μL,记录色谱图,以进样量为横坐标(X),以峰面积为纵坐标(Y),按最小二乘法,进行线性回归,绘制标准曲线,计算黄芩苷回归方程为Y=2 147.24X-3 726.83(r=0.999 6),结果表明黄芩苷进样量在2.482~24.82 μg含量范围内线性关系良好;计算黄芩素回归方程为Y=3 764.36X-4 437.15(r=0.999 5),结果表明黄芩素进样量在2.25~22.50 μg含量范围内线性关系良好;计算汉黄芩素回归方程为Y=1 759.81X-247.32(r=0.999 6)。结果表明汉黄芩素进样量在2.206~22.06 μg含量范围内线性关系良好。
2.7精密度实验
2.7.1仪器精密度实验 取上述混合对照品溶液,按“2.1”项下色谱条件注入液相色谱仪,各连续自动进样20 μL,共6次,记录色谱图,黄芩苷、黄芩素和汉黄芩素峰面积RSD值为0.29%,0.66%和0.91%,表明该方法精密度良好。
2.7.2日内精密度实验 取自制的芩术痛经巴布剂(批号:171220),除去盖衬,称取该制剂约1.5 g(含黄芩生药量0.40 g),精密称定,按照“2.3”项下方法制备,取出6份作为供试品溶液,按“2.1”项下色谱条件,记录色谱图,按峰面积计算,分别计算黄芩苷、黄芩素和汉黄芩素RSD值分别为0.47%,0.98%和0.86%,RSD均小于1%,表明方法日内精密度良好。
2.7.3中间精密度实验 取自制的芩术痛经巴布剂(批号:171220),除去盖衬,按照“日内精密度实验”项下方法,分别配制6份相同浓度的供试品溶液,由两个不同的分析人员使用Waters e2695型高效液相色谱仪和岛津LC-16高效液相色谱仪进行测定,记录峰面积,分别计算黄芩苷、黄芩素和汉黄芩素RSD值分别为1.14%,0.71%和1.45,RSD均小于2%,表明方法中间精密度良好。
2.8稳定性实验 取自制的芩术痛经巴布剂(批号:171220),除去盖衬,称取该制剂约1.5 g(含黄芩生药量0.40 g),精密称定,按照“2.3”项方法制成供试品溶液,按“2.1”项下色谱条件,于1,2,4,8,12,24 h 分别进样20 μL,记录色谱图,计算黄芩苷、黄芩素和汉黄芩素峰面积RSD值分别为1.51%,1.78%和0.84%,表明供试品溶液各组分在24 h内稳定性良好。
2.9重复性实验 取自制的芩术痛经巴布剂(批号:171220),除去盖衬,称取该制剂约1.5 g(含黄芩生药量0.40 g)各6份,精密称定,分别按照“2.3”项下方法制得供试品溶液6份,按“2.1”项下色谱条件分别进行测定,记录色谱图,计算各成分平均含量,结果黄芩苷、黄芩素和汉黄芩素平均含量分别为12.710 88,5.804 24和2.298 91 mg·g-1,计算RSD分别为1.89%,1.34%和1.99%,表明该方法的重复性良好。
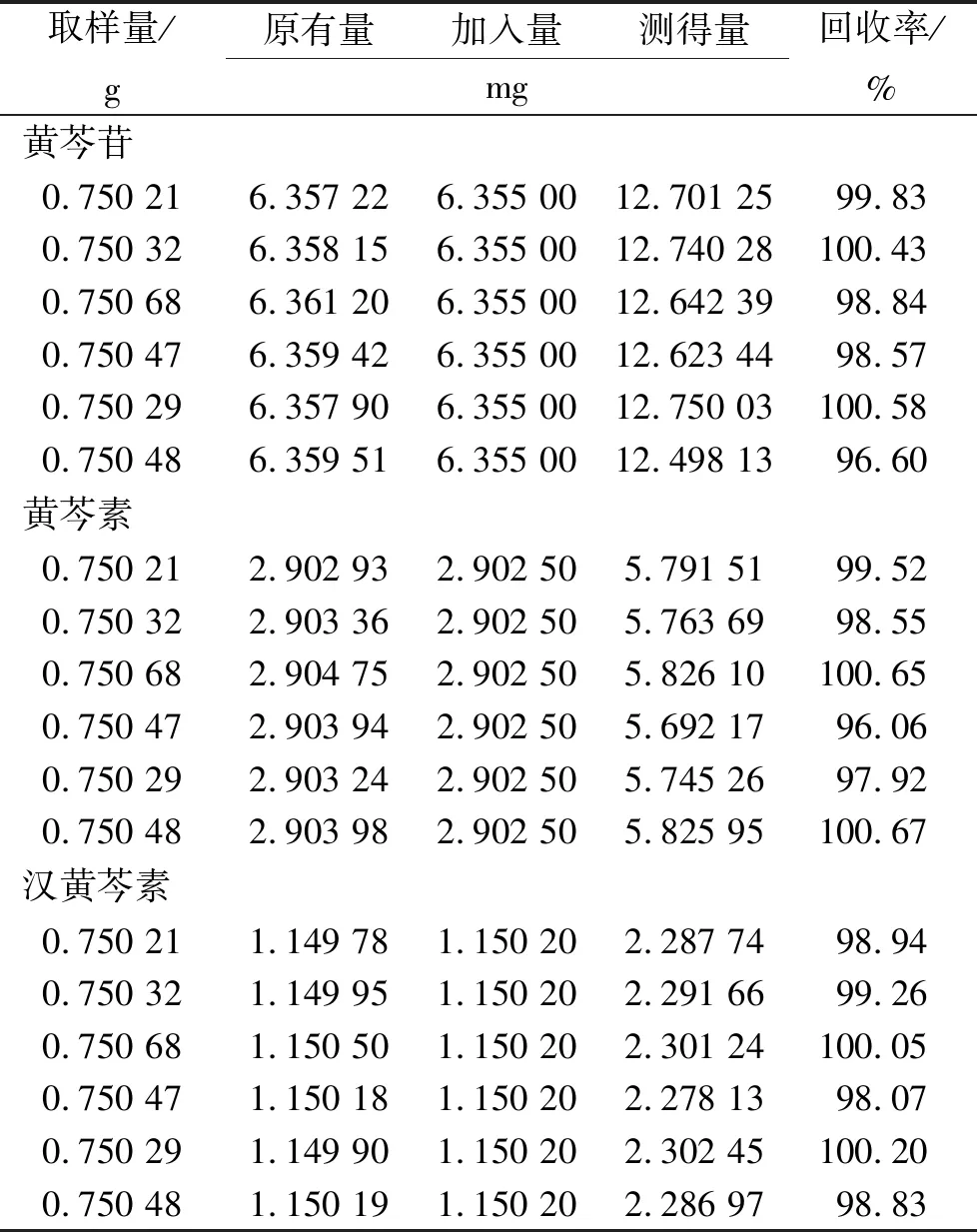
2.10加样回收实验 称取已知含量的自制芩术痛经巴布剂(批号:171220)6份,每份约0.75 g,精密称定,分别加入混合对照品适量,按“2.3”项制成供试品溶液,按“2.1”项下色谱条件,分别进样20 μL,计算回收率。结果黄芩苷、黄芩素和汉黄芩素平均回收率分别为99.14%,98.90%和99.23%,计算RSD分别为1.50%,1.79%和0.81%,表明该方法测定结果准确可靠。见表1。
表1 黄芩苷、黄芩素及汉黄芩素的加样回收率考察
Tab.1Studyonrecoveryrateofbaicalin,baicaleinandwogonin
取样量/g原有量加入量测得量mg回收率/%黄芩苷0.750 216.357 226.355 0012.701 2599.830.750 326.358 156.355 0012.740 28100.430.750 686.361 206.355 0012.642 3998.840.750 476.359 426.355 0012.623 4498.570.750 296.357 906.355 0012.750 03100.580.750 486.359 516.355 0012.498 1396.60黄芩素0.750 212.902 932.902 505.791 5199.520.750 322.903 362.902 505.763 6998.550.750 682.904 752.902 505.826 10100.650.750 472.903 942.902 505.692 1796.060.750 292.903 242.902 505.745 2697.920.750 482.903 982.902 505.825 95100.67汉黄芩素0.750 211.149 781.150 202.287 7498.940.750 321.149 951.150 202.291 6699.260.750 681.150 501.150 202.301 24100.050.750 471.150 181.150 202.278 1398.070.750 291.149 901.150 202.302 45100.200.750 481.150 191.150 202.286 9798.83
2.11样品含量测定 取的芩术痛经巴布剂制剂(批号:171220),按“2.2.2”项下的供试品溶液制备方法制备,按“2.1”项下的色谱条件进行测定,记录峰面积,以标准曲线法分别计算黄芩苷、黄芩素和汉黄芩素的含量依次为12.710,5.805,2.298 mg·g-1。
2.12离体小鼠透皮率测定研究 取SPF小鼠,处死,用8%硫化钠(自制)脱毛,用剪刀从腹部剥离整个皮肤,用0.9%氯化钠溶液洗净[3]。采用改良的Franz扩散池(接收池体积6.5 mL,接收池有效面积2.8 cm2),将鼠皮背部向下,腹部朝上,固定于接收池上,称取芩术痛经巴布剂约0.5 g,精密称定(0.500 28 g),紧贴于小鼠肚皮,接收池内加满0.9%氯化钠溶液,设置水浴温度为(37±1)℃水浴恒温,开启磁力搅拌棒以200 r·min-1的速度搅拌,分别于2,4,6,8,10,12 h时,取出接收池中全部接收液,同时取出接收液后立即补充相同体积温度为(37±1) ℃的新鲜0.9%氯化钠溶液[4]。
2.12.1芩术痛经巴布剂供试品溶液的制备 将分别6次所得接受液分别水浴浓缩至干,残渣加70%乙醇溶液洗涤至1 mL量瓶中,并定容至刻度,摇匀,过微孔滤膜即得2,4,6,8,10,12 h的离体透皮吸收供试品。
2.12.2离体透皮率含量测定 分别将上述不同时间所得供试品溶液按上述“2.1”项下色谱条件注入高效液相色谱仪,各进样20 μL,检测,分别计算供试品中黄芩苷、黄芩素、汉黄芩素的含量以及经皮渗透的动力学拟合。
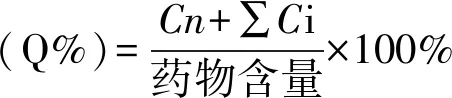
Cn:第n个时间点的透皮量;∑Ci:第i(i=n-1)个累积透皮量
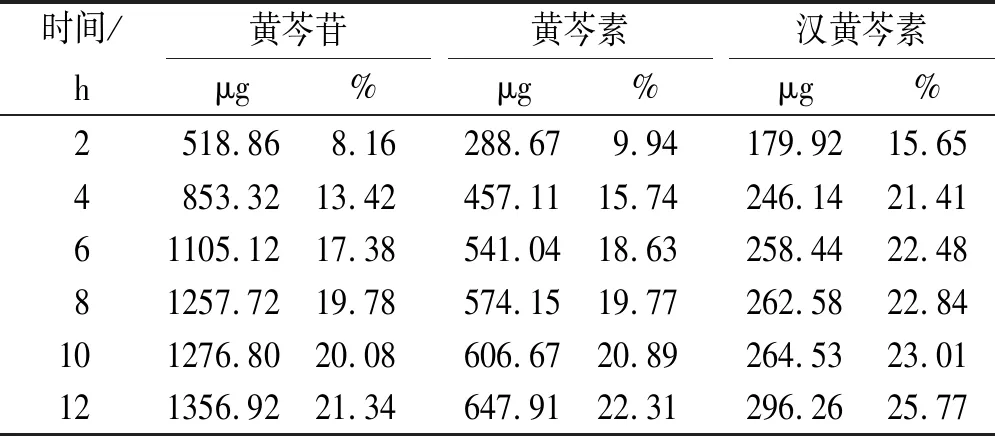
结果显示,芩术痛经巴布剂的小鼠体外经皮渗透行为3个成分均以Higuchi方程拟合为优,拟合度为最高,表明芩术痛经巴布剂是缓释制剂,属于骨架溶蚀型释药系统[5]。见表2,3。
表2 黄芩苷、黄芩素及汉黄芩素离体透皮率测定结果
Tab.2Resultsofinvitrotransdermalrateofbaicalin,baicaleinandwogonin
时间/h黄芩苷μg%黄芩素μg%汉黄芩素μg%2518.868.16288.679.94179.9215.654853.3213.42457.1115.74246.1421.4161105.1217.38541.0418.63258.4422.4881257.7219.78574.1519.77262.5822.84101276.8020.08606.6720.89264.5323.01121356.9221.34647.9122.31296.2625.77
3 讨论
笔者考察了甲醇-0.1%磷酸、乙腈-0.1%磷酸、甲醇-水、乙腈-水等体系进行梯度洗脱,结果显示,当流动相采用乙腈-0.1%磷酸时,所测定的成分都达到基线分离,分离效果良好。皮肤角质层类似脂质膜,芩术痛经巴布剂中3种成分,主要为黄酮类成分,亲脂性较强,通过超临界提取后,提取率较高,透过皮肤屏障,透过量较高,其中黄芩苷分子量较其他两个成分较大,极性较高,故其透皮率低于其他两个成分[6]。缓释制剂释药主要是溶出、扩散及溶蚀与扩散,溶出结合作用。骨架型主要有3种类型:溶蚀性骨架片,不溶性骨架片
表3 黄芩苷、黄芩素及汉黄芩素经皮渗透的动力学拟合结果
Tab.3Dynamicfittingresultsofpercutaneousosmosisofbaicalin,baicaleinandwogonin
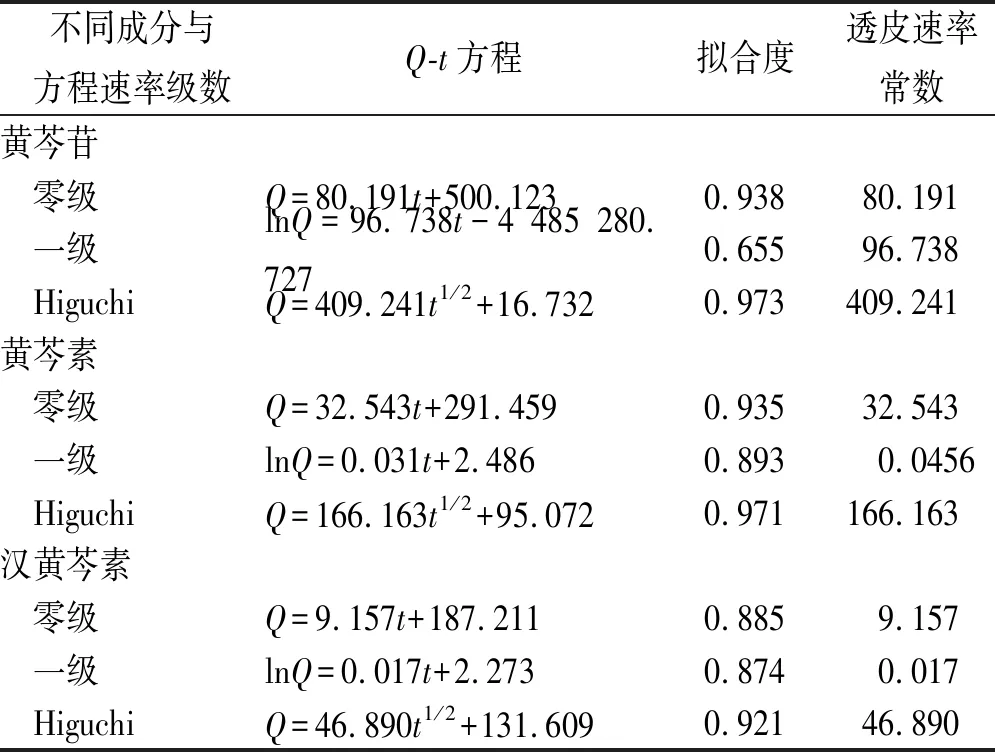
不同成分与方程速率级数Q-t方程拟合度透皮速率常数黄芩苷 零级Q=80.191t+500.1230.93880.191 一级lnQ=96.738t-4 485 280.7270.65596.738 HiguchiQ=409.241t1/2+16.7320.973409.241黄芩素 零级Q=32.543t+291.4590.93532.543 一级lnQ=0.031t+2.4860.8930.0456 HiguchiQ=166.163t1/2+95.0720.971166.163汉黄芩素 零级Q=9.157t+187.2110.8859.157 一级lnQ=0.017t+2.2730.8740.017 HiguchiQ=46.890t1/2+131.6090.92146.890
和亲水性凝胶骨架片,释药机制各不相同[7-9]。由不可溶解但可溶蚀的蜡质材料制成的溶蚀性骨架片是通过孔道扩散与蚀解控制药物来释放。不溶性骨架片的药物释放是液体穿透骨架,将药物溶解然后从骨架的沟槽中扩散出来,故孔道扩散为限速步骤,释放符合Higuchi方程。
