茶叶中游离氨基酸总量的测量不确定度评定
2019-08-01谢颖颖
谢颖颖
(1.国家茶叶产品质量监督检验中心(四川),四川 雅安 625000;2.四川省雅安市产品质量监督检验所,四川 雅安 625000)
测量不确定度是“表征合理地赋予被测量之值的分散性,与测量结果相关联的参数”[1]。测量不确定度可以衡量测量过程是否持续受控,测量结果是否保持稳定一致,可以找出影响测量结果的最主要因素,并加以控制改进。测量不确定度越大,表示测量能力越差;反之,表示测量能力越强。
茶叶水浸出物中具有α-氨基的有机酸且呈游离状态存在者,均称茶叶游离氨基酸。该指标与茶叶的“鲜香”特征有关。有关测量茶叶中游离氨基酸总量的不确定度评定,未见文献报道。本文以四川省雅安市蒙顶山甘露茶叶为例,根据国家质量监督检验检疫总局发布的JJF 1059.1-2012计量技术规范《测量不确定度评定与表示》[1]和中国金属学会分析测试分会发布的CSM 01 01 01 02-2006《分光光度法测量结果不确定度评定规范》[2],对分光光度法测定茶叶中游离氨基酸总量的不确定度进行了测量和评估。
1 材料与方法
1.1 材料与仪器
甘露茶叶为委托检样,产自四川省雅安市蒙顶山。
721分光光度计,上海第三分析仪器厂,出厂编号9209Y059,5 mm比色杯。
电子天平,赛多利斯BT125D,出厂编号22591458。
L-茶氨酸,纯度99%,北京百灵威科技有限公司,CAS:3081-61-6。
茚三酮、磷酸氢二钠等均为分析纯。
实验用水为超纯水。
1.2 实验方法
样品试液制备:按GB/T 8314-2013[3]中的规定,称取3 g(精确至0.001 g)磨碎试样于500 mL锥形瓶中,加沸蒸馏水450 mL,立即移入沸水浴中,浸提45 min(每隔10 min摇动1次),浸提完毕后立即趁热减压过滤,残渣用少量热蒸馏水洗涤2~3次。将滤液转入500 mL容量瓶中,冷却后用水定容至刻度,摇匀。
样品测定:准确吸取样品试液1 mL,注入25 mL比色管中,加入0.5 mL pH8.0 磷酸盐缓冲液和0.5 mL 2% 茚三酮溶液,在沸水浴中加热15 min,待冷却后加水定容至25 mL,放置10 min后,用5 mm比色杯,在570 nm处,以试剂空白溶液作参比,测定吸光度。
标准曲线的制作:称取250 mg L-茶氨酸溶于适量水中,转移定容至25 mL,摇匀后即得标准储备液。再移取0.0 mL、1.0 mL、1.5 mL、2.0 mL、2.5 mL、3.0 mL标准储备液,分别加水定容至50 mL,摇匀后该系列标准工准液1 mL分别含有0 mg、0.2 mg、0.3 mg、0.4 mg、0.5 mg、0.6 mg茶氨酸。按照样品测定方法测定该系列标准工作液的吸光度,将测得的吸光度与对应的茶氨酸浓度进行计算,绘制标准曲线。
最后通过测定样品的吸光值测得样品的浓度。
1.3 环境温湿度
温度25±1 ℃,相对湿度64%。
1.4 计算方法
X=(C/1000×V1/V2×100%)/(m×w)
式中:X——游离氨基酸总量(%);
C——根据测得的吸光度从标准曲线上查得的茶氨酸毫克数(mg);
V1——试液总量(mL),本实验中为500 mL;
V2——测定用试液量(mL),本实验中为1 mL;
m——试样用量(g);
w——试样干物质含量(质量分数)(%)。
2 不确定度的来源分析
从试验过程和数学模型分析,不确定度主要来源于(1)标准溶液配制及测定引起的相对不确定度,其中包括定容标准储备液、标准工作溶液配制、标准曲线拟合等引入的不确定度;(2)样品制备后定容体积、称量质量、干物质含量、多次重复测量所引入的相对不确定度;(3)分析仪器的相对不确定度。其来源分析详见表1。
3 不确定度的计算与评定
3.1 标准溶液配制及测定引起的相对不确定度
3.1.1 配制标准储备液引入的相对不确定度urel(C1)
称取L-茶氨酸(纯度不低于99%)250 mg溶于适量水中,转移定容至25 mL,摇匀。该标准储备液1 mL含有10 mg的茶氨酸。

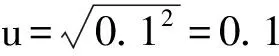
(3)定容25 mL容量瓶,主要涉及体积校准和水溶液温度变化两个不确定度分量来源。

表1不确定度的来源分析

Tab.1 Source analysis of uncertainty
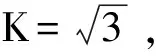
3.1.2 配制标准工作溶液引入的相对不确定度urel(C2)
移取0.0 mL、0.5 mL、1.0 mL、1.5 mL、2.0 mL、2.5 mL、3.0 mL标准储备液,分别加水定容至50 mL,摇匀,制成系列标准工作液。再分别吸取1 mL系列标准工作液于一组25 mL比色管中,各加pH8.0磷酸盐缓冲液0.5 mL和2%茚三酮溶液0.5 mL,在沸水浴中加热15 min,冷却后加水定容至25 mL,放置10 min后,用5 mm比色杯,在570 nm处,以试剂空白溶液作参比,测定吸光度。
配制标准工作溶液过程中,使用到1 mL移液管A级、50 mL容量瓶A级、25 mL比色管,其各自的相对标准不确定度计算原理与3.1.1(3)相同。
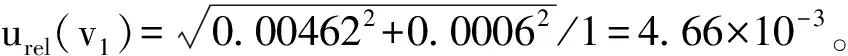
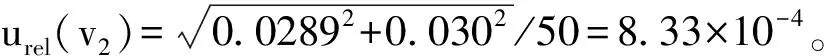

3.1.3 标准曲线拟合引入的相对不确定度urel(Q)
用721分光光度计测定所配制的标准工作溶液的吸光度,每个浓度测定两次,结果见表2。
表2标准工作溶液吸光度
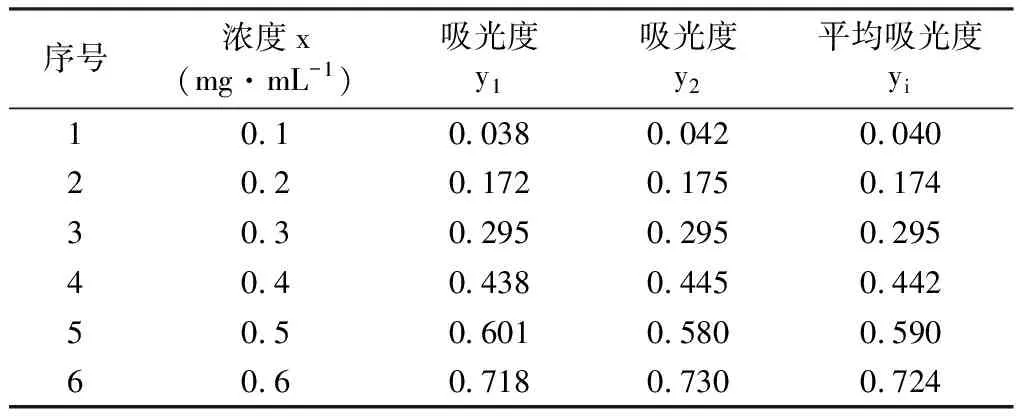
Tab.2 Absorbance of standard work solution
根据平均吸光度计算得出标准曲线为:y=1.375x-0.104,其中斜率b=1.375,截距a=-0.104,相关系数R2=0.999。标准曲线相关数据如下,见表3。
表3标准曲线相关数据

Tab.3 Standard curve data

n:测试标准溶液的次数,n=6×2=12;
p:测试样品的次数,p=4;


b:工作曲线的斜率,b=1.375;
j:下标,测试标准溶液的次数。
3.2 样品定容体积、称样质量、重复测定所引入的相对不确定度
3.2.1 样品处理过程中定容体积的相对不确定度urel(V)
样品经前处理后的滤液用500 mL的A级容量瓶进行定容,再分别吸取1 mL定容滤液于一组25 mL比色管中,各加pH8.0磷酸盐缓冲液0.5 mL和2%茚三酮溶液0.5 mL,在沸水浴中加热15 min,冷却后加水定容至25 mL,放置10 min后,用5 mm比色杯,在570 nm处,以试剂空白溶液作参比,测定吸光度。
定容500 mL容量瓶、移取1 mL滤液和最后定容于25 mL比色管中,均涉及体积校准、水溶液温度变化两个不确定度分量来源。计算原理同3.1.2。
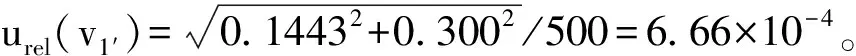
(2)根据3.1.2的计算可知,1mL移液管的相对标准不确定度urel(v2′)=4.66×10-3。
(3)根据3.1.2的计算可知,25mL比色管的相对标准不确定度urel(v3′)= 5.79×10-3。
3.2.2 样品称量产生的相对不确定度urel(M)
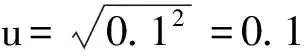
3.2.3 样品重复性测量的相对不确定度urel(X)
实际测定样品溶液4次,茶叶中游离氨基酸总量平行测试的结果(%)见表4和表5。
表4样品实测数据
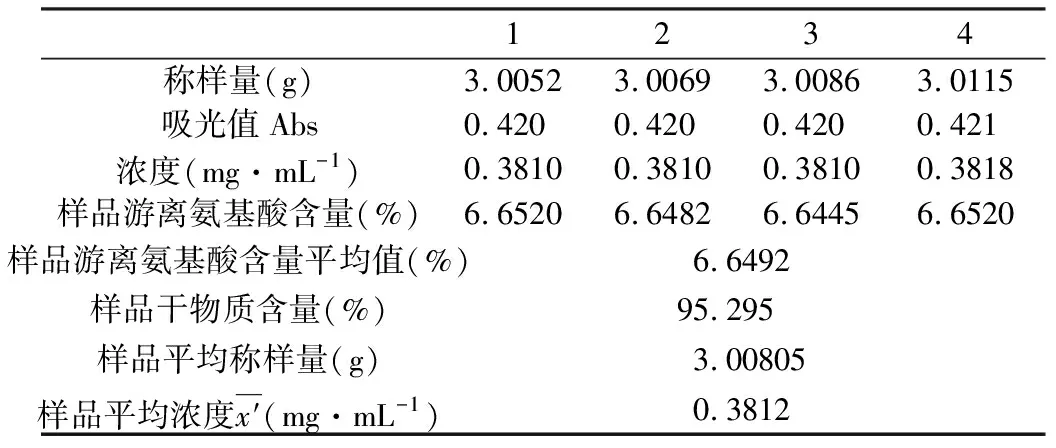
Tab.4 Sample measured data
表5样品游离氨基酸含量平行测试结果
Tab.5Paralleltestresultsoffreeaminoacidcontentinsamples

nxi(%)︱xi-x︱(xi-x)216.65200.00287.84×10-626.64820.00101.0×10-636.64450.004722.09×10-646.65200.00287.84×10-6x(%)6.6492
实验标准偏差根据贝塞尔公式有:
重复性测量的标准不确定度
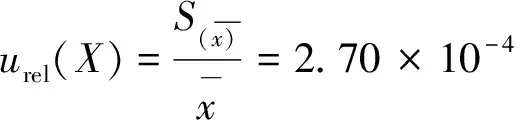
3.3 样品干物质含量测定引入的相对不确定度urel(W)
包含样品干物质重复性测量的相对不确定度urel(r)和干物质称量产生的相对不确定度urel(w1),同时要考虑恒重问题。
表6干物质含量测量数据
Tab.6Measurementdataofdrymattercontent
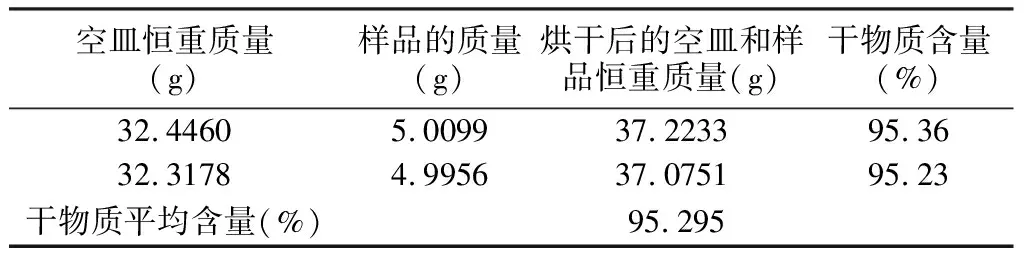
空皿恒重质量(g)样品的质量(g)烘干后的空皿和样品恒重质量(g)干物质含量(%)32.44605.009937.223395.3632.31784.995637.075195.23干物质平均含量(%)95.295
3.3.1 样品重复性测量的相对不确定度urel(r)
根据GB/T 8314-2013[3]的要求,样品干物质独立测量两次,则测量重复性的实验标准偏差为
=0.0919 %
样品干物质平均含量为95.295 %,则重复性的相对不确定度urel(r)=0.065%/95.295%=6.82×10-4。
3.3.2 干物质称量产生的相对不确定度urel(w1)
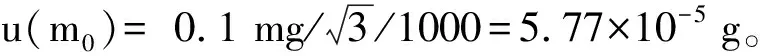
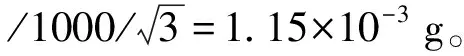
干物质测定中包含3次称量,分别是干燥前称量皿恒重称量,样品称量,干燥后称量皿与样品恒重称量。
称量皿平均质量为32.3819 g,urel(m1)=1.151×10-3g/32.3819 g=3.55×10-5。
(2)样品称量只与天平秤量有关,故u(m2)= u(m0)=5.77×10-5g。
样品干物质平均称样量为5.00275 g,则天平称重的相对标准不确定度
urel(m2)=5.77×10-5g/5.00275 g=1.15×10-5
(3)干燥后称量皿与样品恒重,涉及了天平秤量和恒重,故u(m3)= u(m1)=1.151×10-3g。
干燥后称量皿与样品平均质量为37.1492g,urel(m3)=1.151×10-3g/37.1492 g =3.1×10-5。
综合4.4.1和4.4.2,样品干物质含量测定引入的相对不确定度
=6.84×10-5。
3.4 分析仪器的相对不确定度urel(J)
721分光光度计的校准证书上提供了透射比示值误差测量结果不确定度可见光段Urel=0.6%,k=2,则urel(J)=0.6%/2=0.3%=3.0×10-3。
4 合成相对不确定度
根据表7,合成相对不确定度。
表7不确定度总览表

Tab.7 The uncertainty of the list
合成相对不确定度的计算如下:
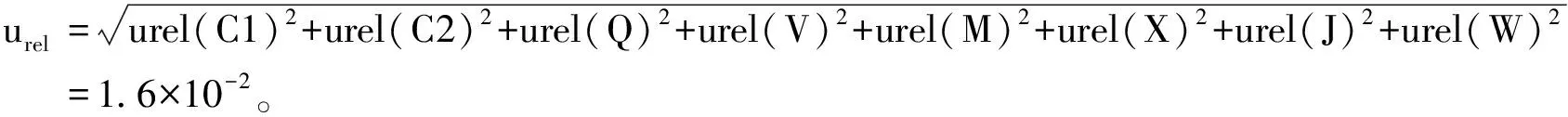
5 相对扩展不确定度评估
取置信概率p=95%,且取扩展因子k=2,则相对扩展不确定度为Urel=1.6×10-2×2=3.2×10-2。
6 结论
本文对GB/T 8314-2013茶 游离氨基酸总量的测定过程做了详细的测量不确定度评估,发现标准曲线拟合是关键步骤,其相对不确定度分量达到1.17×10-2,将会对茶叶游离氨基酸总量的测定产生显著影响,故在测定时应对其重点控制,这对提高检测结果的准确性有重要的参考意义。
本次实验所测的游离氨基酸总量为6.6492%,修约后为6.6%,Urel=3.2×10-2,k=2,p=95%。
