基于MIL-100(Fe)的磁性纳米碳材料的制备及其在内源性肽富集中的应用
2019-07-30赵雅梦张凌怡鲁誉浩张维冰
赵雅梦,王 敏,张凌怡,鲁誉浩,张维冰
(华东理工大学化学与分子工程学院,上海 200237)
全血直接离心得到的人血清中存在蛋白质、脂质、肽段等多种组分[1,2],是一种极其重要的生物样品,广泛用于疾病的检测与诊断。其中,内源性肽段参与了许多重要的生理病理进程[3],是寻找疾病标记物的重要来源。目前,质谱是鉴定内源性肽段的主要方法,但由于血清成分复杂,在鉴定中容易受到其他物质的干扰。因此,在进行质谱分析前,对人血清进行高效、高选择性的预富集十分重要。目前,多种预富集方法已被用于人血清中内源性肽段的富集,如溶剂沉淀法[4,5]、离心超滤法[6]、固相萃取法[7-9]等。
基于金属有机框架(MOFs)的固相萃取材料具有MOFs材料有序的孔道、比表面积大和尺寸排阻效应的特点,可以从复杂的生物样品中富集低丰度的小分子肽段,同时排阻相对分子质量较高的蛋白质,因此被广泛应用于高效分离富集多肽[10-14]。Zhao等[15]合成了一种表面修饰Zr-MOFs的磁性纳米材料Fe3O4@PDA@Zr-MOF,并将其应用于磷酸化肽段的富集。Xiong等[16]采用层层自组装法制备得到了磁性介孔材料Fe3O4@MIL-100(Fe),并将其应用于人血清中内源性肽的富集。金属框架有机物高温煅烧得到的介孔碳材料,具有高度有序结构、化学惰性及强疏水性的优点,是一种良好的富集肽段的材料[17,18]。Sun等[19]以MOFs材料Co-ZIF-67为牺牲模板,合成了一种磁性纳米多孔碳材料(NPC)。该材料具有强磁性、高比表面积、有序的介孔结构以及高含碳量的特点,可以高效地富集生物样品中的N-糖链。Li等[20]等高温碳化Zn-MOFs,得到了具有高比表面积(1 700 m2/g)的碳材料,将其用于N-糖链的富集取得了良好的效果。Zhao等[21]高温煅烧ZIF-67,得到了高度有序的介孔碳材料并将其用于内源性肽段的富集,取得了较好的效果。
本文采用层层自组装法制备得到了具有核壳结构的磁性纳米材料Fe3O4@MIL-100(Fe),在氮气保护下高温煅烧,得到最终的磁性介孔碳材料Fe3O4@MC。该材料具有高碳含量,可以有效吸附内源性肽段。此外,该材料具有超顺磁性,可以实现材料与样品的快速分离。
1 实验部分
1.1 仪器与试剂
4800plus型基质辅助激光解吸电离飞行时间质谱仪(MALDI-TOF MS,美国AB Sciex公司);S3400型真空式扫描电子显微镜(SEM)、JEM-2100型透射电子显微镜(TEM)(日本JEOL公司);Max2550VB/PC型X-射线衍射仪(日本Rigaku公司);APOLLO X型能谱仪(EDS,美国EDAX公司);TriStar II 3flex型氮气吸附/脱附分析由全自动比表面及孔隙度分析仪(美国Micromeritics公司)。
1,3,5-苯三甲酸(H3Btc)、六水合氯化铁(FeCl3·6H2O)、无水乙酸钠(NaAc)、巯基乙酸(MAA)均购于上海阿拉丁生化科技股份有限公司;乙二醇(EG)、乙醇(EtOH)、乙腈(ACN)、三氟乙酸(TFA)购于上海凌峰试剂有限公司;尿素(urea)、碳酸氢铵(NH4HCO3)购于国药集团化学试剂有限公司;牛血清白蛋白(bovine serum albumin,BSA)、胰蛋白酶(trypsin)、二硫苏糖醇(DTT)、碘乙酰胺(IAA)均购于美国Sigma Aldrich公司。人血清由华东理工大学校医院提供。
1.2 Fe3O4@MC的制备
称取1.35 g FeCl3·6H2O和3.6 g NaAc,分散于75 mL EG中,搅拌30 min,将混合均匀的溶液转移至反应釜中,于200 ℃反应16 h,得到Fe3O4颗粒。
称取400 mg Fe3O4颗粒,分散于60 mL EtOH中,随后加入20 μL MAA,室温搅拌24 h,得到Fe3O4@MAA。
称取100 mg Fe3O4@MAA材料,分散于5 mL含10 mmol/L FeCl3·6H2O的EtOH溶液中,于室温下超声15 min,用EtOH清洗3次,除去未吸附的FeCl3·6H2O。将材料分散于5 mL含10 mmol/L H3Btc的EtOH溶液中,于70 ℃水浴加热30 min,用EtOH清洗3次。上述步骤重复30次,得到Fe3O4@MIL-100(Fe)。
在氮气保护下,将Fe3O4@MIL-100(Fe)材料置于管式炉中,于700 ℃反应2 h,最终得到磁性纳米材料Fe3O4@MC。
1.3 样品前处理
称取1.2 mg BSA,溶于1.2 mL含8 mol/L尿素和50 mmol/L NH4HCO3的水溶液中,加入24 μL 1 mol/L DTT,于60 ℃反应1 h,加入8.6 mg IAA,于暗室反应45 min,加入30 μg胰蛋白酶,于37 ℃下酶解16 h,分装冻干,置于-20 ℃冰箱中备用。
量取10 μL人血清,加入90 μL超纯水稀释,煮沸5 min,以5 000 r/min离心10 min后,置于-20 ℃冰箱中备用。
1.4 肽段/内源性肽段富集流程
将0.5 mg Fe3O4@MC材料分散于400 μL超纯水中,加入2 μL 1 μg/μL的BSA酶解液,将10 μL预处理的人血清或者0.5 μL 1 μg/μL的BSA酶解液与50 μg或200 μg的BSA混合,孵育30 min,磁铁辅助下分离,弃除上清液,用超纯水清洗材料。加入10 μL ACN-H2O-TFA洗脱液(80∶19.9∶0.1,v/v/v),孵育10 min,磁分离后收集洗脱液,洗脱过程重复两次,将收集到的洗脱液用于后续MALDI-TOF MS分析。
1.5 质谱分析
利用MALDI-TOF MS鉴定酶解液及人血清中多肽,脉冲激光波长设定355 nm,模式为反射正离子,采用掺钕钇铝石榴石晶体(Nd/YAG)激光源。将0.5 μL洗脱液与0.5 μL 2,5-二羟基苯甲酸(DHB)基质依次滴在样品靶上,结晶后即可进行质谱分析。
2 结果与讨论
2.1 Fe3O4@MC的表征
通过扫描电子显微镜和透射电子显微镜观察Fe3O4@MIL-100(Fe)和Fe3O4@MC的形貌和结构。如图1所示,Fe3O4@MIL-100(Fe)和Fe3O4@MC均为球型结构,粒径约为300 nm,MOFs层厚度约为20 nm。对比Fe3O4@MIL-100(Fe)和Fe3O4@MC的TEM图可知,高温煅烧后,材料的形貌和结构没有发生明显变化。

图1 Fe3O4@MIL-100(Fe)和Fe3O4@MC的扫描电镜图和透射电镜图Fig.1 Scanning electron microscope(SEM)and transmission electron microscope(TEM)images of Fe3O4@MIL-100(Fe)and Fe3O4@MC
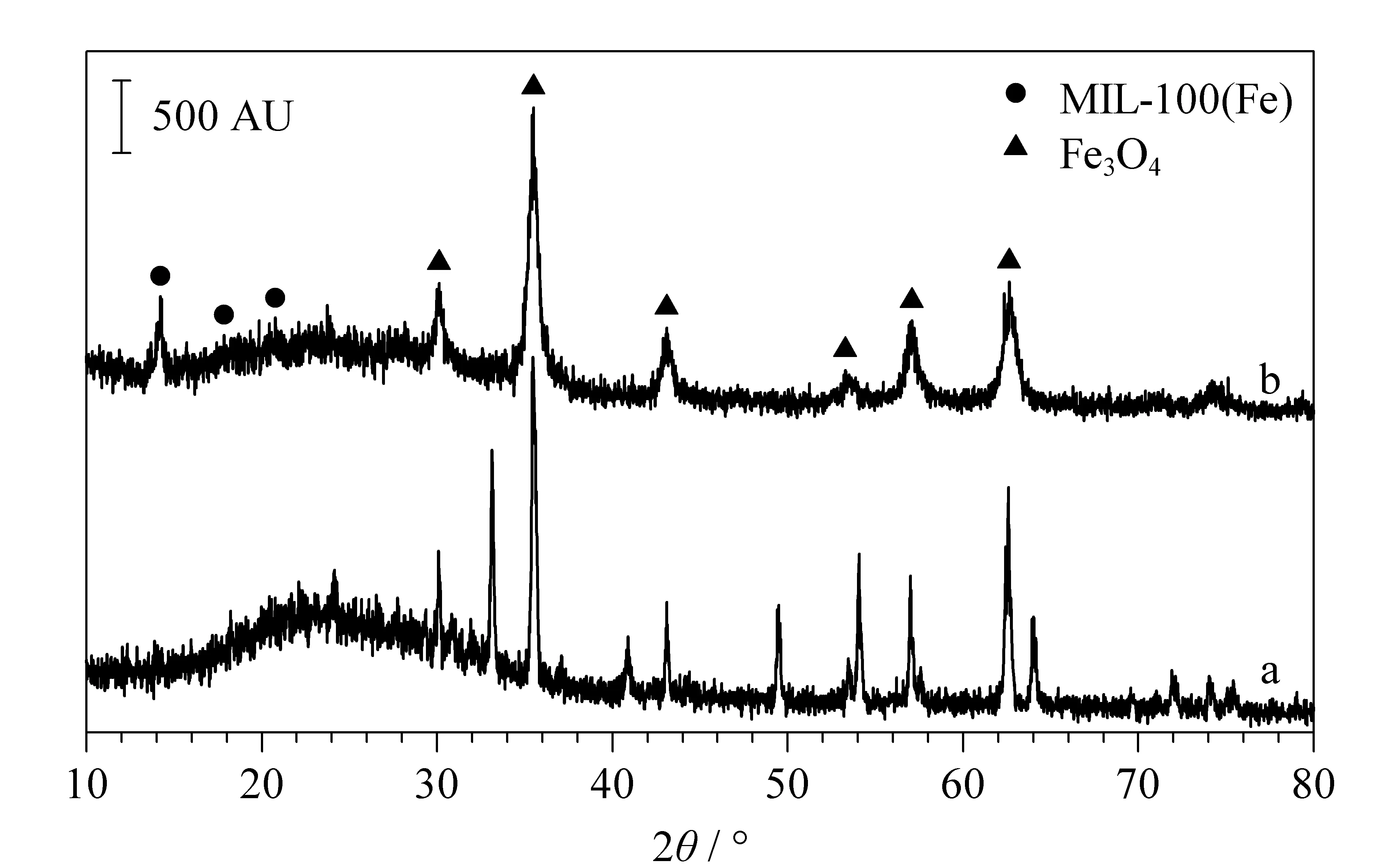
图2 (a)Fe3O4@MC和(b)Fe3O4@MIL-100(Fe)的X-射线衍射图Fig.2 X-ray diffraction(XRD)spectra of(a)Fe3O4@MCand(b)Fe3O4@MIL-100(Fe)
采用EDS对Fe3O4@MIL-100(Fe)和Fe3O4@MC的元素组成和含量进行分析。与Fe3O4@MIL-100(Fe)相比,Fe3O4@MC中碳含量由2.51%增加到6.79%(见图S1,详见http://www.chrom-China.com,下同),这主要是因为在氮气保护下高温煅烧,MIL-100(Fe)中有机组分发生碳化导致碳含量增加。
X-射线衍射仪用于表征材料的晶型结构。如图2所示,14.1°、18.2°和20.2°处出现的衍射峰是MOFs材料MIL-100(Fe)的特征峰,经过高温煅烧后,MIL-100(Fe)的衍射峰消失,23.6°出现的宽峰归属于石墨化碳的002晶面。说明经过高温煅烧,MIL-100(Fe)中的碳组分成功转化为石墨化碳。
氮气吸附/脱附仪用于测定Fe3O4@MIL-100(Fe)和Fe3O4@MC磁性纳米材料的比表面积与孔径分布。如图S2a所示,Fe3O4@MIL-100(Fe)纳米材料为Ⅳ型吸附脱附等温线,计算得到该材料的比表面积为138.40 m2/g;孔径分布如图S2c所示,平均孔径为4.24 nm。经过高温煅烧后,比表面积降为5.18 m2/g,Fe3O4@MC纳米材料的粒径分布如图S2d所示,孔分布范围较宽,平均孔径为17.78 nm。推测Fe3O4@MC磁性纳米材料呈现高尔夫状大孔结构,高温煅烧时MOFs结构改变,形成了多种孔径分布,可用于体积排阻的介孔数量明显减少,随之形成了一些较大的孔道,导致了比表面积下降。
2.2 Fe3O4@MC磁性纳米材料用于标准蛋白质酶解液中肽段的富集
样品酶解过程中由于加入的尿素、碳酸氢铵等无机盐的干扰,直接对牛血清白蛋白酶解液进行质谱分析只检测到了少量的肽段,且信号较低、信噪比很差(见图3a)。经Fe3O4@MC磁性纳米材料的富集,检测到33条高信号、高信噪比的肽段(见图3b),肽段质荷比、序列和位点见表S1。优越的富集效率得益于Fe3O4@MC磁性纳米材料的高碳含量。基于碳组分与肽段间的强疏水相互作用,牛血清白蛋白酶解液中大部分肽段被Fe3O4@MC磁性纳米材料吸附。

图3 经Fe3O4@MC富集(a)前、(b)后BSA酶解液的MALDI-TOF MS质谱图Fig.3 MALDI-TOF MS spectra of the bovine serumalbumin(BSA)digest(a)before and(b)afterenriching by Fe3O4@MC magnetic nanoparticles* Peptides from BSA digest.
为了考察Fe3O4@MC磁性纳米材料的选择性,以牛血清白蛋白作为干扰物。当BSA酶解液与BSA质量比为1∶100时,直接分析BSA酶解液与BSA的混合溶液(见图4a),由于高浓度蛋白质的干扰,只检测到12条肽段,且信号较弱,氨基酸序列为LGEYGFQNALIVR(m/z1 480.7 062)的肽段的信噪比(390.93)极低。经Fe3O4@MC磁性纳米材料富集后,检测到26条肽段(见图4b),氨基酸序列为LGEYGFQNALIVR(m/z1 480.7 062)的肽段的信噪比(1 168.43)明显增强。当酶解液与蛋白质质量比高达1∶400时,仍能检测到25条高信号、高信噪比的肽段(见图4c),所选肽段信噪比(1 029.29)基本保持不变。这一结果说明在高浓度蛋白质的干扰下,Fe3O4@MC磁性纳米材料仍可以高效、高选择性地富集肽段。

图4 不同比例的BSA酶解液与BSA混合物的MALDI-TOF MS质谱图Fig.4 MALDI-TOF MS spectra of different mass ratios of BSA digest and BSA a.direct analysis,m(BSA digest∶BSA)=1∶100;b.enriched by Fe3O4@MC magnetic nanoparticles,m(BSA digest∶BSA)=1∶100;c.enriched by Fe3O4@MC magnetic nanoparticles,m(BSA digest∶BSA)=1∶400.
2.3 Fe3O4@MC纳米材料用于人血清中内源性肽段的富集
Fe3O4@MC磁性纳米材料对于标准蛋白酶解液中的肽段有着优异的富集效果,因此,将其进一步应用于复杂生物样品人血清中内源性肽段的富集。从图5a可以看出,直接对人血清进行质谱分析,血清中存在的高丰度蛋白质、脂质等组分严重干扰了内源性肽段的检测。因此,只检测到少量内源性肽段,且肽段信号峰的强度极弱。经Fe3O4@MC磁性纳米材料富集后,检测到大量高信号、高信噪比的内源性肽段(见图5b),说明Fe3O4@MC磁性纳米材料对于复杂的实际样品有着较好的富集效果。
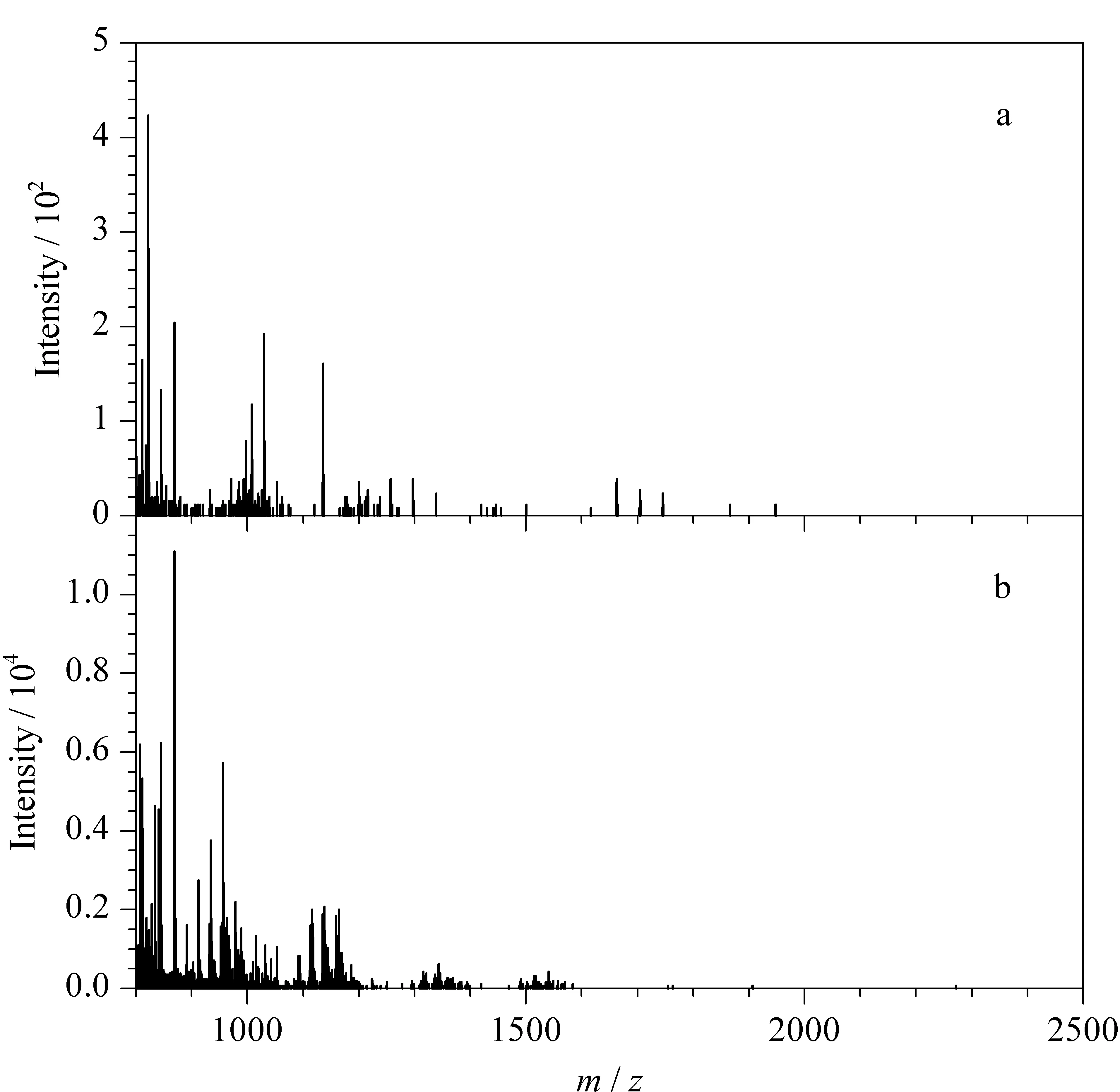
图5 经Fe3O4@MC磁性纳米材料富集(a)前、(b)后人血清的MALDI-TOF MS质谱图Fig.5 MALDI-TOF MS spectra of human serum(a)before and(b)after enriching by Fe3O4@MC magnetic nanoparticles
3 结论
本文制备得到了高碳含量、大孔径的磁性纳米材料Fe3O4@MC。基于碳材料与肽段间的强疏水作用及强磁性,Fe3O4@MC可以高效富集BSA酶解液中的33条特征肽段。此外,该材料对于复杂样品人血清中内源性肽段也具有较好的富集效果。Fe3O4@MC磁性碳材料的成功制备为多肽组学的
分离分析提供了更多的选择。
