银电解液中游离硝酸、铜和银的连续测定分析
2019-07-26蒙英宁
蒙英宁
广西南丹南方金属有限公司 广西南丹 547204
银电解液中游离硝酸、银和铜一直都是单独进行取样和测定,操作比较繁琐,试剂消耗比较大,丢弃具有大量银的试液,导致出现浪费。本文使用一份试样进行连续测定,不仅能够使工作效率得到提高,还能够节约试剂。
1 主要试剂和操作方法
使用8+1硝酸,配制之后煮沸冷藏到室温。溴甲酚绿1g/L,氢氧化钠0.02mmol/L,乙醇1g/L,硫酸高铁铵100g/L。
使用32g的无水乙酸钠和适量的水相互融合,添加冰乙酸200ml,使用水稀释到1L,搅拌均匀。
使用1ml银电解液放置到100mL蒸馏水的烧杯中,添加两滴溴甲酚绿指示剂,利用氢氧化钠标准溶液滴到蓝色定(为终点),通过消耗的氢氧化钠标准溶液对硝酸游离(游离硝酸)含量进行计算[1-2]。
对杯壁进行冲洗,使烧杯放置到电炉中加热到50-60℃,添加两滴PAP指示剂与3ML醋酸钠缓冲液,使用EDTA标准溶液进行滴定,溶液从紫红色转变成为黄绿色表示终点。通过消耗EDTA标准溶液对铜含量进行计算。如果试液中的Br3+和Fe3+含量比较多,能够使用硝酸调整pH1.5-1.7,添加1mL坦试剂,滴定溶液为亮黄色,以以上步骤络合滴定。
冲洗杯壁,添加20mL硝酸与10mL铁铵矾指示剂,利用硫磬酸钾(硫氰酸钾)标准溶液滴定,溶液为浅红色为终点,对银含量计算。
2 结果和讨论
2.1 选择指示剂
利用氢氧化钠进行测试过程中,能够使用溴甲酚绿、甲基红等酸碱指示剂,但是因为下步滴定Cu2+的时候,PAR-Cu2+(II)属于红色络合物,蓝色能够对红色进行衬托,从而明确滴定的终点,所以使用溴甲酚绿[3-4]。
2.2 消除Fe3+和Br3+干扰
银电解液中的Fe3+和Br3+微量,在电解液电解期限不断增加的过程中增加。相关原始资料表示,铋含量在0.01-0.40g/L范围中波动,铁在0.01-0.15g/L范围中波动。以此可以看出来,在Fe3+和Br3+含量比较高的时候,对于Cu2+滴定结果就会出现一定的误差。因为Fe3+和Br3+与EDTA络合稳定常数比较大,所以能够使用酸效应方法将干扰消除。本文基于pH值1.5-1.7,将钽试剂作为指示剂,首先使用EDTA对Fe3+和Br3+滴定,之后调整pH值3.5,使用EDTA对Cu2+进行滴定。通过消除情况表示,假如pH值比较低,那么1mg以下Fe3+和Br3+对于Cu2+测定影响比较小。表1为不同pH值中EDTA滴定Cu2+结果。
2.3 滴定Cu2+的pH值
通过EDTA酸效应曲线可以看出来,在pH>3的时候,Cu2+能够使用EDTA定量进行滴定,但是在实际测定过程中并没有充分考虑其他的因素。比如试液中具有其他微量,在滴定Cu2+时pH>3.5的时候,微量也会被滴定。另外,Cu2+在高pH值的时候会出现水解沉淀的情况,从而拖长了终点。在不同pH值条件中滴定Cu结果(表2),通过结果表示,在pH>4.0的时候,Pb2+、Zn2+的干扰比较大。所以,EDTA滴定Cu2+最佳的pH值为pH3.5-4.0之间。
2.4 选择滴定Bi3+、Fe3+的指示剂
滴定Bi3+、Fe3+中具有多种指示剂能够进行选择,比如黄基水杨酸(磺基水杨酸)、二甲酚橙、钽试剂等。通过实验表示,二甲酚橙能够封闭Bi3+、Fe3+,磺基水杨酸在测定高含量Cu2+过程中显色并不明显,钽试剂适合。在Fe3+完全络合滴定之后,在10%的硝酸溶液中,钽试剂和Fe3+络合物破坏,基本无色,不会对铁铵矾指示剂测定银造成影响[5]。
2.5 试样分析和加标回收的结果

表1 不同pH值中EDTA滴定Cu2+结果
以实验步骤,表3为实验分析与加标测定的结果。
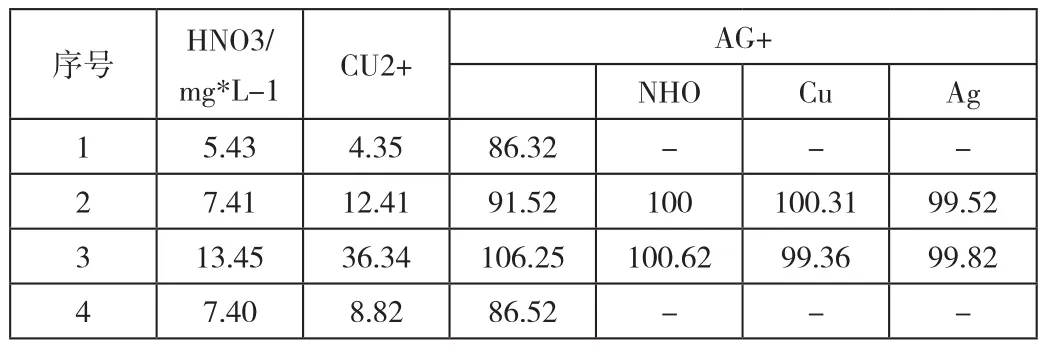
表3 实验分析与加标测定的结果
通过试样平行测定十次,铜、硝酸、银测定标注偏差为0.72%、0.47%、0.1%。
3 结语
通过本文实验表示,并且实现同个试样测定十次,银电解液中有利铜、硝酸与银的连续测定方法精准,操作方便。
