公民逝世后器官捐献合并AKI供体肾移植的疗效观察
2019-07-17张建强蒋鹏顾新伟
张建强 蒋鹏 顾新伟

摘要:目的 探討公民逝世后器官捐献(DCD)合并急性肾损伤(AKI)供体肾移植的临床疗效。方法 回顾性分析2015年1月~2017年11月我院纳入的DCD 42例,其中合并AKI供体13例,非AKI供体29例,比较两组供者、受者一般资料、两组受者术后指标及并发症发生率。结果 本研究共13例AKI供体,其中标准供体7例,扩大标准供体6例;对照组29例非AKI供体,标准供体28例,扩大标准供体1例。两组供体年龄、性别、死亡原因、初始Scr及热缺血时间比较,差异无统计学意义(P>0.05);AKI组EDC供体占比、获取前Scr水平均高于对照组,差异有统计学意义(P<0.05)。AKI组中13例AKI供体行肾移植24例,对照组29例非AKI供体行肾移植56例。两组受者年龄、性别、体重指数、人类白细胞抗原错配数、群体反应性抗体>10%、冷缺血时间、灌注流量、灌注阻力指数比较,差异无统计学意义(P>0.05);AKI组肾脏机械灌注占比高与对照组,差异有统计学意义(P<0.05)。AKI组受者DGF发生率、DGF天数、住院时间,术后1周、1月Scr水平均高于对照组,差异有统计学意义(P<0.05);两组术后1年Scr水平、术后1年肾小球滤过率、术后1年移植肾存活率及术后1年患者存活率比较,差异无统计学意义(P>0.05)。AKI组并发症总发生率为37.50%,高于对照组的12.50%,差异有统计学意义(P<0.05)。结论 DCD合并AKI的供体肾移植受者能获得较好的疗效,可作为扩大供体池的一种选择。
关键词:急性肾损伤;肾移植;公民逝世后器官捐献
中图分类号:R617 文献标识码:A DOI:10.3969/j.issn.1006-1959.2019.12.029
文章编号:1006-1959(2019)12-0096-04
Abstract:Objective To investigate the clinical efficacy of organ donation (DCD) combined with acute kidney injury (AKI) donor kidney transplantation after the death of citizens. Methods A retrospective analysis of 42 cases of DCD included in our hospital from January 2015 to November 2017, including 13 cases of AKI donors and 29 cases of non-AKI donors, comparing the donors and recipients of the two groups, the two groups were Postoperative indicators and complication rates. Results A total of 13 AKI donors were included in the study, including 7 standard donors and 6 expanded standard donors; 29 non-AKI donors in the control group, 28 standard donors, and 1 expanded standard donor. There were no significant differences in donor age, gender, cause of death, initial Scr and warm ischemia time between the two groups (P>0.05). The proportion of EDC donors in the AKI group and the Scr level before the acquisition were higher than the control group,the difference was statistically significant (P<0.05). In AKI group, 13 AKI donors underwent renal transplantation in 24 cases.56 renal transplantation was performed in 29 cases of non-AKI donors in the control group. There were no significant differences in age, gender, body mass index, human leukocyte antigen mismatch, population reactive antibody >10%, cold ischemia time, perfusion flow, and perfusion resistance index between the two groups (P>0.05). The renal mechanical perfusion ratio in the AKI group was higher than that in the control group,the difference was statistically significant (P<0.05). The incidence of DGF, the number of days of DGF, the length of hospital stay in AKI group, the level of Scr in 1 week and 1 month after operation were higher than those in the control group, the difference was statistically significant (P<0.05). The Scr level was 1 year after operation. There was no significant difference in the glomerular filtration rate, the survival rate of transplanted kidneys and the survival rate of patients after 1 year after operation in the first year (P>0.05). The total incidence of complications in the AKI group was 37.50%, which was higher than that in the control group 12.50%,the difference was statistically significant (P<0.05). Conclusion DCD combined with AKI donor kidney transplant recipients can obtain better curative effect and can be used as an option to expand the donor pool.
Key words:Acute kidney injury;Kidney transplantation;Organ donation after citizen's death
对于越来越多急需肾移植的尿毒症患者,供肾短缺依然是个很严峻的话题。我国自开展公民逝世后器官捐献(DCD)以来,捐献工作突飞猛进,但供需矛盾依然十分突出,扩大捐献的标准,将合并急性肾损伤(AKI)的供体作为供肾者有望一定程度缓解这种供需矛盾。本探讨DCD合并AKI供体肾移植的临床疗效,现报道如下。
1资料与方法
1.1一般资料 回顾性分析2015年1月~2017年11月广西中医药大学附属瑞康医院纳入的DCD供体42例,依据AKIN标准定义其中48 h内血肌酐(Scr)升高绝对值≥26.5 μmol/L(0.3 mg/dl)或Scr较基础水平上升50%,或尿量<0.5 ml/(kg·h)并持續6 h以上为AKI组(13例),剔除因临床数据缺乏无法判定是否存在AKI的供体,其余供体肾移植29例为对照组。
1.2免疫抑制方案 两组均给予巴利昔单抗40 mg(诺华制药,批号:JYSB1400082,20 mg/支)进行免疫诱导,分2次给予, 20 mg/次,首剂在术前2 h内给予,第2剂于移植术后4 d给予,维持的免疫抑制方案为他克莫司(安斯泰来制药,批号:JYHZ1400142,1 mg)+吗替麦考酚酯分散片(浙江瑞邦药业,批号:CXHR0900194,0.25 g)+泼尼松(重庆汉华制药,批号:H50021083,5 mg)。他克莫司术后1~2 d开始给予,术后第1个月浓度维持在8~10 ng/ml,之后为6~8 ng/ml。吗替麦考酚酯在术后1~2 d开始给予0.75 g,2次/d;术后2周减量为0.5 g,2次/d。泼尼松术后给予0.5 mg/(kg·d)口服,术后1个月减为10 mg/d。
1.3观察指标 比较两组供者一般资料(年龄、性别、死亡原因、供体类型、初始Scr、获取前Scr、热缺血时间)、受者一般资料(年龄、性别、体重指数、人类白细胞抗原错配数、群体反应性抗体、冷缺血时间、肾脏机械灌注、灌注流量、灌注阻力指数)、受者术后指标(DGF发生率、DGF天数、住院时间,术后1周、1月、1年Scr水平、术后1年肾小球滤过率、术后1年移植肾存活率及术后1年患者存活率)及并发症发生率。依据美国器官资源共享网络(UNOS)扩大标准供体(ECD)指年龄>60岁或>50岁且满足以下3项条件中至少2项:死亡原因为脑血管意外、高血压病史、Scr>1.5 mg/dl,其余的供体则为标准供体[1]。肾移植术后7 d内受者需要透析治疗被定义为移植肾功能延迟恢复(DGF)[2]。用Lifeport肾脏转运器进行肾脏机械灌注(灌注液为KPS-1,灌注温度4~8℃,设定灌注收缩压30 mmHg),如灌注6 h后流量<80 ml/min、阻力指数>0.40 ml/(min·1.73 m2)或病理提示肾皮质坏死、中到重度慢性病变的供肾将被丢弃。
1.4统计学方法 采用SPSS 13.0软件进行统计学分析。正态分布计量资料以(x±s)表示,采用t检验;计数资料以(%)表示,比较采用?字2检验。P<0.05为差异有统计学意义。
2结果
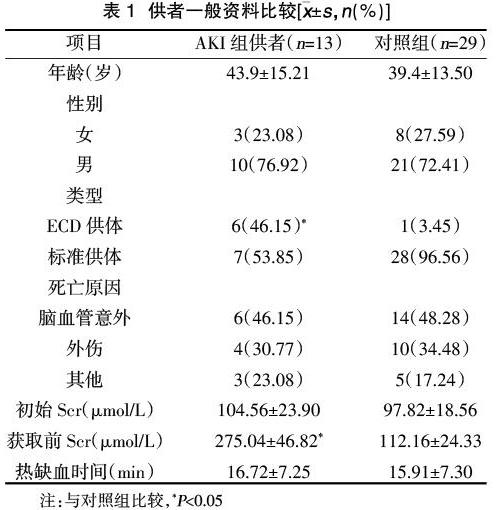
2.1供者一般资料比较 本研究共13例AKI供体,其中标准供体7例,扩大标准供体6例;对照组29例非AKI供体,标准供体28例,扩大标准供体1例。两组年龄、性别、死亡原因、初始Scr及热缺血时间比较,差异无统计学(P>0.05);AKI组EDC供体占比、获取前Scr水平均高于对照组,差异有统计学意义(P<0.05),见表1。
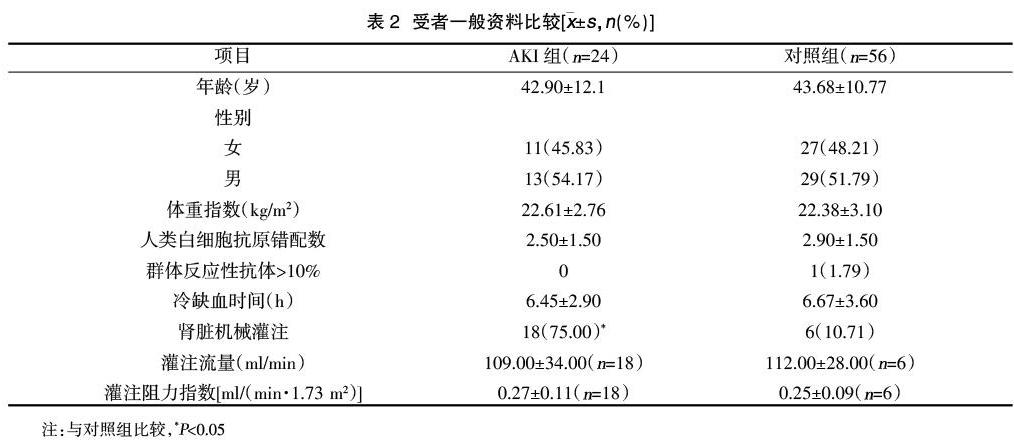
2.2受者一般资料比较 AKI组中13例AKI供体行肾移植24例(2例供肾因病理证实严重的慢性病变丢弃),对照组29例非AKI供体行肾移植56例(1例因右肾多发结石丢弃,1例通过中国人体器官分配与共享计算机系统分配至外院)。两组年龄、性别、体重指数、人类白细胞抗原错配数、群体反应性抗体>10%、冷缺血时间、灌注流量、灌注阻力指数比较,差异无统计学意义(P>0.05);AKI组肾脏机械灌注占比高与对照组,差异有统计学意义(P<0.05),见表2。
2.3两组受者术后指标比较 AKI组DGF发生率、DGF天数、住院时间,术后1周、1月Scr水平均高于对照组,差异有统计学意义(P<0.05);两组术后1年Scr水平、术后1年肾小球滤过率、术后1年移植肾存活率及术后1年患者存活率比较,差异无统计学意义(P>0.05),见表3。
2.4两组住院期间并发症发生率比较 AKI组1例患者术后第2天出现影像学证实血肿形成;8例患者出现移植肾功能延迟恢复,其中有2例合并急性排斥反应,4例继发肺部感染。对照组有2例患者出现急性排斥反应,其中1例合并肺部感染;4例患者出现移植肾功能延迟恢复,其中2例出现急性排斥反应,2例继发肺部感染;1例患者术后3天出现血肿形成且术后9天继发尿漏。AKI组并发症总发生率为37.50%(9/24),高于对照组的12.50%(7/56),差异有统计学意义(P<0.05)。
3讨论
肾移植因更高的生活质量和更好的经济效益,是终末期肾病的最佳治疗方式[3]。我国自DCD全面开展以来,现捐献及移植数量稳居全球第2位,但相对于越来越多的等待移植患者,供肾数量仍是杯水车。为此,积极探索扩大供体池成为目前研究的热点,其中合并AKI供体器官捐献为研究的热点中心,但目前对可否使用AKI供肾仍无统一的定论。
DCD供者治疗期间常存在肾缺血性损伤,可能与肾毒性药物应用、心肺复苏热缺血损伤、血容量不足引起肾灌注不良、肌红蛋白致肾小管阻塞等有关。据报道[4],约有27.6%器官捐献患者会继发AKI。本研究包含42例DCD供体,其中13例AKI供体,含标准供体7例,扩大标准供体6例;对照组为非AKI供体29例,含标准供体28例,扩大标准供体1例。AKI组DGF发生率为33.33%,高于对照组的7.14%,比未发生AKI的肾移植患者高,且恢复时间长,说明AKI肾脏在移植前很容易发生缺血再灌注损伤,再加上术后钙调神经蛋白酶抑制剂等肾毒性药物应用,术后更容易出现DGF。Seo CH等[2]报道191例肾移植患者中,发生DGF患者31例(占16.2%)。Molnar MZ等[5]研究中8961例肾移植患者中,发生DGF患者1951例(22%)。本研究中DGF发生率低于文献报道,可能与供肾冷缺血时间(CIT)短有关,CIT短可能与器官获取后供肾通过中国人体器官分配与共享计算机系统分配至本院受者,肾移植均在本院完成导致手术前等待时间短有关。有研究报道[6],CIT、透析时间、供者年龄、Scr水平等为DGF发生的危险因素,DGF可能会导致住院时间长、出院时Scr水平较高,这也与本研究结果相符。此外,AKI组患者出院时Scr高,可能还与AKI供肾的肾实质、肾小管未完全修复有关系。
本研究中,两组受者术后1年Scr水平、术后1年肾小球滤过率比较,差异无统计学意义(P>0.05)。这说明合并AKI的DCD供体经过积极治疗维护,肾移植术后有可能获得与非AKI供体肾移植同样的远期效果,可能与发生AKI后机体迅速启动“修复”机制,经历损伤、修复及重塑过程,促进内皮细胞修复及肾小管细胞再生,重建正常的肾脏结构及功能有关。其中关键步骤是肾小管上皮细胞的正常增殖与纤维性修复的适度调控,这个过程大概持续3个月~6个月。最迟6个月~1年后,移植肾有望保持稳定的肾小球滤过率[4,7]。但Khalkhali HR等[8]从1534例肾移植患者中筛选214例慢性移植肾功能减退的患者进行研究,DGF显著影响到远期的移植肾功能(RR=6.087,P<0.001)。Nagarajan M等[9]认为70.53%的AKI供肾受者在术后5年会出现慢性肾病,而非AKI供肾出现慢性肾病的概率只有27.67%。Farney AC等[10]研究指出AKI供肾出现DGF并不影响远期移植肾功能,而非AKI供肾出现DGF可能会影响移植肾3年存活率。本文因研究时长的限制,只对肾移植术后1年内主要指标进行观察,尚需更进一步的研究加以验证,本研究中术后1年移植肾存活率及术后1年患者存活率比较,差异无统计学意义(P>0.05),表明AKI供肾并未影响1年的移植肾功能及移植肾存活率。并非每个AKI供肾均可用于移植,除零点穿刺病理和机械灌注参数作为评估取舍的手段,国际上通用的供肾分配制度(KDPI)可作为一个参考[11]。
本研究结果显示,AKI组并发症总发生率为37.50%(9/24),高于对照组的12.50%(7/56),差异有统计学意义(P<0.05),但AKI组并未因较高的并发症导致患者死亡或影响移植肾长期功能。Kovacs CS Jr等[12]认为,如果Scr水平持续下降或感染没有得到完全控制,此时行供肾获取手术后受者并发症多,甚至导致移植肾失败。因此,针对合并AKI的潜在捐献者应常规进行脏器功能维护,如控制感染、避免肾损害加重因素等。
综上所述,合并AKI的供体肾移植受者可获得较好的疗效,可作为扩大供体池的一种选择。但鉴于本研究样本量少,研究期限短,且属于回顾性研究,故在临床实践工作中,是否接收合并AKI的供肾建议肾内科、移植科、病理科等多学科协作讨论,并结合供者与受者情况综合评估风险及获益来决定。
参考文献:
[1]Nagaraja P,Roberts GW,Stephens M,et al.Impact of expanded criteria variables on outcomes of kidney transplantation from donors after cardiac death[J].Transplantation,2015,99(1):226-231.
[2]Seo CH,Ju JI,Kim MH,et al.Risk factors and long-term outcomes of delayed graft function in deceased donor renal transplantation[J].Ann Surg Treat Res,2015,89(4):208-214.
[3]Jay CL,Abecassis MM.The"opportunity costs"of kidney transplantation[J].Am J Transplant,2018,18(5):1044-1045.
[4]Lee MH,Jeong EG,Chang JY,et al.Clinical outcome of kidney transplantation from deceased donors with acute kidney injury by Acute Kidney Injury Network criteria[J].J Crit Care,2014,29(3):432-437.
[5]Molnar MZ,Kovesdy CP,Bunnapradist S,et al.Associations of pre-transplant serum albumin with post-transplant outcomes in kidney transplant recipients[J].Am J Transplant,2011,11(5):1006-1015.
[6]Salazar Meira F,Zemiacki J,Figueiredo AE,et al.Factors associated with delayed graft function and their influence on outcomes of kidney transplantation[J].Transplant Proc,2016,48(7):2267-2271.
[7]Iortiz A,Ucero AC,Egido J.Unravelling fibrosis:two newcomers and an old foe[J].Nephrol Dial Transplant,2010,25(11):3492-3495.
[8]Khalkhali HR,GhafariA,Hajizadeh E,et al.Risk factors of long-term graft loss in renal transplant recipients with chronic allograft dysfunction[J].Exp Clin Transplant,2010(8):277-282.
[9]Nagarajan M,Ramanathan S,Dhanapriya J,et al.Impact of acute kidney injury on renal allograft survival[J].Ren Fail,2017,39(1):40-44.
[10]Farney AC,Rogers J,Orlando G,et al.Evolving experience using kidneys from deceased donors with terminal acute kidney injury[J].J Am Coll Surg,2013(216):645-655.
[11]Chopra B,Sureshkumar KK.Kidney transplantation in older recipients:Preemptive high KDPI kidney vs lower KDPI kidney after varying dialysis vintage[J].World J Transplant,2018,8(4):102-109.
[12]Kovacs CS Jr,Koval CE,van Duin D,et al.Selecting suitable solid organ transplant donors:reducing the risk of donor-transmitted infections[J].World J Transplant,2014,4(2):43-56.
收稿日期:2019-4-29;修回日期:2019-5-9
編辑/杜帆
