蛋白质质谱检测技术在临床中的应用*
2019-07-16刘晓慧申华莉陆豪杰刘宝红杨芃原
刘晓慧 申华莉 张 莹 陆豪杰④ 刘宝红 杨芃原④*
高效地将科研成果转化到临床应用一直是生物医学、转化医学和政府工作者努力的重要方向。以往,对于新研发的临床诊断试剂或者仪器,需要等到其获得食品药品监督管理局(Food Drug Administration,FDA)批准进入商业化生产后,才能被应用到患者身上,一定程度上推迟了科研成果对医生和患者的帮助,延缓了其对医学发展的促进,尤其是当相关试剂盒或者检测方法很难被研发出来时,这个问题尤为凸显[1]。
近来年,针对蛋白质的酶联免疫吸附测定(enzymelinked immunosorbent assay,ELISA)试剂盒,其抗体制备有效性、可靠性以及交叉反应问题已严重困扰科研和临床工作者,针对有意义的翻译后修饰,如与肿瘤发生发展相关的重要激酶通路蛋白的磷酸化等,抗体的制备更是难上加难[2-4]。因而,新的诊断仪器与方法以及新的法规需要被发展,以缩短科研成果转化的进程。质谱仪器技术和方法学的快速进展,对临床标志物尤其是蛋白质标志物的检测,形成了巨大的冲击和推动。临床标志物的质谱检测,将成为今后临床检验的主流工具。
1 质谱检测技术与定量技术
1.1 质谱检测技术
回顾质谱仪器技术和方法学的主要发展,质谱技术是一种测量分子的离子形式的质荷比技术。20世纪末,出现溶液态的电喷雾电离化(electrospray ionization,ESI)技术和固体态的激光解析基质辅助激光解吸电离(matrix-assisted laser desorption ionization,MALDI)技术,很好地解决了大分子如蛋白质和多肽的电离问题,发明人因此获得2002年的诺贝尔奖。质谱仪器利用了离子光学和电子学技术,神奇地控制被导入的离子,再把不同质荷比的离子巧妙地分离开,再用合适的检测器鉴定这些离子的分子归属。测量离子质量的技术原理可以分为两大类:一类是观测离子的受控圆周运动,轻的离子转得快,重的离子转得慢,如果再有外加的交变电场,离子将做胁迫振荡(四级杆)或受激共振(离子阱);另一类是依据离子的受控直线运动,轻的离子飞得快,重的离子飞得慢,即形成所谓的飞行时间质量分离器。也可以将离子的直线运动在外电场胁迫下转变成圆周运动,即形成近来发展很快的静电轨道离子阱(图1)。
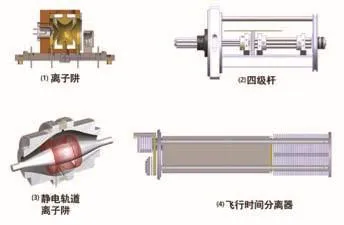
图1 离子阱、四级杆、静电轨道离子阱和飞行时间分离器质谱示意图
1.2 质谱定量技术
质谱分析大分子离子的灵敏度在近20年有了4个数量级的提高,主要得益于:①纳电喷雾技术(细的雾滴具有更好的离子化效率);②高效的色谱分离(微量成分信号不再受干扰);③离子漏斗技术(离子在漏斗电场中的去溶和富集);④脉冲同步和离子累加技术(离子在阱电场中的捕获和累积);⑤傅里叶变换技术(分辨率和灵敏度上升)。此外,质谱本身优异的定性和定量功能也被充分的发挥。近年来科学家基于质谱信号发展了各种半定量方法,如基于信号强度的绝对定量(intensity-based absolute quantification,iBAQ)方法的发展,加入单标或多标同位素标记参比物或标准物定量的方法,如细胞培养条件下稳定同位素标记(stable isotope labeling with amino acids in cell culture,SILAC)技术、同位素标记相对和绝对定量(isobaric tags for relative and absolute quantification,iTRAQ)和串联质量标签(tandem mass tag,TMT);同时也开发了不同的质谱采集模式和检测方法,如数据依赖(data dependent acquisition,DDA)、多反应离子监测(multiple reaction monitoring,MRM)和非数据依赖(data independent acquisition,DIA)以及所有理论质谱的序贯窗口采集(sequential window acquisition of all theoretical mass spectra,SWATH-MS)。这些定量和采集方法的发展,使得质谱方法可以准确地定量蛋白和肽的含量。
2 质谱检测技术的临床应用
蛋白和肽的准确定性以及和疾病的关联还依赖于数据库和搜索软件的发展。近年来,各种基因组库、转录组库、翻译组库、蛋白质组库和多肽库不断的涌现,极大地丰富了数据检索并提高了检索准确性。因此,随着临床蛋白质组、多肽组数据的不断增加,国家专项、国家基地和各大医院的疾病组库的建设已经呈现出很好的态势,而这些数据为即将到来的大数据、建模预测和精准医疗的发展提供了坚实的基础,很大程度上促进了临床检测标志物的开发。
随着近年来仪器性能的提升,质谱法以其方法开发高效快速且成本低,加之其高灵敏度、高特异性和高准确性的特点,目前已满足临床检测需求,在产前诊断、新生儿筛查[5]、药物滥用检测[6]、代谢物(如氨基酸,脂质)、类固醇[9]和临床微生物检测[10]等方面获得了广泛的应用。质谱技术成为了基于抗体的检测,如ELISA法的有效补充,针对某些分析物,甚至表现出优于ELISA的临床表现,质谱技术是极具开发前景的高效快速临床诊断方法发展的技术。尤其因为质谱技术具有较高的特异性,在与可重复的色谱分离技术联用时,可作为特定分子浓度检测手段的校准方法。将该方法作为参考方法且严格按照书面程序进行检测,可以作为定量“金标准”。由于质谱仪器操作复杂,获得准确的结果并达到要求的精密度尚需非常小心,因此质谱技术常被视作“无其他方法可用时的最佳技术”。
鉴于质谱技术在临床检测领域的作用日渐凸显,以及其技术方案发展的实际需求,美国FDA在2014年10月发布的实验室开发测试(laboratory developed test,LDT)指南草案中明确指出,基于质谱发展的可进入临床检测的服务包含其体外诊断(in vitro diagnostics,IVD)试剂相关产品,可以申报医疗器械的一类(低风险)和二类(中度风险)[11]医疗器械注册证。FDA也同时对申报相应方法本身的准确度、线性度、分析灵敏度、特异性与干扰、定量数据要求、质量控制体系和样品结转10余项提供了严格对应的指导文件(如510 k)[12]。因而也刺激了基于质谱的临床检测方法的快速发展,不少针对小分子和代谢物质谱诊断试剂盒和方法已经获得了美国FDA的许可(Clear)或者批准(approved)。
3 蛋白质标志物临床质谱检测
近年来,蛋白质作为生物体生理和病理状态的重要指征和生命功能执行者,一直是生物医学领域研究的热点,越来越多研究表明,监测蛋白质群(Protein panels)表达量的变化,被发现在疾病诊断方面具有优于单诊断标志物的表现,如OVA1组合已获得美国的批准[13];最近在Science刊物上更有研究表明,蛋白质群与基因检测联合诊断,将极大提高诊断的准确性[14-15]。此外,蛋白质的表达形式变化,如翻译后修饰变化,也成为对疾病进行监测的重要方向[16]。蛋白质磷酸化被报道是肿瘤相关信号通路中关键作用分子,也是很多药物作用的靶标[17];蛋白质的糖基化被报导在肿瘤的转移复发过程中对细胞和蛋白质功能起到重要调节作用,也是细胞免疫和应答的重要分子。因而针对蛋白质的诊断标志物研究取得了优异的研究成果[18]。然而尽管蛋白质标志物的重要性不断被证实,大部分被发现的潜在诊断标志物都未能在大量临床样品中获得证实和确证。美国获得许可或批准的蛋白质标志物一直维持在1.5个/年的低速增长[19-20]。其中,重要的原因即在于这些诊断标志物对应的定量检测方法研发周期长,难度大,而发展不依赖抗体的质谱定量技术,给研究者提供了一个新的选择[21]。
3.1 蛋白质标志物检测的主要质谱技术
目前,广泛应用的蛋白质质谱绝对定量技术-多反应监测(multiple reaction monitoring,MRM)技术,是小分子领域广泛使用的选择反应监测(selected reaction monitoring,SRM)技术在蛋白质和(或)多肽领域的应用。目前,临床MRM质谱定量检验中主要采用三重四级杆质谱(图2)。

图2 三重四级杆质谱结构示意图
三重四级杆最简单的模式是全扫描,采集生成的全部离子的信号,Q2设置为所有离子可通过,Q1与Q3同时进行扫描。①子离子扫描:Q1设置为仅特定m/z的离子可通过,Q2中充入碰撞气体令离子碎片化,Q3对子离子产物进行扫描;②母离子扫描:识别共同碎片并观察产生该碎片的所有母离子,由Q1进行扫描,在Q2中通过碰撞气体使离子碎片化,Q3仅识别特定m/z的离子,该模式还可检测糖基化类型;③中性丢失扫描:对Q1与Q3同时进行扫描,将两者质量抵消偏移,Q2中充入碰撞气体进行离子片段化处理;④选择反应监测SRM:用于定量分析,Q1与Q3用于质量分析,Q2通过碰撞气体进行碎片化反应。
SRM进一步升级即为MRM,MRM以SRM为基础,利用仪器控制系统循序选择多重反应,从而实现对多个待测目标物的检测。多重母子离子对即母离子与碎片离子的组合,结合色谱分离保留时间信息,可在特定时间内对色谱洗脱出的特定分析物进行监测,准确地监测待测物。采用化学性质与分析物相同的同位素标记标准品,与待测物的母子离子对同样可通过MRM进行监测可以有效对待测物进行绝对含量测定。SRM与MRM的特异性大幅提升了试验信噪比,提高了定量准确性。
临床质谱MRM技术主要基于液质联用的三重四级杆质谱来分析已知碎裂特征的离子:第一级四级杆选择感兴趣的母离子,在第二级四级杆中发生碎裂,再经由第三级四级杆选择特征离子碎片进行靶向检测,进而比对和计算标准品和测试品的母子离子峰面积信息进行绝对定量。将MRM技术应用于肿瘤标志物的检测方面,具有如下优点:①分析方法建立快速经济,标准品运输保存较方便;②通量高,一次分析可以最多监测到50~100个分析物;③高灵敏度(低至attomole);④较大动态范围,即4~5个数量级;⑤可以分辨出同分异构体,从而实现对蛋白质更加准确的定量;⑥重现性好等特点[22-24]。Steven A Carr[25]领导了数个实验室,在样品前处理的不同阶段(血清酶解之前和酶解之后)加入标准肽和待研究的蛋白,分析了实验室内和实验室间的结果重现性,绝大部分结果偏差在CV25%以内[25]。进一步通过富集方法对蛋白质复合物的研究中则显示,同一个实验室内部的SRM方法重复性为98%,实验室之间的重复性为81%[26]。针对蛋白质样品的MRM定量偏差,一部分因素来源于样品前处理的重复性。为了实现高效、快速及高重现的蛋白质样品前处理,Geyer等[27]报道,Mann研究组研发了一整套基于Stage tip的研究方法,在2 h内完成血液样品的前处理和质谱检测,并评价其数据准确性。研究中检测到40个美国FDA批准的血清诊断标志物的CV值均<20%。高重现的血清蛋白质前处理方法以及MRM技术,辅以对整个方法流程的严格控制以对应质量管理体系的要求,将帮助建立高效的蛋白质和(或)多肽临床定量检测方法[28](图3)。
3.2 蛋白质标志物检测技术开发方案
目前,迫切需要各大临床医院开发实验室自建检测项目(LDT),尤其是临床蛋白质和(或)多肽质谱定量检测技术及其试剂组(盒),其整个研发方案可分为下述3部分。

图3 临床蛋白质和(或)多肽质谱定量方法示意图
(1)血清蛋白质酶解和质量控制标准操作规程(standard operating procedures,SOP)的建立。需要摸索并建立高效的血清蛋白质酶解和质量控制方法,实现对血清中高、中、低丰度蛋白质的定量CV值≤20%,并对酶解所需的试剂、质量控制标准蛋白质和标准方法进行标准化摸索,并形成SOP(标准方法①),为整个研究定量结果可靠性提供基础。
(2)高可信度诊断标志物的筛选。通过设定标准对重要疾病诊断标志物相关的研究进行文献和(或)实验调研和筛选,挑选出重要疾病相关的潜在诊断标志物,并用靶向PRM方法验证在血清中检出可能性,并结合定量结果,初步挑选高可信度的潜在血清诊断标志物,并合成其独有肽段的重标同位素标记肽段(标肽组1)。继而以空白血清为基质,摸索和确定标肽组1的LC-MRM液相分离条件和质谱采集参数,并将之应用于100~200例血清的目标蛋白初步定量研究中,根据定量结果、受试者工作特征(receiver operating characteristic,ROC)曲线,评价并找出高灵敏度和高特异性的重要疾病诊断标志物群。
(3)试剂盒和标准方法的组合及评测。通过同位素氨基酸标记的方法,合成标志物群的定量曲线标准品(标准品②)。将标准品②加入空白血清中,采用标准方法①进行酶解。多次重复实验,测试并计算定量试剂盒相关指标,进一步优化参数,形成定量测定标准方法(标准方法③)。最后将标准方法①、标准品②和标准方法③组成为试剂盒,并在对血清中的标志物进行准确定量,为常规样品分析提供指导和参考。
针对上述高灵敏度和高特异性的重要疾病诊断标志物肽段的独有肽段,合成一组同位素标准肽段。将定量曲线加入空白血清中,作为测试标准品。采用血清酶解的SOP和针对重标肽开发的液相色谱和质谱联用方法,多次数据采集并优化相关参数,评价测试方法的线性、定量限、重现性、准确性、精密度、基质效应以及回收率等指标,使之符合美国发布的510 k对定量测试试剂盒的标准。如满足保证浓度最高点的CV值<15%, 浓度最低点的CV值<20%等指标。进一步确定试剂组(盒)中试剂的组成、标准曲线组成和稳定性,确定整体操作流程标准化(SOP 2)。该定量曲线的制定可用于临床血清样品中目标蛋白的准确含量测定。
4 现状与展望
目前,实验室自建检测LDT项目的标准化严重不足,许多临床实验室开展LDT检测的方法相似,仍缺乏标准化的基础[29-30]。尽管供应商正在着手开发所有针对特定待测物检测所需的试剂、色谱柱以及包括分析软件在内的“试剂盒”,但大部分临床实验室对流动相、校准措施、质量控制措施以及其他检测所需组件仍采用自行研发的方式。虽然在监管、标准化及室间比对等方面已做了一些努力,但不同临床实验室间的检测结果仍存在差异,缺少合适的内标。经同位素标记的“重”标准品已经十分普遍,其与待测物化学性质完全相同,但特定元素被较重的同位素所代替,如2H、13C、15N与18O等。被替代的元素数目各异,但待测物分子质量的增加要求其可与标准品易于区分,所以有必要为每个待测物都设立特定标记内标,但在检测多个待测物或仍缺乏标记物时,可考虑采用替代标准品。这种情况下,标准品的化学性质应尽可能与待测物接近,由于待测物洗出时存在干扰物质会减弱质谱信号,采用同位素标记标准品可部分补偿这类离子抑制效应[31-32]。
2017年,国家原卫生计划生育委员会和科技部在“2017年度精准医学国家重大专项”中设立了“临床定量蛋白质组的质谱仪及配套试剂的研发”的重大专项课题,确定由复旦大学为牵头单位,联合北京蛋白组研究中心、杭州景杰生物、深圳华大基因、北京毅新博创和广州达瑞共6家单位承担。目前,我国临床的质谱检测还处于萌芽状态,仅有少数机构开始尝试,且缺乏统一的体系和标准。此外,国内的质谱仪器和相关试剂几乎完全被国外数家大企业所垄断,导致了我国的临床质谱检测投入成本高、技术支持有限的局面。健康事业是关乎国计民生大业,因此打破国外的技术壁垒,开发我国独立自主知识产权的质谱仪器和配套检测方法则显得至关重要。
本综述未涉及与临床质谱相关的代谢物质谱、微生物质谱、成像质谱、ICP-质谱及流式细胞质谱。
