单核细胞增生李斯特氏菌能力验证结果讨论
2019-07-15张弓,周露,马蓉
张 弓,周 露,马 蓉
(1.扬州市产品质量监督检验所,江苏 扬州 225000;2.江苏省宝应县有机食品质量监督检验中心,江苏 宝应 225800)
1 引言
单核细胞增生李斯特氏菌(Listeria monocytogenes)简称单增李斯特菌,是一种人畜共患病的病原菌,是常见的食源性致病菌之一,其主要的传播途径为食源性传播,可导致爆发流行[1]。李斯特氏菌具有强致病性,可引起人的败血症和脑膜炎,该菌广泛存在于自然界中,其中,食品中存在单增李氏菌,比如海产品等食品该菌检出率较高,人类食用含有该菌的食品之后,会造成极大的危害。该菌生命力较强,能在4 ℃的环境中生长并繁殖。因此,在食品卫生微生物检验中,必须加以重视。
能力验证是实验室进行质量控制和提高检测能力和水平以及发现检测过程中存在问题的重要手段,能力验证利用实验室间比对来判定实验室和检查机构能力的活动[2],在实验室进行资质认定和评审的过程中,能力验证是必查的部分,是对检验能力的一种评价。能力验证结果是CNAS判定申请认可和获准认可实验室是否维持其技术能力的重要依据之一[3]。为此,本实验室参加了中国检验检疫科学研究院测试评价中心组织的关于单核细胞增生李斯特氏菌的能力验证。
BAX System Q7全自动病原微生物快速检测系统是近年来比较流行的,应用比较广泛的一种快速筛选方法。其原理是以病原菌的特定基因为靶标,利用实时荧光定量PCR对其进行扩增,具有灵敏性和高特异性的特点。虽然食品微生物检验国家标准中没有指定该种方法作为特定检测方法,但是因为其具有准确、快速的优势,当面对批量检测时,可作为辅助方法,快速筛选疑似菌,并结合传统鉴定方法,能提高工作效率。
2 实验操作部分
2.1 检测依据
食品中单核细胞增生李斯特氏菌检验国家标准GB 4789.30-2016《食品安全国家标准 食品微生物学检验 单核细胞增生李斯特氏菌检验》[4]和中国检验检疫科学研究院测试评价中心作业指导书。
2.2 仪器和试剂
(1)仪器:高压灭菌器(日本Hirayama),电子天平(上海卓精电子科技有限公司),生化培养箱(上海博迅实业有限公司医疗设备厂),均质器(interscience),恒温水浴锅(金坛市中大仪器厂),BAX System Q7全自动病原微生物快速检测系统(美国杜邦公司)
(2)培养基和试剂:含0.6%酵母浸膏的胰酪胨大豆肉汤(TSB-YE),含0.6%酵母浸膏的胰酪胨大豆琼脂(TSA-YE),李斯增菌肉汤LB(LB1,LB2),PALCAM琼脂,李斯特氏菌显色培养基。BAX System Q7全自动病原微生物快速检测系统试剂盒为美国杜邦公司生产。
2.3 样品
样品:单核细胞增生李斯特氏菌能力验证样品2瓶,编号为18-C660,18-F999。样品来自于中国检验检疫科学研究院测试评价中心。
2.4 检测和鉴定过程
2.4.1 前增菌、增菌和初筛
根据本次参加能力验证的作业指导书要求进行样品前处理,在P2实验室无菌条件下将2瓶西林瓶打开,每瓶用4 mL稀释液进行再水化,待样品充分溶解后,将溶解液用移液枪吸出放入预先配制的无菌LB1培养液中(可反复用余下的稀释液清洗西林瓶内壁,保证样品在西林瓶中无残留)。操作各环节应保证无菌,在检验的过程中设置阳性对照和阴性对照。将上述增菌液放置于30 ℃生化培养箱中培养24 h。从增菌液中吸取0.1 mL转种于10 mL LB2灭菌培养液内,置于30 ℃生化培养箱培养24 h。
用BAX Q7试剂盒对增菌液进行处理,具体为在PCR试管中加入200 μL裂解液和2.5 μL蛋白酶,配成预混液,吸取50 μL增菌液至预混液中,设置阳性对照和阴性对照,55 ℃处理60 min,95 ℃处理10 min,4 ℃冷却5 min,上机。结果见图1和图2,单核细胞增生李斯特氏菌会在85 ℃附件出现峰值。经仪器检测,样品18-C660为阳性,18-F999为阴性。
2.4.2 分离
在无菌条件下用接种环将LB2增菌液划线接种于PALCAM琼脂培养基,同时接种于李斯特氏菌显色培养基,置于36 ℃生化培养箱中培养48 h。具体结果见表1。
2.4.3 初步筛选
在培养后的平板上用接种环挑取3~5个可疑菌落,分别接种木糖和鼠李糖发酵管,不灭菌,直接在TSA-YE培养基上接种划线,将各发酵管和TSA-YE培养基分别置于36 ℃生化培养箱中培养24 h。木糖阴性、鼠李糖阳性的培养物(李斯特氏菌生化特性为木糖阴性和鼠李糖阳性)继续鉴定。经培养,编号为18-C660的样品木糖发酵管为阴性,鼠李糖发酵管为阳性。编号为18-F999的样品木糖、鼠李糖发酵管均为阳性。阳性菌种符合。
2.4.4 鉴定
镜检:从TSA-YE平板上挑取菌落,做革兰氏染色,并进行镜检,镜检结果:编号18-C660染色结果为革兰氏阳性短杆菌,与阳性菌种革兰氏染色后的镜检结果一样。
动力试验:从TSA-YE平板上挑取菌落穿刺接种SIM生化管,培养后观察结果:18-C660分离的细菌有动力,并呈伞状生长。
生化鉴定。用阳性单核细胞增生李斯特氏菌做对照(图3)。对样品18-C660进行生化鉴定,生化鉴定结果与阳性菌株一致。表2为生化鉴定结果 。
溶血试验:经溶血试验,样品18-C660溶血。
协同溶血试验:样品18-C660在靠近金黄色葡萄球菌的接种端溶血增强。
3 结果
通过以上实验得到编号18-C660样品检出单核细胞增生李斯特氏菌,编号18-F999样品未检出单核细胞增生李斯特氏菌。
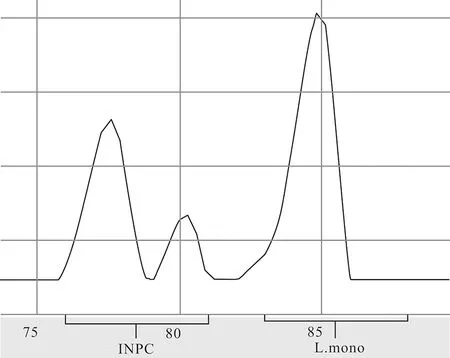
图1 (18-C660)
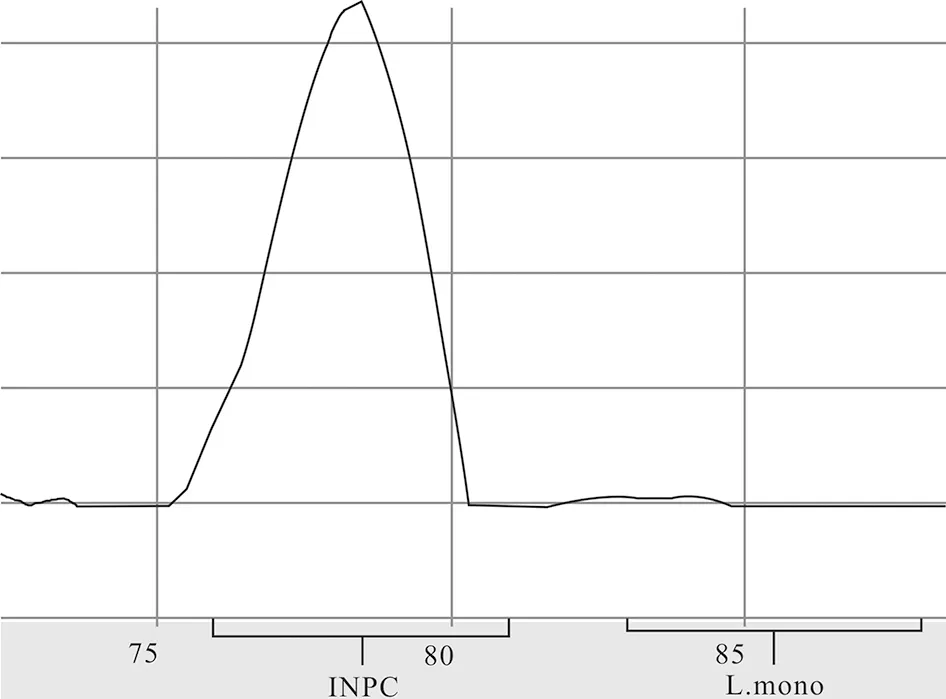
图2 (18-F999)
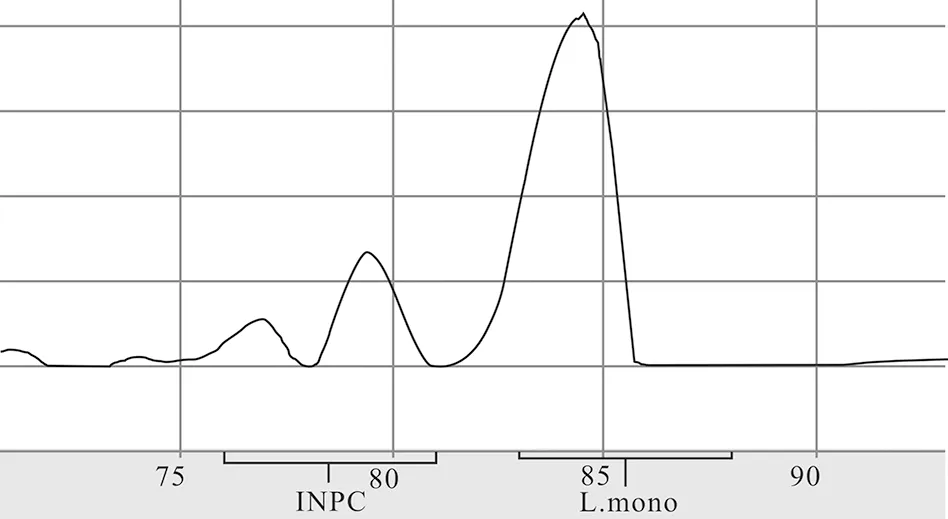
图3 阳性对照
4 讨论
能力验证是检测人员技术能力提升的有效途径,能力验证结果满意,则可以认为该检测人员具备该项分析检测技术的能力,同时能力验证是对仪器设备检查和期间核查的有效方法。实验室可通过参加能力验证提高实验室内部质量管理、考核检测人员的检验能力、建立新的检测方法[5]。本次实验室参加的能力验证结果满意。
随着食品检验数量的日趋增多,各实验室在不断的提升检测技术和水平。如何更快捷、更准确的检测食品中的微生物,从而提高检测工作效率和缩短检测周期,是实验室能否在食品检测领域提高竞争力和可信度的重要手段。目前针对食品安全检测主要有两种方法:一是按照食品安全国家标准通过传统传统方法检测,经过培养、增菌、平板鉴定和传统生化鉴定。二是利用快速筛选系统和全自动鉴定系统,实现食品微生物快速检测。虽然传统的生化鉴定方法准确,但是其过程繁琐,在面对大批量检验任务时,不能提高检测效率。因此,本实验室采用了传统的生化鉴定方法和BAX Q7快速筛选方法,检测结果一致,但是用BAX Q7系统更快捷方便,也缩短了检测时效。
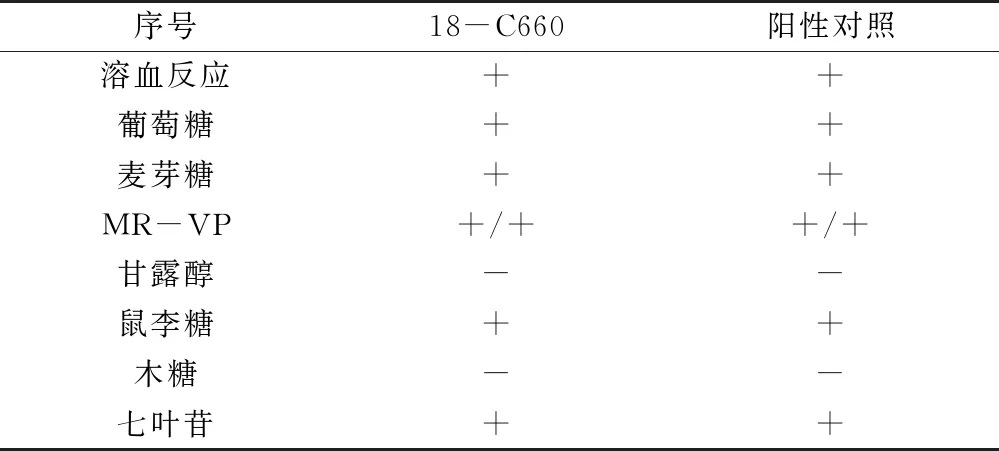
表2 TSA-YE平板上可疑菌落纯培养物生化结果
杜邦BAXQ7筛选系统灵敏性高,特异性好,在食品检测和疾病预防控制中心病原微生物检测得到了广泛的应用,可大批量的检测,缩短了检测时间,提高了检测效率。为检测提供明确的方向[6]。但也存在弊端:一是在操作的过程中容易造成交叉污染;二是食品中的死细菌也能检测出来。这两种弊端容易造成假阳性结果因此,在操作的过程中应注意,而传统的生化鉴定则避免了假阳性的检测结果。
本次能力验证采用两种方式检测,结果一致,同时也获得了能力验证满意的结果,提高了检测水平,提升了检验人员信心,对以后食品中单核细胞增生李斯特氏菌的检测提供经验,在做大批量检测任务时,对培养后的产物利用BAX Q7快速筛选系统进行初筛,并结合传统的生化鉴定系统,能更好、更快、更准确地完成检测任务。
