地质封存条件下CO2在模拟盐水层溶液中的溶解度研究
2019-07-06金旸钧陈乃安盛溢徐艳梅王军良潘志彦
金旸钧,陈乃安,盛溢,徐艳梅,王军良,潘志彦
(浙江工业大学环境学院,浙江杭州310032)
由CO2过度排放所引起的温室效应已经越来越受到人们的广泛关注。CO2的捕获与封存技术(Carbon capture and storage,CCS)是将工业生产中的CO2气体分离收集后压缩,然后注入到具备合适封存条件的地点中与大气隔绝,进行长期封存的技术,是目前最受关注的CO2减排技术之一[1]。CCS技术主要包括以下几个方面:地质封存、海洋封存、矿物封存、生态封存及工业利用[2-6]。其中,CO2的地质封存技术最具减排效果与发展前景,是各个科研机构与学者研究的热点。CO2的地质封存技术简单地说是将分离收集后的CO2压缩至超临界状态(温度高于31.1 ℃,压力高于7.38 MPa),然后注入到具备封存条件的地层(一般埋存深度≥800 m)中,并依靠地质结构进行永久性地封存。封存场地主要包括深部盐水层、废弃油气藏或正在开发的油气藏、不能开采的煤层等[7]。其中,CO2的地下深部盐水层的封存因其具有埋存量大、封存时间长和封存场地分布广泛等优势,成为了最具发展前景的一项CO2地质封存技术[8]。
CO2在深部盐水层中封存,根据封存机理的不同,可分为地质构造封存、毛细力封存、溶解封存和矿物封存。随着封存时间的增加,前两种封存方式会逐渐向后两种封存方式转变[9]。因此,为了评估各封存场地的CO2地质封存能力,对地质封存条件下深部盐水层溶液中CO2溶解度的研究必不可少。截至目前,已有不少研究者做了相关方面的研究。Prutton等用平衡液取样体积分析法测量了0~70 MPa,75~120 ℃条件下,CO2在质量分数分别为10 wt%、20 wt%和30 wt%的CaCl2溶液中的溶解度[10];Nighswander 等也用此方法测定了纯水以及1 wt %NaCl 溶液中,2~10 MPa,80~200 ℃温压条件下CO2的溶解度[11]。除了以上单一盐溶液体系,也有研究者对多元混合盐溶液体系展开了研究。Teng等测量了温压条件为5~20 ℃,6.44~29.49 MPa,CO2在合成海水中的溶解度[12];Liu等研究了35~55 ℃,2~16 MPa条件下,CO2在KCl、NaCl、CaCl2及其混合溶液中的溶解度[13]。而针对实际深部盐水层溶液中CO2的溶解度探究,也有不少研究者展开了模拟研究。万玉玉等对鄂尔多斯盆地石千峰组咸水层盐溶液进行了化学成分分析与模拟,研究了55 ℃和70 ℃,18 MPa 条件下,CO2在模拟深部盐水层溶液中的溶解度[9];胡丽莎等通过实验模拟鄂尔多斯盆地山西组地下盐水层溶液,测得了40~80 ℃、8~12 MPa条件下,CO2在其中的溶解度[14]。
模拟NaCl-CaCl2-MgCl2-KCl-Na2SO4型深部盐水层溶液,根据温度和压力梯度计算不同埋存深度下的温压条件,利用课题组自主建立的盐溶液体系中CO2溶解度测定方法,研究了CO2在模拟部盐水层溶液中的溶解度及溶解度随埋存深度的变化规律,并对CO2封存量进行了估算。
1 实验装置与方法
实验采用的装置示意图见图1。该装置由一套循环体系(耐高温高压微型可视石英毛细管平衡釜(fused silica capillary cell,FSCC,665 μm OD,300 μm ID)与80 MPa相平衡釜、循环泵用高压不锈钢管(ID 800 μm,OD 1/16″,ID 2.175 mm,OD 1/8″)连接构成)、高精密温控冷热台(控温范围196~400oC、控温精度0.1oC、最高升降温速度50oC/min)、手动加压系统(压力范围0.1~70 MPa、控压精度±0.25%FS)、显微DVD 数字实时录像系统及拉曼光谱原位在线检测系统组成。

图1 溶解度测定装置示意图Fig.1 Solubility measuring device
实验仪器:显微共聚焦激光拉曼光谱(Lab RAM HR800);Linkam 冷热台(CAP500);温度控制器(T95);压力传感器(ModelDG1300-BZ-B-2-5/CJ、Model PS600-CR-BZ-A1-B-70/D);80 MPa相平衡釜(JY-80);手摇定量泵(STB-3);循环泵(GYX-2);高压不锈钢管(ID 800 μm,OD 1/16″,ID 2.175 mm,OD 1/8″);真空泵(FY-1H-N);石英毛细管(TSP300665,ID 300 μm,OD 665 μm,);高压针阀(15-11AF1、15-15AF1);直通接头(15-21AF1NFA、15-21AF1NFB);压紧螺母(15-2AM1)、卡套(15-2A1)。
实验试剂:氯化钠(≥99.5 %);无水氯化钙(≥99.0%);氯化钾(≥99.5%);氯化镁(≥98.0%);无水硫酸钠(≥99.0%);超纯水(实验室自制);高纯CO2(≥99.995%)。
实验方法:
1)模拟盐溶液制备与实验温压条件确定:模拟的深部盐水层盐溶液矿化度分别为8.25 g/L与99 g/L(其中不同种盐的质量配比为NaCl∶CaCl2∶MgCl2∶KCl∶Na2SO4=20∶40∶4∶1∶1),用电子天平称量各类盐质量后加超纯水溶解备用。根据文献提出的地热梯度25~35 ℃/km、压力梯度10.5 MPa/km。实验选取800 m、1 300 m、1 800 m、2 300 m、2 800 m不同埋存深度,计算对应的温压条件[15]。
2)微型可视石英毛细管平衡釜的制作:截取一段长约28 cm 的石英毛细管,然后用火焰燃烧封住毛细管两端,以防后续制作过程中,毛细管被外界杂质污染;截取两段长约2.8 cm 的高压不锈钢管(ID 800 μm,OD 1/16″),并用环氧树脂将其固定在之前截取的石英毛细管两端,静置24 h;随后切除石英毛细管两端外露于不锈钢管的透明部分,并套上紧压螺母和卡套,将石英毛细管与高压针阀连接;用注射器分别吸取无水乙醇与超纯水,通过高压针阀对石英毛细管内壁进行反复冲洗;最后用氮气吹干石英毛细管内壁,并用火焰燃烧去除石英毛细管中间表面约2 cm长的褐色聚酰亚胺层,作为可视窗口,用于后期实验测定过程中观察毛细管内的相态变化(如装置图1中A所示,溶液中CO2未达到饱和时,只能观察到溶有CO2的单一相溶液;当CO2达到饱和时,则能观察到CO2气泡)。
3)装置连接与检漏:将上一步制备好的微型可视石英毛细管反应器接入循环加压管路,使其与循环泵和相平衡釜相连接,并同时置于冷热台的样品槽内,将冷热台固定在显微镜载物台上;随后向循环管路内充入氮气,封闭后加压,恒温观察24 h内管路体系压力变化情况;若压力变化较大,则检查管路各段气密性,直至整个循环管路体系气密性良好;最后对整个循环管路抽真空,等待装样。
4)标准曲线绘制:将事先配置好的一定量待测盐溶液加入到循环管路体系中;随后通过30 MPa 定量泵向反应体系中充入一定量的CO2;用相平衡釜相连的80 MPa 手动加压泵向装置体系加压,使体系达到一个刚性压缩状态;开启相平衡釜搅拌装置,使得CO2溶解于待测盐溶液中;结合装置体系中的循环泵,每静置2 h 约循环15 min,以确保整个循环平衡系统内溶液传质完全;约12 h 后,待系统内溶液静止,通过冷热台及相平衡釜相连的80 MPa 手动加压泵控制反应体系在一定埋存深度的温压条件,对石英毛细管平衡釜内溶液进行拉曼测定;读取CO2费米尔双键与水的O—H伸缩振动键的拉曼峰强度,待数据基本不变时,认为体系达到传质平衡,计算两者的拉曼峰强度比(vCO2/vH2O);最后根据CO2和H2O的拉曼特征峰峰强度比与溶液中CO2浓度建立关系式,绘制标准曲线。
5)溶解度测量:在上述温压条件下加入过量的CO2,至反应体系中有气泡产生不消失,且隔一定时间前后,使用拉曼光谱仪获取的CO2和H2O的拉曼峰强度比基本不变,则认为待测盐溶液中CO2达到饱和,最后利用峰强度比和预先建立的标准曲线获得CO2溶解度。
2 实验结果与讨论
按照上述实验过程,得到了8.25 g/L 与99 g/L 模拟盐溶液中不同埋存深度温压条件下的CO2浓度与拉曼峰强度比的标准曲线(相同矿化度模拟盐溶液中,不同埋存深度温压条件下同一CO2浓度的拉曼峰强度比基本相同),见图2。
建立CO2浓度与拉曼峰强度比标准曲线后,继而测定CO2达饱和时体系的拉曼峰强度,即向装置体系中加入过量的CO2,根据不同埋存深度下的温压条件,控制装置相平衡体系的平衡温度与压力,得到不同埋存深度的温压条件下CO2达饱和时的拉曼峰谱图,见图3。
依据实验所得标准曲线以及CO2达饱和时的拉曼峰强度比数据,计算得到不同矿化度模拟盐溶液中,不同埋存深度的温压条件下CO2的溶解度,见图4。
从图4 中可以看出,随着埋存深度的增加,CO2在不同矿化度模拟深部盐水层盐溶液中的溶解度均呈先减小后增大的趋势。由此可知,随着深度的递增,先是温度对CO2的溶解度影响占主导,当超过一定深度后,由压力对CO2的溶解度影响占主导。因此在进行CO2深部盐水层封存,当埋存深度不高时,从经济效益以及溶解度方面考虑可以适当选取较浅层的深部盐水层。此外,随着盐水层矿化度的增加,CO2在其中的溶解度有所下降。
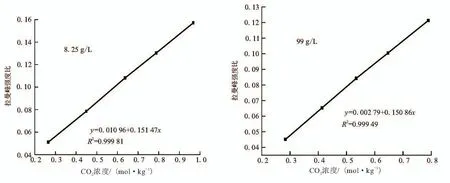
图2 CO2浓度与拉曼峰高比标准曲线Fig.2 Standard curve of CO2 concentration and Raman peak height ratio
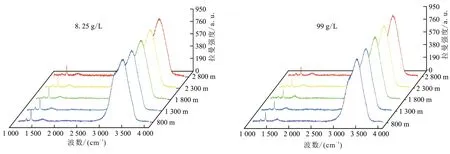
图3 CO2达饱和时不同埋深条件下拉曼峰谱图Fig.3 Raman peak spectra under different burial depths when CO2 is saturated
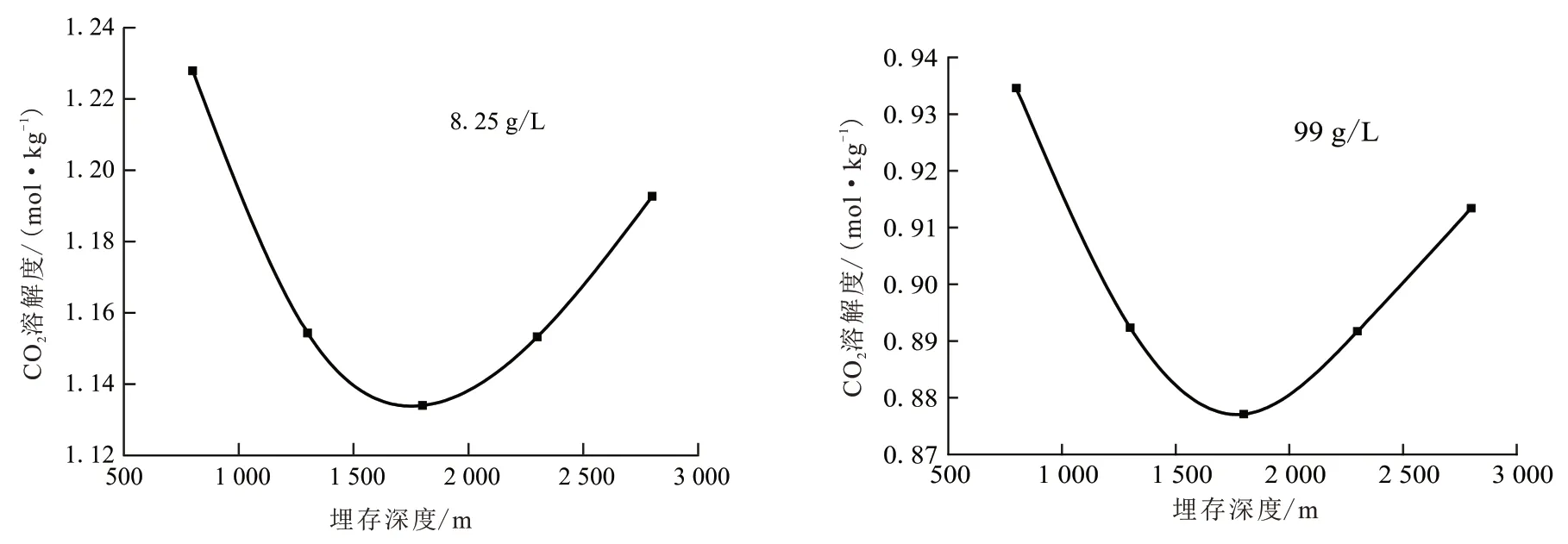
图4 不同埋存深度温压下CO2溶解度Fig.4 CO2 solubility under different buried depth,temperature and pressure
根据对于超临界态CO2的物理性质研究:在达到临界温压条件时,超临界CO2的密度近似于液体。同时,在温度、压力超过临界温压条件时,其密度也会随着温度上升而减小,随着压力上升而增大。因此,对于实验研究中CO2溶解度随深度的变化规律做出如下可能原因分析:在800~1 700 m的地层范围内,此时由于温度相对较低,其对超临界CO2密度的影响力不及压力变化所带来的影响,因此,随着深度的增加,超临界CO2的密度逐渐增大。此时,超临界水溶液体系中的CO2越发地接近于液—液体系,压力对超临界CO2溶解度的影响不及温度的影响明显,所以CO2溶解度随着深度的增加而减小。而在1 700 m~2 800 m的地层范围内,随着温度的不断升高,其对超临界CO2密度的影响力逐渐变大,超过了压力变化所带来的影响。因此,随着深度的增加,超临界CO2的密度逐渐增小,此时,压力对超临界CO2溶解度的影响大于温度的影响,所以CO2溶解度随着深度的增加而增大。
根据实验数据,对两个矿化度下的不同埋存深度CO2溶解度的变化进行了拟合,拟合方程如下:
矿化度8.25 g/L:
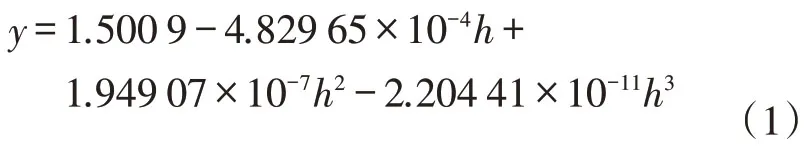
矿化度99 g/L:
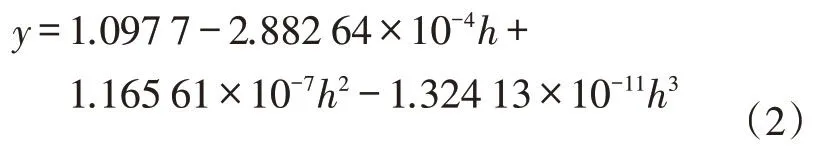
式中:y为CO2溶解度,mol/kg;h为埋存深度,m。
根据拟合方程,即可计算得到不同埋存深度下,在实验模拟的深部盐水层盐溶液中CO2的溶解度。根据该方程及现场勘测调查所得的埋存场地的面积以及埋存深度,即可进一步估算出埋存场地的CO2封存量。以鄂尔多斯盆地石千峰组为例,若经勘测调查埋存场地平面面积为A,埋存顶板深度为h1,底板深度为h2,则所能溶解封存的总CO2量为:
矿化度8.25 g/L:
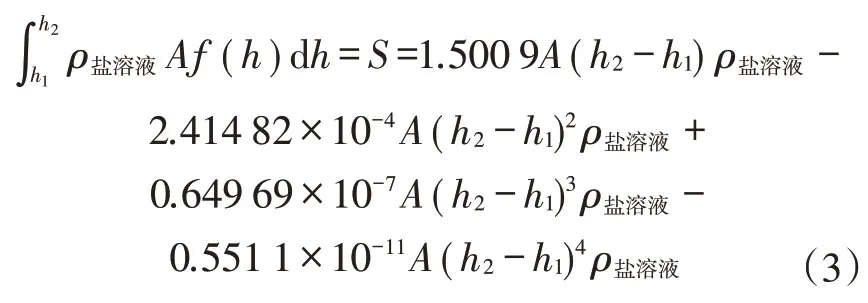
矿化度99 g/L:
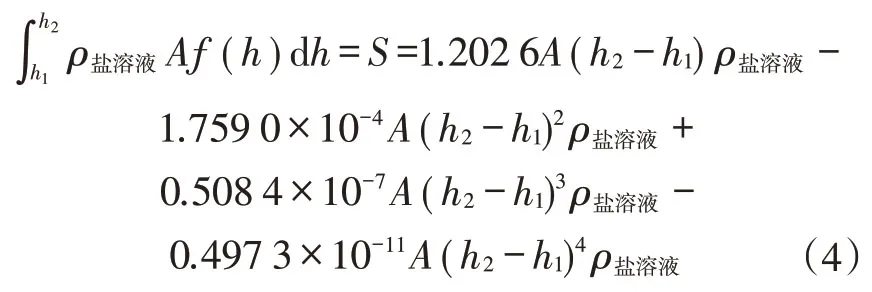
式中:A为封存场地面积,m2;S为CO2封存量,mol;ρ盐溶液为盐溶液密度,kg/m3。
根据上述所得计算模型,以地层以下800 m深度为起始埋深,分别对200 m、300 m、400 m 厚的地层CO2封存量进行了估算,结果见表1、表2。
从表1、表2 的计算结果可以看出,在相同盐水层厚度情况下,随着封存面积的扩大,深部盐水层的CO2封存量也逐渐增加,且封存量的增长幅度与封存面积的扩大量成一定比例关系。在相同封存面积情况下,CO2封存量与盐水层厚度也呈正相关,但是随着盐水层厚度的增加,CO2封存量的涨幅略有下降。
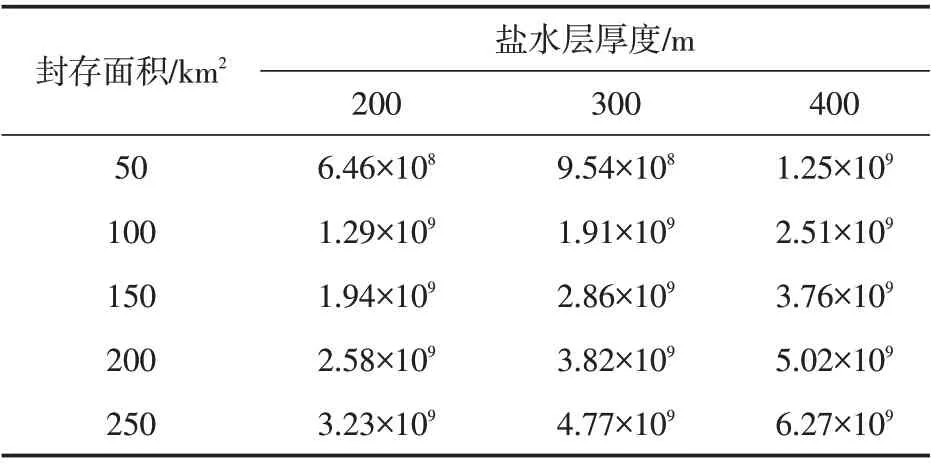
表1 不同厚度盐水层中CO2封存总量估算(8.25 g/L)Table 1 Estimation of total CO2 storage in saline layer with different thickness(8.25 g/L)
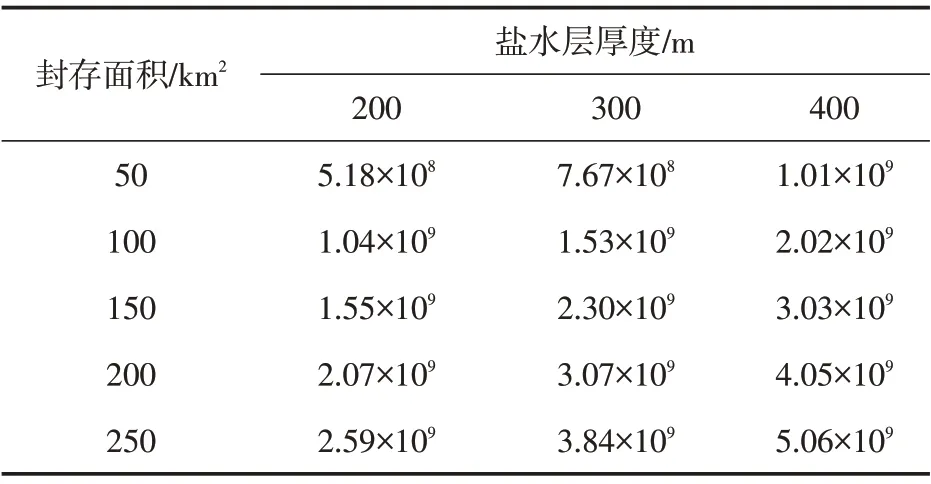
表2 不同厚度盐水层中CO2封存总量估算(99 g/L)Table 2 Estimation of total CO2 storage in saline layer with different thickness(99 g/L)
3 结论
以石英毛细管结合拉曼光谱技术为核心的实验装置测得了深部盐水层不同埋存深度条件下的模拟盐溶液中CO2溶解度,并对CO2封存总量进行了估算,主要结论如下:
1)随着埋存深度的递增,CO2溶解度呈先减小后增大的趋势,溶解度变化情况的拐点出现在1 700 m左右深度。
2)深部盐水层溶液矿化度越高,CO2溶解度越小。
3)根据对深部盐水层埋存深度与CO2溶解度的函数拟合,发现两者之间存在三次多项式非线性关系。
4)根据实验拟合所得埋存深度与CO2溶解度函数关系,利用积分法得到了不同矿化度深部盐水层CO2溶解封存总量估算模型,并进行了不同封存面积与盐水层厚度情况下的溶解封存总量估算。
