不同诊断标准下亚临床甲状腺功能减退症发病率及对妊娠结局的影响
2019-06-27刘成程巩振华
刘成程,巩振华,岳 欣
(淄博市妇幼保健院 检验科,山东 淄博255000)
目前妊娠期亚临床甲状腺功能减退的诊断仍存在争议。以2011年美国甲状腺学会(AmericanThyroid Association,ATA)提出的孕早期促甲状腺激素(TSH)>2.5 mIU/L,孕中晚期TSH>3.0 mIU/L为诊断标准[1],我国妊娠期亚临床甲状腺功能减退的患病率高达16.24%,这意味着我国1/3的妊娠妇女存在妊娠期亚临床甲状腺功能减退;而我国2012年制定的《妊娠和产后甲状腺疾病诊治指南》指出,应建立本地区特异性的孕期甲状腺激素正常参考区间,同时提出我国血清TSH值比其他国家偏高,采用我国的标准[2],亚临床甲状腺功能减退的患病率仅为2.41%;2017年美国甲状腺学会(AmericanThyroid Association,ATA)又将TSH>4.0 mIU/L作为新的亚甲减诊断标准[3]。为此,本研究采用不同的TSH诊断标准对妊娠期妇女进行筛查,旨在探讨不同TSH诊断标准对亚甲减发病率及不良妊娠结局的影响,从而指导临床上对妊娠期亚临床甲状腺功能减退进行准确诊断,协助妊娠期并发症的预测及治疗。
1 资料与方法
1.1 临床资料
采用前瞻性研究的方法,2016年1月至2016年8月在淄博市妇幼保健院产科首次产检建档的单胎健康孕妇2168例,追踪其整个孕期及产后1个月,其中失访13例,最终纳入本研究2155例,其中孕早期713例,孕中期710例,孕晚期732例,年龄18岁-42岁。妊娠周数根据末次月经计算并辅以孕早期B超检查确定。具体入选标准:(1)孕妇年龄在20-42岁; (2)无既往甲状腺、糖尿病、高血压疾病史,无其他严重疾病史及其他自身免疫性疾病史;(3)无服用影响甲状腺功能药物史;(4)无地方性甲状腺肿病区生活史;(5)触诊及B超检查未发现甲状腺疾病。
1.2 诊断标准
1.2.1国外旧标准组 2011年美国甲状腺协会(ATA)推荐的孕早期血清TSH水平>2.5 mIU/L、孕中晚期>3.0 mIU/L,血清游离甲状腺素(FT4)水平在妊娠期正常范围内为妊娠合并亚甲减。
1.2.2国外新标准组 2017年美国甲状腺协会(ATA)推荐的血清TSH水平>4.0 mIU/L,血清游离甲状腺素(FT4)水平在妊娠期正常范围内为妊娠合并亚甲减。
1.2.3国内标准组 按照2012年我国推荐标准,根据美国临床生化研究院(NACB)的相关方法,本研究建立了不同孕期特异性TSH和血清FT4参考值,即血清TSH水平0.22-5.360 mIU/L,以TSH水平>5.360 mIU/L,血清FT4水平正常为妊娠合并亚甲减。
1.2.4正常对照组 选择TSH水平<2.50 mIU/L,且甲状腺过氧化物酶抗体(TPO-Ab)检查结果阴性的264例健康孕妇作为对照组,TPO-Ab≥9 uIU/mL为结果阳性。
1.2.5妊娠不良结局的判定标准 流产、早产、围产期胎儿死亡、出生缺陷、妊娠相关性疾病及并发症。
1.3 实验试剂和仪器
实验仪器为美国Beckman Coulter全自动化学发光仪DXI 800,检测试剂使用Beckman Coulter有限公司提供的原装配套试剂。
1.4 试验方法
采集受检者晨起空腹静脉血3 ml,室温静止30 min,3 500 r/min离心5 min,分离血清;使用全自动化学发光仪进行游离甲状腺素(FT4)、促甲状腺激素(TSH)及甲状腺过氧化物酶抗体(TPO-Ab) 的水平检测。所有孕妇充分告知并签署知情同意书,填写问卷调查,记录孕妇基本身体状况、妊娠并发症及妊娠结局等。
1.5 统计学分析
统计学处理使用SPSS 19.0统计软件进行数据处理和统计分析,不同标准组间的发生率比较采用卡方检验,检验水准α=0.05,P<0.05为差异有统计学意义;不同妊娠期甲状腺激素水平的参考值范围采用百分位数计算方法,结果以中位数( M 值) 及双侧限值[P2.5,P97.5]表示。
2 结果
2.1 不同TSH诊断标准下各组妊娠合并亚甲减孕妇的发病率比较
以我国亚甲减标准诊断的国内标准组孕妇共52例,发生率为2.41%(52/2155);按2011年ATA亚甲减标准诊断的国外旧标准组孕妇共350例,发生率为16.24%(350/2155);按2017年ATA亚甲减标准诊断的国外新标准组孕妇共73例,发生率为3.39%(73/2155)。以国内标准组孕妇亚甲减发病率与国外旧标准组孕妇的亚甲减发并率比较,差异有统计学意义(χ2=243.63,P<0.01),与国外新标准组孕妇亚甲减发病率比较,差异无统计学意义(χ2=3.63,P>0.05),见表1。
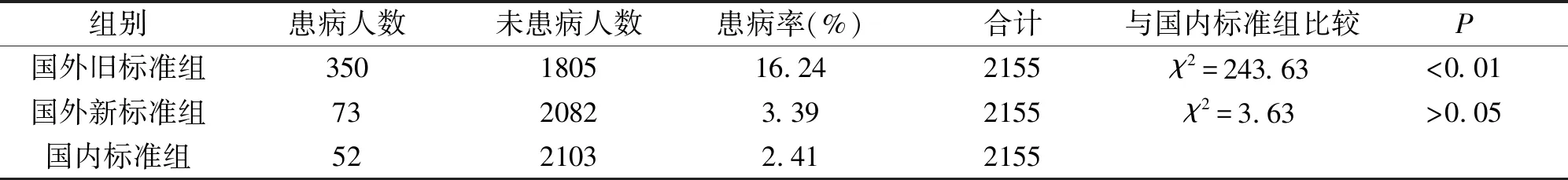
表1 国内标准组与国外新旧标准组孕期亚临床甲减发病率比较
2.2 各组孕妇不良妊娠结局发生率与正常对照组的比较
国内标准组孕妇、国外新标准组孕妇不良妊娠结局的发生率与对照组比较均有显著差异(P<0.01),见表2。
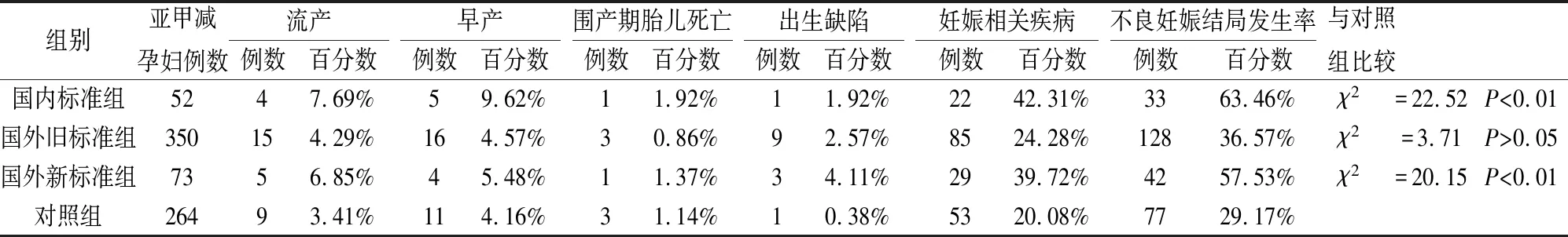
表2 各组亚甲减孕妇的不良妊娠结局与对照组的比较
3 讨论
妊娠期亚临床甲状腺功能减退症(SCH)是指孕妇血清TSH水平高于妊娠期特异的参考区间上限而FT4水平在妊娠特异的参考区间内。研究表明SCH在妊娠期妇女中患病率较高并随妊娠进展[4]逐渐影响甲状腺功能,妊娠使母体处于应激状态,如果机体不能适应这些生理变化,甲状腺激素的产生和代谢会发生改变,可发生甲状腺功能异常[5],所以,妊娠期TSH水平的参考区间不同于非妊娠妇女。在下丘脑-垂体轴调节正常情况下,TSH是反映甲状腺功能变化最敏感的指标,其有三个不同参考水平来诊断亚临床甲减的患病率——2011年美国甲状腺学会(ATA)诊断标准、2017年美国甲状腺学会(ATA)诊断标准、2012年国内《妊娠和产后甲状腺疾病诊治指南》诊断标准。目前孕期亚甲减诊断标准的确立和对不良妊娠结局的影响是争议的热点。
Zubair等[6]认为,家族性甲状腺疾病史、年龄及碘摄入量会影响这项指标。在本研究中的孕妇均选择碘摄入量正常人群,无既往甲状腺疾病史,且亚甲减各组孕妇与对照组孕妇在年龄、孕周方面均无差异。按照2011年ATA推荐的孕早期TSH水平参考区间<2.5 mIU/L,中晚期TSH水平<3.0 mIU/L为诊断标准,亚甲减发生率高达16.24%,2017年ATA推荐的TSH水平参考区间<4.0 mIU/L,亚甲减发生率为3.39%,而采用我国2012年标准,本研究孕妇亚甲减发生率为2.41%,与2017年ATA新颁布的诊断标准相符合。
妊娠期甲状腺功能减退对妊娠结局的不良影响已被证实,并较少有争议。已报道的妊娠不良结局包括:流产、早产、围产期胎儿死亡、出生缺陷、妊娠相关性疾病及并发症[7]。但目前关于亚甲减与妊娠不良结局相关性报道存在争议。近年来的临床研究显示,妊娠早中期的亚临床甲减与后代神经发育受损密切相关[8-10],高TSH 水平也是流产和早产的危险因素[11]。有研究表明,孕期亚甲减的妇女与甲状腺功能正常的妇女相比,前者的子代更易发生胎儿窘迫[12]。Wang 等[13]也发现,亚甲减孕妇的自然流产率明显高于甲状腺功能正常组孕妇。 Ashoor 等[14]研究表明,孕早期母体患亚甲减可导致自然流产和早产率上升,还可能引起胎儿脑发育损伤,造成子代不良神经心理发育[15]。所以有必要建立合适的诊断标准对孕妇进行甲状腺功能检测,并予以早期治疗。本研究将三个诊断标准组分别与正常对照组比较发现,国内标准组及国外新标准组的亚甲减人群有高风险不良妊娠结局,而国外旧标准组其不良妊娠发生率与正常对照组无明显差异,即国外新标准组、国内标准组其流产、早产、围产期胎儿死亡、出生缺陷、妊娠相关性疾病及并发症的发生率会有显著升高。这提示按照国外旧诊断标准来筛查孕期亚甲减,TSH水平切入点较低,若以孕早期2.5 mIU/L、中晚期3.0 mIU/L作为上限会导致70%-80%的过度诊断[16],其不良妊娠结局无明显影响,容易增加孕妇的经济负担和心理负担。
本研究进一步把国内标准组的不良妊娠发生率分别与国外新旧标准组比较,与国外旧标准组有统计学意义(P<0.01),与国外新标准组无统计学意义(P>0.05)。因此,当本地区没有条件建立适宜的参考区间时,可以使用2017年国际推荐的标准诊断治疗,对妊娠结局没有明显影响。
因此,在临床上应首先使用国内标准诊断亚甲减,推荐各地区制定自己实验室的妊娠期特异性参考区间,若无法达到要求,可采用国外新诊断标准,TSH以4.0 mIU/L为参考上限。这既符合2017年ATA推荐标准又符合我国指南,避免过度治疗和诊断,同时极大限度地减少相关不良妊娠结局的发生率。但这也可能样本量不够大,结果有所偏倚,有待于进一步研究。总之,本研究结果为孕期普遍开展血清TSH水平结果筛查提供了有力的依据,孕期TSH水平的有效控制对孕妇既安全又节省资源,有利于孕期管理及获得良好的妊娠结局。
