MnO2改性累托石/污泥生物炭复合材料的制备及其对Pb(II)和Cd(II)吸附特性研究
2019-06-24张隽晔周培疆
张隽晔,周培疆,管 鲲
(武汉大学资源与环境科学学院,湖北省生物质资源化学与环境生物技术重点实验室,湖北 武汉 430079)
生物炭是生物质在氧气限制条件下热解的副产物之一,由于其原料来源丰富、性能优良和环境友好等特点而被广泛应用于污水处理和污染土壤修复领域[1-4]。其中,污泥生物炭以污水处理过程中难以处置的副产物——污泥作为原料,可实现污泥的减量化、无害化和资源化。
尽管生物炭具有原料来源丰富和环境友好等优良的特性,但是相比于活性炭,生物炭的制备温度较低(300~700℃),其对污染物的吸附性能相对较差,因此对生物炭进行改性以提高其吸附性能将有利于其更广泛的应用。目前,生物炭-黏土复合材料被广泛运用于废水中污染物的去除和土壤修复领域[5-8],且在以往的研究中,也已成功制备出吸附性能优于污泥生物炭和累托石的累托石/污泥生物炭复合材料。在此基础上,为了进一步提高该复合材料的吸附特性,在其中加入功能材料是十分必要的。为此,本文在通过混合热解法制备的累托石/污泥生物炭复合材料的基础上,利用氧化还原反应制备得到MnO2改性的累托石/污泥生物炭复合材料,分析了MnO2改性的累托石/污泥生物炭复合材料对Pb(II)和Cd(II)的吸附特性以及吸附动力学和热力学特征,并初步探讨了其吸附机理,为该改性复合材料对重金属废水吸附的应用研究提供理论基础。
1 材料与方法
1.1 试验材料与试剂
试验所用的污泥来自于湖南岳麓污水处理厂,将其直接烘干,磨碎,过60目筛备用;累托石来自于湖北名流公司。试验所用试剂包括硝酸铅、氯化镉、硝酸、氢氧化钠、乙酸锰、高锰酸钾等,均为分析纯。
1.2 复合材料的制备
(1) 累托石/污泥生物炭复合材料的制备:首先将清洗干净的累托石2.4 g放入60 mL的去离子水中,超声分散30 min;然后将磨碎的污泥粉末0.8 g加入上述溶液中,搅拌2 h,抽滤,并将所得固体产物放于烘箱中60℃条件下干燥过夜;再将上述反应物置于管式炉中,在通氮气(N2)的条件下以5 ℃/min的升温速率升至400℃,并保持该温度2 h;最后将上述产物研磨后过60目筛,制备得到累托石/污泥生物炭复合材料。
(2) MnO2改性累托石/污泥生物炭复合材料的制备:首先将1.5 g累托石/污泥生物炭复合材料和0.316 g高锰酸钾在装有50 mL去离子水的烧杯中混合,超声分散30 min;然后逐滴滴入0.3 M乙酸锰溶液10 mL,待其发生下列反应:

(1)
最后,将上述装有反应物的烧杯置于80℃的水浴锅中保持30 min,抽滤,并将所得固体产物放于烘箱中80℃条件下干燥过夜,研磨后过60目筛,制备得到MnO2改性的累托石/污泥生物炭复合材料。
1.3 复合材料的表征
复合材料的比表面积以及相关的孔径分布利用BELSORP-Mini II比表面和孔隙分析仪测定,即以高纯液氮作为吸附质,在77K条件下测定复合材料的吸附曲线,并采用BET方法分析比表面积,采用BJH公式分析孔径分布;复合材料的晶体结构通过X射线粉末衍射仪(MiniFlex,Rigaku)测定;复合材料表面的有机官能团和电位分别通过红外光谱仪(FT-IR,Nicolet 5700)和Zeta电位仪(Nano-ZS series Model ZEN3600,Malvern,UK)测定。
1.4 Pb(II)和Cd(II)的吸附试验
重金属的吸附试验采用摇瓶法,将50 mg复合材料置于装有100 mL溶液的250 mL锥形瓶中,放于空气浴摇床,转速为200 r/min,并用注射器取2 mL的剩余溶液通过0.22 μm的滤膜。
吸附动力学试验是采用初始浓度分别为100 mg/L和25 mg/L的Pb(II)和Cd(II)溶液(25℃,pH值为5),研究由不同时间间隔(5~1 440 min)剩余溶液中Pb(II)和Cd(II)的浓度。
pH值影响因素试验是研究溶液的pH值为2~6(0.2 M稀硝酸和氢氧化钠溶液调节)时复合材料吸附容量的变化。
吸附等温线和热力学试验是采用初始浓度分别为50~700 mg/L和20~400 mg/L的Pb(II)和Cd(II)溶液(pH值为5),研究复合材料在15℃、25℃和35℃条件下对Pb(II)和Cd(II)的吸附容量。
复合材料对Pb(II)和Cd(II)的吸附容量(即吸附量)由下式计算:
(2)
式中:qe为达到吸附平衡时的吸附量(mg/g);c0、ce分别为初始和达到吸附平衡时溶液中Pb(II)或Cd(II)的浓度(mg/L);V为Pb(II)或Cd(II)溶液的体积(L);m为吸附剂的质量(g)。
2 结果与讨论
2.1 复合材料的表征
2.1.1 复合材料的比表面积和孔径分布
MnO2改性前后累托石/污泥生物炭复合材料的N2吸-脱附等温线和BJH孔径分布曲线见图1,其比表面积等微观结构特征见表1。

图1 MnO2改性前后累托石/污泥生物炭复合材料的 N2吸-脱附等温线和BJH孔径分布曲线Fig.1 BET N2 adsorption-desorption isotherms and the BJH pore size distribution of the pristine and the modified rectorite/sludge derived biochar composites
由图1可见:MnO2改性前后复合材料的N2吸-脱附等温线都为IV型等温线且存在H3型滞后环,说明该复合材料中存在介孔[9-10],且MnO2改性的复合材料对N2的吸附量远高于未改性的复合材料[见图1(a)]。此外,由表1也可以看出:MnO2改性后复合材料的比表面积比改性前更大;改性前和MnO2改性后的复合材料中都含有微介孔,且MnO2改性后的复合材料中所含的微孔和介孔的比例更大[见图1(b)]。

表1 MnO2改性前后累托石/污泥生物炭复合材料的微观结构特征
2.1.2 复合材料的傅里叶红外光谱分析
图2为MnO2改性前后累托石/污泥生物炭复合材料的傅里叶红外光谱(FTIR)谱图。

图2 MnO2改性前后累托石/污泥生物炭复合材料的 FTIR谱图Fig.2 FTIR spectra of the pristine and the modified rectorite/sludge derived biochar composites
由图2可见,MnO2改性前后复合材料的表面官能团的改变不大,且复合材料表面都含有丰富的含氧官能团,其中位于3 640 cm-1处的峰为有机物中—OH的伸缩振动[11-12],1 030 cm-1处的峰为C—O键的伸缩振动,544 cm-1和480 cm-1处的峰为复合物中无机铝盐的峰[13-14],但MnO2改性后的复合材料在该处的峰为无机硅铝盐的峰与Mn—O键(510 cm-1)处所出峰的叠加峰[15]。
2.1.3 复合材料的X射线衍射光谱分析
图3为MnO2改性前后累托石/污泥生物炭复合材料的X射线衍射光谱(XRD)谱图。

图3 MnO2改性前后累托石/污泥生物炭复合材料的 XRD谱图Fig.3 XRD spectra of the pristine and the modified rectorite/sludge derived biochar composites
由图3可见,改性前后复合材料中最明显的衍射峰为26°左右出现的石英(SiO2)衍射峰[16],同时也出现了累托石和赤铁矿(Fe2O3)的特征峰,但MnO2改性的复合材料中类似的特征峰的强度有所降低,这可能是由于MnO2负载在材料表面影响了其他晶相的峰强度,说明本试验所制备的负载在累托石/污泥生物炭复合材料表面的MnO2是无定形结构的,这与Liang等[15]的研究结果相一致。
2.2 复合材料对Pb(II)和Cd(II)的吸附特性分析
2.2.1 MnO2改性前后累托石污泥生物炭复合材料对Pb(II)和Cd(II)的吸附效果
图4为MnO2改性前后累托石/污泥生物炭复合材料对Pb(II)和Cd(II)吸附量的对比。

图4 MnO2改性前后累托石/污泥生物炭复合材料 对Pb(II)和Cd(II)吸附量的对比Fig.4 Comparison of the adsorption effects of the pristine and the modified rectorite/sludge derived biochar composites for Pb(II) and Cd(II)
由图4可见:MnO2改性的复合材料对Pb(II)和Cd(II)的吸附量分别为96.15 mg/g和27.7 mg/g,远高于未改性的复合材料对Pb(II)和Cd(II)的吸附量(分别为24.56 mg/g和9.9 mg/g);同时,MnO2改性前后复合材料对Pb(II)的吸附量均高于Cd(II),这是因为Pb(II)的水合离子半径较小,电荷密度较高,其发生离子交换的能力更强[17]。由此可见,MnO2改性的复合材料对重金属具有更好的的吸附性能。其原因一方面是由于MnO2具有较大的比表面积,且其本身具有良好的吸附性能;另一方面是由于累托石/污泥生物炭复合材料是良好的载体,MnO2颗粒可以较好地负载并分散在其表面,从而增强了材料的吸附性能[15,18]。
2.2.2 MnO2改性累托石/污泥生物炭复合材料对Pb(II)和Cd(II)的吸附动力学研究
为了研究MnO2改性的累托石/污泥生物炭复合材料与Pb(II)和Cd(II)之间的相互作用[19-21],本文采用伪一阶动力学模型、伪二阶动力学模型、颗粒内扩散作用模型和Elovich动力学模型对MnO2改性的累托石/污泥生物炭吸附材料对Pb(II)和Cd(II)的吸附动力学过程进行了拟合。其吸附动力学模型如下:
伪一阶动力学模型为
qt=qe×(1-e-k1t)
(3)
伪二阶动力学模型为
(4)
颗粒内扩散作用模型为
qt=kit0.5+C
(5)
Elovich动力学模型为
(6)

MnO2改性的累托石/污泥生物炭复合材料对Pb(II)、Cd(II)的吸附动力学拟合曲线和拟合参数分别见图5和表2。

重金属离子伪一阶动力学模型伪二阶动力学模型颗粒内扩散作用模型Elovich动力学模型q1,cal/(mg·g-1)k1/(min-1)R2q2,cal/(mg·g-1)k2/(g·min-1·mg-1)R2ki/(mg·g-1·min-0.5)C/(mg·g-1)R2αβR2Pb(II)0.129 477.260 00.849 782.220 00.002 170.929 91.685 245.300 00.538 6583.140 00.122 40.996 9Cd(II)0.122 523.210 00.896 324.700 00.006 830.955 80.485 413.720 00.483 7174.210 00.410 50.975 0
注:q1,cal为通过伪一阶动力学模型计算出的理论平衡吸附量;q2,cal为通过伪二阶动力学模型计算出的理论平衡吸附量。
由图5可见,MnO2改性的复合材料对Pb(II)和Cd(II)的吸附都是刚开始时吸附速率较快,之后吸附量缓慢增加。由表2可知,Elovich动力学模型的决定系数(R2)均高于其他的吸附动力学模型,表明Elovich动力学模型可以较好地反映MnO2改性的复合材料对Pb(II)和Cd(II)的吸附动力学过程。
Elovich动力学模型描述了一个双相反应的过程,即开始时吸附速率较快的反应过程和之后逐渐缓慢的反应过程,该模型常被用于推断受运输过程限制的反应机制,包括材料内部和表面扩散。由此说明,Pb(II)和Cd(II)在MnO2改性复合材料上的吸附过程是受材料内部孔扩散所限制的吸附过程[19]。
2.2.3 pH值对MnO2改性累托石/污泥生物炭复合材料吸附Pb(II)和Cd(II)的影响
图6为MnO2改性累托石/污泥生物炭复合材料对Pb(II)、Cd(II)的吸附量和Zeta电位随pH值的变化曲线。
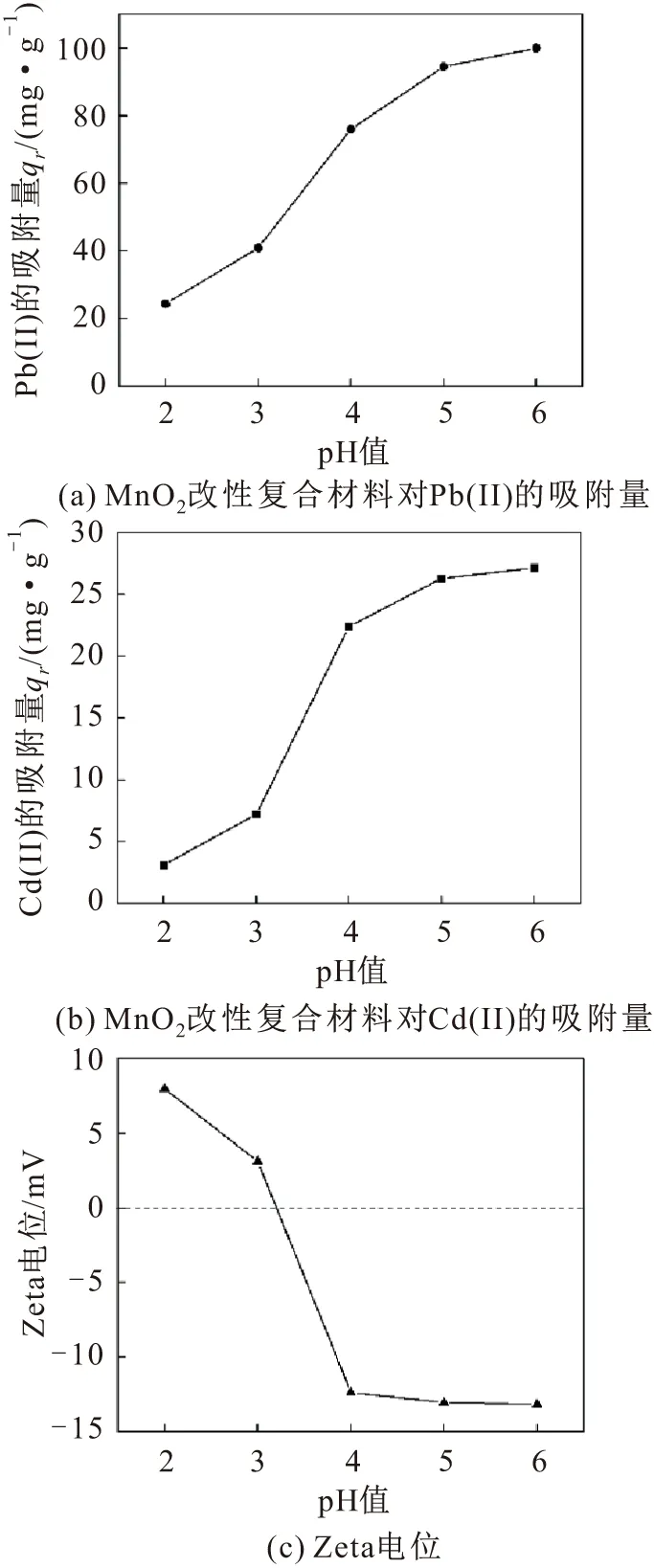
图6 MnO2改性累托石/污泥生物炭复合材料对 Pb(II)、Cd(II)的吸附量和Zeta电位随 pH值的变化曲线Fig.6 Effects of pH on Pb(II) and Cd(II) adsorption capacity and zeta potentials of the pristine and the modified rectorite/sludge derived biochar composites
由图6可见,MnO2改性复合材料对Pb(II)和Cd(II)的吸附过程受pH值的影响较大,pH值较低时该改性复合材料对Pb(II)和Cd(II)的吸附容量都相对较小,且吸附容量随着pH值的升高急剧上升并趋于平稳。这是因为:一方面,在pH值较低时,溶液中的H+较多,带正电的质子与带正电的重金属离子竞争材料表面的吸附位点,随着pH值的升高,羟基与氢离子反应发生去质子化作用,因此H+与重金属离子Pb(II)和Cd(II)的竞争作用减弱;另一方面,在较低pH值条件下,材料表面的Zeta电位为正值,且随着pH值的增加Zeta电位逐渐降低[见图6(c)],即材料表面发生去质子化作用,因此静电排斥作用随着pH值的增加而降低,其吸附容量也随之提高[17,22-23]。
2.2.4 MnO2改性累托石/污泥生物炭复合材料对Pb(II)和Cd(II)的吸附等温线拟合
MnO2改性累托石/污泥活性炭复合材料对Pb(II)和Cd(II)的吸附过程可分别采用Langmuir和Freundlich等温线方程进行拟合[14]。其等温线方程表达式如下:
Langmuir等温线方程为
(7)
Freundlioh等温线方程为
(8)
式中:qm为Langmuir吸附容量(mg/g);KL为Langmuir常数(L/mg);KF和n为Freundlich常数。
基于Langmuir等温线方程得出的分离常数RL可由下式计算得到:
(9)
式中:KL为Langmuir常数(L/mg)。
由RL值可以判定该吸附过程是否是热力学有利的。当RL>1时,表明该吸附过程不是热力学有利的;当RL=1时,表明该吸附过程为线性吸附过程;当0 MnO2改性累托石/污泥生物炭复合材料对Pb(II)、Cd(II)的吸附等温线拟合曲线和拟合参数见图7和表3。 图7 MnO2改性累托石/污泥生物炭复合材料对 Pb(II)和Cd(II)的吸附等温线拟合曲线Fig.7 Adsorption isotherms for Pb(II) and Cd(II) onto MnO2 modified rectorite/sludge derived biochar composites 由图7和表3可以看出:MnO2改性复合材料对Pb(II)、Cd(II)的吸附量在溶液浓度较低时随着Pb(II)和Cd(II)浓度的增加而增加,之后其吸附量的增加逐渐缓慢并趋于平衡;MnO2改性复合材料对Pb(II)和Cd(II)的吸附过程更符合Langmuir等温线方程,说明该吸附过程可能是单层吸附[14,24-25];基于Langmuir等温线方程计算得出的RL值在0~1之间,表明MnO2改性复合材料对Pb(II)和Cd(II)的吸附过程是热力学有利的[26]。 表3 MnO2改性累托石/污泥生物炭复合材料对Pb(II)和Cd(II)的吸附等温线拟合参数 2.2.5 MnO2改性累托石/污泥生物炭复合材料对Pb(II)和Cd(II)的吸附热力学研究 为了研究温度对MnO2改性累托石/污泥生物炭复合材料吸附Pb(II)和Cd(II)的影响,对该复合材料在288.15 K、298.15 K和308.15 K温度条件下对Pb(II)和Cd(II)的吸附量进行了拟合,其拟合结果见图7。 由图7可见,随着温度的升高MnO2改性复合材料对Pb(II)和Cd(II)的吸附量增加,说明该复合材料对Pb(II)和Cd(II)的吸附是一个吸热的过程。该吸附过程的热力学参数吉布斯自由能(ΔG)、焓(ΔH)和熵(ΔS)可由下式计算得到[14]: ΔG=-RTlnK (10) ΔG=ΔH-TΔS (11) 式中:R为通用气体常数[8.314 J/(mol·K)];T为开尔文温度(K);K为热力学平衡常数,该值可通过绘制lnKd对ce的曲线且将ce外推至零计算得到,其中Kd=qe/ce;ΔS和ΔH可由ΔG与T关系曲线的斜率和截距获得。 MnO2改性累托石/污泥生物炭复合材料对Pb(II)和Cd(II)的吸附热力学参数(ΔG、ΔH和ΔS)的计算结果,见表4。 表4 MnO2改性累托石/污泥生物炭复合材料对Pb(II)和Cd(II)的吸附热力学参数 由表4可知,ΔG为负值,说明MnO2改性复合材料对Pb(II)和Cd(II)的吸附过程是混乱度增加的过程,且随着温度的增加ΔG值降低,说明高温更有利于其吸附过程;ΔH和ΔS都为正值,也同时说明该吸附过程是吸热且混乱度增加的过程[24,27]。 本文通过制备MnO2改性的累托石/污泥生物炭复合材料,对改性前后的复合材料进行了表征,并研究了其对Pb(II)和Cd(II)的吸附特性,得出如下结论: (1) MnO2改性的累托石/污泥生物炭复合材料相比未改性的累托石/污泥生物炭复合材料具有更大的比表面积,且改性后复合材料的表面含有丰富的含氧官能团。 (2) Elovich动力学模型和Langmuir吸附等温线模型可以很好地拟合Pb(II)和Cd(II)在MnO2改性后的累托石/污泥生物炭复合材料上的吸附动力学和吸附等温线过程,说明该吸附过程受材料内部孔扩散控制,且为单层吸附。 (3) MnO2改性累托石/污泥生物炭复合材料对Pb(II)和Cd(II)的吸附热力学过程是自发的吸热过程,且混乱度增加。 (4) MnO2改性累托石/污泥生物炭复合材料对Pb(II)和Cd(II)的吸附过程受pH值的影响较大。 (5) MnO2改性累托石/污泥生物炭复合材料是一种性能优良的重金属吸附剂。

3 结 论
