老年腰椎融合术后早期下肢深静脉血栓形成的影响因素探究
2019-06-18刘明永刘佰易刘瑶瑶赵建华
殷 翔,刘明永,刘佰易,刘瑶瑶,刘 鹏,赵建华
深静脉血栓(deep venous thrombosis,DVT)是指血液在深静脉不正常凝结的病症,多发生于下肢,血栓易脱落成为栓子而形成肺栓塞,可发生在各类手术之后。腰椎融合术是治疗腰椎疾病的一项基本技术,通过手术使腰椎各椎体之间发生骨性融合,从而建立和维持腰椎稳定性[1]。腰椎融合术具有植骨融合率高、疗效确切、并发症少、安全可靠等优势,但腰椎融合术的手术时间相对较长,术后卧床时间亦相对延长,因此DVT形成的可能性增加[2]。而下肢DVT形成严重时可产生肢体感觉和运动功能障碍,严重影响术后康复甚至引起致命的肺梗死[3]。本研究通过对接受腰椎融合术患者术后早期(术后2周内)并发DVT的影响因素进行分析,探讨DVT形成的主要影响因素。
临床资料
1 一般资料
2015年7月—2018年6月陆军军医大学大坪医院脊柱外科行腰椎融合术治疗患者165例, 其中男性76例,女性89例;年龄55~78岁,平均64.0岁。病程2.9~20年,平均3.5年。其中胸腰段骨折19例,腰椎间盘突出症56例,腰椎滑脱症34例,腰椎管狭窄症51例,腰椎内固定翻修术5例。均于全身麻醉下手术,患者手术操作均由技术熟练的医师完成。本研究所有患者知情同意,自愿参与本研究。
2 纳入指标
DVT的诊断标准:术后出现下肢肿胀、疼痛、小腿后方和(或)大腿内侧有压痛,且经过双下肢的血管多普勒彩超检查有下列情况: 静脉管腔不能压闭;管腔内为低回声或无回声;脉冲多普勒显示无血流或频谱不随呼吸变化;血栓段静脉内完全无血流信号或者仅探及少量血流信号。术中相关指标:腰椎融合节段数;手术时间;是否输血。术后相关指标:术后卧床时间,一般术后2~4d取掉引流管后即可嘱患者在使用辅助支具适当下床活动行康复锻炼,并行双下肢多普勒彩超检查;是否使用低分子肝素抗凝;术后均预防性予以物理抗凝(穿戴抗血栓压力带和下肢气压泵)治疗[4]。
3 方法
术后发生DVT患者21例作为DVT组,其余144例患者作为非DVT组,对两组患者年龄、性别、体重指数(BMI)、高血压和糖尿病的患病情况、血清甘油三酯(TG)水平、凝血四项、D-二聚体、是否使用抗凝药、是否输血、手术情况(手术时间、融合节段数)、卧床时间等一般资料进行回顾性分析,以探究DVT形成的独立危险因素。出现临床症状的DVT患者请相关科室进行会诊并予对症处理,无临床症状的下肢DVT患者则给予1次/d皮下注射4 000U的低分子肝素钠(意大利 ALFA)治疗。
4 检验指标
早晨空腹采集静脉血2.0mL,将其缓慢沿着试管壁注入有0.2mL枸橼酸钠的真空抗凝管中,马上颠倒且充分混合均匀,以3 000r/min离心12min,分离血浆[5],采用凝固法检测血浆凝血酶原时间(PT)、凝血活酶时间(TT)、部分凝血活酶时间(APTT)、纤维蛋白原(FIB)和免疫比浊法检测D-二聚体水平。全部检测步骤和仪器均严格按照仪器(沃芬公司ACLTOP 700)及试剂使用标准说明规范操作。 术前血液检查指标:(1)术前凝血四项包括PT(正常范围8.8~12.8s)、TT(正常范围12~18s)、APPT(正常范围28~42s)、FIB(正常范围2.0~4.4g/L),将PT、APPT、TT缩短和FIB升高视为阳性;(2)D-二聚体>0.5mg/L为阳性[6]。
5 统计学分析
应用SPSS 18.0统计软件进行分析,各项指标分别进行单因素χ2分析得出其中相关性因素,再进行Logistic多因素回归分析,得出独立危险因素。P<0.05为差异有统计学意义。
结 果
1 腰椎融合术患者一般资料分析
165例腰椎融合患者中术后有下肢DVT形成21例,发生率为12.7%,其中男性9例,女性12例。经多普勒超声检查结果显示,下肢DVT形成患者血栓均位于小腿远端,主要症状为小腿后方疼痛及肿胀,体征有局部压痛及Homans征阳性。见表1。
2 腰椎融合术后并发下肢DVT的单因素分析
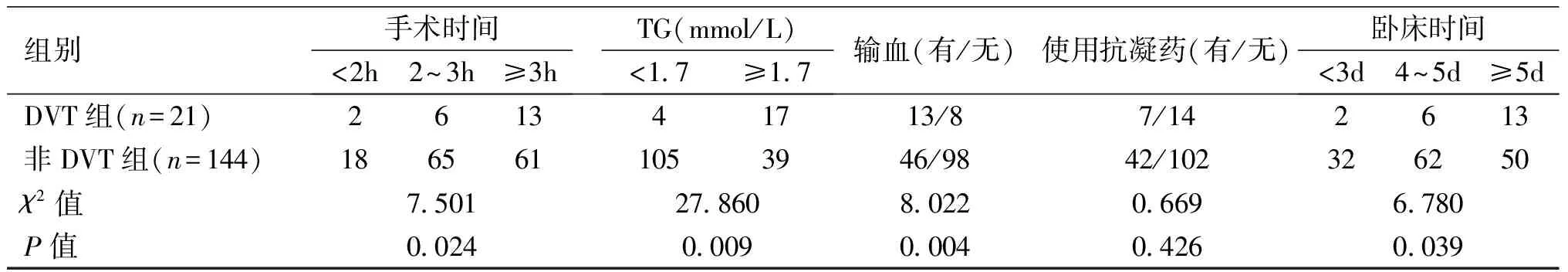
所有患者分组后各指标经χ2检验显示:年龄、BMI、手术时间、TG水平、是否输血和卧床时间等指标差异有统计学意义(P<0.05),DVT组明显高于非DVT组,即这些指标和腰椎融合术后发生下肢DVT有相关性。见表1、2。
3 腰椎融合术后患者并发DVT的多因素Logistic回归分析
将单因素分析对腰椎融合术后患者下肢DVT形成有显著性影响的因素,引入多因素Logistic回归模型,并进行多因素分析。结果显示:年龄≥70 岁、BMI≥24kg/m2、输血、卧床时间≥5d、TG水平增高是老年腰椎融合术患者术后并发下肢深静脉血栓的危险因素。其中各因素的 RR值分别为6.013、4.531、3.250、3.068、4.734。见表3。
4 两组患者凝血情况比较
比较分析术后两组患者间血小板、PT和D-二聚体所测值,差异无统计学意义(P>0.05,表4)。
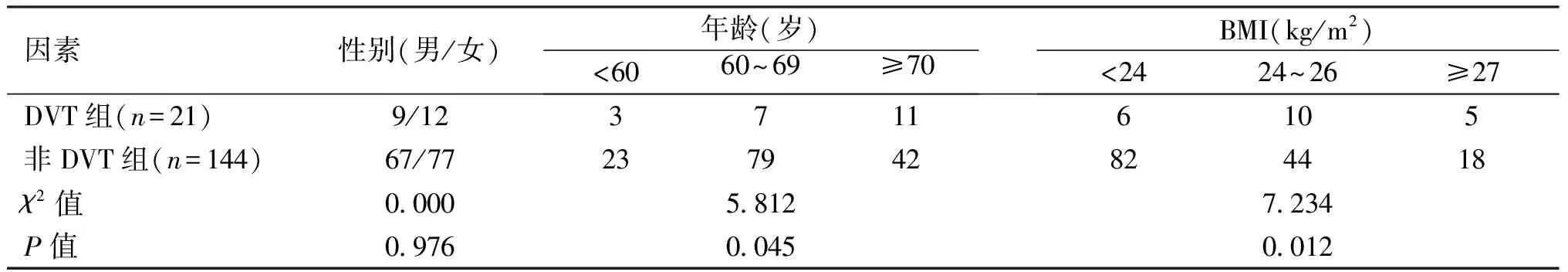
表1 腰椎融合术患者一般资料分析(n)

表2 腰椎融合术后并发DVT单因素分析(n)
组别手术时间<2h2^3h≥3hTG(mmol/L)<1.7≥1.7输血(有/无)使用抗凝药(有/无)卧床时间<3d4^5d≥5dDVT组(n=21)261341713/87/142613非DVT组(n=144)1865611053946/9842/102326250χ2值7.50127.8608.0220.6696.780P值0.0240.0090.0040.4260.039
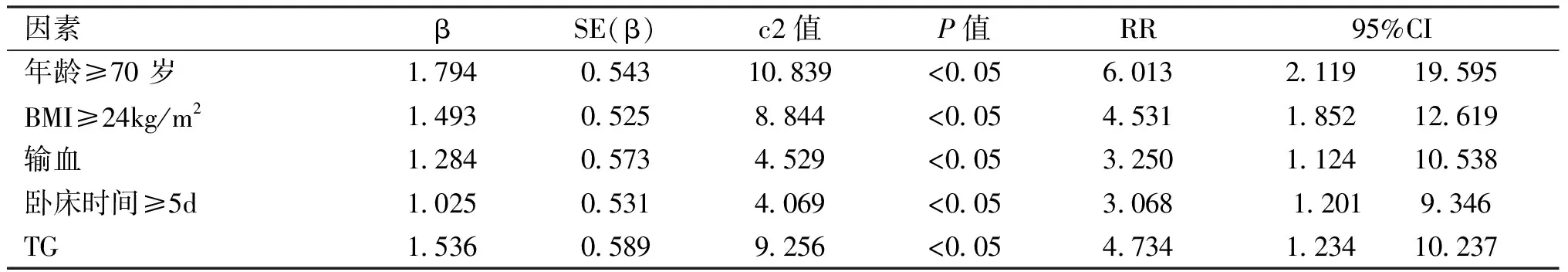
表3 腰椎融合术后患者并发DVT多因素Logistic回归分析

表4 两组患者凝血情况比较
讨 论
静脉血流缓慢、管壁内膜损伤、血液高凝状态是公认的血栓形成的三大病理基础。研究发现,下肢DVT好发于高龄、体弱、严重骨折患者,是骨科术后常见并发症之一,严重影响患者预后[7]。脊柱外科手术患者以老年人居多,且其体质较中青年患者有一定差距,合并其他较多病症,当患者术后长期卧床,易造成下肢血流缓慢,从而血流淤滞,导致下肢血管腔阻塞[8],进而增加下肢DVT的发生率。腰椎融合术存在麻醉和手术本身带来的创伤和失血,术中长时间的俯卧位对下腔静脉、髂静脉和股静脉的压迫促使DVT形成[9]。腰椎融合术后发生下肢DVT的诊断主要是结合临床症状、体征及多普勒彩超等常规必要的检查手段[10]。如患者出现下肢肿胀或疼痛,或不敢主动做踝关节背伸运动,应警惕DVT发生的可能。美国胸科医师学会建议的择期脊柱手术的DVT预防指南为:(1)除早期、持续活动外,对没有其他危险因素的患者无需常规采取血栓预防措施;(2)对于有其他危险因素的患者可采取下列任意一种预防措施:术后单用低剂量普通肝素,单用低分子量肝素,或单用物理方法如下肢充气加压装置等,对有多个危险因素的患者推荐联合使用肝素和物理方法[11]。
本研究纳入的165例行腰椎融合术后患者发生DVT 21例,发生率为12.7%。经多普勒超声检查结果显示,所有下肢DVT形成患者血栓均位于小腿远端。主要症状为小腿后方疼痛及肿胀,有局部压痛及Homans征阳性。所有患者分组后各指标经χ2检验显示:年龄、BMI、手术时间、TG水平、是否输血和卧床时间等指标差异有统计学意义,DVT组的发病率明显高于非DVT组,即这些指标和腰椎融合术后发生下肢DVT有相关性。利用多因素Logistic回归模型进行多因素分析显示:年龄≥70岁、BMI≥24kg/m2、输血、卧床时间≥5d、TG水平增高是老年腰椎融合术患者术后并发下肢DVT的危险因素。而术后两组患者间血小板、PT和D-二聚体所测值进行比较分析差异无统计学意义。
综上所述,高龄、BMI≥24kg/m2、输血、卧床时间≥5d、TG水平增高等是老年腰椎融合术患者术后并发下肢DVT的高危因素,在临床工作中应充分重视具有高危因素的患者,及时给予针对性治疗,以防血栓脱落进入肺或大脑等重要脏器。首先进行常规抗凝治疗,并且术后要严密观察双下肢情况,及早进行康复锻炼并机械性预防DVT[12]。在采取术后康复指导、术后穿戴抗血栓压力带、下肢气压治疗泵等物理预防措施的基础上,围手术期充分的镇痛治疗也是减少下肢DVT形成的关键[13]。同时在物理预防措施得当的前提下,物理预防与抗凝药物预防下肢DVT的疗效相当[14]。必要时行多普勒超声检查有无DVT发生,并依据检查结果给予及时治疗,以避免发生严重的不良后果。
