铁络合物混合吸收体系脱除氮氧化物的研究
2019-06-13朱怀志吴依玲聂兆广胡艳芳王翠苹
朱怀志,吴依玲,聂兆广,胡艳芳,王翠苹
(1.青岛大学 化学化工学院,山东 青岛 266071;2.青岛大学 机电工程学院,山东 青岛 266071)
氮氧化物是大气中的主要污染物之一,NOx的排放主要来自化石燃料的燃烧过程,大气中的NOx不仅是是PM2.5的前体物,还会形成光化学烟雾,有强烈的刺激作用,对人类健康产生威胁[1-3]。要减少氮氧化物排放对我们的生态环境和日常生活所产生的影响,不仅要按照国家标准严格控制污染物的排放,而且还要对排放出来的污染物进行行之有效的吸收处理,此时,脱硝工作就显得尤为重要。利用NO和络合剂之间的络合反应脱除NOx的方法称为络合吸收法[4]。由于某些金属离子与其配体构成的络合剂对NO具有良好的捕集吸收作用,避免了酸碱吸收法对NO2/NO气体比例有要求的弊端,有较广泛的适用范围,是湿法脱硝技术研究的热点之一[5-6]。常用的NO络合剂多为亚铁螯合剂和钴螯合剂,如FeSO4、Fe(II)-EDTA、Fe(II)-EDTA-Na2SO3、钴胺和乙二胺合钴([Co(en)3]2+)等[7-8]。
本文以EDTA二钠为配体,铁络合物为研究对象,在原有的基础上加入柠檬酸钠,通过改变配体比例对模拟烟气中氮氧化物的脱除进行了研究,考察了不同因素(络合剂,pH,温度,液气比(L/G))对脱硝效率的影响。铁氨基羧酸类络合物以FeII(L)表示,铁巯基类配体以FeII(RS)2表示,其中EDTA二钠和柠檬酸盐都属于氨基羧酸类配体,它们吸收NO的反应如下:
NO从气相到液相:
NO(g)→NO(aq)
络合剂吸收NO:
FeII(L)(aq)+NO(aq)→FeII(L)NO(aq)
1 实验部分
1.1 仪器与试剂
1.1.1 主要试剂
N2(99.9%),NO(99.9%),硫酸亚铁铵((NH4)2Fe(SO4)2·6H2O),柠檬酸钠(Na3C6H5O7·2H2O),乙二胺四乙酸二钠(C10H14N2Na2O8·2H2O),pH值(3~10)由2mol/L的NaOH和1mol/L的H2SO4溶液进行调节,溶液体积为500mL,以上试剂均为分析纯。温度由恒温水浴进行调节。
1.1.2 主要仪器
紫外可见分光光度计,减压阀,转子流量计,便携式pH检测器,恒温鼓风干燥箱,空压机,烟气分析仪,数显恒温水浴锅,可调直流稳压电源(0~30V),电子天平,电动水泵(12V)。
1.2 试验方法
首先连接好实验装置,在连接完成后检查各装置和各管路的气密性。开启烟气分析仪,待各项指标正常后开始实验。依次打开N2钢瓶、NO钢瓶以及空气压缩机,调节转子流量计使各个气体均以一定的比例通入缓冲罐内,实时监控模拟烟气中各气体的浓度并进行必要的调节。待烟气分析仪的数据趋于稳定以后开始记录数据。配置一定浓度的铁络合吸收溶液,打开水泵,使溶液从塔顶进入并开始雾化喷淋,同时每隔30s记录模拟烟气中NO的含量来监测吸收效率,实验装置如图1所示。
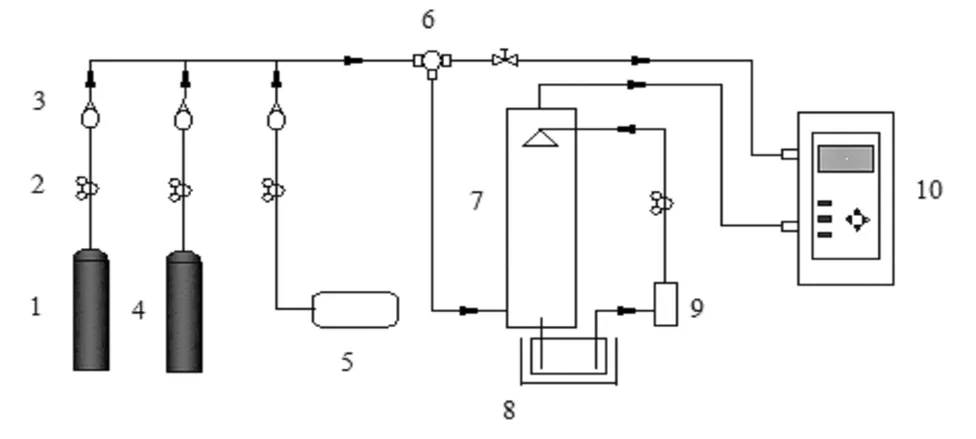
注:1-N2钢瓶;2-减压阀;3-转子流量计;
反应中出口模拟烟气的浓度由烟气分析仪实时监测,根据出口烟气的浓度变化来反映模拟烟气的脱除效率。其脱除效率可以表示如下:
γNO=(φ0-φ)/φ0
γNO:NO的脱除效率,%;
φ0:进口模拟烟气中NO的含量;
φ:出口模拟烟气中NO的含量。
2 结果与讨论
2.1 络合剂对脱硝效率的影响
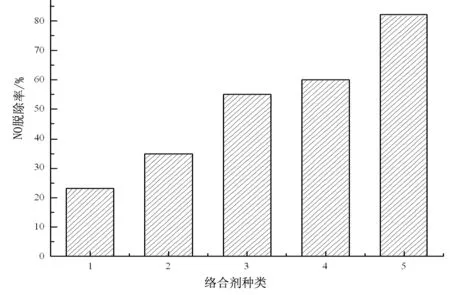
图2 络合剂对脱硝效率的影响,络合剂浓度0.05mol/L,pH值=6,T=30℃,L/G=10
由于不同络合物对氮氧化物的吸收能力不同,因此有必要研究络合物种类对脱硝的影响。铁络合物由于效果显著,也成为研究的热点。采用相同浓度不同配体(EDTA二钠和柠檬酸钠)的铁络合物进行实验,由图2可知在5种铁络合物(1和2分别代表EDTA二钠和柠檬酸钠,3-5代表EDTA二钠和柠檬酸钠的混合物)的实验中,EDTA二钠和柠檬酸钠单独为配体时的效果不如混合吸收剂的效果好。比例在1∶1∶1时效果突出,这是因为柠檬酸钠比EDTA二钠的抗氧化性要强,采用混合吸收吸收体系,用柠檬酸钠代替部分的EDTA二钠,在保证较高效率的前提下,不仅减少了经济成本,还提高了环境效益。在此基础上增加EDTA二钠或柠檬酸钠的量对实验基本上没有明显变化。由此可见硫酸亚铁铵,EDTA二钠和柠檬酸钠最佳配比为1∶1∶1,接下来的实验均采用这一配比。
2.2 pH值对脱硝效率的影响
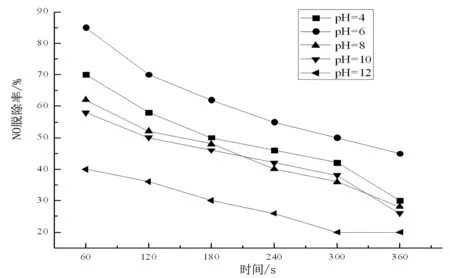
图3 pH值对脱硝效率的影响,混合吸收剂的浓度为0.05mol/L,T=45℃,L/G=10
由图3可以发现,在不同pH值条件下,混合吸收液对NO的脱除效率是不同的。当pH值=6时,脱除效率达到最大,此后随着pH值的升高,一氧化氮脱除效率逐渐降低,这说明强酸和强碱条件下对吸收不利。这是因为在强酸性条件下会发生(1)即溶液中的H+会把Fe(II)催化氧化成Fe(Ⅲ),而NO的脱除率主要取决于溶液中Fe(Ⅱ)的浓度。在碱性条件下会发生(2),溶液中游离的Fe(II)易于和OH-结合生成(FeOH)2沉淀,不利于NO的脱除。由此可见混合吸收液的最佳pH应该保持在弱酸性。
2NO+2FeII(L)+2H+→N2O+2FeⅢ(L)+H2O
(1)
Fe2++2OH-→Fe(OH)2↓
(2)
2.3 温度对脱硝效率的影响

图4 温度对脱硝效率的影响,混合吸收剂的浓度为0.05mol/L,pH=6,L/G=10
在图4可以看到温度变化之初温度由15℃到45℃,脱硝效率随之增大,温度由45℃到75℃脱硝效率反而降低,由Arrhenius equation可知,升高温度会加快吸收反应速率,温度升高会使物质内部能量升高,分子运动加剧,进而使反应速率的提升有利于反应的进行即氮氧化物的吸收,但由于吸收氮氧化物包括多个反应步骤和过程,且吸收NO的反应为放热反应,当温度过高时会对反应产生不利的影响。加之温度过高会降低NO在水中的溶解度。因此综上所述,络合脱硝的温度在45℃为宜。
2.4 液气比对脱硝效率的影响

图5 液气比对脱硝效率的影响,混合吸收剂的浓度为0.05mol/L,pH值=6,T=45℃
由图5可知随着液气比的增大,脱硝效率逐渐上升,但当液气比达到10以后,脱硝效率基本趋于稳定。这是因为由于液体的喷淋量增加,会提高吸收剂的喷淋密度,使得填料表面更加湿润,有效气液接触面积增大,有助于促进气液接触反应。但当液气比继续增大时,液气比的增加并不是提高脱除效率的决定性因素,出于对运行成本以及经济性的考虑,最佳液气比为10。
3 结论
湿法脱硝与其他方法相比,有诸多优势,与以往单一铁络合物脱硝相比铁络合物混合吸收体系对氮氧化物的去除有较好的效果,柠檬酸钠的加入不仅提高了脱除效率还减少了经济成本。此外,脱硝效率还受温度,pH值,液气比的影响,在最佳操作条件:混合络合物浓度为0.05 mol/L,温度为45℃,液气比为10,pH值为6,脱硝效率高达85%。
