PPY@Fe3O4的制备及其磁共振成像和光热性能
2019-06-10金磊
金磊
摘 要: 通过合理转化残余铁(Fe)在聚吡咯(PPY)纳米粒子原位生产了磁性四氧化三铁(Fe3O4)晶体,从而合成PPY@Fe3O4纳米粒子.得到的PPY@Fe3O4纳米粒子具有突出的横向弛豫时间(T2)加权磁共振成像(MRI)效果和良好的光热性能,在肿瘤的诊断和治疗中具有良好的应用前景.
关键词: PPY@Fe3O4纳米粒子; 光热性能; 横向弛豫时间(T2)加权; 磁共振成像(MRI)
中图分类号: O 614.24文献标志码: A文章编号: 1000-5137(2019)02-0178-06
0 引 言
利用光热转换试剂将激光的光能转换为热能,从而达到高温杀死细胞的目的.光热治疗技术所使用的近红外激光的波长范围为700~1400 nm,对生物组织的穿透能力强,光衰减弱[1].光热治疗技术研究较多的纳米光热材料主要包括4种:① 贵金属光热材料,包括金和钯[2];② 碳基光热材料,包括碳纳米管和石墨烯;③ 半导体光热材料,这类材料的种类较为丰富,且制备成本低[3];④ 有机化合物光热材料,主要包括普鲁士蓝(PB)和吲哚菁绿纳米粒子等[4].近来,近红外吸收有机物质作为肿瘤光热治疗材料也逐渐受到关注[5].聚吡咯(PPY)纳米粒子[6]表现出高的光热性质和良好的光稳定性.本研究所制得的PPY@Fe3O4纳米粒子作为多功能纳米复合光热材料,可以集诊断和治疗为一体.
1 实验部分
1.1 实验试剂
各实验试剂的质量分数为:吡咯(98%),六水合氯化铁(III)(97%),聚乙烯醇(PVA,相对分子质量为9000~10000,水解度为80%)和氢氧化铵(28.0%~30.0%),使用的所有化学品无需进一步纯化.
1.2 实验仪器
JEOL JEM-2100透射电子显微镜(TEM);DU-730紫外可见分光光度计;VISTAMPXICP Varian电感耦合等离子体原子发射光谱仪(ICP-AES);NM120-Analyst核磁共振成像(MRI)分析仪(上海纽迈公司);808 nm激光器(上海兴隆光电科技有限公司);SZCL-2温控磁力搅拌器.
1.3 PPY@Fe3O4纳米粒子合成
将吡咯单体加入到含有Fe3+离子和PVA-Fe3+络合物的PVA水溶液中.通过Fe3+离子诱导吡咯的氧化聚合,形成的PPY粒子被PVA包覆,PVA用作封端剂以控制粒子尺寸以及使粒子高度亲水.同时,Fe2+离子、未反应的Fe3+离子与PPY纳米粒子表面上的PVA形成络合物,得到PPY@Fe3O4纳米粒子[7].
1.3.1 PPY纳米粒子的制备
0.373 g的FeCl3加入到10 mL的质量分数为7.5%的PVA中(相对分子质量为9000~10000),搅拌混合物1 h.然后,向其中滴加69.2 μL的吡咯,在3 ℃下进行氧化聚合,在相同温度下加热4 h.产生的深绿色PPY纳米粒子溶液直接用于下一步骤合成PPY@Fe3O4纳米粒子.
1.3.2 PPY@Fe3O4納米粒子制备
取2.5 mL上述步骤得到的PPY纳米粒子溶液,用15 mL去离子水和2 mL乙醇稀释,混合物在搅拌下加热至70 ℃.30 min后,注入另外1 mL质量分数为1.0%的氨水溶液,并将混合物在70 ℃下再保持30 min.然后,通过11000 r/min离心20 min分离产物,用水洗涤2次,并分散在水中.水溶液分散的PPY@Fe3O4纳米粒子储存在玻璃瓶中,然后用于MRI和光热性能研究.
1.4 溶液MRI实验
配置不同浓度的PPY@Fe3O4纳米粒子,分散在水中,通过电感耦合等离子体光谱仪(ICP)确定样品中Fe的含量.0.5 T磁场条件下,进行横向弛豫时间(T2)加权成像,并测试其纵向弛豫时间(T1).T2加权成像参数为:中心频率为539465.45 Hz,重复时间为8000 ms,谱宽为100 kHz.T2由硬脉冲CPMG(Call-Purcell-Meiboom-Gill)序列测得.得到T2后,以样品的横向弛豫时间的倒数(1/T2)为纵坐标,物质的量浓度为横坐标,拟合得横向弛豫率(r2).
1.5 溶液光热实验
用去离子水配置4个不同浓度的PPY@Fe3O4纳米粒子溶液,分别取2 mL样品置于宽度为0.5 cm,体积为2 mL的石英比色皿中,然后在808 nm激光器照射下(激光密度为 0.3 W·cm-2),光照20 min,每隔1 s检测一次实时温度,检测完后用温度变化值ΔT做纵坐标,时间t为横坐标拟合作图,得到不同物质的量浓度的纳米粒子溶液在20 min内的升高温度曲线.
2 结果与讨论
2.1 PPY@Fe3O4纳米粒子合成与物理表征
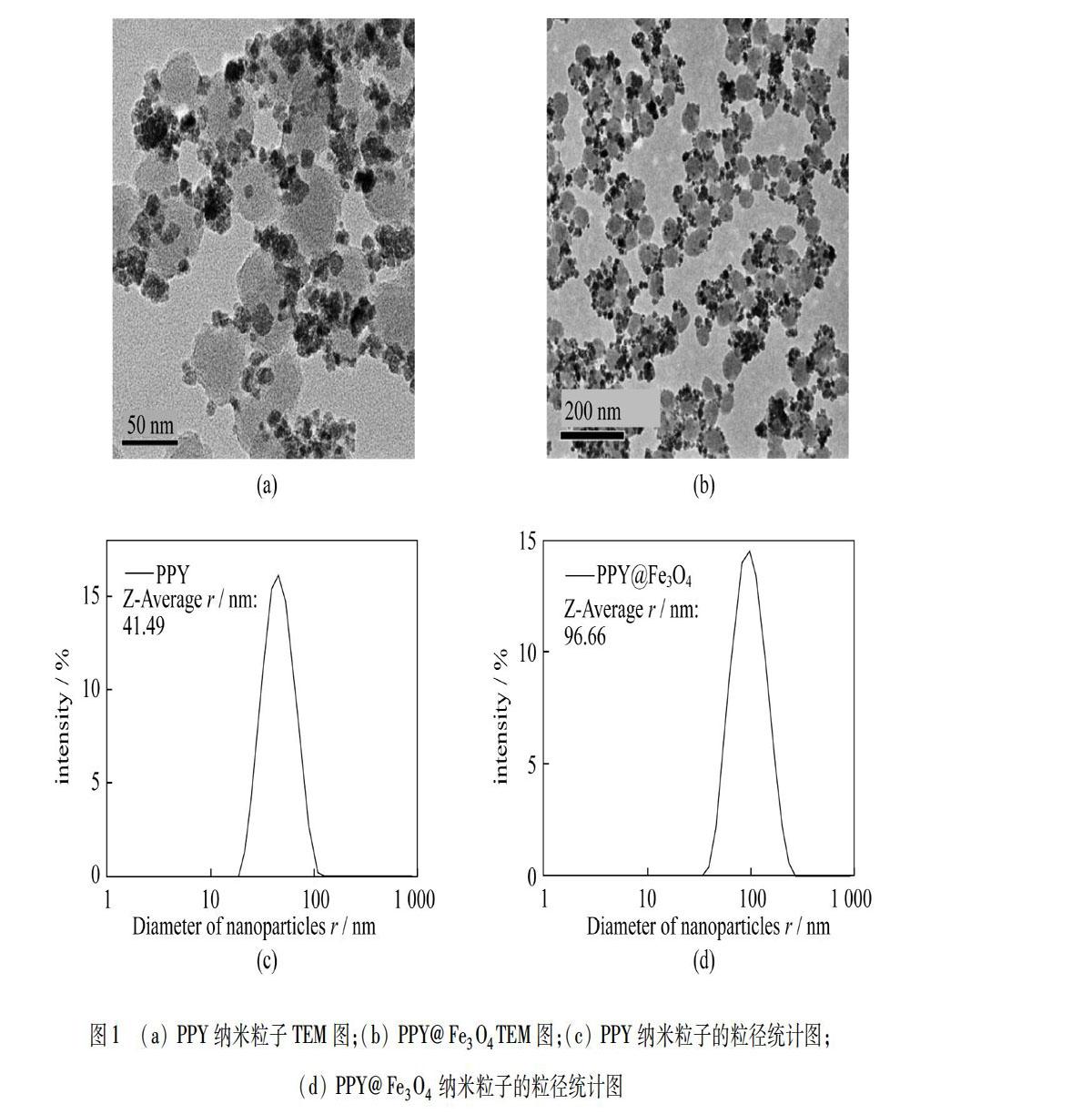
根据TEM图像可知,所制备的PPY纳米粒子尺寸非常均匀(直径为50 nm),如图1(a)所示.在70 ℃恒温将氨溶液加入系统中沉淀Fe3+和Fe2+离子,生成的Fe3O4晶体分散在PPY纳米粒子上.通过TEM图清楚地验证了Fe3O4与PPY的成功结合,如图1(b)所示,每个PPY纳米粒子结合几个Fe3O4晶体,总体粒子直径增加到100 nm,这与紫外吸收分析一致,如图1(c),(d)所示.
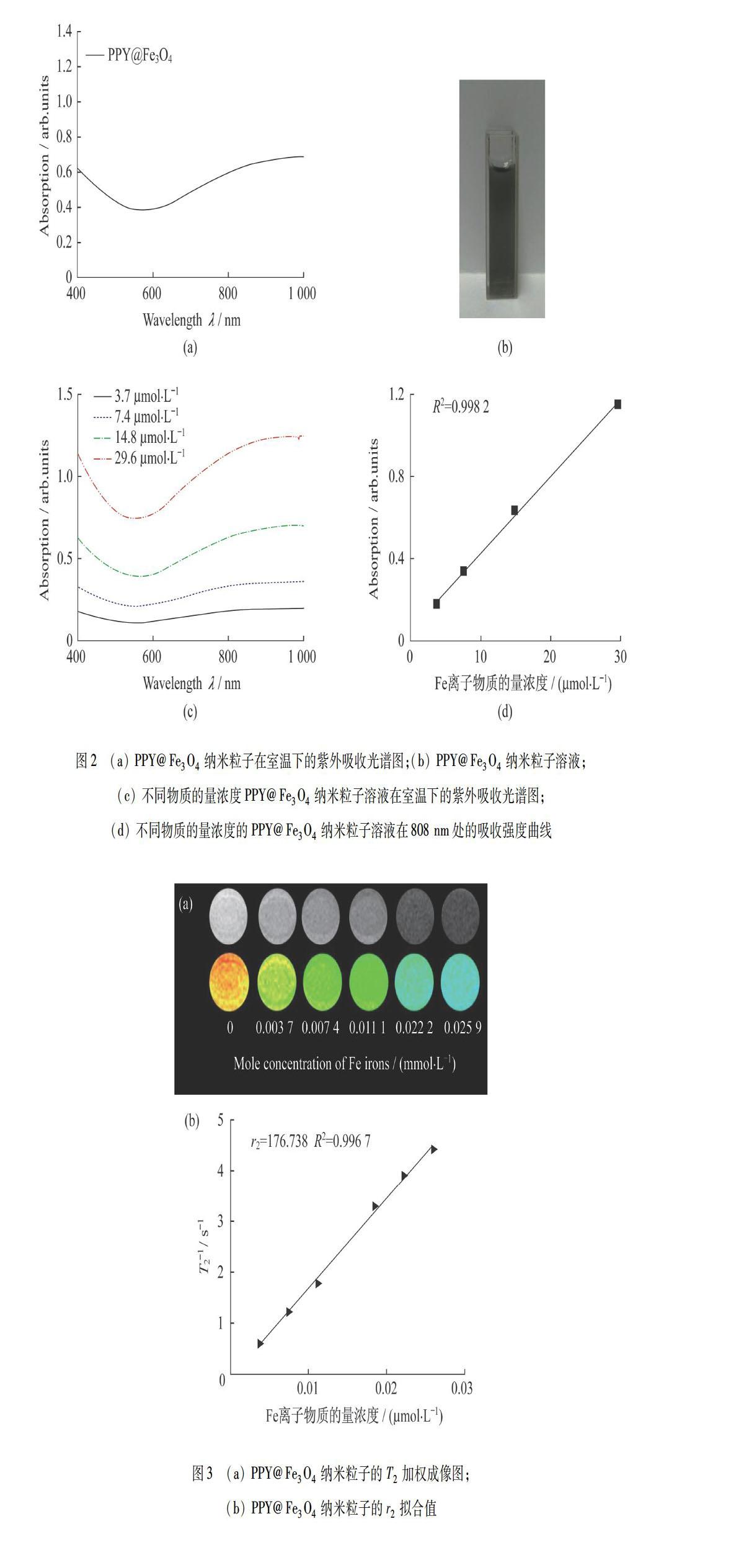
通过紫外近红外吸收光谱分析,PPY@Fe3O4纳米粒子的最大吸收峰在900~1000 nm处,如图2(c)所示.PPY在水中通过使用PVA作为封端剂,具有更高的分散能力,PPY@Fe3O4纳米粒子也容易分散在水中,并且获得的悬浮液非常稳定,几乎没有粒子聚集,如图2(b)所示.其次,分别取Fe离子的物质的量浓度为3.7,7.4,14.8,29.6 μmol·L-1的PPY@Fe3O4纳米粒子溶液,测其紫外近红外吸收[图2(c)],发现在808 nm处的吸收强度随着粒子浓度增加而线性增加,如图2(d)所示,这进一步证实了PPY@Fe3O4纳米粒子在水中的良好分散性.
2.2 核磁成像
对PPY@Fe3O4纳米粒子进行了MRI的研究.在0.5 T下检测水溶液的T2加权成像和T2值.随着物质的量浓度的增大,成像也越来越暗,如图3(a)所示,且呈现明显的成像梯度,适合于T2加权成像;r2值[8]为176.738 L·mmol-1·S-1,如图3(b)所示.PPY@Fe3O4纳米粒子具有较大的r2值,适合用作T2造影剂.
2.3 光热性质
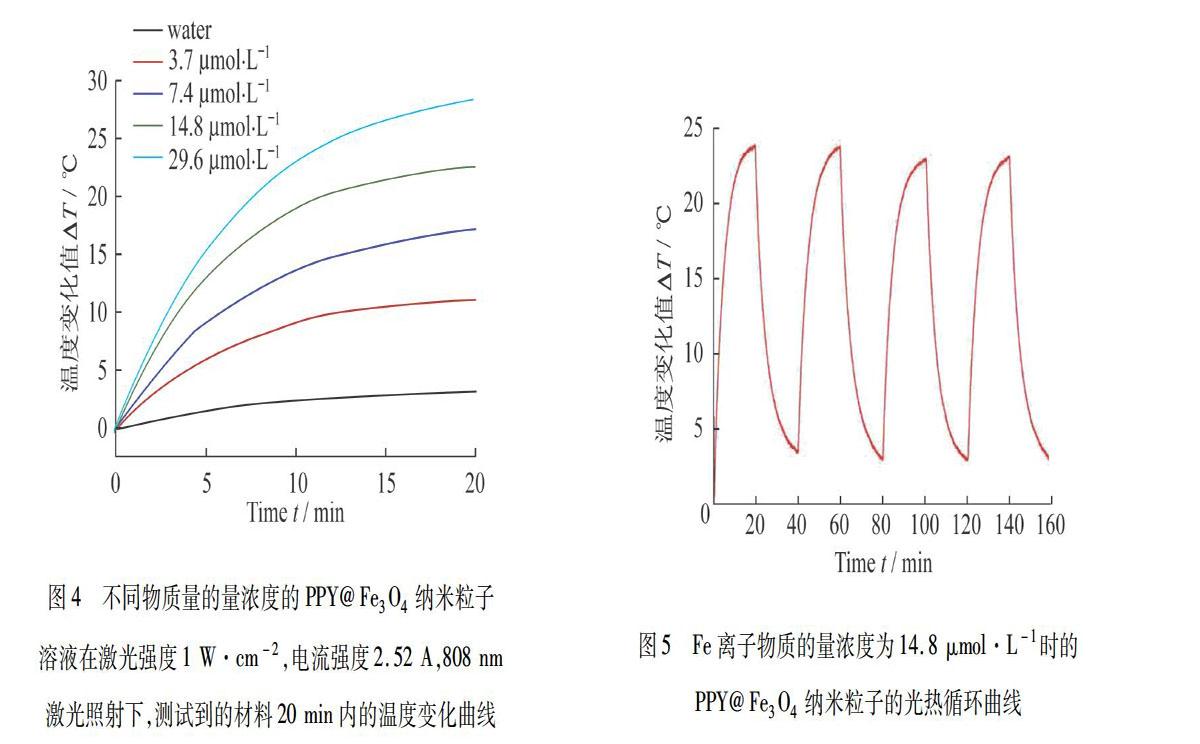
为检测PPY@Fe3O4纳米粒子是否是理想的光热升温试剂,用808 nm激光器在较小激光密度(1 W·cm-2)条件下,照射材料20 min,观测其温度变化(图4).由图4所示,当PPY@Fe3O4纳米粒子溶液的物质的量浓度分别为3.7,7.4,14.8,29.6 μmol·L-1时,纳米粒子依次上升11.2,17.1,19.4,22.7 ℃,同样条件下水温升高3.2 ℃.可以看出:随着纳米粒子浓度增加,温度也逐渐升高,但是升高的趋势逐渐减小;同一物质的量浓度的纳米粒子,光照开始阶段升温速度很快,随着光照时间的延长,升温的速度减慢.以上两个现象的原因在于:实验环境是室温,随着样品温度的升高,样品向周围环境释放热量的趋势变大.
光热循环曲线(图5):取Fe离子物质的量浓度为14.8 μmol·L-1的PPY@Fe3O4纳米材料进行了4个升温—降温的循环之后,测试到溶液在每一个循环中温度都可以升高23.8 ℃,即最大温差值均为20.4 ℃左右,温差没有明显的变化,在一定程度上说明了PPY@Fe3O4纳米粒子的光热稳定性良好,纳米粒子并没有受到高温的破坏,以及具有良好的光热效果.所以,该材料用于光热治疗具有一定的优势.
3 结果与展望
Fe离子可用作制备PPY纳米粒子的氧化剂,大量的Fe3+和Fe2+保留在所获得的PPY纳米粒子中.这些残留的Fe离子会作为前体,在预合成PPY纳米粒子的表面上原位生产Fe3O4晶体.实验表明PPY@Fe3O4纳米粒子是一种形貌均一、分散性好、水溶性好、有突出的MRI效果,且具有良好的光熱效果、光热稳定性的材料,在肿瘤诊疗方面具有很大的应用潜力.
参考文献:
[1] 王仡桐.多功能纳米材料用于骨肿瘤的光热治疗 [D].上海:华东师范大学,2018.
WANG Y T.Multifunctional nanoparticles for photothermal therapy of bone tumors [D].Shanghai:East China Normal University,2018.
[2] 宋国胜.纳米半导体光热转换材料的合成及在光热治疗和化疗上的应用探索 [D].上海:东华大学,2014.
SONG G S.Synthesis of semiconductor photothermal nanomaterials for photothermal and chemotherapy [D].Shanghai:Donghua University,2014.
[3] 苑晓贞.Fe3O4基光热复合材料的制备及性能研究 [D].青岛:青岛科技大学,2015.
YUAN X Z.Preparation and performance of Fe3O4 based photo-thermal composites [D].Qingdao:Qingdao University of Science and Technology,2015.
[4] 宋雪娇,刘庄.有机纳米材料在肿瘤光热治疗中的应用 [J].化学通报,2015,78 (4):292-298.
SONG X J,LIU Z.Organic nanomaterials for photothermal therapy of cancer [J].Chemistry Bulletin,2015,78(4):292-298.
[5] 杨涛.复合诊疗纳米粒用于多模态成像和光热治疗的研究 [D].苏州:苏州大学,2015.
YANG T.Theranostic nanocomposites for multimodal imaging and photothermal tumor ablation [D].Suzhou:Soochow University,2015.
[6] LIU M H,HAN M F.Synthesis of nanopolypyrrole [J].Chinese Journal of Synthetic Chemistry,2008,16(5):583-585.
[7] XIE J,LIU G,EDEN H S,et al.Surface-engineered magnetic nanoparticle platforms for cancer imaging and therapy [J].Accounts of Chemical Research,2011,44(10):883-892.
[8] 乔乐,李勇,周丽霞.不同浓度FeCl3·6H2O,CuSO4·5H2O和MnCl2·4H2O溶液核磁共振横向弛豫时间研究 [J].物理实验,2013,33(8):37-39.
QIAO L,LI Y,ZHOU L X.Transverse relaxation time of nuclear magnetic resonance of FeCl3·6H2O,CuSO4·5H2O and MnCl2·4H2O solutions [J].Physics Experimentation,2013,33(8):37-39.
(责任编辑:郁 慧)
