多功能纳米基因载体的制备与分析
2019-06-10刘诗音
刘诗音


摘要:本文通过反向微乳聚合等化学方法,成功制备出一种集磁性、荧光于一体的SiO2纳米粒子,并以多聚赖氨酸(PLL)对其表面进行修饰,修饰后的纳米粒子能够有效地与DNA结合和分离,并保护DNA免受DNaseI的降解。该纳米基因载体能够介导外源DNA转化至植物细胞当中,为纳米基因载体在转基因植物的研究中及应用打下了基础。
关键词:纳米粒子;基因载体;转基因植物
中图分类号:R944.9 文献标识码: A DOI编号: 10.14025/j.cnki.jlny.2019.12.022
纳米技术指制造出0.1~100nm量度的物质材料,直接操纵原子、分子、原子團或分子团,探究原子或分子的运动特性和规律[1-3]。生物纳米技术是生物技术和纳米技术的融合技术,是有关生命科学和纳米技术的新方法、新技术[4-6]。纳米技术在生物技术中的应用目前主要包括以下方面:基因载体[7-11];纳米尺度上的单细胞活体实时检测[12-17];药物的靶向和定向释放细胞[18-24]、DNA的分离等[25-27]。
本文拟构建一种新型的多功能纳米基因载体,即集荧光、磁性于一体的二氧化硅纳米基因载体。将荧光量子点和磁性纳米微粒同时集成到尺寸可控的硅纳米粒子中,并在纳米粒子表面修饰多聚赖氨酸(Polylysine,PLL)。荧光量子点被包埋在纳米载体内部,便于实时、稳定、高效检测。引入磁性功能,可在外磁场的作用下,提高外源基因进入细胞的效率,这将为纳米基因载体在植物转基因中的研究与应用提供崭新的途径。
1 实验方法
1.1荧光磁性SiO2纳米粒子(Fluorescence-magnetismsilicananopaticles,FMSNPs)的制备
取100ml三口瓶,加入25ml环己烷,4ml正己醇,5ml TritonX-100,0.25ml正硅酸乙酯,0.25ml Fe3O4,剧烈搅拌30min后形成反胶束。水浴加热25℃,机械搅拌,加入CdTe溶液0.25ml,氨水0.075ml,避光反应24h。反应结束后,取反应液体滴加丙酮破乳,静止沉淀,有乳白色微粒生成。8000rpm,10min,弃上清,收集沉淀。沉淀用乙醇洗涤3次,100℃真空干燥,室温贮存备用。通过扫描电镜检测荧光磁性SiO2纳米粒子的尺寸分布。
1.2 荧光磁性SiO2纳米粒子的表面修饰
PBS磷酸缓冲液的配制,按比例称取磷酸氢二钠与磷酸二氢钠,配制成pH=7.4的0.2mol/ml溶液,取2.5ml,稀释20倍至50ml。
取1mg荧光磁性SiO2粒子(FMSNPs)溶于1ml PBS,再加入0.05ml(1mg/ml)多聚赖氨酸(PLL),室温震荡1h,用Zata电位仪检测纳米粒子是否成功被PLL修饰。
1.3修饰PLL的荧光磁性SiO2纳米粒子与DNA的结合
纳米粒子与质粒DNA按照50∶1,30∶1,10∶1,5∶1,
2∶1,1∶1的比例将PLL-NPS与质粒DNA混合,同样将无纳米粒子的PBS与DNA按照上述比例充分混合均匀,室温放置0.5h,进行琼脂糖凝胶电泳检测。
1.4 PLL修饰的荧光磁性SiO2纳米粒子与DNA的分离
配制0.9%NaCl pH值为7.4 PBS溶液,按1∶1的比例(各5ul)与NPS-PLL-DNA结合物混合,37℃放置2h。
1.5 荧光磁性SiO2纳米粒子对DNA的保护作用
将DNAaseI按1U∶10ul的比例加入NPS-PLL-DNA结合物溶液中,37℃放置2h。
1%琼脂糖凝胶电泳检测PLL修饰的荧光磁性SiO2纳米粒子与DNA的结合和分离。
2 结果与分析
2.1荧光磁性SiO2粒子的尺寸
电镜分析:荧光磁性SiO2的粒子电镜图见图1,尺寸:50~80nm。
性状:白色粉末,溶液成乳白色,340nm紫外灯照射下成粉红色。
2.2 荧光磁性SiO2纳米粒子的表面修饰的结果与分析
zeta电位仪检测,未经修饰的荧光磁性SiO2纳米粒子的电位值-3.6mV,经PLL修饰后的荧光磁性SiO2纳米粒子的电位值为12.4mV,说明PLL已经成功地修饰到荧光磁性SiO2纳米粒子表面上,并具有较强的正电性。
2.3修饰PLL的荧光磁性SiO2纳米粒子与DNA结合分析
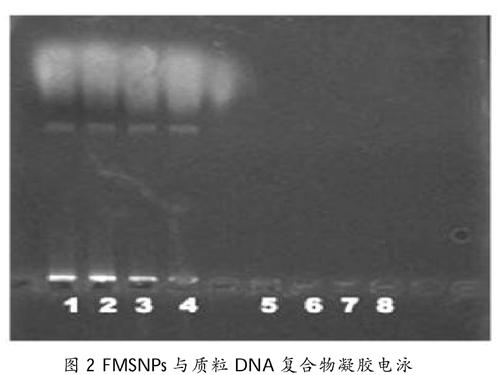
FMSNPs与质粒DNA按50∶1,30∶1,10∶1,5∶1,2∶1,1∶1的比例进行混合,FMSNPs与质粒DNA结合状况见图2,1~4号孔道代表空白对照,即不含FMSNPs,5~8号FMSNPs与质粒DNA混合的样本。从电泳图上可以清晰地看到FMSNPs与质粒DNA混合的样本均没有DNA条带。当质粒DNA结合到NPS-PLL上时,在电泳过程中,因为NPS-PLL粒径很大,无法在胶板上移动,被滞留在胶空内,说明质粒DNA已经结合到NPS-PLL上。
2.4 修饰PLL的荧光磁性SiO2纳米粒子与DNA的分离分析
PLL修饰的荧光磁性SiO2纳米粒子与DNA的分离:0.9%NaCl pH=7.4 PBS溶液可将NPS-PLL-DNA结合物上的质粒DNA洗脱下来,从照片可以看出,第7~11的试样在260nm紫外光出现DNA条带,说明质粒DNA已经从NPS-PLL-DNA结合物上洗脱下来,如图3。
2.5修饰PLL的荧光磁性SiO2纳米粒子对DNA的保护实验的结果与分析
修饰PLL的荧光磁性SiO2纳米粒子对DNA的保护:DNaseI可将质粒DNA酶切,切除下來的DNA可在胶板上泳动并在260nm紫外光出现DNA条带。从照片上可以看到2~6孔的试样并没有出现DNA条带,说明质粒DNA没有被DNAaseI酶切,所以说NPS-PLL对DNA有保护作用。
3 结语
本文通过微乳聚合等化学方法成功制备了一种集荧光、磁性于一体的PLL SiO2纳米粒子,并以PLL对其进行表面修饰,修饰后的纳米粒子能够成功地与DNA结合和分离,并保护DNA免受DNaseI的降解作用,同时,该纳米基因载体能够介导外源DNA转化植物细胞中,这为纳米基因载体在植物转基因中的进一步应用打下了基础。
参考文献
[1]Yanson A I,Bollinger G R,Brom H E.Formation and manipulation wire of single gold atoms.Nature,1998,395(6700):783-785.
[2]Fishlock T W,Oral A,Egdell R G,et al.Manipulation of atoms acat room temperature.Nature,2000,404(6779):743-745.
[3]Pascal A,Franklin A H,Eric W,et al.Halogen bonds in biologi Proc.Natl.Acad.Sci.USA,2004,101(48):16789-16794.
[4]Merkle R C.Biotechnology as a route to nanotechnology.Trends.
[5]Catherine Z.Cell nanotechnology:The tiny toolkit.Nature,2010-12.
[6]Mehmet S,Candan T,Alex K Y J,et al.Molecular biomimetics:nathrough biology.Nat.Materials,2003,2(9):577-585.
[7]Divis S S.Biomedical application of nanotechnology-implicat targeting and gene theraphy.Trends in biotech.,1997,15(6):217-2.
[8]Roy K,Mao H Q,Huang S K,et al.Oral gene felivery with nanoparticles generates immunologic protection in a murine moallergy.Nature Med.,1999,5(4):387-391.
[9]Indrajit R,Tymish Y O,Dhruba J B,et al.Optical tracking modified silica nanoparticles as DNA carriers:A nonviral,approach for gene delivery.Proc.Natl.Acad.Sci.USA,2005,102.
[10]肖苏尧,刘选明,童春义,等.多聚赖氨酸淀粉纳米颗粒基因载体用.中国科学B辑,2004,34(6):473-477.
[11]刘俊,刘选明,肖苏尧,等.基于超声波下淀粉纳米颗粒作载体[J].高等学校化学学报,2005,(04).
[12]Lewin M,Carlesso N,Tung C H,et al.Tat peptide-derivat nanoparticles allow in vivo tracking and recovery of progenit Biotech.,2000,18(4):410-414.
[13]Zhao X J,Hilliard L R,Mechery S J,et al.From the Cover:A rapisingle bacterial cell quantitation using bioconjugated nanoparticl Acad.Sci.USA,2004,101(42):15027-15032.
[14]Chan W C,Nie S M.Quantum dot bioconjugates for ultrasensitive detection.Science,1998,281(25):2016-2018.
[15]Medintz I L,Konnert J H,Clapp A R,et al.A fluorescence restransfer-derived structure of a quantum dot-protein bioconjugate Proc.Natl.Acad.Sci.USA,2004,101(26):9612-9617.
[16]James J S,Adam D L,Viswanadham G,et al.Homogeneousunamplified genomic DNA sequences based on colorimetric snanoparticle probes.Nat.biotech.,2002,22(7):883-887.
[17]Gao X H,Cui Y Y,Levenson R M,et al.In vivo cancer targetin with semiconductor quantum dots.Nat.Biotech.,2004,22(8):969.
[18]Tsapis N,Bennett D,Jackson B,et al.Trojan particles:Large pornanoparticles for drug delivery.Proc.Natl.Acad.Sci.USA,12001-12005.
[19]David A L,David M L,Robert L.Timline:moving smaller in dand delivery.Nat.Rev.Drug Discov.,2002,1(1):77-84.
[20]Yin W K,Feng S S.Effects of particle size and surface coatiuptake of polymeric nanoparticles for oral delivery of antiBiomaterials,2005,26(15):2713-2722.
[21]Müller R H,Mider K,Gohla S.Solid Lipid Nanoparticles(SLN)drug delivery-a review of the state of the art.Eur.J.Pharm.Bio50(1):161-177.
[22]Hreczuk-Hirst D,Chicco D,German L,et al.Dextrins as potentdrug targeting:tailored rates of dextrin degradation by introductigroups.Int.J.Pharm.,2001,230(1-2):57-66.
[23]Maillard S,Ameller T,Gauduchon J,et al.Innovative nanosystems improve the anti-tumor activity in vitro and anti-estrogens in human breast cancer and multiple myelom Biochem.Mol.Biol.,2005,94(1-3):111-121.
[24]Chilkoti A,Dreher M R,Meyer D E.Design of thermallrecombinant polypeptide carriers for targeted drug delivery.AdvRev.,2002,54(8):1093-1111.
[25]Sonti S V,Bose A.Cell separation using protein-A-coated magnet J.Colliod.Interface.Sci.,1995,170(01):575-585.
[26]Hawkins T.M13 single-strand purification using a biotinylat streptavidin coated beads.DNA sequ.,1992,3(02):65-69.
[27]Mari T,Masanori U,Noritada K,et al.Nanospheres for DNA sep Nat.Biotech.,2004,22(3):337-340.
