雷珠单抗联合玻璃体切割术治疗DR合并新生血管性青光眼
2019-06-10李家臣黄亚琳
姜 辉,李家臣,黄亚琳
0引言
糖尿病视网膜病变(diabetic retinopathy,DR)是糖尿病患者较为常见的并发症,是糖尿病血糖控制不佳,视网膜血管出现病变,也是导致患者最终失明的主要原因[1]。糖尿病视网膜病变病理表现为视网膜新生血管大量形成,发展越严重会导致患者新生毛细血管破裂,血液直接进入玻璃体腔,导致玻璃体出现积血,纤维增殖膜出现收缩,使视网膜被牵拉脱离[2-3]。目前临床上对于DR的常规治疗方案是采用药物、手术等干预,但单一治疗方案临床效果均欠佳,不能完全抑制疾病发展[4]。玻璃体切割术是眼科常用的治疗DR的手术方案,可有效去除玻璃体内积血,改善视网膜牵拉受力作用,利于患者视网膜复位,恢复视力[5]。但该手术方案,只能解除积血问题,并不能从源头改善新生血管形成。新生血管性青光眼(neovascular glaucoma,NVG)是一种病因复杂,对视功能和眼球结构破坏严重的继发性青光眼,常规的抗青光眼药物和手术治疗效果均不佳[5]。雷珠单抗是一种可抑制新生视网膜血管的药物,对DR有一定临床意义[6]。本试验就以我院眼科收治的198例糖尿病视网膜病变合并新生血管性青光眼患者的临床资料进行回顾性研究,探究其临床疗效。具体分析如下。

组别眼数手术时间(min)新生血管出血次数(次)电凝次数(次)观察组103103.41±10.820.59±0.180.67±0.28对照组95121.30±11.211.35±0.221.63±0.31t11.42426.68922.894P<0.001<0.001<0.001
注:观察组:术前注射雷珠单抗联合玻璃体切割术治疗;对照组:单纯采用玻璃体切割术治疗。
1对象和方法
1.1对象选取2016-01/2018-02我院眼科收治的198例糖尿病视网膜病变合并新生血管性青光眼患者作为研究对象。根据患者治疗方案不同分为观察组(103例103眼)和对照组(95例95眼),观察组患者采用术前注射雷珠单抗联合玻璃体切割术治疗,对照组单纯采用玻璃体切割术治疗。观察组:男53例,女50例;年龄50~76(平均56.7±6.4)岁;糖尿病病史5~16(平均10.9±2.8)a;青光眼分期:Ⅰ期58例,Ⅱ期45例。对照组:男46例,女49例;年龄51~78(平均57.3±6.6)岁;糖尿病病史6~15(平均11.2±2.6)a;青光眼分期:Ⅰ期52例,Ⅱ期43例。两组患者年龄、性别、糖尿病病史、青光眼分期等一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究已通过我院医学伦理委员会批准通过。
1.1.1纳入标准(1)患者均符合第八版《内科学》[7]糖尿病视网膜病变合并新生血管性青光眼的诊断标准;(2)糖尿病视网膜病变处于Ⅳ~Ⅴ期;(3)青光眼分期处于Ⅰ~Ⅱ期;NVG分期[6]:Ⅰ期(青光眼前期):虹膜或前房角红变,但不危及滤过功能,眼压正常;Ⅱ期(开角型青光眼期):前房角无关闭,但新生血管形成并伸入小梁网,房水外流受阻,眼压升高;Ⅲ期(闭角型青光眼期)新生血管收缩,前房角粘连,关闭,眼压急剧升高;(4)患者为双眼发病,取病变较重眼入组研究,如双眼程度一致,统一取右眼为研究对象;(5)患者或家属签署知情同意书。
1.1.2排除标准(1)患者有眼部外伤史;(2)患者已有视网膜脱离;(3)患者伴有晶状体混浊;(4)患者为高度近视;(5)患者眼睛出现感染;(6)患者伴有其他的血液系统疾病;(7)患者伴有严重的甲状腺功能亢进。
1.2方法所有患者均为同一术者实施手术。对照组患者术前不注射雷珠单抗治疗,直接采取玻璃体切割术,使用0.02g/mL利多卡因(国药准字H37022147)和7.5g/L布比卡因(国药准字H20020570)按照1∶1混合后对眼球进行麻醉,待麻醉起效后进行标准三通道玻璃体切除,清除眼球内积血,剥离视网膜前增殖膜,全视网膜光凝,手术完毕后填充硅油。观察组患者采用雷珠单抗(注册证号S20140003)进行预处理,在注射前3d采用5g/L左氧氟沙星滴眼液(国药准字J20100046),4次/d,持续到注射当天,再采用盐酸丙美卡因滴眼液(注册证号H20160133)进行表面麻醉,冲洗结膜囊,在角膜缘后约4mm进针注入10mg/mL雷珠单抗0.05mL,在注射后1h严格控制眼压稳定,并在1wk后进行玻璃体切割术。两组患者术后均使用可吸收线进行缝合,并给予妥布霉素地塞米松眼膏(3.5g/支,批准文号H20140737)进行涂眼。
Ⅱ期手术:玻璃体切割术后10~15d,待虹膜新生血管基本消退,前房炎症反应明显减轻后行Ⅱ期Ahmed房水引流阀植入术。术中采用球后阻滞麻醉,在颞上象限做以穹窿为基底的结膜瓣,将引流盘固定于角膜缘后9~10mm处浅层巩膜上,将AGV引流管修剪到合适长度后插入前房,固定于浅层巩膜上,缝合后妥布霉素地塞米松眼药膏包眼,术后妥布霉素地塞米松滴眼液4次/d,复方托吡卡胺滴眼液2次/d滴眼,1~2wk。
观察指标:两组患者玻璃体切割手术时间,玻璃体切割手术中出血次数、电凝次数。检测两组患者术前以及玻璃体切割手术后1wk,Ⅱ期Ahmed房水引流阀植入术后1mo最佳矫正视力(best corrected visual acuity,BCVA)情况、采用Goldmann测量眼内压变化情况。采用光相干断层扫描测定Ⅱ期Ahmed房水引流阀植入术后1mo黄斑中心凹厚度值。玻璃体开始手术前、Ⅱ期Ahmed房水引流阀植入术开始前房水中血管内皮生长因子(vascular endothelial growth factor,VEGF)水平,在患者开眼睑后生理盐水冲洗结膜囊,在角膜缘穿刺进入抽取0.1mL房水、在-70℃冰箱中保存,采用ELISA检测VEGF水平,操作按照试剂盒说明书操作。

2结果
2.1两组患者手术一般情况比较观察组患者的玻璃体切割手术时间、玻璃体切割手术中新生血管出血次数、电凝次数均显著低于对照组,差异均有统计学意义(P<0.001),见表1。
2.2两组患者BCVA比较两组患者手术前后BCVA比较差异有统计学意义(F组别=19.736,F时间=939.645,均P<0.001)。两组患者术前BCVA比较差异无统计学意义(P>0.05),观察组患者在术后1wk,1mo BCVA值均显著低于对照组,差异均有统计学意义(P<0.001),见表2。

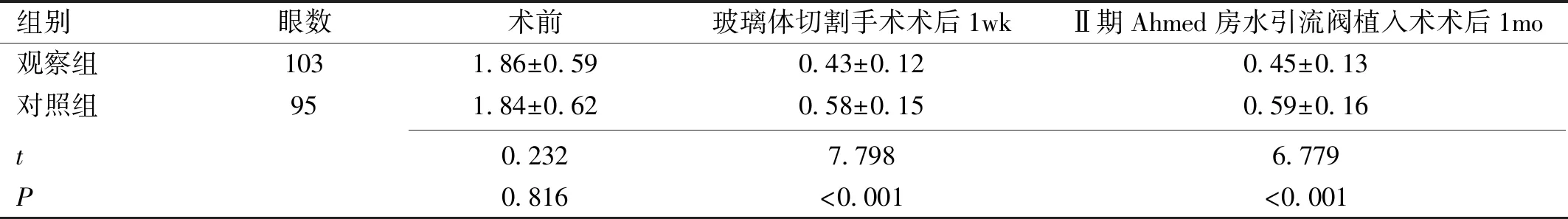
组别眼数术前玻璃体切割手术术后1wkⅡ期Ahmed房水引流阀植入术术后1mo观察组1031.86±0.590.43±0.120.45±0.13对照组951.84±0.620.58±0.150.59±0.16 t0.2327.7986.779P0.816<0.001<0.001
注:观察组:术前注射雷珠单抗联合玻璃体切割术治疗;对照组:单纯采用玻璃体切割术治疗。
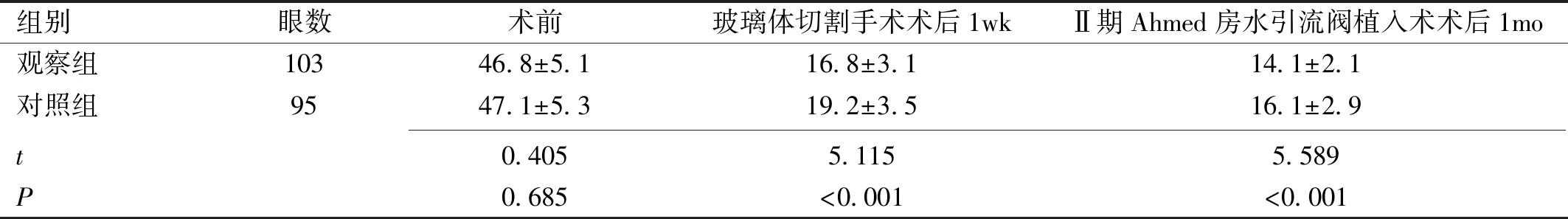
组别眼数术前玻璃体切割手术术后1wkⅡ期Ahmed房水引流阀植入术术后1mo观察组10346.8±5.116.8±3.114.1±2.1对照组9547.1±5.319.2±3.516.1±2.9 t0.4055.1155.589P0.685<0.001<0.001
注:观察组:术前注射雷珠单抗联合玻璃体切割术治疗;对照组:单纯采用玻璃体切割术治疗。

组别眼数VEGF(pg/mL)玻璃体切割手术术前Ⅱ期Ahmed房水引流阀植入术前Ⅱ期Ahmed房水引流阀植入术后1mo视网膜黄斑中心凹厚度值(μm)观察组103350.1±56.4115.8±22.4262.2±35.4对照组95348.4±55.3141.3±26.4289.3±37.6 χ20.2137.3465.223P0.830<0.001<0.001
注:观察组:术前注射雷珠单抗联合玻璃体切割术治疗;对照组:单纯采用玻璃体切割术治疗。
表5 两组患者并发症比较眼(%)

组别眼数玻璃体出血一过性眼压升高视网膜脱离合计观察组1033(2.9)8(7.8)011(10.7)对照组955(5.3)19(20.0)3(3.2)27(28.4)
注:观察组:术前注射雷珠单抗联合玻璃体切割术治疗;对照组:单纯采用玻璃体切割术治疗。
2.3两组患者眼压测定比较两组患者手术前后眼压比较差异有统计学意义(F组别=35.989,F时间=2081.013,均P<0.001)。两组患者术前眼压比较,差异无统计学意义(P>0.05),观察组患者在术后1wk,1mo眼压均显著低于对照组,差异均有统计学意义(P<0.001),见表3。
2.4两组患者VEGF和视网膜黄斑中心凹厚度值比较两组患者术前VEGF比较差异无统计学意义(P>0.05),引流阀植入术前VEGF和引流阀植入术后1mo视网膜黄斑中心凹厚度值均显著低于对照组,差异均有统计学意义(P<0.001),见表4。
2.5两组患者并发症比较观察组患者总并发症发生率10.7%,显著低于对照组总并发症发生率28.4%,差异具有统计学意义(χ2=10.030,P=0.002),见表5。
3讨论
玻璃体切割术是目前对糖尿病视网膜病变常用的治疗方案,在糖尿病视网膜病变中,眼部视网膜新生血管本身通透性较大,容易出现视网膜水肿,因此单纯采用玻璃体切割术可能会导致患者出现血管破裂出血,使手术视野不清,手术操作不便,清除不彻底等缺点[8-10]。VEGF是一种高度特异性的促血管内皮生长因子,具有增加血管通透性、增殖和血管形成的功能,近年来已有研究表明糖尿病视网膜病变与VEGF密切相关[11-12]。VEGF是眼内新生血管的刺激因子,当视网膜出现缺血,机体应激性出现VEGF的高表达,房水中的VEGF会显著升高,在虹膜、前房角等位置大量出现新生血管,并且能够一定程度上破坏血-视网膜屏障,导致出现新生血管性青光眼[13-14]。糖尿病视网膜病变合并新生血管性青光眼单纯采用玻璃体切割术手术难度较大。
NVG是一种与新生血管形成有关的青光眼,对眼球和视功能破坏严重,常常继发于全身或眼部的严重缺血性视网膜疾病,主要临床表现为虹膜和前房角新生血管膜形成,眼压显著升高,同时伴有明显的眼部充血、角膜水肿等症状。雷珠单抗是一种单克隆抗体片段,主要作用是靶向抑制人VEGF,并且亲和力较高,使VEGF无法与其受体结合,阻碍新生血管的生成,并降低血管通透性[15-16]。本试验研究发现玻璃体切割术中观察组患者的手术时间、新生血管出血次数、电凝次数均显著低于对照组,且差异具有统计学意义(P<0.001),表明术前采用雷珠单抗进行预处理,对新生血管有一定抑制作用,视网膜水肿缓解,进行手术时视野清晰便于操作,牵拉时不易出现视网膜脱落,可显著降低手术难度,减少手术时间、新生血管出血次数以及电凝次数。同时本研究结果显示,Ⅱ期手术前房水中VEGF显著低于对照组,且差异具有统计学意义(P<0.001),分析原因在于观察组术前采用雷珠单抗进行预处理,通过手术可将房水中VEGF进行清除,并破坏新生血管支架,雷珠单抗具有抑制VEGF的作用,术后可显著减少新生血管的产生,通透性降低,使房水中VEGF减少,有利于阻碍患者病情进展。本文创新点在于先进行玻璃体切割术控制原发病,Ⅱ期行引流阀植入,使Ⅱ期手术效果更好。通过对患者进行随访发现,观察组患者在术后1wk,1mo BCVA、眼压、视网膜黄斑中心凹厚度值以及并发症均显著低于对照组,且差异具有统计学意义(P<0.001),以上结果均表明术前使用雷珠单抗进行预处理,可使VEGF合成、分泌减少,在一定程度上缓解视网膜水肿,使视网膜黄斑中心凹厚度值下降,同时能够使手术视野清晰,降低手术难度,使术后并发症显著减少,新生血管减少,虹膜、房角血管萎缩,使房内压出现下降,视力矫正较好。Brown等[16]指出,雷珠单抗能抑制眼底新生血管形成,在改善黄斑水肿、提高视力水平方面具有积极意义,与本研究结果一致。宋莉等[17]采用雷珠单抗辅助PPV治疗PDR,发现术后70%患者视力提高,且随访期间未出现与药物有关的不良反应。章晖等[18]以174例PDR患者作为对象,均行23G PPV治疗,注射雷珠单抗组医源性视网膜裂孔及术后并发症发生率显著低于未注射雷珠单抗组,均与本文研究结果一致。
综上所述,雷珠单抗联合玻璃体切割术治疗糖尿病视网膜病变合并新生血管性青光眼的临床效果显著,抑制VEGF的合成、分泌,减少新生血管的产生,术后并发症显著降低,视力恢复良好。本文不足之处是随访时间过短,样本量不足,后期将继续进行随访,扩大样本量,多中心合作,为临床治疗提供更多的指导。
