活性炭/硒化钼近红外光催化降解氨氮的研究
2019-06-10顾勤勤刘守清
顾勤勤, 刘守清
(苏州科技大学 化学生物与材料工程学院,江苏 苏州 215009;江苏省环境功能材料重点实验室,江苏 苏州 215009)
光催化降解污染物是一项绿色技术,其主要利用了清洁的太阳光能,而且不会产生二次污染。其中,半导体材料是实现光催化降解的关键因素。宽带隙半导体材料如TiO2、ZnO、SrTiO3等只吸收利用紫外光和近紫外光,从而产生光电子和空穴驱动氧化还原反应[1-2]。太阳光是由紫外光、可见光和红外光组成。其中紫外光区(λ<400 nm)的辐射能最少只有4%,可见光区(400~760 nm)辐射能占43 %,红外光区(760~3 000 nm)辐射能则为53%[3-7]。在过去的几十年里,人们的研究主要集中在紫外光和可见光区域,对红外光的研究开发才刚刚开始。二硒化钼(MoSe2)是一种类似于石墨烯的二维材料。MoSe2是灰黑色的共价化合物,其结构为Se-Mo-Se 层状结构[8-10],层和层之间靠范德华力维系。MoSe2的每个Mo 原子被六个Se 原子包围,呈现三棱柱状[11-12]。研究表明,MoSe2具有较窄的带隙(1.09~1.54 eV)[13-15]。因此,可以吸收利用近红外光。笔者设计合成活性炭/硒化钼(AC/MoSe2)复合光催化剂,并研究其在近红外光下光催化降解氨氮。
1 实验
1.1 药品
活性炭(AC),国药集团化学试剂有限公司;Na2MoO4·2H2O,中国上海胶体化工厂;硒粉,国药集团化学试剂有限公司;水合肼,无锡市晶科化工有限公司;KMnO4,中国上海试剂总厂;NH4Cl,上海润捷化学试剂有限公司,均为分析纯。所有溶液都是用去离子水配制。
1.2 AC/MoSe2的合成
取0.316 g(0.004 mol)硒粉,10 mL 水合肼置于容积为100 mL 的烧杯中,密封放于通风干燥且避光环境下24 h。然后,准确称取AC(质量为MoSe2的5%),超声分散于10~15 mL 去离子水中。
然后,取0.483 g Na2MoO4·2H2O(0.002 mol)在搅拌条件下溶于40 mL 的去离子水中,在磁力搅拌下将超声分散均匀的AC 悬浊液逐滴加入到Na2MoO4水溶液中,继续搅拌30~40 min。将硒粉和水合肼混合溶液在搅拌下逐滴加入到Na2MoO4和AC 混合液中,搅拌30 min 至溶液均匀后将其转入100 mL 的高压反应釜内,密封,置于鼓风烘箱加热至180 ℃,水热反应48 h。反应结束后,自然冷却,过滤,用去离子水和乙醇反复洗涤多次,除去可溶物。将得到的黑色固体在40 ℃烘箱中干燥6 h,制得AC/MoSe2复合材料。
1.3 AC/MoSe2的结构表征
采用日本D/max 2500 pC 型号的X射线粉末衍射(XRD)仪(Cu-Kα 射线,波长为0.154 nm)测定样品的晶相结构,用场发射扫描电子显微镜(SEM,S4800)和高分辨透射电子显微镜(TEM)观测样品的表面形貌及晶面间距,用紫外/可见/近红外光谱仪(UV-Vis Near Infrared Spectrometer,UV 3600plus)测试样品漫反射光谱(UV-VIS-NIR DRS),用拉曼光谱仪(Raman spectra ,USA)测定官能团的振动频率。
1.4 氨氮的降解
实验光源是德国欧司朗300 W 的紫外可见光光源,用波长λ>780 nm 的滤光片获得近红外光。氨氮的降解在一个100 mL 的玻璃烧杯中进行,烧杯四周用锡纸包裹,光源和测试溶液之间的距离大约是10 cm。在反应器中加入一定浓度的50 mL 氨氮溶液,加入适量的催化剂,用NaHCO3-Na2CO3(0.1 mol·L-1)缓冲溶液控制反应液pH值。
在磁力搅拌条件下,将装有反应混合液的反应器放置于近红外光下。采用纳氏试剂比色法测定反应液中氨氮含量(每隔一定时间,取1.0 mL 氨氮反应溶液,在比色管内定容至50 mL,加入1.0 mL 酒石酸钾钠,1.0 mL 纳氏试剂,混合振荡,静置10 min,利用紫外可见分光光度计测定氨氮反应液的吸光度)。
根据上述方法测得每小时氨氮反应液的吸光度。根据朗伯比尔定律,在一定浓度范围内,氨氮浓度与吸光度成正比关系,计算氨氮的降解率
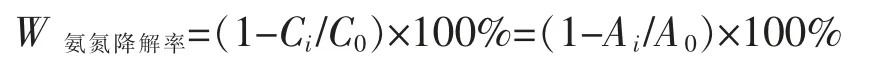
其中,C0为氨氮的初始浓度,A0为初始溶液的吸光度,Ci为剩余氨氮的浓度,Ai为剩余氨氮的吸光度。
2 结果与讨论
2.1 X射线粉末衍射表征
图1 是MoSe2、AC 和AC/MoSe2样品的XRD 衍射图。图1中(a)、(b)、(c)分别为MoSe2、AC 和AC/MoSe2样品的衍射曲线。曲线(a)在2θ=13.7°、31.42°、34.40°、37.88°、55.92°处的衍射峰分别对应于MoSe2的 (002)、(100)、(102)、(103)、(110)晶面,与MoSe2的标准图谱(JCPDS 卡片,No.29-0914)一致[16]。比较曲线(a)、(b)和(c)可以看出,其中(b)在2θ=26.4°是AC 的特征峰,并且AC/MoSe2的图谱中也出现了该衍射峰,说明该样品中含有AC。
观察曲线(a)、(b)和(c)的衍射峰,可以看出峰形比较宽,说明生成的材料颗粒较小。根据曲线(a)、(c)的(002)晶面衍射峰的半峰宽,按照Debye-Scherrer 公式D=kλ/(Wcosθ),可以计算出MoSe2和AC/MoSe2中MoSe2的粒径大小。其中D 为晶粒的平均直径;k 为晶粒形状因子,取0.89;λ 为X射线波长,取0.154 nm;W 为衍射峰的半峰宽;θ 为衍射角。通过计算得出MoSe2和AC/MoSe2中MoSe2的平均粒径大小分别为5.1 nm 和5.0 nm,二者几乎没有差异。
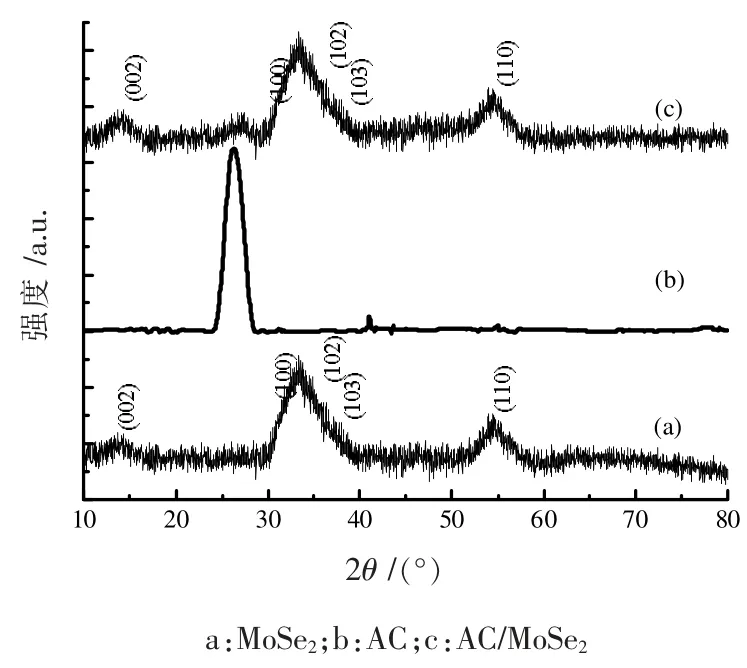
图1 样品的XRD 图
2.2 拉曼光谱表征
根据对称性,MoSe2具有4 个拉曼活性的振动模式:E2g2,E1g,E2g1,A1g[17-18]。其中A1g取决于Se 元素的面外振动;E2g1取决于Mo 和Se 的面内位移;E1g取决于Se 的面内振动, 但该呼吸模在Raman 探测中是探测不到的;E2g2是两层过渡金属硫族化合物之间的剪切模,出现在小于50 cm-1,一般不会配置这么低的波数范围。因此,一般MoSe2的拉曼特征峰只有两个振动模式,如图2 所示。由图3(a)曲线可以看出,位于285 cm-1以及238 cm-1处的拉曼峰分别归属于E2g1和A1g,符合MoSe2的拉曼活性振动。
由图3(b)曲线可观察到活性炭位于1 595 cm-1的G 带和1 340 cm-1的D 带,分别对应于AC 的E2g振动模式和活性炭结构的无序化度。其中D 峰强度越强说明非石墨化的边界数量越多,无序化越大,边界原子数越多。
图3(c)曲线是AC/MoSe2的拉曼光谱图,在236 cm-1和275 cm-1处出现了MoSe2的Raman 特征峰,同时在1 599 cm-1和1 343 cm-1处观测出两个小峰,分别代表AC 的G、D 带。说明复合材料中既含有MoSe2,也含有AC。
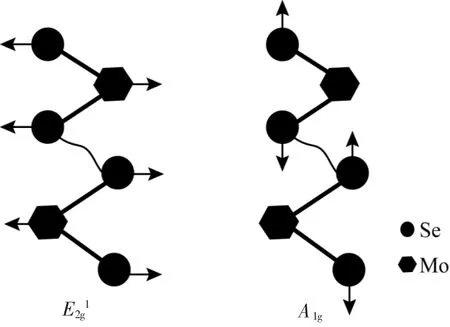
图2 MoSe2 拉曼振动模式
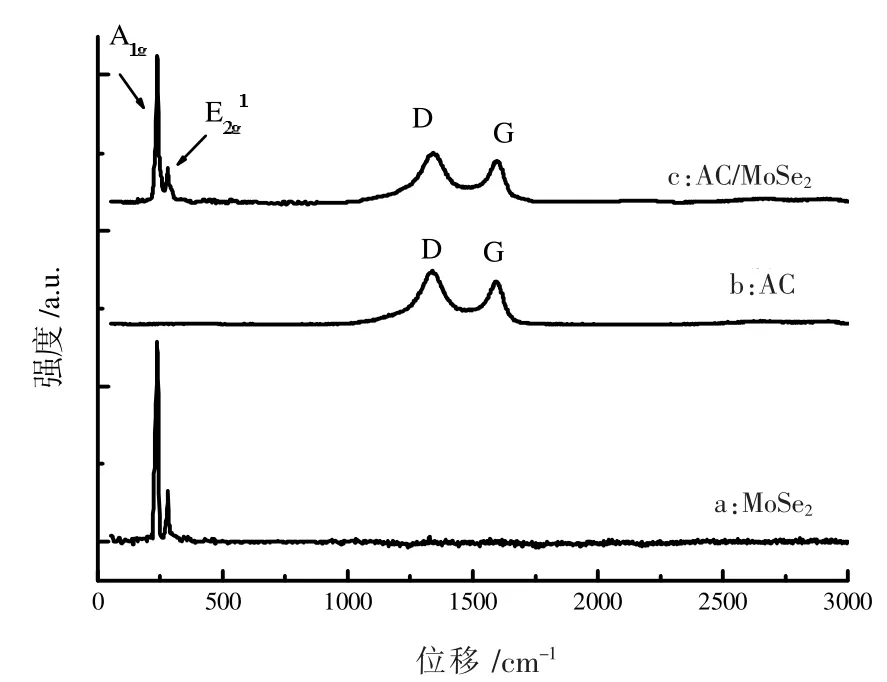
图3 拉曼光谱
2.3 产物的形貌表征
图4 为MoSe2、AC 和AC/MoSe2样品SEM图。从图4(a)可以看出,MoSe2颗粒聚集构成了微米球,这些微米球分布均匀,且尺寸均一。图4(b)为AC 的形貌图。图4(c)不仅有微米球状的硒化钼,同时也观察到周围还分布有AC,这表明MoSe2和AC 这两种物质较好地结合在一起。

图4 样品的SEM图
图5(a)为AC 的TEM图,图5(b)为MoSe2的TEM图,C、D 为MoSe2/AC 的高、低放大倍率下的TEM图。
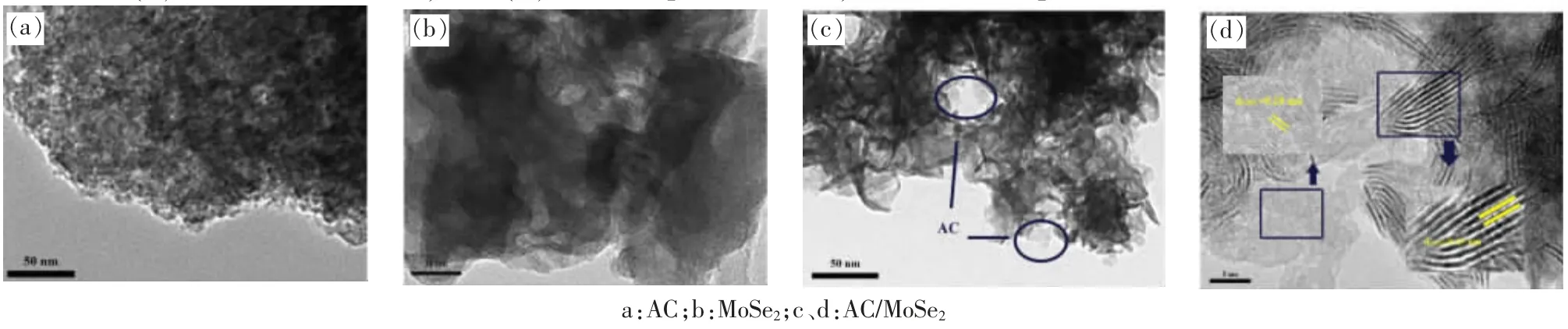
图5 样品的透射电镜图
从图5(a)可见,活性炭呈典型的多孔结构。从图5(b)可见,所制备的纳米MoSe2呈典型的层状结构,粒径大小为6 nm 左右,与上述XRD 测试的粒径相近。从图5(c)可以看出,MoSe2很好地负载在AC 表面,在经过30 min 的超声分散后,其形貌结构依然保持,说明合成的复合材料具有比较好的稳定性。MoSe2/AC 的高分辨率透射显微镜图像显示其晶格条纹间距为0.68 nm,对应于MoSe2(JCPDS 卡片,No.29-0914)的(002)面间距。同时也可以清晰地看出晶格条纹周围活性炭材料,再次证实MoSe2与AC 充分结合在一起。
2.4 紫外可见近红外漫反射光谱表征
图6 给出了MoSe2、AC 和AC/MoSe2样品的漫反射光谱。由图6 可以看出纯MoSe2在近红外区从856 nm开始逐渐增加的吸收带。从图6 中曲线(a)和曲线(b),可以看出样品在可见光区和近红外区有良好的吸收性能。基于UV-VIS-NIR DRS 光谱图根据Tauc 方程,可以计算出MoSe2和AC/MoSe2的直接带隙
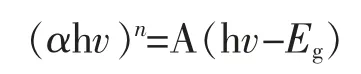
其中,A 是半导体材料常数,h 是普朗克常数,v 是光的频率,α 是吸光系数,Eg是半导体的禁带宽度,n 为2时是直接带隙。
图7 是根据图6 中数据计算并作成的两条反应直接带隙的Tauc 曲线,MoSe2和AC/MoSe2的直接带隙值分别为1.46 eV 和1.41 eV。由于负载了AC,降低了禁带宽度,显然,吸收边界扩展到近红外区域,这有利于充分利用太阳辐射。
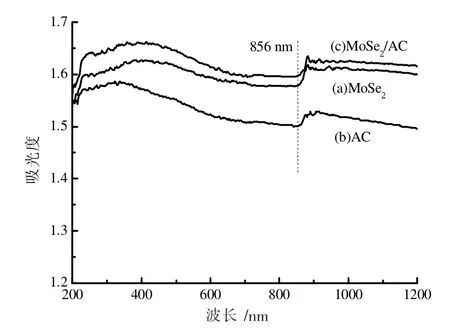
图6 紫外-可见-近红外光漫反射光谱图
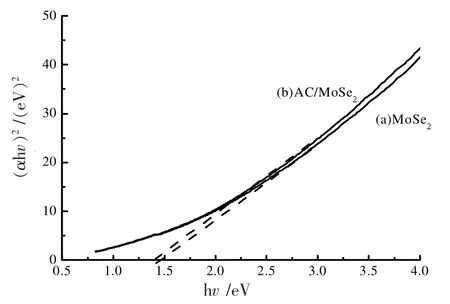
图7 (αhv)2 与hv 曲线图
2.5 X射线光电子能谱
XPS 研究表明,MoSe2样品中含有Mo、Se、O 元素(如图8 所示)。一般来说,少量的O 可能是由MoSe2表面吸附的氧。C 的1s 峰值位于284.6 eV[19-20]。位于231.1 eV 结合能属于Mo 3d 自旋轨道的峰值,证实存在Mo IV 状态;55 eV 对应于Se 峰值,进一步说明产品是MoSe2。
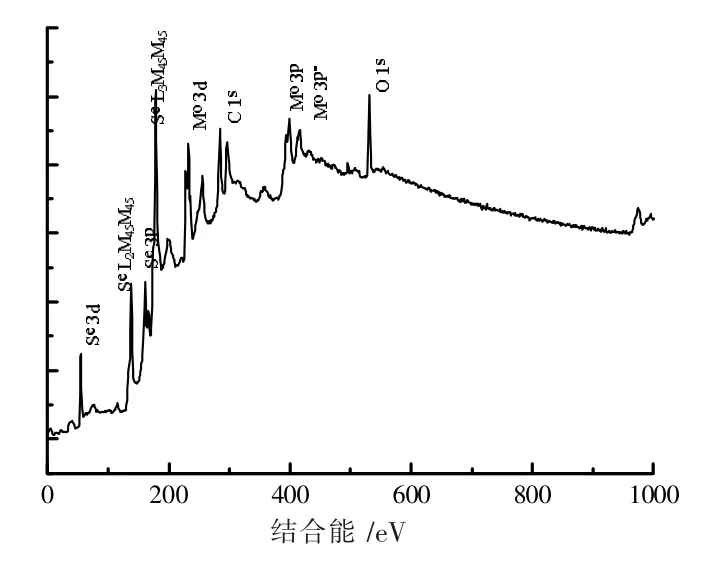
图8 MoSe2 的XPS 宽扫描图
3 氨氮的降解
3.1 近红外光下降解氨氮
MoSe2和AC/MoSe2在近红外光以及暗反应条件下的降解氨氮如图9 所示。AC/MoSe2作为光催化剂,在近红外光照射下降解初始浓度为100 mg·L-1的50 mL 的氨氮溶液(pH=10.5),11 h 降解率可达到95.7%左右,如图9 曲线(a)所示。而纯MoSe2作为催化剂,在类似条件下,11 h 降解率只有68%左右,如图9 曲线(b)所示。这说明负载AC 大大提高了MoSe2的催化活性。图9 曲线(c)是AC/MoSe2催化剂在暗反应条件下氨氮的脱去曲线,11 h 氨氮脱去率仅有35.0 %。无催化剂在红外光照射情况下,氨氮的挥发率在11 h 只有12.3%,如图9 曲线(d)所示。上述结果表明,在暗反应条件下仅有少量氨氮被吸附,仅光照而无催化剂时,氨氮溶液的挥发率也比较低,只有AC/MoSe2复合催化剂在近红外光辐射下才显示出最大的降解率。
3.2 pH值对降解氨氮的影响
图10 是溶液pH值对光催化降解氨氮的影响。降解条件:近红外光下,溶液体积V=50 mL,氨氮初始浓C=100 mg·L-1,AC/MoSe2质量m=0.15 g。从中可以看出,当溶液pH值为7 时,氨氮降解率仅为25.0%;当溶液pH值为8 时,降解率上升到34.0%左右;当溶液的pH值大于9 时,降解率明显提高;当pH值达到10.5 时,降解率达到最大值91.0%。在弱碱性以及酸性溶液中,降解率明显偏低。NH4+的pKa 值为9.3,当pH值小于9.3 时,溶液中的NH3容易被质子化[19],被质子化后孤对电子填充到质子氢的S 轨道中,因此,不再与过渡金属原子发生配位作用,氨也就不能吸附在催化剂表面。当pH值大于9.3 时NH4+便会去质子化,催化剂表面就会吸附大量氨,所以在pH值逐渐升高时氨氮降解率也会不断升高。
3.3 催化剂用量对降解氨氮的影响
图11 主要是探究催化剂用量对光催化降解氨氮的影响。取一定范围质量的AC/MoSe2作为催化剂,在近红外光照射下降解初始浓度为100 mg·L-1的50 mL 的pH值为最佳值10.5 的氨氮溶液。从图中曲线可以看出,在催化剂用量为0.1 g 时,降解氨氮率达到最佳值。当催化剂用量从0.05 g 增加到0.10 g 时,降解氨氮的效率逐渐提高。当催化剂用量从0.10 g 增加到0.20 g 时,降解氨氮的效率反而在降低。这是由于催化剂用量少时,根据质量的作用定律,溶液的反应速率不高;当增加催化剂的用量时,由于过多的催化剂会悬浮在溶液中从而阻碍溶液被光照的面积,因而降解效率反而降低。
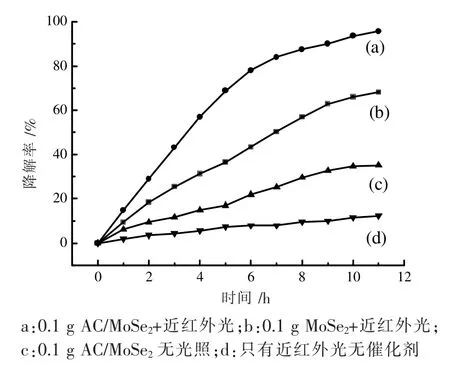
图9 近红外光光催化降解氨氮曲线
3.4 AC掺杂量对降解氨氮的影响
催化剂AC 的百分含量对氨氮降解效果的影响如图12 所示。制备了一系列不同比例AC 的复合催化剂,取0.1 g MoSe2/AC 作为催化剂, 在近红外光照射下降解初始浓度为100 mg·L-1的50 mL 的pH值为10.5 的氨氮溶液。结果如图显示,当AC 的含量为硒化钼质量的5 %时,降解氨氮的效率最佳,11 h 降解率可达到95.7 %。当AC 的含量超过5 %继续增加时,降解氨氮的效率反而在下降。
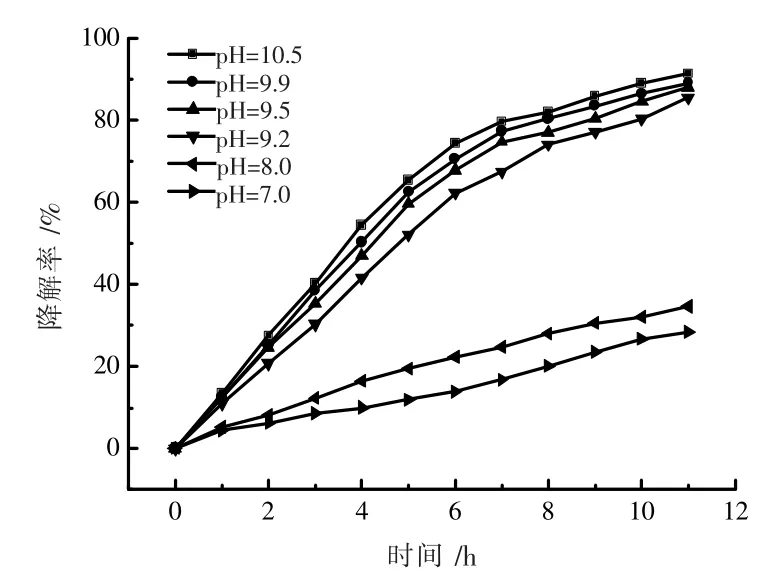
图10 pH值对于降解氨氮率的影响
3.5 动力学研究
该反应条件里主要是改变氨氮初始的浓度, 溶液的pH值、 复合催化剂的用量、AC 的掺杂量均采用上述实验的最佳值,结果如图13 所示。分析表明ln(C0/Ct)与反应时间t 呈线性关系(如图14 所示),因此,可得出氨氮降解反应是遵循了一级反应动力学方程。从而可以计算得到其一级反应动力学反应常数Kapp,其平均值为0.188 2 h-1。计算公式
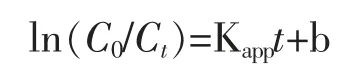
3.6 催化剂稳定性和重复利用
为了评估合成催化剂的稳定性,做了一系列循环利用实验。将0.1 g AC 含量为5 %的AC/MoSe2作为催化剂,在近红外光照射下降解初始浓度100 mg·L-1的50 mL 的pH值为10.5 的氨氮溶液,每隔1 h 取样,测定溶液的吸光度。反应11 h 后,离心分离回收催化剂,洗涤、真空烘干,催化剂循环使用降解氨氮7 次如图15 所示。7 次循环降解氨氮后,氨氮去除率仍在86.5%以上。这说明AC/MoSe2催化剂比较稳定,可重复使用。
3.7 反应机理
氨氮降解紫外-可见吸收光谱如图16 所示。在光催化过程中氨氮随时间的延长在不断降低。根据相关文献报道, 氨氮降解是根据反应1~11, 经过一系列的中间产物(NH2、NH、N2H(x+y),x+y=0,1,2)后,最终转化生成N2[21-23]。
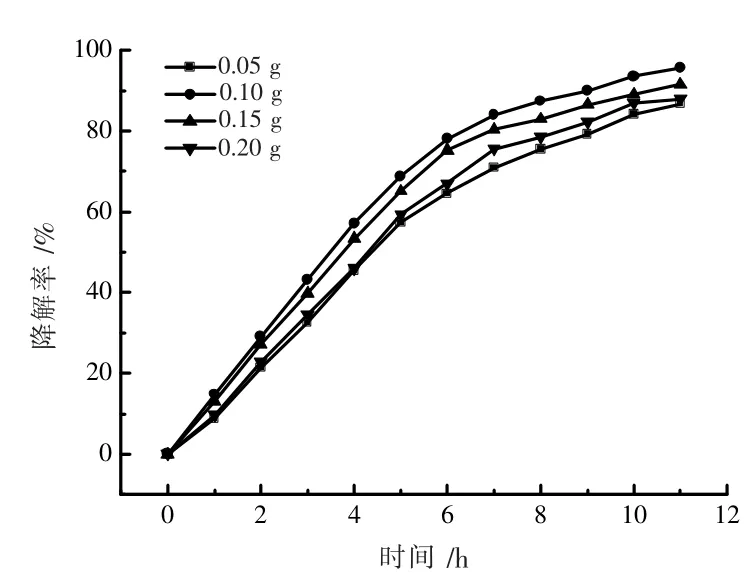
图11 催化剂用量对降解氨氮率的影响
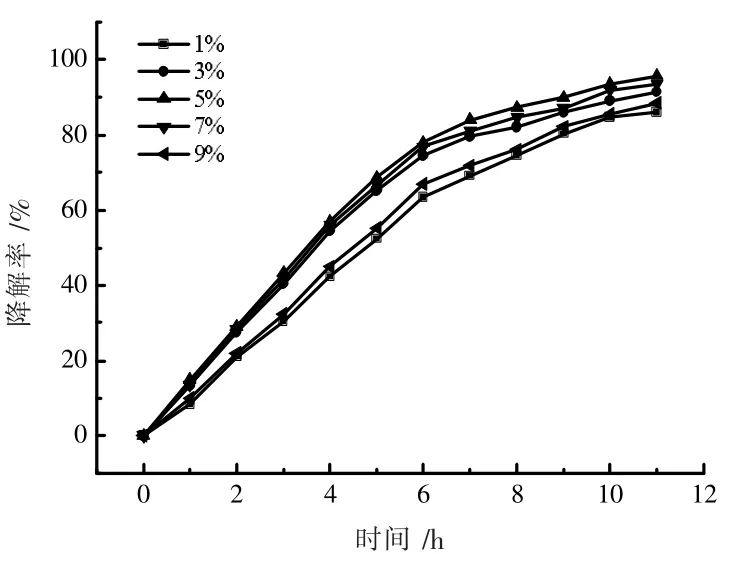
图12 AC 含量对降解氨氮率的影响
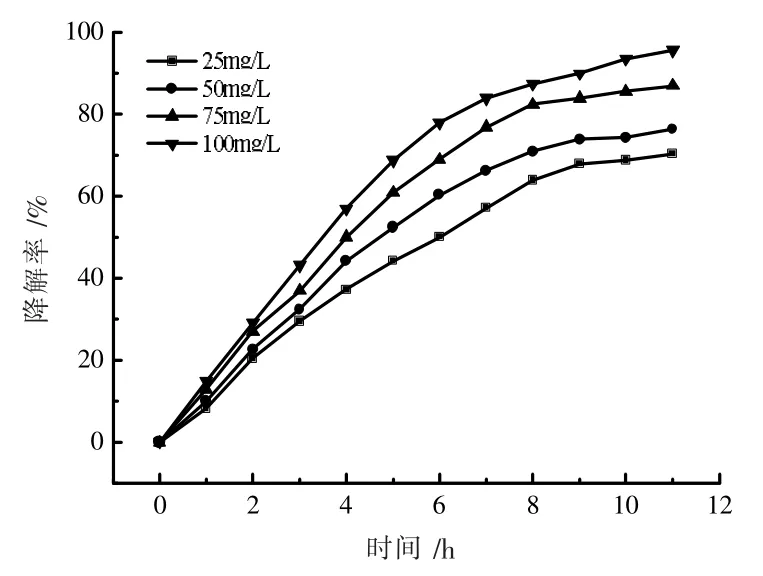
图13 氨氮浓度对于降解氨氮率的影响
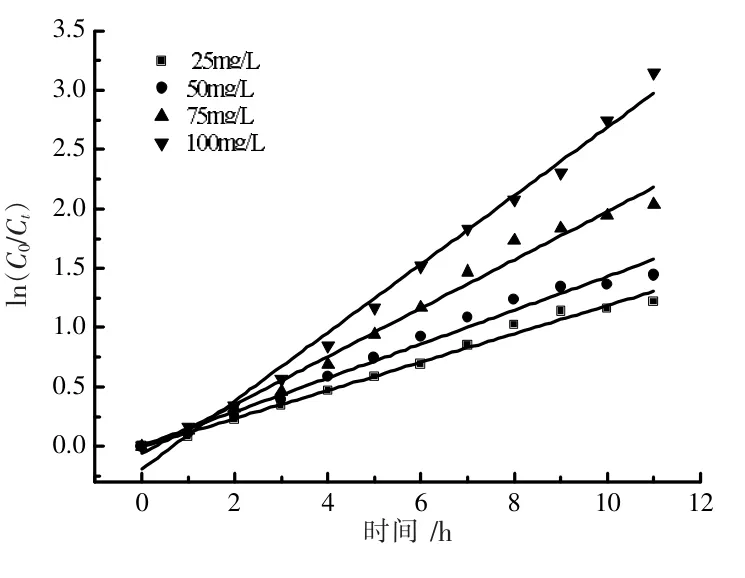
图14 不同氨氮初始浓度下了ln(C0/Ct)和时间t 的关系
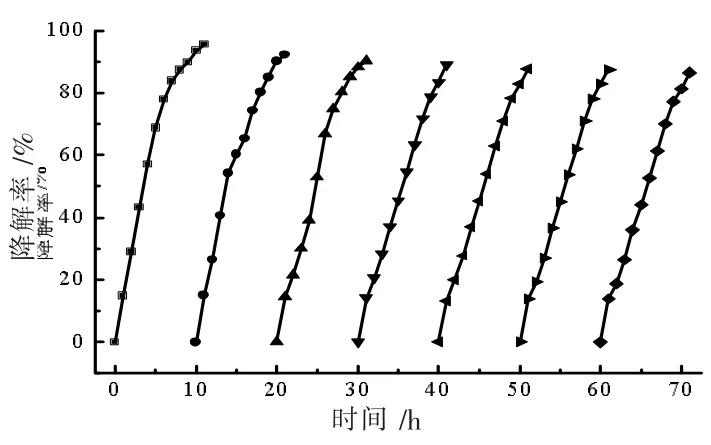
图15 催化剂循环利用及稳定性
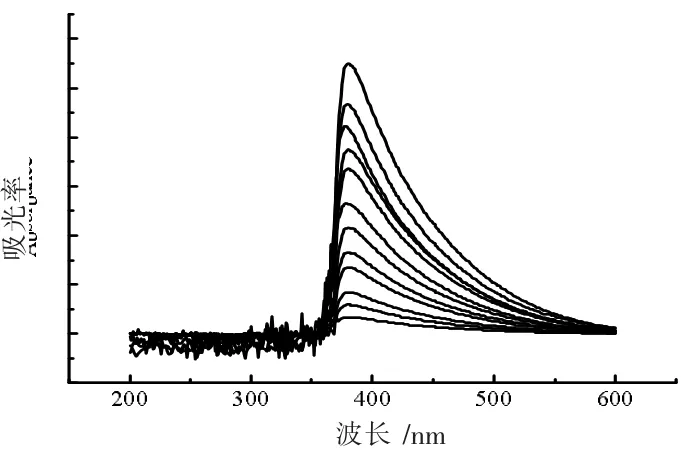
图16 氨氮降解紫外-可见吸收光谱
为了证实产物是N2气,笔者通过气相色谱对产物进行了跟踪检测,如图17 所示。由图17 可以看出O2在不断被消耗,N2的峰面积随着反应时间的增加不断上升,由此可见,降解产物就是N2。图18 可以得到,通过XPS 测得MoSe2的Ev=0.00 eV。
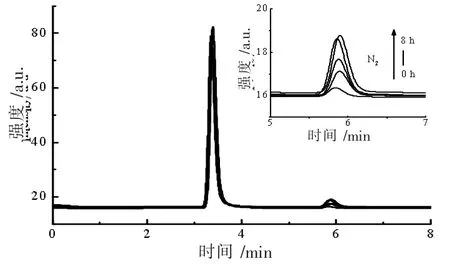
图17 氨氮降解生成氮气的气相色谱图
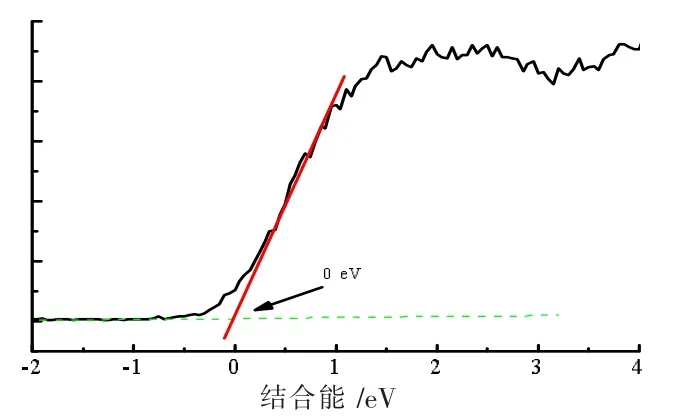
图18 MoSe2 价带能谱图
根据上述UV-VIS-NIR-DRS 光谱图可以得出MoSe2直接带隙为1.46 eV, 因此,MoSe2的Ec=-1.46 eV。MoSe2吸收近红外光后生成光生电子-空穴对,而Ec=-1.46 eV,光生电子能被O2捕获,生成H2O2,H2O2进一步与光生电子结合产生·OH,把NH3氧化成N2。同时,考虑到溶液pH值的影响,当pH=10.5 时,E(N2/NH3)=-0.53 eV,而MoSe2的Ev=0 eV,因此,光生空穴也可以直接氧化NH3生成N2。
4 结语
通过简单的水热法一步合成了AC/MoSe2这种窄禁带宽度的复合材料。研究结果表明, 复合催化材料AC/MoSe2比纯MoSe2降解氨氮的活性高。当氨氮初始浓度为100.0 mg·L-1、溶液的pH值为10.5、催化剂量为0.1 g、AC 含量为5%,近红外光照射11 h 时,AC/MoSe2复合材料降解氨氮的效率达到95.7%。动力学研究表明,氨氮降解遵循一级反应动力学规律,其表观速率常数的平均值为0.188 2 h-1。气相色谱检测表明,氨氮降解产物是氮气,实现了近红外光辐射脱氮。
