脊柱感染的MRI表现及鉴别诊断研究现状
2019-06-03张宁曾献军何来昌刘志礼刘家明张志宏陈宣银舒勇
张宁,曾献军,何来昌,刘志礼,刘家明,张志宏,陈宣银,舒勇
脊柱感染是由不同病原微生物引起的脊柱不同部位(椎体、椎间盘、小关节、硬膜外间隙等)感染的一系列疾病[1-3],约占全身肌骨系统感染的2%~7%[4]。由于人口老龄化、免疫缺陷人群增多等原因,脊柱感染的发病率逐年增高。但本病起病隐匿,表现不典型,对诊断造成很大困扰。化脓性脊柱炎和结核性脊柱炎为脊柱感染的最常见的两种类型,近年来我国脊柱结核发病率呈下降趋势,化脓性炎呈升高趋势[4-5]。MRI在脊柱感染性疾病诊断方面起着重要作用,尤其对早期骨髓异常、椎旁软组织及椎管内结构的显示优势明显,其灵敏度和特异性高达90%以上[6-8],但对于一些不典型改变仍需要仔细分析,不同病原类型的脊柱感染治疗方法不同,脊柱感染与非感染性病变治疗方法更不相同,因此相关病变的MRI鉴别诊断意义重大。
1 相关概念
一般将脊柱感染按致病菌不同分为化脓性(细菌)、肉芽肿性(结核/真菌)、寄生虫性(包虫等)三类[3,9],按累及部位不同,包括脊椎炎(spondylitis)、椎间盘炎(discitis)、脊椎-间盘炎(spondylodiscitis)、小关节炎、硬膜外脓肿,甚至包括脊膜炎及脊髓炎等一系列疾病[1-2],相关文献中可能用其中一种名称泛指这一类疾病,最常用的脊椎炎,又称椎体骨髓炎(osteomyelitis),因此关于脊柱感染在概念上存在交叉,使用上存在一些混乱。Hadjipavlou等[9]将化脓性脊柱炎的命名做了总结(图1)。结核性脊柱炎,也称Pott's disease[10],由英国外科医生Pott报道而得名。
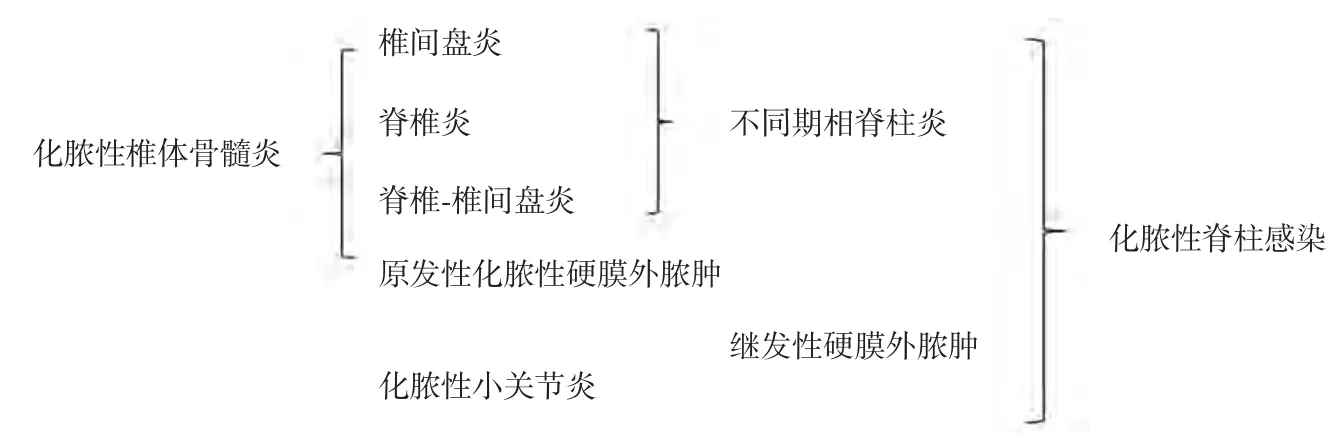
图1 不同部位化脓性脊柱炎命名及相互关系Fig.1 Nomenclature and relationship of suppurative spondylitis in different parts.
2 流行病学
化脓性脊柱炎中,最常见的致病菌为金黄色葡萄球菌,约占50%以上[1,11],其他包括大肠埃希菌(常发生于合并尿路感染的患者)、铜绿假单胞菌(多见于有静脉药物滥用史患者)、肺炎链球菌(多见于合并糖尿病的患者)、沙门氏菌(多见于镰状细胞病或无脾患者)[12]。化脓性脊柱炎年发病率约为(0.2~2.4)/10万[2-4]。结核性脊柱炎,约占结核病的1.5%~3%[7],是由结核分枝杆菌引起的一种慢性破坏性脊柱特异性感染,2015年全球发病率为1040万例[13],2002~2011年美国脊柱结核的发病率由0.07/10万人下降至0.05/10万人[14],香港大学医院进行的两项研究[4-5]发现,1955~1960年间2000例脊柱感染病例中结核性脊柱炎占比为59%,2004~2008年91例脊柱感染中结核性脊柱炎占24.2%,反映了我国南方地区脊柱感染类型的变化。
3 感染途径及发病机制
化脓性脊柱炎通常由远处部位的细菌经血行播散感染,分为经动脉和静脉途径,细菌可来自泌尿系统、呼吸系统、盆腔或皮下。脊柱椎体-间盘在解剖结构上类似于关节,终板区相当于干骺端,动脉血管终末支分布丰富,尤其在椎体前部[6],此为成人血源性感染最先、最常累及椎体前部终板下骨质的解剖学基础,炎症随后可突破皮质,向韧带下、椎间盘、邻近椎体、后柱及椎管侵犯;静脉途径为通过无瓣膜的Batson静脉丛进行,是泌尿系统及盆腔器官感染脊柱的主要血源扩散途径;非血源性途径包括穿透性创伤、直接暴露于皮肤或开放性伤口、介入性操作(腰穿、硬膜外阻滞、神经阻滞等)直接扩散,以及可来自头颈、胸部、腹部的邻近感染。结核性脊柱炎多经血源性感染,结核杆菌可由肺部、淋巴结、消化道等处通过血行播散,约50%的脊柱感染不合并肺结核。儿童和成人的血管解剖结构存在差异,因此儿童脊柱感染的首先累及椎间盘,而20岁以后的成人椎间盘无血供,通常是先感染终板后累及椎间盘[15]。可由邻近的脊椎-间盘炎或小关节炎直接蔓延而来,也可经血源性播散或行介入性操作治疗后感染,后者多见于胸椎,且70%以上位于椎管背侧[16]。原发性小关节炎多由非血源性途径传播。
4 临床特征及实验室检查
两者均好发于50岁以上患者[11,14],化脓性脊柱炎男女比例男∶女=1.5∶1~3∶1[6,11]。儿童及青少年脊柱感染相对少见,约占1.3%[3]。化脓性脊柱炎好发于腰椎,约占45%~50%[2,4,11],结核性脊柱炎好发于胸椎/胸腰段[17]。化脓性脊柱炎主要症状为急性、亚急性发作的背痛和发热,多数患者以不明原因的发热为主诉。结核性脊柱炎患者可出现乏力、不适、体重减轻、夜间出汗等症状,在慢性愈合期患者出现背部僵硬、畸形和神经系统症状。多数患者可不伴发热,Butle等[11]报道中发热病例仅占12.5%,白细胞计数可升高或不升高,Tali等[1]总结的13%~60%患者出现血白细胞升高;炎症指标红细胞沉降率(erythrocyte sedimentation rate,ESR)、C-反应蛋白(C-reactive protein,CRP)可做为活动性脊柱感染标志物,敏感性高达90%~100%[4,9],但特异性差,只能用于排除活动性感染。诊断标准之一为病原学分离出致病菌,仅约1/2~2/3脊柱感染的培养呈阳性结果[4,11,15],可能与低毒性细菌感染或活检技术有关。有研究应用Gene Xpert检测结核分枝杆菌特异性DNA序列并联合MRI,将诊断敏感性提高到97.9%[18]。糖尿病、终末期肾病、肝硬化等合并症为脊柱感染高风险因素[19]。临床上通常会根据临床特征及影像学表现进行早期试验性治疗以减少椎体压缩和脊髓受压等并发症,但仅基于临床和成像特征难以达到病原菌的诊断,因此,影像引导下的经皮脊柱活检术开展得越来越多,以获得足够的组织用于培养致病微生物[12],但脊柱感染活检确诊率约30%~40%[20]。
5 MR成像技术
常规MR成像基本序列包括T1和T2WI矢状位和轴位扫描,脂肪抑制(fat suppressed,fs)的T2WI序列或短时反转恢复(short TI inversion recovery,STIR)序列可用于增加显示骨髓水肿的敏感性。一般来说,增强扫描对于在脂肪抑制的T2WI或STIR图像上无骨髓水肿的病例价值不大[21],因为超早期炎性反应不明显。MR增强扫描的主要作用在于显示椎旁软组织的强化特点及椎管内结构的异常强化,对于鉴别诊断意义重大,并可明确区分硬膜外脓肿与硬膜外蜂窝织炎,硬膜外脓肿形成多需要进行手术治疗,而是蜂窝织炎通常选择保守治疗[22]。在有肾功能不良或过敏等MR增强扫描禁忌证患者,扩散加权成像(diffusion weighted imaging,DWI)有助于脓肿的诊断[23]。
6 化脓性脊柱炎和结核性脊柱炎的MRI特征
6.1 化脓性脊柱炎
早期细菌感染通常由于终末动脉栓塞缺血、炎性渗出,在MRI上典型表现为单发椎体或邻近两个椎体骨髓呈T1W低信号和T2W高信号,在脂肪抑制的T2WI或STIR序列显示更明显,且以椎体前部受累为主。增强后病灶呈明显弥漫、均匀强化[24],随着炎症进展,终板区出现侵蚀破坏,程度较轻,一般不超过椎体高度的一半,但椎间盘破坏明显[24-25],表现为边缘不规则,内可见T2明显高信号及不同程度的强化[26],可伴有椎间盘和椎体高度下降,但后突畸形少见。炎症可在椎旁、前后纵韧带下蔓延,或延伸到邻近的软组织如腰大肌、膈肌等结构,一般范围较局限,边界多模糊,增强后椎旁以形成蜂窝织炎为主,少数可形成厚壁小脓肿[17]。临床上,随着炎症蔓延化脓性脊椎炎、化脓性椎间盘炎、硬膜外脓肿和脊膜炎等常合并存在,当炎症累及椎管时,增强扫描的意义更明显,主要用于评估硬膜外间隙、椎管内感染及对神经根侵犯,继发性硬膜外脓肿呈环状强化,压迫脊髓或马尾,脊膜或脊髓受累时可见强化,此时临床症状重,需及时行手术引流脓肿及药物治疗[21]。化脓性小关节炎不常见,但在老年患者、免疫功能低下患者、介入性操作或脊髓手术后患者可出现,MRI表现为小关节及周围软组织结构紊乱,边缘模糊不清,T1WI呈等信号,T2WI呈高信号,椎管内可疑等低异常信号致椎管狭窄,相应椎体及间盘可以不受累,增强扫描异常软组织明显弥漫性强化,局部可见脓肿形成,椎管内硬膜外炎症明显强化,此时合并硬膜外脓肿多位于椎管背侧[2,6],提示原发性硬膜外脓肿,较脊椎-间盘炎在临床症状上更呈急性表现,以L4~5小关节最常见。
6.2 结核性脊柱炎
典型的结核性脊柱炎表现为相邻两个或两个以上椎体骨质破坏并累及相应椎间盘,椎体在T1WI上呈低信号,在T2WI上呈混杂信号、高信号、低信号,Chang等[27]的研究中29%的椎体呈低信号,认为T2W信号对诊断价值不大,且难以鉴别骨髓水肿、脓肿与组织充血;椎体破坏较明显,增强后呈局限性、不均匀强化,该特点在多项研究中被认为具有特异性[17,27],合并压缩骨折及后突成角多见[25];椎间盘破坏相对轻,由于结核杆菌缺乏蛋白分解酶,表现为仅部分髓核正常信号消失而保留部分正常或退变髓核信号,此征象为与化脓性脊柱炎早期表现鉴别的要点之一[25];椎旁脓肿多见,呈环形强化,边界清晰,溶通性脓肿脓腔大,可与椎体相通,多为薄壁光滑大脓肿[17,24,27];韧带下蔓延范围广,常多节段累及[17];部分研究认为结核性脊柱炎更容易形成硬膜外脓肿、脊膜累及及小关节累及[17,27]。在慢性阶段,T1WI和T2WI上的低信号强度表示椎板塌陷伴终板硬化。不典型结核性脊柱炎可表现为单发椎体异常、单发椎体及邻近椎间盘异常、多个椎体异常但相应椎间盘正常、单纯附件病变、横突病变[28],椎间盘不受累及的感染常易误诊为肿瘤性病变,尤其是多个非连续性(跳跃性)椎体破坏时,易误诊为转移瘤或淋巴瘤,此型多发于青少年或免疫力低下患者,可伴脊柱外骨骼侵犯。治疗后的MRI随访复查中,在T1WI上出现椎体信号增高代表椎体脂肪化[29],增强后强化程度下降、范围缩小[30],提示病灶好转。
7 鉴别诊断
7.1 布氏杆菌性脊柱炎
布氏杆菌感染引起的一种人畜共患的变态反应性疾病累及脊柱,感染途径多为接触过受污染的动物产品或通过食用由未经高温消毒的乳制品。MRI表现为受累椎体及相应椎间盘信号异常,好发于下腰椎;骨质破坏以椎体边缘或终板中央区局限性破坏为主[31],周围可呈弥漫性椎体骨髓炎表现,但椎体形态基本完整;椎体前缘骨质硬化,可见鸟嘴状骨赘形成;椎旁脓肿小;T2WI椎间盘信号增高,增强可强化;易累及小关节;后突畸形罕见;如有牧区生活史则更支持诊断。
7.2 椎间盘退变性终板炎(Modic I型)
MRI表现为相邻两个椎体骨髓水肿信号,但退变的椎间盘由于髓核脱水在T2WI上信号减低;可见真空征;终板皮质一般连续无破坏;椎旁软组织及硬膜外间隙不受累;DWI上出现“claw sign”,即在异常终板炎及邻近骨髓与正常骨髓交界面处出现边界清楚线状高信号影[32]。
7.3 急性许莫氏结节
MRI表现为终板软骨下结节周围单发椎体的骨髓水肿信号,呈围绕突出的结节周围同心环状水肿区,边界不清弥漫分布为急性病程的征象,可无弥漫性椎间盘信号异常。
7.4 强直性脊柱炎
此病晚期常出现Andersson病变,即椎体/脊椎-椎间盘非炎症性破坏性病变[33],可合并横贯性累及三柱的脊柱骨折,为应力性、自发性或外伤后导致,好发于颈胸段或胸腰段交界处,如骨折未经及时处理出现假关节形成,则会出现终板侵蚀及软骨下骨硬化,但强直性脊柱炎另见竹节椎、广泛性韧带钙化、小关节融合、椎间隙不狭窄等表现。
7.5 SAPHO综合征
为主要累及皮肤、骨和关节的一种包括滑膜炎(synovitis)、痤疮(acne)、脓疱病(pustulosis)、骨肥厚(hyperostosis)和骨髓炎(osteomyelitis)在内的一组慢性病。约1/3累及脊柱,MRI表现终板侵蚀及椎间隙狭窄,但多呈2个以上连续椎体呈多节段受累,椎体前角骨侵蚀;脊柱曲度改变呈曲线或“半圆形”改变,椎间盘信号一般正常,少数也可增高,前纵韧带下可见软组织增厚,范围较广;无椎旁或硬膜外脓肿[34]。
7.6 神经性脊柱关节病
由于缺少保护性感觉而反复受到创伤导致的脊柱改变,常合并糖尿病、脊髓空洞症、梅毒或其他神经性疾病。好发于胸腰椎交界处和腰椎,可累及一个或多个椎体节段;真空征;椎体的破坏可致骨折,随后出现骨质硬化、大量骨赘形成和椎间盘间隙消失,在T2WI呈低信号;晚期可见假关节形成。
7.7 肿瘤和(或)转移瘤
不累及椎间盘(除脊索瘤),椎间盘高度正常;软组织占位边界清楚。
8 结论
临床上保持对脊柱感染的高度警惕和怀疑是诊断的核心,了解化脓性脊柱炎和结核性脊柱炎的临床特征和病理生理基础有助于理解其MRI表现及不典型类型的少见表现,增强扫描对鉴别诊断意义重大;熟悉脊柱感染的相关鉴别诊断有助于减少误诊,尽量提高诊断准确率,实现早期诊断和及时进行适当的治疗,以减少或避免并发症、脊柱畸形和神经功能缺陷等后遗症。
利益冲突:无。
对SMA—13沥青混合料而言,由人工进行纤维材料的投放,先干拌12~17s,再添加SBS改性沥青,继续湿拌40~45s,将总拌和时间控制在55~60s范围内。对于拌和时间,应以实际情况为依据进行调整。因纤维的质量较轻,很难通过拌和达到均匀,所以在必要时应延长一定拌和时间。考虑到生产这种沥青混合料时,机械效率相对较低,所以为保证摊铺施工的连续性,需将摊铺速度限制在1.5~2.5m/min范围内,具体的碾压工艺如表1所示。
