氨基硅烷修饰的荧光磁性复合纳米粒子的合成
2019-05-31朱彦涛张志刚
朱彦涛,张志刚
(山西大学 分子科学研究所,化学生物学与分子工程教育部重点实验室,山西 太原 030006)
0 引言
以纳米粒子载运抗癌药物正成为化学、医学及材料科学领域的研究热点,受到了人们的广泛关注[1-2]。当纳米粒子用于载运抗癌药物时,可使药物避免被人体网状内皮组织体系清除,从而延长药物在血液中的循环时间,还可使药物更易进入肿瘤组织的毛细血管中,从而使药物更高效地分布于肿瘤细胞中,为此已发展出了各种各样的纳米粒子载药体系,如金纳米粒子、聚合物纳米粒子等等[3-4]。在这些众多的纳米粒子载药体系中,氨基硅烷修饰的Fe3O4@SiO2磁性复合纳米粒子因具有良好生物相容性且其表面可通过氨基偶联各种靶向分子,引起了各国研究者的广泛兴趣[5]。目前这类复合纳米粒子已被广泛应用于生物医学领域,如蛋白质固定、DNA纯化、磁共振成像中的细胞标记等方面[6-8]。包裹荧光体的氨基硅烷修饰的Fe3O4@SiO2磁性复合纳米粒子用于抗癌药物的载体时,将会使其具有实时可追踪的特性,有利于肿瘤的诊断和治疗,因而具有重要的应用前景,但目前尚未见到包裹荧光体的氨基硅烷修饰的Fe3O4@SiO2磁性复合纳米粒子的报道。本文合成了一种新的包裹荧光体罗丹明6G的氨基硅烷修饰的荧光磁性复合纳米粒子,并对影响复合纳米粒子的粒径因素进行了初步探索。
1 实验部分
1.1 材料
正硅酸乙酯(TEOS),国药集团化学试剂公司;3-氨丙基三乙氧基硅烷(APTES),国药集团化学试剂公司;四甲基氢氧化铵(TMAH),阿拉丁试剂公司;罗丹明6G (R6G),西亚试剂公司;其他试剂均为分析纯。
1.2 Fe3O4磁性纳米粒子的合成
根据文献方法[9]以共沉淀法制备Fe3O4磁性纳米粒子。具体步骤如下:将0.65 g FeSO4·7H2O 和1.255 g FeC13·6H2O溶于40 mL蒸馏水中,搅拌并恒温30℃的条件下,通入氮气除氧。在持续通入氮气和搅拌加热条件下向反应体系中滴加5 mL浓氨水(质量分数25%),调节溶液pH=10,体系中逐渐有黑色沉淀生成。继续反应10 min后,将反应混合物于室温下静置片刻。以稀氨水、蒸馏水磁分离洗涤黑色固体数次后,得到产物Fe3O4磁性纳米粒子。
1.3 包裹有R6G的荧光磁性复合纳米粒子的合成
称取0.12 g罗丹明6G与2 mL APTES混合,加入5 mL乙醇使其全部溶解,避光放置18 h。将0.8 g新合成的Fe3O4分散于20 mL乙醇中,滴加浓氨水(质量分数25%)调节溶液至pH=9,超声分散15 min。在持续搅拌下将R6G、APTES和乙醇的混合溶液逐滴加入上述体系,搅拌1 h后,将适量TEOS、TMAH及5 mL乙醇的混合溶液缓慢滴加入反应体系,室温反应24 h后通过磁分离得到沉淀,以乙醇、少量蒸馏水交替洗涤数次后50℃烘干,得到荧光磁性复合纳米粒子(Fe3O4/R6G)@SiO2。将不同反应条件下合成的产物分别标记为1a、1b、1c(见表1)。
1.4 氨基硅烷修饰的荧光磁性复合纳米粒子的合成
称取300 mg (Fe3O4/R6G)@SiO2分散于60 mL乙醇中,超声分散30 min。量取200 μL APTES加入2.3 mL乙醇,静置5 min后滴加到前述混合物中,以浓氨水(质量分数25%)调节体系pH=8。50℃水浴中持续搅拌下反应5 h后,磁分离得到沉淀物,并分别以蒸馏水和乙醇洗涤数次,再置于烘箱50℃烘干,得到包裹有R6G且经氨基硅烷修饰的荧光磁性复合纳米粒子 (Fe3O4/R6G)@SiO2-APTES。
1.5 氨基硅烷修饰的荧光磁性复合纳米粒子对pBR322 DNA损伤情况的研究
利用琼脂糖凝胶电泳法研究了(Fe3O4/R6G)@SiO2-APTES对pBR322 DNA的损伤情况。如果复合纳米粒子对DNA造成损伤,DNA的空间构型将可由共价闭环(ccc)转变为开环(oc)甚至线性(Linear)构型,而这三种构型的DNA在电场中的迁移速率不同,因此可通过凝胶电泳法了解复合纳米粒子对DNA的损伤情况。具体步骤如下:
将24.2 g Tris-base、5.71 mL冰醋酸和40 mL EDTA (0.125 mol·L-1)水溶液混合于100 mL烧杯中,再加入40 mL灭菌蒸馏水充分溶解后转移至100 mL容量瓶,并以灭菌蒸馏水定容,得到TAE电泳液,将之摇匀后转移至试剂瓶内保存,用时稀释50倍。
将0.121 g Tris-base、0.036 g NaCl 溶于80 mL灭菌蒸馏水中,以盐酸调节溶液pH值为7.26,并以灭菌蒸馏水定容于100 mL容量瓶,得到实验所需的缓冲液。
称取1.5 mg荧光磁性复合纳米粒子超声分散于1 mL DMF中,按照实验需求以缓冲液稀释成一系列不同浓度的复合纳米粒子分散液,并将适量pBR322 DNA (0.5 μg/μL)以缓冲液稀释8倍。向每个EP管中分别加入3 μL pBR322 DNA稀释液,再分别加入7 μL不同浓度的复合纳米粒子分散液。将各管混合液吹打均匀后,37℃水浴恒温平衡30 min。再向每个EP管中分别加入2 μL 6×Glycerol Gel Loading Dye I (BPB),混合均匀后上样于质量分数为0.8%的琼脂糖凝胶上。
在稀释50倍的TAE电泳液中,保持电压65 V,电泳1 h,于凝胶成像系统下拍照得到凝胶电泳图。
2 结果与讨论
2.1 复合纳米粒子的合成与表征
2.1.1 不同实验条件对复合纳米粒子粒径的影响
据文献报道,粒径介于50~200 nm的纳米粒子最容易被肿瘤细胞摄入[1],因此了解并控制复合纳米粒子的粒径对载药纳米粒子来说显得非常重要。本文以Zetasizer Nano ZS型激光粒度仪测定了不同实验条件下合成的包裹有R6G的荧光磁性复合纳米粒子粒径,其结果如表1所示。
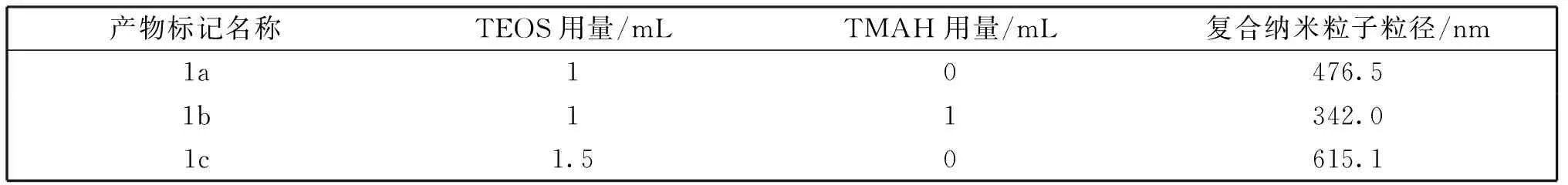
表1 不同实验条件下的1a-1c的粒径
表1中产物1a和1b分别是在其他反应条件相同的情况下,添加TMAH和不添加TMAH时得到的复合纳米粒子(Fe3O4/R6G)@SiO2,它们在水中的粒径分别为342.0 nm 和476.5 nm。由此可见,稳定剂TMAH的存在对纳米粒子的粒径影响显著,这可能是由于带正电荷的TMAH更好地防止了复合纳米粒子的聚集、稳定了复合纳米粒子并使之分散性增强的缘故。此外,从表1还可看出,TEOS的用量不宜过大,增大TEOS的用量会使复合纳米粒子的粒径增大。因此,在制备(Fe3O4/R6G)@SiO2的过程中,产物1b的合成条件最为合适。
2.1.2 红外谱图分析
由图1可见,(Fe3O4/R6G)@SiO2-APTES的红外光谱中,2 926 cm-1可归属为APTES的氨丙基的-CH2-基团的振动[10],1 564 cm-1可归属为APTES上—NH2的弯曲振动[11],1 385 cm-1则对应于Si—CH2的剪式振动[12]。红外光谱的数据表明,氨基硅烷已成功地修饰到了(Fe3O4/R6G)@SiO2的表面。
2.1.3 (Fe3O4/R6G)@SiO2-APTES的DLS表征
将少量(Fe3O4/R6G)@SiO2-APTES超声分散于超纯水中得到该样品分散液,以Zetasizer Nano ZS型激光粒度仪测得其ζ电位为20.0 mV,见图2。结果表明该荧光磁性复合纳米粒子表面带正电荷,进一步证实氨基硅烷已成功修饰于(Fe3O4/R6G)@SiO2表面。

Fig.1 IR spectra: (a) (Fe3O4/R6G)@SiO2(1b),(b) (Fe3O4/R6G)@SiO2-APTES图1 红外光谱:(a) (Fe3O4/R6G)@SiO2(1b),(b) (Fe3O4/R6G)@SiO2-APTES
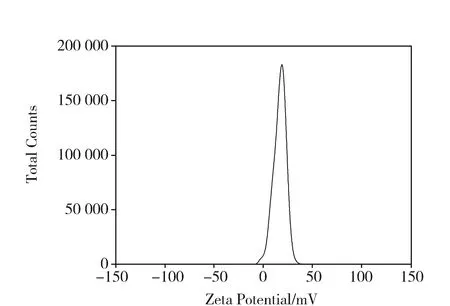
Fig.2 Zeta potential of (Fe3O4/R6G)@SiO2-APTES图2 (Fe3O4/R6G)@SiO2-APTES的Zeta电位
此外,还经DLS测定得知(Fe3O4/R6G)@SiO2-APTES的水合粒径为255.0 nm,相比于未被氨基硅烷修饰的(Fe3O4/R6G)@SiO2(1b)的水合粒径(342.0 nm),其粒径明显减小,这可能也是由于氨基硅烷修饰的(Fe3O4/R6G)@SiO2表面带有正电荷,因静电排斥作用的存在减少了复合纳米粒子的团聚,从而稳定了复合纳米粒子的缘故。
2.1.4 荧光谱图
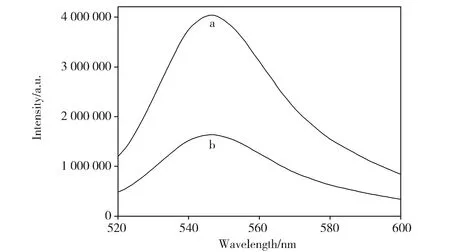
(a) (Fe3O4/R6G)@SiO2, (b) (Fe3O4/R6G)@SiO2-APTES dispersed in water (the concentration was 0.67 mg·mL-1)Fig.3 Fluorescence spectra(a)(Fe3O4/R6G)@SiO2,(b) (Fe3O4/R6G)@SiO2-APTES(浓度均为0.67 mg·mL-1)图3 荧光谱图
分别将适量(Fe3O4/R6G)@SiO2和(Fe3O4/R6G)@SiO2-APTES超声分散于蒸馏水中,得到浓度为0.67 mg·mL-1的样品分散液,将上述两种分散液分别置于FluoroMax-4荧光光度计,固定激发波长480 nm进行谱图扫描,扫描波长范围为500~600 nm。由图3可知,上述两种复合纳米粒子均在最大发射峰位于547 nm处出现较强的荧光发射峰,这与文献中报道的R6G在水中的荧光发射峰位置一致[13],表明荧光染料R6G已被成功地包裹在荧光磁性复合纳米粒子之中。此外,从图3中亦可看到,(Fe3O4/R6G)@SiO2-APTES的荧光强度明显弱于(Fe3O4/R6G)@SiO2,这是由于进一步搅拌反应会降低R6G的包裹率所致。
2.2 氨基硅烷修饰的荧光磁性复合纳米粒子对DNA的损伤情况

Lane 1: 3 μL DNA+7 μL buffer; Lane 2-6: 3 μLDNA+7 μL magnetic nanoparticles(concentration of the dispersion from left to right was 0.2, 0.5, 0.8, 1.2 and 1.5 mg·mL-1, respectively.)Fig.4 Electrophoresis analyses of DNA mixed with different concentrations of (Fe3O4/R6G)@SiO2-APTES1:1:3 μL DNA+7 μL缓冲液;2-6:3 μL DNA+7 μL (Fe3O4/R6G)@SiO2-APTES分散液(分散液浓度从左至右分别为0.2、0.5、0.8、1.2、1.5 mg·mL-1)图4 荧光磁性复合纳米粒子(Fe3O4/R6G)@SiO2-APTES与DNA作用的凝胶电泳图
由图4可知,氨基硅烷修饰的荧光磁性复合纳米粒子(Fe3O4/R6G)@SiO2-APTES几乎不会对pBR322 DNA造成损伤,即使纳米粒子的浓度达到1.5 mg·mL-1时,DNA的ccc泳带没有发生明显变化。我们以前报道过柠檬酸修饰的磁性纳米复合粒子(Fe3O4/CA)@SiO2有着很好的生物相容性[9],但当纳米粒子的浓度达到0.33 mg·mL-1时,即会对DNA造成明显的损伤,DNA的oc泳带条纹亮度明显增强,可见本文合成的氨基硅烷修饰的荧光磁性复合纳米粒子要比(Fe3O4/CA)@SiO2具有更好的生物相容性。
3 结论
本文合成并表征了一种包裹荧光染料罗丹明6G的氨基硅烷修饰的荧光磁性复合纳米粒子,初步探索了影响这类复合纳米粒子粒径的因素。这类纳米粒子在水中具有很好的分散性和稳定性,且有良好的生物相容性,有望成为一种新型抗癌药物载体,值得进行深入研究。
致谢:本工作中所用到的Zetasizer Nano ZS型激光粒度仪由山西大学大型仪器中心提供。
