核酸检测与酶联免疫检测对输血相关传染性疾病的检测效果对比分析
2019-05-29曹华琳刘亚军
曹华琳 刘亚军
[摘 要] 目的 对比分析核酸检测与酶联免疫检测对输血相关传染性疾病的检测效果。方法 选取我站采集的26325份无偿献血的检验样本作为研究对象,通过进行2次酶联免疫检测或者必要时联合1次核酸检测,并对检测结果进行分析。结果 经过对26325份血液标本进行酶联免疫检测和核酸检测,酶联免疫检测检出318例阳性,核酸检测检出373例阳性,其中核酸检测出含有乙肝表面抗原(HBsAg)的血液样本296例,检出含有丙型肝炎病毒(HCV)的血液样本53例,检出含有人类免疫缺陷病毒(HIV)的血液样本24例,两者比较差异有统计学意义(P<0.05);核酸检测与酶联免疫检测联合应用后,检出381例阳性,提示联合检测的检出率高于任何单独检测。结论 核酸检测在输血传播疾病的筛查过程中具有重要的价值,其能够降低单独酶联免疫吸附测定的漏诊率,提高乙肝病毒、丙肝病毒和HIV病毒等的筛查水平,而核酸检测联合酶联免疫检测具有更高的检出效果。
[关键词] 核酸检测;酶联免疫检测;血液传播
中图分类号:R446.6;R446.1
文献标识码:A文章编号:1009-816X(2019)02-0171-03
doi:10.3969/j.issn.1009-816x.2019.02.021
乙肝病毒感染、丙肝病毒感染、HIV病毒感染能够通过血液途径进行传播,流行病学研究证实,每年输血导致的乙肝病毒传播的病例可达5万~10万人左右[1,2]。临床上输血治疗前通过对血液制品的相关传染性病毒的检测,能够提高血液制品的安全性。现阶段临床上采用酶联免疫吸附法检测输血相关病毒的阳性情况,虽然其能够提高乙肝病毒、丙肝病毒和HIV病毒的检出水平,但长期的随访观察研究证实,酶联免疫吸附法检测的局限性较为明显,其漏诊率较高,假阴性率可超过8%以上[3]。核酸检测能够通过对血液制品中的相关病毒颗粒DNA或RNA的扩增,特异性的检测不同的病毒感染情况[4]。部分研究者探讨了核酸检测在输血相关感染性疾病中的作用,认为其可以有效预防输血相关疾病的传播[5],但与酶联免疫吸附测定的对比研究不足。为了提高输血治疗的安全性,本次研究选取我站采集的26325份无偿献血者的检验样本作为研究对象,探讨了核酸检测与酶联免疫检测联合预防输血相关疾病传播的临床效果,报道如下。
1 资料与方法
1.1 标本:选取我站在2017年2月至2018年2月间采集的26325份无偿献血者的检验样本作为研究对象,献血者经过干式生化仪检测丙氨酸氨基轉移酶(ALT)和快速金标法检测乙肝表面抗原(HBsAg)后,分别抽取2管静脉血,每管5mL,其中一管含有分离胶,用于核酸检测;另一管不含分离胶,用于酶联免疫检测。含有分离胶的样本需在4小时内进行离心处理,所有血液标本采集处理完毕后均放于2~8℃的冰箱内,等待统一检测。
1.2 仪器与试剂:
1.2.1 主要仪器:酶免检测系统:全自动酶联免疫检测处理系统(深圳爱康UranusAE280)、Freedom EVO clinical全自动加样仪(瑞士TECAN公司);核酸检测仪器:HAMILTON STAR全自动混样仪、Roche cobas s 201核酸提取扩增系统(瑞士Roche公司)。
1.2.2 主要试剂:HBsAg ELISA试剂(北京万泰生物药业股份有限公司、美国雅培公司),抗-丙型肝炎病毒((HCV)ELISA试剂(北京万泰生物药业股份有限公司、珠海丽珠诊断试剂有限公司),抗-人类免疫缺陷病毒(HIV)ELISA试剂(法国伯乐公司、北京万泰生物药业股份有限公司),HBV、HCV、HIV核酸提取和扩增检测试剂(罗氏诊断公司,MPX1试剂)。所有试剂均经过批批检,严格按照SOP进行操作并在有效期内使用。
1.3 检测方法:
1.3.1 ELISA检测:对献血者的血液标本采用2种ELISA试剂平行检测HBsAg、抗-HCV、抗-HIV。其中:HBsAg检测S/CO值在0.8~1.0设置为灰区,S/CO值≥0.8即判为有反应性;抗-HCV检测S/CO值在0.7~1.0设置为灰区,S/CO值≥0.7即判为有反应性;抗-HIV检测S/CO值在0.7~1.0设置为灰区,S/CO值≥0.7即判为有反应性。双试剂有反应性的标本直接判为不合格;单试剂有反应性标本采用同种试剂对标本进行2孔复测,复测结果2孔均无反应性为合格,2孔任1孔有反应性判为不合格。
1.3.2 核酸检测:将2种ELISA检测结果呈阴性的26007份标本送陕西省血液中心进行核酸集中化检测。采用6个标本混合检测模式,对有反应性的标本进行拆分,混合检测有反应性拆分后还呈有反应性的标本判为有反应性,混合检测有反应性拆分无反应性的标本判为无反应性。拆分有反应性的标本,在进一步鉴别后结果为有反应性的最终判定为有反应性,鉴别为无反应性的最终判定为不确定,拆分后为有反应性结果的所有血制品均做报废处理。
1.4 统计学处理:统计软件采用SPSS 16.0计数资料采用百分率表示,组间比较采用χ2检验;P<0.05表示差异具有统计学意义。
2 结果
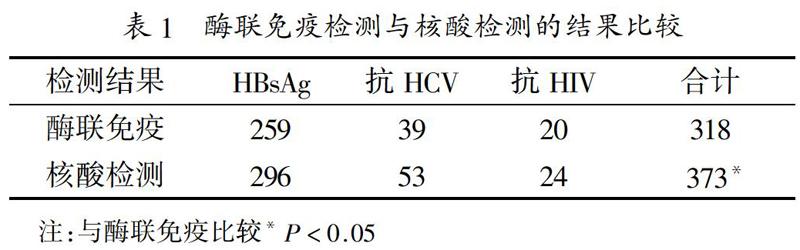
2.1 酶联免疫检测与核酸检测的结果比较:通过对26325份血液标本进行酶联免疫检测,检测出318例阳性,通过核酸检测,检测出373例阳性,结果显示存在部分含有病毒且处于变异、窗口期、隐性感染时的样本,使用酶联免疫检测无法检出的情况,其中核酸检测新检出含有HBsAg的血液样本37例,新检出含有HCV的血液样本14例,新检出含有HIV的血液样本4例,两者比较差异有统计学意义(P<0.05),见表1。
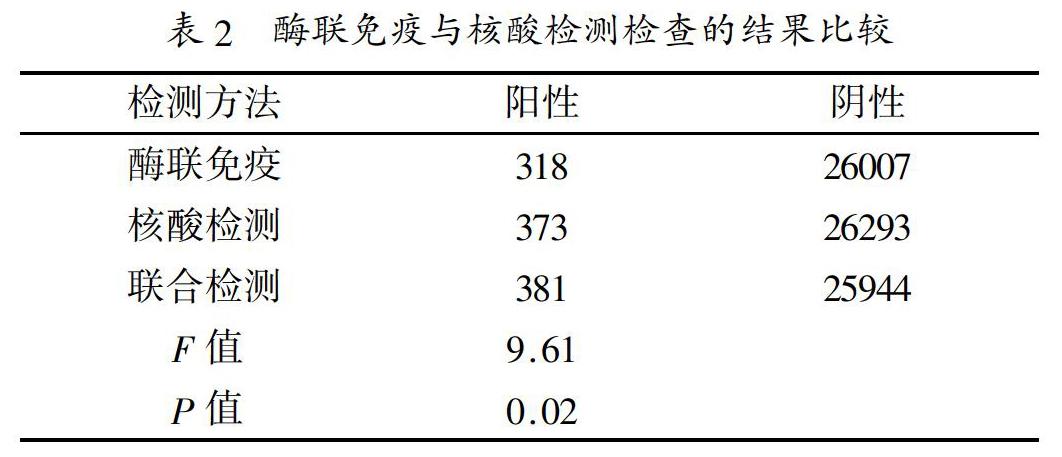
2.2 不同检测方法的结果比较:经过对26325份血液标本中进行酶联免疫检测和核酸检测,并对结果进行汇总,分别统计单独应用酶联免疫、核酸检测与联合检测的结果,显示联合检测具有更好地检出效果,将各种检测方法的结果进行汇总对比,结果显示联合检测的检出率更高,可以进一步提高检测结果的准确性,降低输血传播疾病的风险。
3 讨论
乙肝病毒感染、丙肝病毒感染、HIV病毒感染通过输血传播的风险明显上升,乙肝病毒感染、丙肝病毒感染等感染导致的患者多器官功能衰竭和远期并发症的发生率也明显的升高[5]。特别是在偏远或者经济欠发达的地区,由于检测技术的落后,血制品乙肝病毒感染、丙肝病毒感染等漏诊而导致疾病传播的风险有进一步增高的趋势[6]。对于相关血液制品中不同感染性病毒的检测,不仅能够保证血液制品的安全性,同时还能够降低输血相关因素导致的正常人群的感染和感染性疾病的扩散。临床上通过酶联免疫吸附测定法检测血清中乙肝病毒等颗粒蛋白,其检测环境要求相对较低,检测试剂盒的操作较为简便[7]。但一项囊括了217例样本量的血液制品的病毒筛查分析结果提示,两次酶联免疫吸附测定筛查相关传染性病毒感染的灵敏度不足78%,漏诊率或者误诊率可达6%~10%[8]。核酸检测能够通过对于相应病毒颗粒RNA的扩增,采用PCR方式检测基因的扩增产物,进而识辨不同病毒感染的风险。核酸检测对于血液制品中相关病毒的基础性浓度要求较低,在较低的基线水平上即可实现对于病毒的检测效果。同时核酸检测不受到环境温度的影响,对处于窗口期、免疫变异病毒或无应答状态的病毒颗粒等,均具有较高的检测灵敏度[9]。在本次研究中,对病毒处于窗口期、病毒变异或者隐性感染的患者中,酶联免疫吸附测定的局限性较为明显,其无法进行相关血液标本的检测。而核酸检测在酶联免疫检测阴性的标本中筛查出了不同数量的乙肝病毒、丙肝病毒和HIV病毒感染情况,表明酶联免疫检测存在明显的漏诊情况,而核酸检测能够提高输血相关病毒的检测能力。通过汇集不同的相关文献,认为这主要考虑与下列几个原因有关[10~12]:(1)核酸检测的特异性较高,不论病毒是否处于窗口期、静止期或隐性感染期,核酸检测方法均能够通过对于病毒DNA的扩增,从而实现筛查作用;(2)核酸检测受操作方法、步骤、试剂盒的影响较小,由于病毒DNA短期内不存在变异,因此HBsAg变异等并不会影响到核酸检测的灵敏度。赵红娜等[13]也发现,核酸检测能够提高5%左右的输血相关传播性疾病的筛查灵敏度,同时能够显著降低酶联免疫检测的漏诊水平。单独应用酶联免疫与核酸检测检查结果分析可见,单独采用核酸检测的检出效果更为明显,这主要由于核酸检测的稳定性、对于标本的要求相对较低、检测结果的抗干扰能力较强。特别是对于气候或温度变化较为明显的地区,核酸通过扩增病毒颗粒DNA进而进行检测的方式,稳定性更高。本研究还发现联合核酸检测+酶联免疫检测能够进一步提高单独核酸检测的效果,提示了联合筛查在血液制品检测过程中的作用。但部分研究者并不认为联合核酸检测+酶联免疫检测的效果优于单独核酸检测,认为联合检测的费用较高而灵敏度并无明显的上升[14],这与本次研究的结论存在一定的差别,考虑可能与PCR仪器的精度、PCR引物设计等的差异有关。
综上所述,核酸检测在输血传播性疾病的筛查过程中具有重要的价值,其能够降低单独酶联免疫吸附測定的漏诊率,提高乙肝病毒、丙肝病毒和HIV病毒等的筛查水平,而联合核酸检测和酶联免疫检测具有更高地检出效果。
参考文献
[1]Yang H, Anderson S, Forshee R, et al. Modeling complete removal of risk assessment questions in the USA predicts the risk of HIV exposure in blood recipients could increase despite the use of nuckic acid testing[J]. Vox Sanguinis,2016,110(4):324-328.[2]Babic I, Maslovic M, Vuk T, et al. Detection of three blood donors with multiple myeloma by routine viral individual-donor nucleic acid testing screening[J]. Transfusion,2017,57(11):2813-2814.
[3]虢娟,邓凯航,林雪珍,等.分析核酸检验与酶联免疫检测血液病毒的应用及检验准确率[J].中国现代药物应用,2017,11(13):57-58.
[4]李玉泉.核酸检测与酶联免疫检测血液病毒的比较分析[J].中国卫生产业,2016,13(31):45-47.
[5]刘丽,杨忠思,单玉.血液检测新模式在无偿献血者血液筛查中的应用分析[J].中国输血杂志,2015,28(3):304-306.
[6]Mafirakureva N, Mapako T, Khoza S, et al. Cost effectiveness of adding nucleic acid testing to hepatitis B, hepatitis C, and human immunodeficiency virus screening of blood donations in Zimbabwe[J]. Transfusion,2016,56(12):3101-3103.
[7]黄成垠,蒋昵真,陈显,等.血液HIV、HBV和HCV筛查策略的探讨[J].中国输血杂志,2015,28(7):784-786.
[8]高景波,刘艳春,王芳.血站实验室酶联免疫检测性能验证方法的探讨[J].中国卫生检验杂志,2016,26(21):3186-3187.
[9]吴宝军.核酸检测与酶联免疫检测血液病毒的对比分析[J].中国实用医药,2015,10(7):115-116.
[10]张巧琳,田耘博,张琴,等.2012~2013年重庆市无偿献血者HIV感染情况分析[J].重庆医学,2015,44(8):1120-1121.
[11]周丽君,郭伟鹏,谭湘涛,等.病毒核酸检测对降低输血传播疾病残余风险的分析研究[J].新疆医科大学学报,2014,37(2):214-217.
[12]陈肖潇,田绿波,樊学军,等.2007~2013年出入境人群丙肝实验室检测结果分析及检测流程探讨[J]. 中国国境卫生检疫杂志,2015,25(2):99-102.[13]赵红娜,王艺芳,李俊英,等.核酸检测与酶免检测在郑州地区血液筛查中的联合应用[J].中国输血杂志,2015,28(10):1269-1271.
[14]Sertz R, Biceroglu S, Kayin M, et al. Nucleic acid testing of blood donors-Ege University Hospital short term experience[J]. J Clin Viro,2016,82(5):35-36.
(收稿日期:2018-9-6)
