3-碘-N-苄氧羰基-L酪氨酸甲酯的合成
2019-05-29刘娜娜黄宇昌郝海静王家贤李声桐范文静孙保平
刘娜娜,黄宇昌,郝海静,王家贤,李声桐,范文静,孙保平
(安阳工学院化学与环境工程学院,河南安阳455000)
酪氨酸骨架广泛存在于环肽类天然产物中,例如deoxybouvardin(RA-V)[1]、Arylomycin A2[2]、TMC-95A[3]、万古霉素(Vancomycin)[4]等抗肿瘤或抗菌效果显著的化合物分子中都具有酪氨酸结构(具体分子结构见图1)。在这些天然产物的合成中氨基酸的选择性保护对于控制反应位点、提高反应效率至关重要。因此,开展酪氨酸衍生物的合成研究对这类天然产物的合成意义重大。
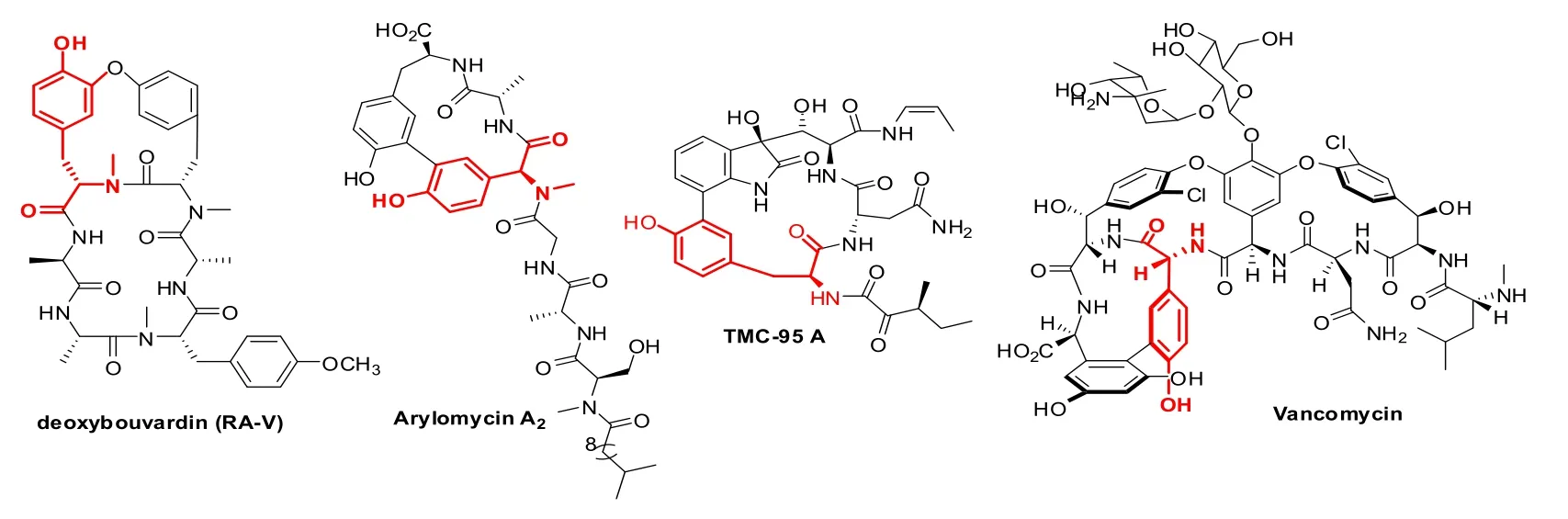
图1 含酪氨酸结构的天然产物结构式
目前,文献报道的酪氨酸衍生物的合成方法主要有几种:
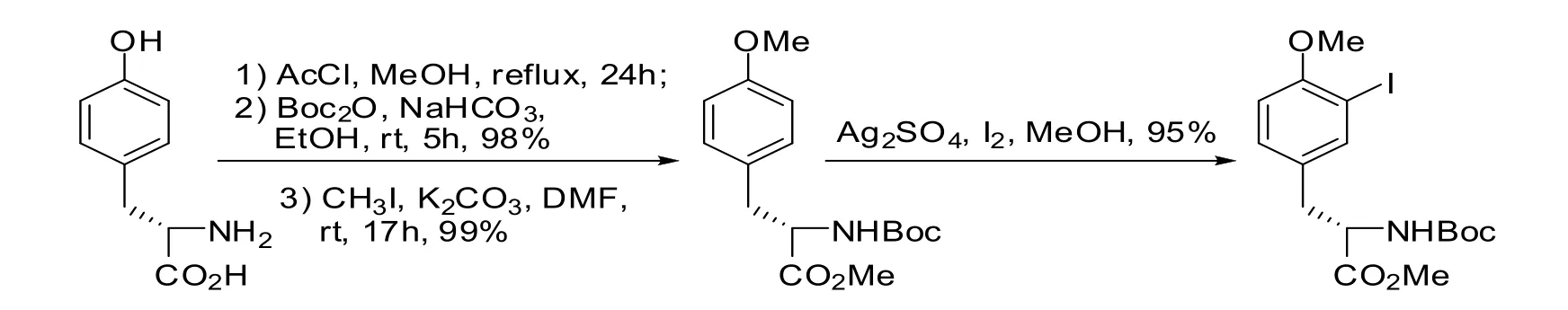
1)本课题组前期报道的3-碘-N-叔丁氧羰基-L酪氨酸甲酯的合成是由酪氨酸为原料,经甲酯化、酰胺化、醚化得到O-甲基-N-叔丁氧羰基-L酪氨酸甲酯,然后经过碘代后得到3-碘-N-叔丁氧羰基-O-甲基-L酪氨酸甲酯,总收率为92%[5]。该路线的不足之处是酪氨酸的酚羟基用甲基保护,脱保护时需要用到三溴化硼、三氟化硼乙醚等强路易斯酸,不耐酸的官能团会发生反应。
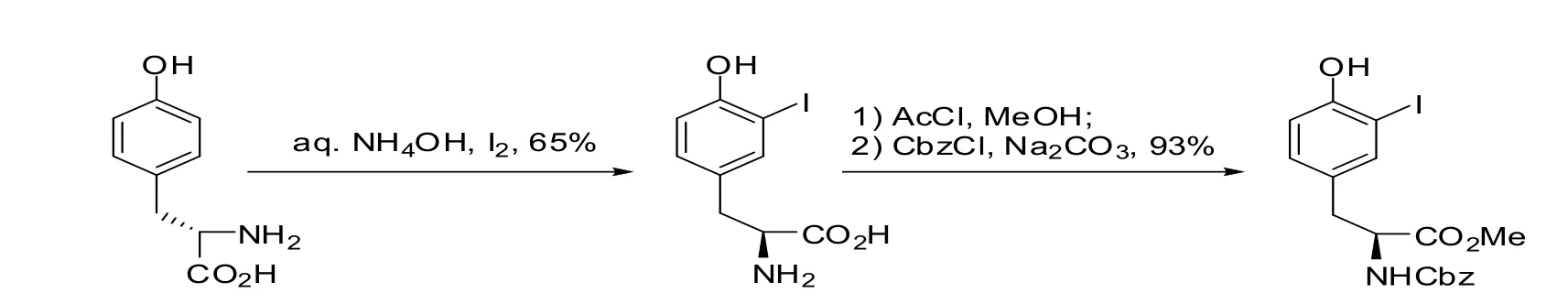
2)Luc Neuville and Jieping Zhu课题组将酪氨酸与氨水和碘反应以65%的收率得到3-碘-L酪氨酸[6]。Craig A.Hutton课题组将3-碘-L酪氨酸先后与甲醇-乙酰氯、苄氧酰氯(CbzCl)反应得到3-碘-N-苄氧羰基-L酪氨酸甲酯,收率为93%[7]。该路线总收率为60%,收率较低,反应中用到的氨水易燃易爆,后处理需要使用大量酸中和氨水,成本高,环境污染严重。
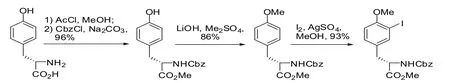
3)Samuel J.Danishefsky课题组将酪氨酸与甲醇-乙酰氯、CbzCl反应得到N-苄氧羰基-L酪氨酸甲酯,然后与硫酸二甲酯反应得到N-苄氧羰基-O-甲基-L酪氨酸甲酯,最后与碘反应得到3-碘-N-苄氧羰基-O-甲基-L酪氨酸甲酯。该路线总收率为77%,但面临同样的问题是脱酚羟基的保护时,需要用强路易斯酸。
肽类的合成通常需要在温和的反应条件下进行,反应条件剧烈会导致氨基酸消旋或肽链断裂。氨基酸保护基的反应选择性在提高反应效率等方面起到至关重要的作用。以上关于酪氨酸衍生物的合成报道中,对于酚羟基的保护多数是用甲基,这就导致在脱甲基的时候需要用到强路易斯酸,可能会造成肽链中敏感官能团的反应。
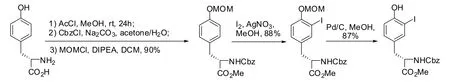
针对以上反应选择性的问题,本课题组设计合成了3-碘-N-苄氧羰基-L酪氨酸甲酯。将酪氨酸先后与甲醇-乙酰氯、CbzCl和氯甲基甲醚(MOMCl)反应,得到N-苄氧羰基-O-甲基甲醚-L酪氨酸甲酯,随后与碘反应得到3-碘-N-苄氧羰基-O-甲基甲醚-L酪氨酸甲酯,最后在氢气和钯碳的作用下脱MOM得到3-碘-N-苄氧羰基-L酪氨酸甲酯,总收率69%。其中氢化脱MOM是关键步骤,常规脱MOM的方法会用到盐酸、乙酸、三氟化硼乙醚三氟乙酸等强路易斯酸,会导致分子中不耐酸基团脱除,甚至引起重排、降解等反应,导致反应难以控制,反应收率降低。本研究发现了在钯碳和氢气作用下选择性脱MOM的方法,且分子中Cbz基团不受影响,该反应条件为中性,选择性高,是其他脱MOM的方法无法比拟的。
1 实验部分
1.1 实验仪器与试剂
本实验所用原料和试剂(AR级)购买于上海柏卡化学技术有限公司和安耐吉化学技术有限公司等国内试剂公司。所用检测仪器有Bruker Avance 400核磁共振仪等。
1.2 试验方法
1.2.1 N-苄氧羰基-O-甲基甲醚-L酪氨酸甲酯的合成
将1.18 g(10 mmol)L-酪氨酸放入100 mL圆底烧瓶中,用50 mL甲醇溶解,然后缓慢滴加入乙酰氯1.4 mL(20 mmol),室温条件下反应24小时。减压蒸干溶剂,得酪氨酸盐。然后加入20 mL丙酮:水=1∶1的混合溶液,用冰浴冷却至0 °C,然后加入碳酸钠0.43g(40 mmol)和苄氧羰基氯0.85g(10 mmol),在室温条件下反应24小时后,减压除去溶剂,加10 mL水,用乙酸乙酯(3×50 mL)萃取,合并的有机溶剂用10 mL饱和食盐水洗涤后,再用无水硫酸钠干燥,浓缩得到粗产物。该粗产物用20 mL二氯甲烷溶解,然后加入二异丙基乙基胺3.5 mL(20 mmol)和MOMCl 0.77 mL(10 mmol),然后反应约5小时,加入10 mL饱和碳酸氢钠水溶液,用乙酸乙酯(3×25 mL)萃取,分离后的有机相用10 mL水和饱和食盐水各洗一次,然后用无水硫酸钠干燥,减压蒸去有机溶剂,用硅胶柱层析(石油醚/乙酸乙酯=5∶1)得到无色液体N-苄氧羰基-O-甲基甲醚-L酪氨酸甲酯3.36 g,收率为90%。
1.2.2 3-碘-N-苄氧羰基-O-甲基甲醚-酪氨酸甲酯的合成
称取N-苄氧羰基-O-甲基甲醚-L酪氨酸甲酯180 mg(0.39 mmol)和硝酸银67 mg(0.40 mmol)放入反应瓶中,加入10 mL甲醇,然后加入碘100 mg(0.40 mmol)。反应4小时后,加入饱和硫代硫酸钠水溶液,用乙酸乙酯(3×30 mL)萃取。有机相依次用10 mL水、10 mL饱和食盐水洗,然后用无水硫酸钠干燥,溶剂用减压法蒸干。粗产物经硅胶柱层析(石油醚/乙酸乙酯=5∶1)得171 mg无色液体3-碘-N-苄氧羰基-O-甲基甲醚-酪氨酸甲酯,收率为88%。
1H-NMR(300MHz,CDCl3):δ(ppm)7.53(1H,d,J=1.8 Hz),7.39-7.29(5H,m),7.02-6.92(2H,m),5.33-5.28(1H,m),5.23-5.20(2H,m),5.15-5.05(2H,m),4.63-4.57(1H,m),3.73(3H,s),3.49-3.46(3H,m),3.05-2.94(2H,m).13C-NMR(75MHz,CDCl3):δ(ppm)171.83,155.69,155.37,140.22,136.29,131.25,130.40,128.66,128.30,128.17,116.49,111.85,95.09,94.54,87.30,67.14,56.52,56.09,54.91,52.51,36.94.
1.2.3 3-碘-N-苄氧羰基-L酪氨酸甲酯的合成
3-碘-N-苄氧羰基-O-甲基甲醚-酪氨酸甲酯150 mg(0.3 mmol)用5 mL甲醇溶解后,加入30 mg 10%钯碳,在氢气氛下室温反应5小时。过滤除去固体,减压蒸干有机溶剂后,粗品经硅胶柱层析(石油醚/乙酸乙酯=3∶1)得118 mg无色液体3-碘-N-苄氧羰基-L酪氨酸甲酯,收率为87%。
1H-NMR(300MHz,CDCl3):δ(ppm)7.22(5H,m),6.82(1.5H,d,J=8.1 Hz),6.68(0.5H,d,J=8.1 Hz),6.61(1H,d,J=8.1 Hz),5.36(1H,dd,J=16.8,8.1 Hz),5.04-4.95(2H,m),4.50(1H,t,J=6.0 Hz),3.60(3H,s),2.93-2.84(2H,m).13C-NMR(75MHz,CDCl3,mixture of two urethane rotamers):δ(ppm)172.39,172.04,156.01,155.48,154.59,139.22,136.09,130.72,130.34,129.49,128.59,128.55,128.24,128.06,126.96,115.66,115.17,85.03,67.17,55.10,52.50,52.43,37.39,36.87.
2 结果与讨论
2.1 催化剂Pd/C用量对收率的影响
本实验设置5个不同量的Pd/C与固定量的3-碘-N-苄氧羰基-O-甲基甲醚-酪氨酸甲酯在甲醇中氢气氛下室温反应1小时,用于考察Pd/C的用量对反应收率的影响,具体数据如表1所示。

表1 催化剂Pd/C用量对收率的影响
由表1数据显示,随着Pd/C用量的增加,反应收率也随之增大。当Pd/C的用量由15毫克增加到30毫克时,反应收率由37%增加到56%,然后增加Pd/C用量到45毫克,虽然收率有所提高,但提高幅度不大。因此,综合考虑价格等因素,Pd/C用量选用30 mg/150 mg底物。
2.2 反应时间对产率的影响
选择相同的Pd/C和底物的投料量,以甲醇作溶剂,氢气氛下室温反应,研究不同反应时间对收率的影响,如表2所示。
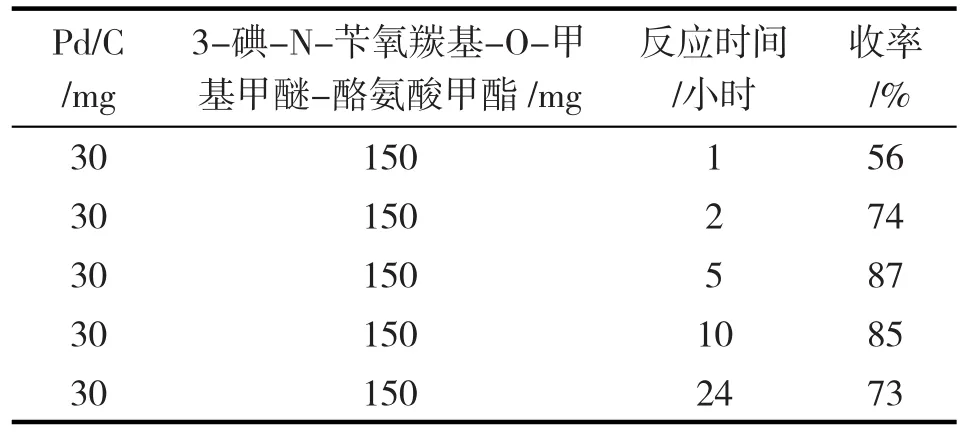
表2 反应时间对产率的影响
表2数据显示,随着时间由1小时增加到5小时,反应收率也随之增大。当反应时间为5小时时,收率达到最大值即87%,然后增加反应时间,收率反而降低。因此,确定当150毫克3-碘-N-苄氧羰基-O-甲基甲醚-酪氨酸甲酯与30毫克Pd/C在氢气氛下室温反应时,最佳反应时间是5小时。
3 结论
以酪氨酸为原料,先后经历甲酯化、苄氧酰胺化、甲氧甲基醚化得到中间体N-苄氧羰基-O-甲基甲醚-L酪氨酸甲酯,然后经碘代反应在3位引入碘,最后在Pd/C氢气的作用下脱去MOM,得到目标化合物3-碘-N-苄氧羰基-L酪氨酸甲酯。本论文主要研究了Pd/C、氢气条件下脱MOM的方法,该方法反应条件温和,选择性好,后处理简单。
