雷珠单抗对PDR患者玻璃体切割术后疗效的影响
2019-05-20董晓
董 晓
0引言
增殖性糖尿病视网膜病变(proliferative diabetic retinopathy,PDR)是以血管新生为主体的增殖性眼底病变,也是糖尿病患者的主要并发症之一[1-2]。25G玻璃体切割术是目前临床治疗严重PDR的常用手段之一,其手术操作切口小,且能很好地维持眼内压稳定,但易发生术中、术后出血,影响手术进度和手术效果[3-5]。本研究对我院60例60眼PDR患者行雷珠单抗辅助25G玻璃体切割术治疗,并取得一定疗效,现将研究报告如下。
1对象和方法
1.1对象选取我院2014-10/2017-11就诊的PDR患者120例120眼作为研究对象。本研究经医院伦理委员会审核批准,入选标准:(1)所有患者均经血糖检查、肾功能检查、胆固醇血脂检查、眼底荧光血管造影等确诊,且符合《我国糖尿病视网膜病变临床诊疗指南》[6]中PDR诊断标准;(2)患者糖尿病视网膜病变分期均为Ⅳ~Ⅵ期;(3)患者均需存在手术指征;(4)患者均清楚本次研究目的和过程,并签署知情同意书。排除标准:(1)存在意识、语言障碍或精神疾病者,无法正常沟通交流;(2)血压、血糖无法稳定者;(3)存在严重心脏、肝脏、肾脏等全身疾病者。将PDR患者120例120眼随机分为两组,常规组患者60例60眼,其中男33例33眼,女27例27眼,年龄20~82(平均56.61±5.32)岁,糖尿病病程2~20(平均11.21±3.31)a;研究组患者60例60眼,其中男35例35眼,女25例25眼,年龄21~84(平均57.31±5.62)岁,糖尿病病程2~22(平均11.62±3.14)a。两组患者年龄、病程等各项临床资料比较,差异无统计学意义(P>0.05),具有可比性。

表1 两组患者术中和术后情况比较眼(%)
注:常规组:行25G玻璃体切割术治疗;研究组:给予雷珠单抗辅助25G玻璃体切割术治疗;-:表示采用Fisher确切概率法。
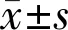
表2 两组患者手术前后眼压和BCVA情况比较
注:常规组:行25G玻璃体切割术治疗;研究组:给予雷珠单抗辅助25G玻璃体切割术治疗。
1.2方法
1.2.1术前准备完善所有患者术前常规检查,如最佳矫正视力(best corrected visual acuity,BCVA)、B超、黄斑OCT、眼压和裂隙灯显微镜等,术前3h经充分散瞳,患者空腹血糖均控制在8.0mmol/L以下。手术室内按内眼手术要求进行常规消毒铺巾。
1.2.2常规组常规组行25G玻璃体切割术治疗:20g/L利多卡因+7.5g/L布比卡因混合(2mL)球后麻醉,从角膜缘后4.0cm处穿刺,经睫状体平坦部切除中央区、周边部、基底部积血和病变玻璃体。电凝止血,眼底填充。术后常规氧氟沙星滴眼液滴眼,视网膜复位良好患者可在术后1~3mo行硅油取出。
1.2.3研究组研究组给予雷珠单抗辅助25G玻璃体切割术治疗。表面麻醉,冲洗结膜囊,距离眼角巩膜缘4mm垂直进针,0.5mL专用注射器向玻璃体腔内注射0.5mg雷珠单抗,压迫注射点出针,注射后3~5d行25G玻璃切割术。两组患者手术操作均由同一术者完成。
1.2.4观察指标术后随访6mo,对比两组患者手术时长、术中与术后情况、术后并发症,以及手术前后BCVA、眼压(正常值为10~20mmHg)和黄斑中心区厚度。术中与术后情况包括术后高眼压、术中电凝使用眼数、医源性视网膜裂孔眼数、术后虹膜新生血管形成(iris neovascularization,INV)共4项。术后并发症包括视网膜再出血和再增生等。
2结果
2.1两组患者手术时间比较常规组患者手术平均时长为80.11±18.22min,研究组患者手术平均时长为61.22±17.91min,常规组患者手术平均时长高于研究组,差异有统计学意义(t=5.727,P<0.05)。
2.2两组患者术中和术后情况比较常规组出现术后眼高压、术中出血明显使用电凝、医源性视网膜裂孔、术后INV等发生率均明显高于研究组,差异有统计学意义(P<0.05,表1)。
2.3两组患者术后并发症比较常规组术后6mo时共10例10眼(16.7%)出现并发症,其中3例3眼出现再出血,7例7眼出现再增生;研究组术后6mo时未见再出血,3例3眼出现再增生,并发症发生率为5.0%。常规组并发症总发生率高于研究组,差异有统计学意义(χ2=4.227,P<0.05)。
2.4两组患者手术前后眼压和BCVA情况比较两组患者手术前眼压和BCVA情况比较,差异均无统计学意义(P>0.05);手术后两组患者眼压和BCVA均有一定改善,研究组眼压低于常规组,且BCVA优于常规组,差异有统计学意义(P<0.05,表2)。
2.5两组患者手术前后黄斑中心区厚度比较术前两组患者黄斑中心区厚度比较,差异无统计学意义(P>0.05);术后6mo研究组黄斑中心区厚度得到明显改善,常规组改善情况不显著,且常规组黄斑中心厚度高于研究组,差异有统计学意义(P<0.05,表3)。
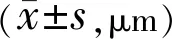
表3 两组患者手术前后黄斑中心区厚度情况
注:常规组:行25G玻璃体切割术治疗;研究组:给予雷珠单抗辅助25G玻璃体切割术治疗。
3讨论
玻璃体手术是目前治疗PDR患者唯一可行的方法,通过清除玻璃体中积血,使玻璃体及其增殖部位对视网膜的张力减轻,从而减轻视网膜的偏移[7-9]。由于视网膜解剖位置特殊,玻璃体和纤维血管膜与视网膜的紧密粘连在进行剥离时易引起出血,故减少术中和术后出血是PDR患者手术成功的关键[10-13]。雷珠单抗是专为眼科设计的第2代人源化的VEGF抑制剂,能完全渗透视网膜全层,可抑制新生血管形成,从而降低剔除增殖膜的难度,可降低并发症发生率[14-15]。
本研究对我院120眼PDR患者进行研究,结果显示,入选者术前眼压高于正常值,其原因是部分患者合并新生血管性青光眼所致。PDR患者视网膜血流状况的改变会引起视网膜缺血,导致视网膜新生血管形成,VEGF表达上调并直接作用于虹膜睫状体,引发INV形成。当病变进展到房角时,小梁网间隙新生血管的形成会导致房水受阻,最终使得眼压升高,新生血管性青光眼发生[16-17]。术后统计发现,研究组患者手术时间明显缩短;术后6mo眼高压、术中出血明显使用电凝、医源性视网膜裂孔、术后INV等发生率均降低,再出血、再增生发生率降低,眼压低于常规组,视力优于常规组。表明雷珠单抗的使用可有效缩短手术时间,降低围手术期不良事件发生率,缓解眼压,改善患眼视力。分析其原因,25G玻璃体切割操作过程中会出现持续性出血现象,术中需多次进行电凝止血;玻璃体切割术实施前注射雷珠单抗可促进部分新生血管闭合,加速新生血管膜萎缩,从而降低术中大出血风险,减少术中眼内电凝止血次数,降低对操作视野的影响,减少手术器械的更换、拿取次数,因此手术时间短;同时,雷珠单抗对手术视野的改善,不仅有助于增殖膜和混浊屈光间质的彻底清除,还可降低术中操作对视网膜的损伤,使得患者术后眼压和视力得到更好恢复,术后再出血率和再增殖率明显降低[18]。医源性裂孔是增殖膜剥离和血凝块切除过程中易出现的并发症[19]。雷珠单抗作为VEGF抑制剂可通过抑制新生血管形成,促进出血的吸收清除,避免凝血块与残留玻璃体、增生黏膜等粘连,从而降低医源性裂孔发生。眼高压和INV是玻璃体切割术后易诱发的常见并发症。硅油是玻璃体切割后主要填充性替代物,可为患者提供一个透明清晰的眼内介质,但该填充介质的使用会增加高眼压发生率[20]。而有报道显示,术前注射雷珠单抗可有效减少眼内填充物使用率[21]。同时,雷珠单抗可抑制视网膜新生血管,延缓病情进展,从而降低术后INV发病率。此外研究组术后6mo黄斑中心区厚度低于常规组,表明雷珠单抗辅助25G玻璃体切割术治疗患者可有效改善PDR患者黄斑水肿情况,使患者术后舒适度提高。
综上所述,雷珠单抗辅助25G玻璃体切割术用于治疗PDR患者可有效缩短手术时间,提高临床疗效,降低术后高眼压、医源性视网膜裂孔、术后INV等并发症,安全有效。但受条件限制,研究中纳入样本量少,研究过程中未对该治疗方案在PDR合并新生血管性青光眼患者治疗中的效果进行单独对比分析,需在以后研究中进一步探讨。
猜你喜欢
杂志排行
国际眼科杂志的其它文章
- Correlations among macular pigment optical density, central macular thickness and body mass index
- 超乳联合房角分离或小梁切除对PACG合并白内障患者血流动力学的影响
- 飞秒激光辅助白内障手术在硬核白内障患者中的应用
- Differences in pain and inflammation between Diclofenac 0.1% and Nepafenac 0.1% after cataract surgery
- 利用577nm阈值下微脉冲激光治疗糖尿病性黄斑水肿
- 隐形遮盖镜与压抑膜疗法治疗大龄单眼弱视的疗效比较
