钛系锂离子筛盐湖提锂的研究进展
2019-05-16曾文文何周坤詹浩然
潘 鑫,曾文文,何周坤,罗 楠,詹浩然*,梅 军*
(1中物院成都科学技术发展中心,成都绿色能源与绿色制造中心,四川成都610207)
0 前言
锂是自然界最轻的金属元素,有许多不同于其它金属的物理性质和化学性质,是极具前景的新型能源和战略资源[1],广泛应用于合金制备、电池、新能源、制药、润滑、橡胶、陶瓷、玻璃和空气处理等行业[2-4]。2017年全球碳酸锂的需求量为26.5万吨,相比较于2016年增长10%。预计2020年全球碳酸锂的需求量将达到40万吨,其中动力电池和消费3C领域对全球锂产量的增长贡献最大。2017年我国动力锂电池领域对碳酸锂需求量已达2.3万吨,较2016年增长39.2%。预计到2020年我国碳酸锂需求量将达6.4万吨,年平均增速预计将高达48%,动力电池领域成该产品增速最快的应用领域[5]。未来由于各国加大对新能源车的政策导向和投入,锂电池及相关行业的消费占比会继续增大,结果必然带动锂资源需求量的持续增长[6,7]。
在自然界中,锂的存在形式主要有矿石和盐湖卤水,代表形式为花岗伟晶岩和盐湖卤水锂床,资源所占比率分别为21.6%和78.3%。根据美国地质调查局(USGS) 2017年发布的数据,全球锂资源探明储量约为1400万吨,约占全球锂资源总储量的29.8%[8,9]。中国的锂资源储量非常丰富,已探明储量为320万吨,仅次于智利的750万吨,排名世界第二。其中,盐湖锂资源所占比率为78%,主要分布在西藏和青海等地[10]。传统锂产品的生产多是源于伟晶岩型矿石,技术成熟,应用广泛,可以制得高纯度的锂产品,但是由于固体锂矿储量不足,并且锂矿煅烧耗能高、污染严重,不利于长期发展,不能满足社会日益增长的锂需求。而对于盐湖锂资源的开采研究,从20世纪90年代开始,研究的盐湖提锂技术一经提出,迅速成为锂原料生产开发的热门研究技术,未来甚至有希望发展成为锂产品生产的主要技术手段。目前为止,盐湖提锂的主要方法有沉淀法、萃取法、离子筛吸附法、膜分离法、电渗析法和纳滤法等。沉淀法是传统的盐湖卤水提锂方法,适用于低镁锂比的盐湖卤水体系[11],例如智利的阿塔卡玛盐湖和美国的银峰盐湖,均使用沉淀法提锂并实现了提锂工业化生产[12]。但沉淀法对于高镁铝比的盐湖卤水,镁锂分离比低,生产的产品纯度不够,距离工业产品纯度有一定差距。萃取法对高镁铝比的盐湖体系有较好的提锂效果,并且也实现了工业化生产,但生产萃取剂需要的成本高,萃取过程常用的萃取剂酮、醚和有机磷等[13]易进入废液,因不能完全回收造成萃取剂回收率低,不环保,抑制了该方法的进一步发展。至于膜分离方法、电渗析法和纳滤法等则是比较新型的提锂方法,虽然可以应对复杂体系盐湖提锂,目前尚处于实验室研究阶段,距离工业化的道路还很长。与之相比,离子筛吸附法具有高吸附选择性,对镁铝的分离效果比较好等优点,而且工艺简单,原料廉价,安全环保,适用于不同条件的卤水体系,受到越来越多的关注。锂离子筛吸附法,目前为止研究最多的有两种体系:锰系离子筛和钛系离子筛[14]。锰系离子筛具有原料丰富,价格低廉,对锂选择性高,吸附量大等优点,但其在吸附循环的过程中由于锰元素的变价产生Mn2+,而Mn2+易溶于酸从而导致锰溶损过大的问题,目前研究者们正在尝试通过掺杂其它金属离子等方法降低其溶损率。钛系离子筛有着和锂离子筛相似的结构,更好的稳定性,更高的吸附容量,而且在循环使用过程中有着极低的溶损率,成为科学家们研究的热点。本文通过综述这些年来钛系离子筛的提锂机理、制备和性能以及实际应用的探索研究,对钛系离子筛在盐湖提锂当中存在的问题提出一些建议,并对未来钛系离子筛的发展进行科学的展望。
1 锂离子筛提锂机理
钛系锂离子筛主要有两种:层状结构的H2TiO3和尖晶石结构的H4Ti5O12,他们都是由前驱体Li2TiO3和Li4Ti5O12经过稀盐酸或稀硝酸等酸洗使H+替代原晶体结构中的Li+,变成H2TiO3和H4Ti5O12。锂离子筛吸锂/脱锂的机理目前尚没有达到广泛的共识,而且不同的结构也有不同的研究解释。
1.1 层状结构H2TiO3吸锂/脱锂机理
层状结构H2TiO3的提锂过程一般认为遵循离子交换机理。Chitrakar等[15]发现H2TiO3或Li2TiO3者的结构间隙只能够容纳Li+和H+,而其他阳离子如Mg2+、K+、Na+、Ca2+等极难进入层状结构中,因此认为该结构在以上离子混合的溶液体系中,层状结构只发生Li+和H+的互相取代置换过程,不涉及其它反应。该种材料的吸锂/脱锂过程如图1所示。

图 1 层状H2TiO3提锂过程(a) Li2TiO3结构(b) H2TiO3和(c) 正发生提锂的H2TiO3结构 [15]Fig.1 The process of lithium recovery by the layered H2TiO3(a)Crystal structure of layered Li2TiO3,(b)H2TiO3and (c)H2TiO3upon lithium exchange[15]
为了研究锂离子筛结构中不同状态锂的先后置换顺序,Hosogi等[16]将处理过的Li2TiO3和熔融的AgNO3一起放在300℃下加热。对合成的材料研究发现,Ag+不能置换出LiTi2层的Li+,但是可以置换出锂层中的Li+而形成一种结构式为Ag[Li1/3Ti2/3]O2的化合物。说明在H+置换出Li+的过程中,优先置换出Li+层的Li+形成H[Li1/3Ti2/3]O2,再置换出LiTi2的Li+形成H[H1/3Ti2/3]O2[17]。但是这个结果又不足以解释离子筛实际置换容量远小于理论值的实验现象。He等[18]通过一些实验发现Li2TiO3的吸锂量最大可达到57.8mg/g,距离该材料的理论值142.9mg/g差距较大,因而认为被H+取代形成的HTi2层不能被Li+重新取代。整个提锂过程如下所示:
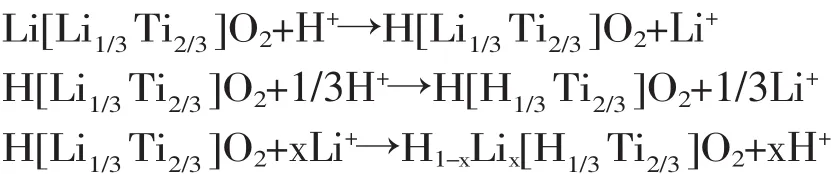
以上过程清楚地描述了H+和Li+的整个置换过程。此外,Zhang等[19]认为Li+易形成离子键,H+易形成共价键,在酸洗的过程中,Li+从Li2TiO3结构中脱出,H+同时进入Li+位,但由于H+是由静电作用掺进原结中,造成Li+和H+的替换非原位形成。这也是造成酸洗前后结构不同,进而导致离子筛吸锂量距离理论容量差距较大的原因。
1.2 尖晶石结构H4Ti5O12吸锂/脱锂机理
尖晶石结构H4Ti5O12的提锂机理,目前相关的报道不多。Vol'khin[20]制备了锆掺杂的尖晶石钛酸锂Li4Ti4.94Zr0.06O12,将其盐酸酸洗得到锂离子筛LiTiZr-H。通过研究晶体结构的变化发现,Ti4+有非常稳定的核外电子结构,导致其不易发生价态变化,故在酸洗和提锂前后,因其他位置(Ti、O、Zr) 的结构几乎不发生变化,只是氢离子和锂离子发生了互换。于是,他认为该锂离子筛的提锂过程是一个简单的离子交换过程,如下;
在酸溶液中,

在锂离子溶液中,
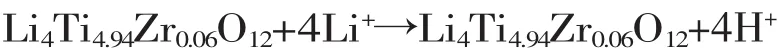
上述机理也能直观解释钛酸锂离子筛溶损率低,稳定性好等特性。董殿权等[21]重点研究提锂时的反应过程,他将Li+从液体进入离子筛的过程分为四步:对流扩散、液膜扩散、颗粒扩散、化学反应,将离子筛置于Li+浓度为20.0mmol/L的溶液中研究上述四个过程对提锂的影响。他发现颗粒扩散过程对离子交换过程起决定作用,故提出离子交换过程受制于颗粒扩散控制。这些只是对H4Ti5O12提锂的一些基础认识,尚需深入探索研究。
2 锂离子筛的制备方法
锂离子筛是由前驱体经过酸洗过程,使前驱体中的被H+取代,形成锂离子筛,锂离子筛前驱体的制备方法主要有固相法、液相法和模板法等。
2.1 固相法
固相法是制备锂离子筛前驱体最为广泛的一种方法,该方法具有工艺简单,原料来源广、易于产业化等优点。固相反应制备钛系锂离子筛,是将原料:锂源 (一般为 LiOH、Li2CO3、C2H3Li5O2、LiNO3等)和钛源(一般为TiO2)混合均匀,然后在一定温度、气体条件下高温煅烧一定时间得到前驱体材料,再用酸洗即得到锂离子筛。固相法的缺点是能耗大、易造成污染,制得的产物杂质含量高、易出现形貌不规则、颗粒尺寸不可控以及严重的团聚现象,影响所得产物的性能[22]。
层状Li2TiO3的固相制备研究已久,Onodera等[23]首先以LiOH和TiO2为原料通过固相反应制备出Li2TiO3,发现酸洗后的产物H2TiO3具有一定的锂离子吸附性能,进而开始引起其他研究者的重视。1991年日本通产省工业技术院东北工业试验所[24]将固相法制备的H2TiO3置于pH=8.5的含锂溶液提锂,通过分析上层水清液中的金属离子浓度,得出H2TiO3对不同金属离子的分配系数,发现该材料对锂有很好的选择性。Chitrakar等[15]以TiO2和Li2CO3为钛源和锂源,通过固相反应制备H2TiO3,在pH=6.5的酸性条件下,锂离子筛的提锂量可以达到32.6mg/g,优于同等条件下其它的锰系锂离子筛。我国对钛系锂离子筛的研究始于学者闫树旺等[25],他们以金红石型TiO2为原料,通过高温固相反应得到锂离子筛前躯体,然后用盐酸溶液酸洗制得二氧化钛锂离子塞,对锂的吸附容量达29.15 mg/g,而钛的溶损率则只有0.1%。为了降低钛原料成本,钟辉[26-28]和Tang等[29]分别以工业钛液和低纯度的含钛炉渣为钛源,制备出可用于提锂的H2TiO3,饱和吸附容量为分别为28.76mg/g和27.8mg/g。这种由廉价的钛原料制备锂离子筛的方法对工业化应用具有非常大的指导意义。考虑到用无机锂盐合成的锂离子筛颗粒容易团聚,从而影响离子筛的提锂能力[30],Gu等[31]以C2H3LiO2·2H2O和TiO2为锂源和钛源,乙醇作为分散剂,使C2H3LiO2·2H2O熔融再与TiO2充分分散,高温煅烧后,最终得到平均直径约为70nm的Li2TiO3颗粒,在pH=10.10的条件下测试,离子筛的锂吸附容量可达到40.16mg/g。至于尖晶石锂离子筛H4Ti5O12的提锂研究及前驱体的固相法合成报道较少。颜辉等[32]采用TiO2与Li2CO3为原料,严格控制二者的配比,并在不同高温条件下发生固相合成反应,生成锂离子筛前体Li4Ti5O12,再用盐酸酸洗得到锂离子筛H4Ti5O12,发现其在pH=10.0的锂浓度为5g/L的LiOH和LiCl混合溶液液中,饱和吸附容量可达到32.29 mg/g。
2.2 液相法
液相法是将反应物置于水中或溶剂中直接合成目标产物或者前驱体进而得到目标产物。常用的液相方法有水热法和溶胶凝胶法。
2.2.1 水热法
水热法通常是反应物在水或有机溶剂的水热釜中,在特定的温度下(一般不高于250℃),原料发生物理化学变化生成目标产物。溶剂热法制备离子筛材料有以下优点:反应过程中材料合成温度低、内部受热均匀、反应较快;制得的目标产物形貌好、含杂质少、颗粒粒径一般较小、不易团聚。Zhang等[33]以TiO2为钛源,先做如下预处理得到纳米级TiO2:TiO2与NaOH溶液混合超声,然后在175℃下水热反应48h,盐酸清洗后,然后用无水乙醇作分散剂烘干。最后再将得到的纳米级TiO2和Li2CO3按化学配比在900℃下焙烧24h得到Li2TiO3,再用盐酸酸洗得到H2TiO3。将离子筛置于锂离子浓度为69.41mg/L,pH=9.19的缓冲体系中做提锂吸附,发现该材料具有非常高的锂钠、锂钾、锂镁和锂钙的分离比,其分离系数可达到664.32、45369.51、813.98和3294.69。水热法合成材料往往受实验条件限制,不同的实验环境(如反应温度、反应时间、原料成分等)往往导致合成的产物物理化学性能有差异。为了合成结晶性良好的 Li2TiO3,Wang等[30]以TiO2、Li2CO3和四丁铵 (TBA) 等为原料先制备出Li2TiO3,再加热转化成为β-Li2TiO3,酸化后得到锂离子筛H2TiO3,在2g/L的LiOH溶液中,吸锂量最高可达到76.7mg/g,这在目前已有的文献报道中,是锂离子筛吸附容量最高的。与此同时,水热法制备尖晶石结构的Li4Ti5O12应用于离子筛研究也有不错的进展。Li等[34]以C12H28O4Ti和CH3COOLi为钛源和锂源,以聚苯乙烯为硬模板,通过水热反应制备出三维大孔-介孔锂离子筛3DM-H4Ti5O12,在0.05mol/L的LiOH溶液中进行提锂研究,一天后提锂容量达到5.51 mmol/g(38.24mg/g)。Moazeni等[35]则通过两步水热反应合成了Li4Ti5O12,第一步先以TiO2、NaOH等为原料水热合成前驱体沉淀物,再酸洗得到纳米钛管(TNT);第二步再以TNT和NaOH等为原料反应生成Li4Ti5O12,酸洗得到直径在100nm以下的纳米管状H4Ti5O12,在pH=9.17的锂浓度为0.5mol/L的LiCl-NH3H2O-NH4Cl缓冲溶液中,得到其饱和吸附容量约为39.43 mg/g,体现出不俗的吸锂性能。
2.2.2 溶胶凝胶法
溶胶凝胶法是以液体试剂为原料,并混合均匀,经过水解或聚合反应,使反应物分子量变大变成溶胶,经过加热等过程逐渐使溶胶变成凝胶,最后干燥焙烧得到目标产物。溶胶凝胶法制备钛系锂离子筛一般选用有机锂源和钛源在特定溶剂中混合交联形成凝胶,然后在特定温度下煅烧制成前驱体材料,最后酸洗即可得到锂离子筛。用溶胶凝胶法制备Li4Ti5O12[36]、Li2TiO3[37,38]很早就受到人们的关注,而且制备出来的材料颗粒比较均匀、不易团聚,表现出优秀的电化学性能,但是利用溶胶凝胶法制备钛系锂离子筛并将其应用于离子筛的研究报道则是近年才开展进行的。董殿权等[21]首先以 Ti(OC4H9)4、CH3COOLi为原料,柠檬酸为络合剂,制成混合干凝胶,然后在750℃下焙烧24h得到Li4Ti5O12,用盐酸酸洗得到Li+抽出率为81.5%,钛的溶损率在4.2%以下的锂离子筛H4Ti5O12,在0.1mol/L的LiOH溶液中进行提锂研究,得到锂离子筛的饱和吸附容量为42.30mg/g,优于固相法制备的离子筛性能。陈念[39]也以Ti(OC4H9)4、CH3COOLi为原料,通过改变原料配比制备出层状Li2TiO3,酸洗得到离子筛,发现其具有较高的Li+选择性,经过多次循环使用后,对 Li的饱和交换吸附量保持在18.62mg/g,Ti4+溶损率在 0.02%以下。为增加离子筛的吸附表面积,提高离子筛吸附效率,Zhang等[40]认为减小颗粒粒径可以增大离子筛比表面积,进而提高吸附效率。他以CH3COOLi和Ti(OC4H9)4为锂源和钛源,利用凝胶溶胶法,在650℃下合成出了粒径为60~80nm的Li2TiO3纳米材料,然后在70℃的条件下用0.25mol/L盐酸酸洗,锂的洗脱率达到78.9%,如图2所示。Li等[41]则巧妙地利用材料复合原理,以PVP为分散剂,LiOH和Ti(SO4)2为锂源和钛源,利用溶胶凝胶法,在500℃下烧结得到Li4Ti5O12微球,再通过水热反应和炭球复合得到核-壳结构的C@Li4Ti5O12。这种材料有着极高的比表面积201.74 m2/g,在pH=13的溶液中吸附效率极高,2h后即达到饱和吸附容量28.46mg/g。

图2 溶胶凝胶法在不同温度下合成Li2TiO3粉末以及脱锂Li2TiO3SEM示意图(a)500℃,(b)650℃,(c)800℃,(d)650℃,-脱出[40]Fig.2 SEM images ofLi2TiO3powders synthesized by the sol-gel process and calcined at various temperatures and Li+-extracted Li2TiO3(a)500℃,(b)650℃,(c)800℃,(d)650℃,Li+-extracted[40]
2.3 模板法
传统的固相法工艺简单,但是合成的固体粉体颗粒较大且不均匀,因而会影响其作为锂离子筛的提锂效率以及循环使用性能。因此一些研究人员为了提升钛系锂离子筛颗粒的比表面积以及材料的合成均匀性,通过制备孔状结构的模板,以模板为原料载体再结合固相、水热、溶胶凝胶等制备方法,合成出离子筛前驱体,然后除去模板,制得颗粒粒径更小,大小更为均匀的锂离子筛材料。郑建国等[42]运用模板法将化学性质稳定的锆离子掺入尖晶石钛酸锂结构中,以改善钛酸锂的提锂性能及稳定性,他以甲基丙烯酸己酯(MMA)为模板原料,通过乳液聚合技术制备出粒径大约100nm的聚甲基丙烯酸甲酯(PMMA)微球模板,进而制备出Li4Ti5-xZrxO12前驱体,0.2mol/L盐酸酸洗得到Li+脱除率为 87.26%的锂离子筛H4Ti5-xZrxO12,在Li+浓度为0.05mol/L的LiCl-LiOH体系当中进行提锂实验,测得饱和锂交换容量为50.61mg/g,达到理论值的79.7%。为了提高层状H2TiO3的提锂性能,提高提锂效率,Xu等[43]则以PS为硬模板,LiNO3和[Ti(OC2)3CH3]4为锂源和钛源,制备出了层状多孔结构的Li2TiO3材料,如图3所示。在强碱性条件下,离子筛吸锂容量可达76.3mg/g,并显示出良好的循环稳定性。另外,董殿权等先以聚苯乙烯(PS)微球为模板,通过溶胶凝胶法制备出三维有序大孔材料3DOMLi4Ti5O12,酸洗得到锂离子筛LiTi-H,测得其大孔直径约90 nm,而且酸稳定性好,对Li+的饱和交换容量达56.70mg/g[44]。又以聚甲基丙烯酸甲酯(PMMA) 为模板,LiAc2H2O和Ti(OC4H9)4为锂源和钛源,用溶胶凝胶法制备出了三维有序孔状结构Li4Ti5O12,制成的锂离子筛在80℃的条件下,对锂的饱和交换容量也高达56.81mg/g[45],显示出模板法制备的三维结构离子筛对材料提锂能力及效率的提升。

图3 SEM图 (a)无孔Li2TiO3(bare-LTO), (b)三维多孔Li2TiO3(porous-LTO), (c)无孔H2TiO3型锂离子筛 (bare-HTO), (d)三维多孔H2TiO3型锂离子筛 (porous-HTO)[43]Fig.3 SEM images of(a)bare Li2TiO3(bare-LTO), (b)three-dimensional porous Li2TiO3(porous-LTO), (c)bare H2TiO3-type LIS(bare-HTO),and (d)three-dimensionalporous H2TiO3-type LIS(porous-HTO) [43]
综上,锂离子筛前驱体的制备方法,各有优劣:普通固相反应工艺简单,易操作,制备的锂离子筛一般粒径较大,且大小不均匀,锂离子筛提锂容量较之其他相对较差,保持了不错的循环性。液相法制备的锂离子筛材料结构比较精细,提锂容量相对较高,循环性能好,但需要用比较昂贵的有机钛源,并且反应是在液体条件下进行,有大量的有机辅助试剂,工艺复杂,不易实现规模化应用,而且工艺比较难控制,制备的离子筛吸锂性能差异较大,往往需要反复尝试工艺。模板法得到的离子筛性能是所有方法里面最优的,由于该种方法往往可以制得颗粒均匀且比表面积大的材料,对材料的吸锂效率有明显的提高,但是模板法对模板的规格和品质要求比较高,所以选用功能性模板,好用易去除,结合溶胶凝胶法等,从而制得性能更好的锂离子筛。
3 锂离子筛应用研究进展
虽然钛系锂离子筛吸附提锂有着众多优点,并且已经取得了不错的研究进展,但由于粉体本身固有的流动性和渗透性差[46],要将钛系锂离子筛应用于实际的盐湖提锂工业当中,仍然面临着许多问题。例如现在锂离子筛使用的多是粉末,若将其直接投入卤水体系进行提锂作业,粉体在循环过滤过程中回收率低,损耗大,回收成本高,不利于工业化的实际应用。因此,需要将粉体加工处理,减少在循环过程中的损耗。常用的锂离子筛成型方法有造粒法、发泡法和成膜法。
3.1 造粒法
造粒法是最常用的离子筛粉末成型方法,通过粘结剂将离子筛粉末制成块状或粒装,然后将其用于盐湖提锂当中。造粒技术应用于锰系锂离子筛的研究比较广泛,常用的造粒剂或粘结剂有珪胶、水玻璃、聚氯乙稀 (PVC)等[8],而关于钛系锂离子筛造粒成型的研究报道相对较少。刘文涛等[47]以二甲基甲酰胺(DMF) 为溶剂,先溶解一定量的聚氯乙烯,再加入锂离子筛前驱体Li1.5Ti1.625O4,加入水锂离子筛前驱体颗粒,如图4所示。通过研究不同PVC含量对颗粒强度的影响,发现在PVC含量为15%时,颗粒强度可达99%。以0.5mol/L盐酸酸洗制得锂离子筛颗粒,发现锂的浸出量可达98%。将Li+质量浓度为11.62mg/L的石油咸水作为锂提取原液,发现该颗粒状锂离子筛的锂交换容量可达11.83mg/g,相比较造粒前26.4mg/g的交换容量有一些差距。陈自正等[48]以聚乙烯吡咯烷酮(PVP) 为粘结剂,Li2TiO3粉末为吸附剂,制成了粒状离子筛,经过优化试验,制成的离子筛的锂吸附容量为26.6mg/g,虽然吸附容量较高,但粉体脱落严重,吸附剂强度不高,容易破裂,稳定性不及其他造粒材料。综上,钛系锂离子筛造粒后基本可以达到预想的降低粉体的损耗,但是材料的提锂性能和稳定性尚需进一步研究。
3.2 发泡法

图4 15%PVC的Li1.5Ti1.625O4颗粒状前驱体示意图 [47]Fig.4 Photograph of the Granular Precursor Li1.5Ti1.625O4with 15%PVC[47]
发泡法是另一种非常有效的粉末成型方法,通过辅助发泡材料,将离子筛制成机械性能好的块状材料,进而应用于盐湖提锂工业当中。Lawrence等[49]以亲水性聚乙烯醇(PVA) 为发泡剂,溶于水后,加入酸洗过的Li2TiO3搅拌均匀后,在低温条件冷冻干燥,制得多孔泡沫材料HTO/PVA,如图5所示。经实验发现,该复合材料与纯粉体相比,最大提锂容量约为纯粉体材料的94%,动力学过程的拟合发现,复合材料的提锂效率与粉体相比仅降低了8%,将该材料用于海水提锂(锂含量约为7mg/L),提锂容量可达14.01mg/g。四川大学张理元等[50,51]则以堇青石基泡沫陶瓷为发泡材料,将该泡沫陶瓷、CH3COOLi和Ti(OC4H9)4等混合制成溶胶-凝胶,最后烧制成泡沫状的H2TiO3离子筛,将其放置在0.50g/L(pH=13.86)的Li+溶液中进行提锂研究,发现其提锂容量可达34.87mg/g,他还发现吸附剂对高浓度的Li+不具有富集的能力,而对低浓度的Li+具有富集的能力,当Li+初始液的浓度为0.1g/L时,最高可以富集26.55倍。离子筛的发泡成型可以在离子筛合成后进行发泡,也可用发泡剂为模板,直接在模板上合成离子筛,发泡后离子筛的提锂容量有所减少,但是却使离子筛的循环使用变得简单,但还需在循环性能上多做研究,提高其循环效率。

图5(a)复合材料HTO/PVA,纯PVA和HTO粉末的光学照片(b)纯PVA泡沫的SEM图(c)200%HTO/PVA泡沫SEM图(插图:低倍镜)(d)HTO/PVA的EDX图(插图:Ti map)[49]Fig.5(a)Optical images of composite HTO/PVA,pure PVA and HTO powder(b)SEM image of(b)pure PVA foam(c)200 wt%HTO/PVA foam(insets:lower magnification)and(d)EDXspectrum of HTO/PVA(inset:Ti map)[49]
3.3 成膜法
成膜法也是一种简单可行的离子筛粉末成型方法,该方法将有一定强度和粘性的成膜剂与离子筛粉末混合制成薄膜结构,再用于盐湖提锂。成膜可以增加盐湖卤水和吸附材料的接触面积,降低Li+扩散到锂离子筛内部的扩散阻力,提升提锂效率。膜成型的载体主要有PVC、聚讽、聚偏氟乙稀、多孔陶瓷等[52]。不过,目前锰系离子筛的成膜研究报道比较多,而关于钛系锂离子筛的成膜应用比较少见。Aya Umeno等[53]用DMF溶解PVC作为成膜剂,尖晶石锰酸锂作为离子筛,制成了PVC含量为20%的离子筛膜体,在海水中对Li+的平衡吸附容量可达2.30mmol/L(15.96mg/g)。为了提高膜体的提锂效率,Chung等[54]将锂离子筛粉体加入到自己制备的聚砜膜/无纺布/拭净纸制成的复合膜容器内,密封后用盐酸酸洗24 h(洗脱率99.5%)后最终制得复合膜提锂容器,该复合膜用于海水提锂,一天后即达到提锂平衡容量。王盼[55]分别以PVC、PVDF(聚偏氟乙烯)、PS(聚砜) 和PES(聚醚砜) 为成膜剂,以Li1.6Mn1.6O4为锂离子筛前驱体,混合均匀后制成锂离子筛前驱体膜,固化后用0.5 mol/L HCl处理,制得锂离子筛膜。将他们用于盐湖提锂,发现PVC-锂离子筛膜吸附容量大(0.16mol/m2),吸附速率快(3h达到平衡),效果好,而其他体系的锂离子筛膜则容量较低或是锂离子筛粉体脱落严重。综上,可以看出成膜会降低离子筛的提锂效率和容量,同时由于膜体往往比较薄,造成破损和粉体脱落严重,而且易污染、拆洗不方便,因此,将其应用于钛系离子筛的成型还需解决上述问题。
综上,前面介绍到的方法都具备了一定的工业化应用可能性,但是每种方法各有不足,造粒法简单有效,但提锂容量和效率较低;发泡法提锂量高,但技术复杂,发泡剂可选择性少;成膜法提锂效率好,但是膜体较薄,强度小,循环使用可操作性不强。而且上述方法均存在离子筛粉体易脱落的情况。因此仍需研究者深入研究,找到改进方法,或者提出其他更适宜的方法以实现钛系锂离子筛应用于盐湖提锂工业的研究。
4 展望
钛系锂离子筛作为一种新型的锂离子吸附剂,具有提锂容量高、选择性好、循环使用性好等优点,对于多离子混合盐湖体系或高镁铝比盐湖体系有着较好的锂分离效率。尽管如此,由于钛系离子筛的研究起步较晚,仍有许多问题值得科学家和研究者们进行深入的研究:1)钛系锂离子筛的提锂机理说法众多,各有依据,仍没有一套可以完全使人信服的机理解释提锂过程;2)钛系离子筛造粒、成型过程探究,做到保证提锂容量、效率和可应用性相结合;3)目前盐湖提锂研究重点是高镁铝比条件下,传统方法分离效果差。离子筛吸附有一定的可实用性,利用离子筛的安全绿色性,开发低污染环保的提锂工艺。总之,盐湖作为锂资源的重要来源,在未来锂工业的发展中有着非常重要的作用。利用锂离子筛吸附剂尤其是钛系锂离子筛吸附提锂在锂工业生产中,发挥着越来越重要的价值。未来,将有更多的研究方向关注于盐湖提锂的研究。同时,我们在专注于盐湖提锂的开发研究中,也应注意与之相关的副产品的开发研究,综合利用盐湖资源,实现可持续发展。
