Mn对Mg-3Al合金腐蚀性能的影响
2019-05-09姚胜
姚 胜
(中南大学粉末冶金研究院,湖南 长沙 410083)
镁合金的密度低、比强度高,在交通、航空航天等领域有着广泛的应用,耐腐蚀性差却是限制镁合金应用的一个瓶颈问题。合金化是改善耐蚀性的一种有效方法,Mn是镁合金中常见的添加元素。Mg-Al体系是商用镁合金AZ系列及AM系列的基础。然而人们对Mn对镁合金腐蚀性能的影响主要集中于商用多组元合金,对Mg-Al二元合金研究相对较少。目前,尚未见Mn对Mg-3Al合金腐蚀性能影响的系统研究。本工作制备了不同Mn含量的Mg-3Al-xMn合金,探究Mn对Mg-3Al合金微观结构及腐蚀性能的影响,并阐述其作用机理,为进一步设计耐腐蚀镁合金提供指导。
1 研究方法
1.1 试样制备
不同Mn含量的Mg-3Al-xMn(x=0,0.2,0.5(%))由电阻熔炼炉制备。制备过程如下:在含SF6和N2的氩气保护气氛下,纯度为99.95%的镁锭加热熔化并升温至690 ℃,随后将纯度为99.97%的铝锭及Mg-5Mn中间合金加入镁熔体中,并在690 ℃保温120 min,以使合金成分达到均匀。之后,将熔体倒入钢模中使合金随炉冷却,冷却后将合金取出。然后去除合金氧化皮,取铸件中部作试样,用原子发射光谱仪(ICP)检测样品成分。合金实际成分如表1所示。样品在400 ℃箱式炉中均匀化退火15 h。
1.2 试样检测
打磨抛光处理后的样品采用JXA-8530F型电子探针(EPMA)观察显微组织及元素分布。为了显示晶界,以高氯酸乙醇(5v%)作为电解液,样品在15 V的直流电源下电解抛光30 s左右。
采用采用静态失重法测定合金在3.5% NaCl溶液中浸泡3 d的腐蚀速率(约25 ℃)。打磨好的样品用无水乙醇清洗、冷风吹干后称重,再悬挂浸泡在300 mL 3.5% NaCl溶液中3 d。之后在铬酸溶液(200 g/L CrO3+10 g/L AgNO3)中浸泡7 min去除腐蚀产物,用无水乙醇清洗、冷风吹干后再次称重,记录腐蚀前后重量变化,取3次实验平均值计算平均腐蚀速率。采用Helios NanoLab G3 UC型场发射扫描电镜(SEM)分析试样在3.5% NaCl溶液中浸泡3 h后的腐蚀形貌。
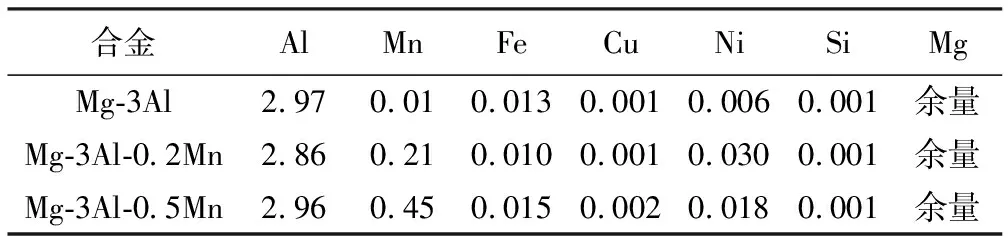
表1 Mg-3Al-xMn(x=0,0.2,0.5)合金实际成分(%)
2 结果与讨论
2.1 微观结构
图1~3分别为Mg-3Al、Mg-3Al-0.2Mn、Mg-3Al-0.5Mn合金在200倍EPMA下的显微组织及合金元素分布。

图1 (a) Mg-3Al合金200倍下EPMA形貌;(b)~(d) 分别为Al、Mn、Fe的元素分布

图2 (a) Mg-3Al-0.2Mn合金200倍下EPMA形貌;(b)~(d) 分别为Al、Mn、Fe的元素分布

图3 (a) Mg-3Al-0.5Mn合金200倍下EPMA形貌;(b~d) 分别为Al、Mn、Fe的元素分布
图1(a)、图2(a)、图3(a)中黑点为凝固过程中产生的缩孔,白色颗粒为中间化合物颗粒,其余为α-Mg基体。由图所示,随着Mn含量增加,合金晶粒尺寸却无显著变化,这表明Mn对铸造Mg-3Al合金不产生晶粒细化作用,这与文献中报道的相一致。Wang等研究了γ2-Al8Mn5与α-Mg的晶体学取向关系,结果表明γ2-Al8Mn5不能作为α-Mg的形核核心,因此不细化镁合金晶粒尺寸。
由EPMA结果可知,相对于Mg-3Al合金,Mg-3Al-0.2Mn和Mg-3Al-0.5Mn合金中白色颗粒的Mn含量高很多。对白色颗粒的成分进行定量分析,结果如表2所示。值得指出的是,由于Mg-3Al合金中的颗粒比较小,而电子束有一定直径,因此打到了Mg基体,因此显示含有比较多的Mg。颗粒中Mn含量很少(约2at%),这表明其很有可能为某种Al-Fe相。从Mg-Fe相图可知,Fe在Mg中溶解度极低(约5×10-6),因此,在无Mn的情况下,Al与Fe容易形成Al-Fe相。
表2 Mg-3Al-xMn(x=0,0.2,0.5(%))合金中中间化合物的成分(at%)
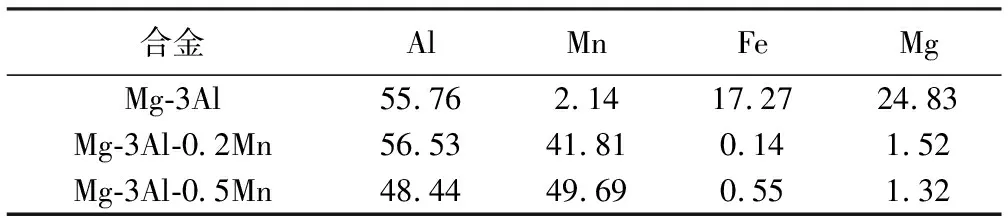
合金Al Mn Fe Mg Mg-3Al55.762.1417.2724.83Mg-3Al-0.2Mn56.5341.810.141.52Mg-3Al-0.5Mn48.4449.690.551.32
结合Al-Mn相图,从成分来看,Mg-3Al-0.2Mn及Mg-3Al-0.5Mn合金中的颗粒为γ2-Al8Mn5。而且γ2-Al8Mn5中含有少量的Fe,这是因为Fe的原子半径与Mn相似,可以相互替换。此外从图1(a)、图2(a)、图3(a)可知,随着合金中Mn含量升高,白色颗粒数量也增加,这表明γ2-Al8Mn5数量随Mn含量增加而增加。
2.2 腐蚀性能
图4为Mg-3Al-xMn(x=0,0.2,0.5(%))合金在3.5% NaCl溶液中浸泡3 d的腐蚀速率。由图可知,随着Mn含量增加,合金腐蚀速率逐渐降低。Mg-3Al合金的腐蚀速率约为Mg-3Al-0.2Mn合金的5倍、Mg-3Al-0.5Mn合金的15倍。这表明Mn的添加能显著改善Mg-3Al合金的耐蚀性。
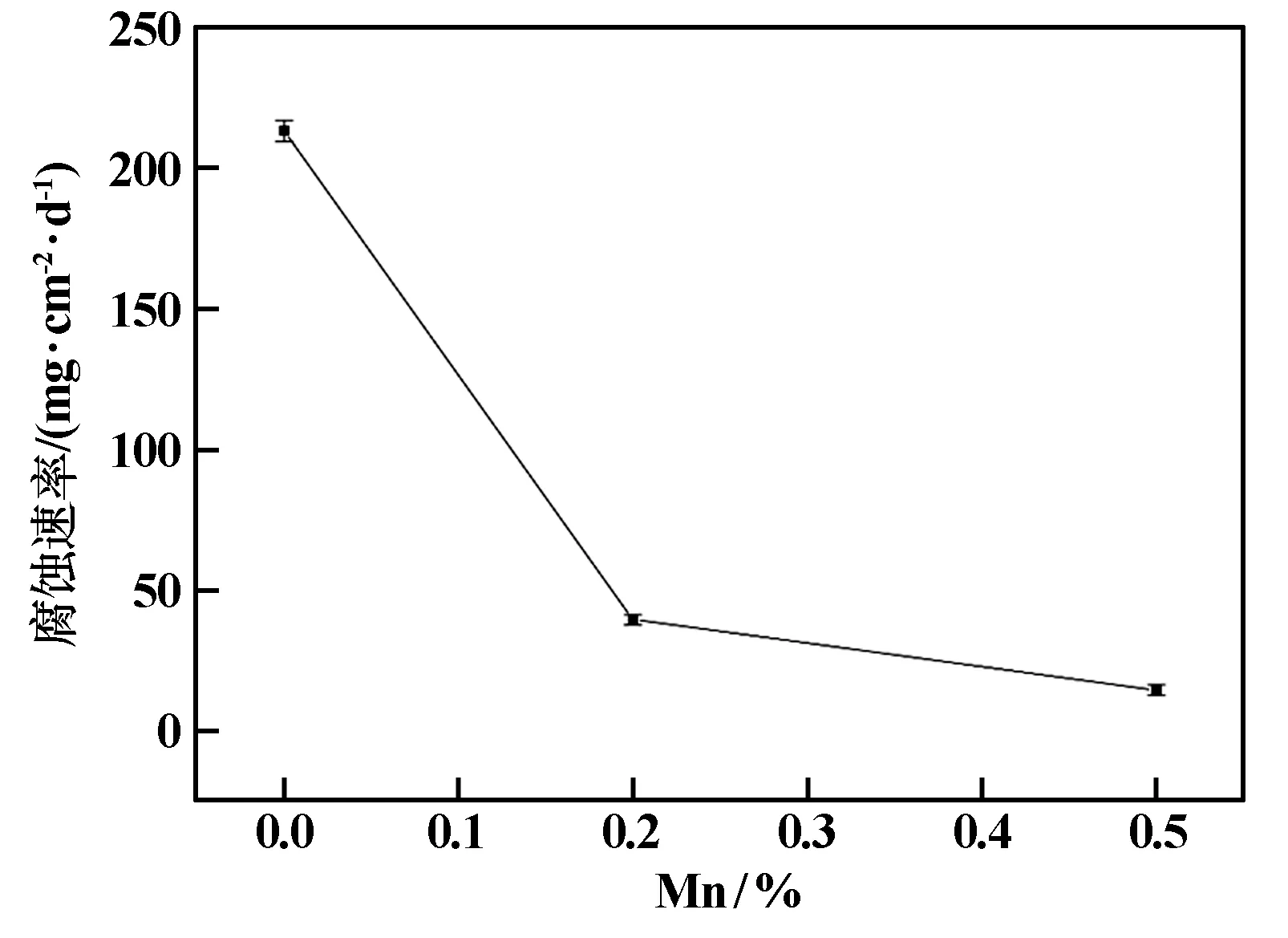
图4 Mg-3Al-xMn(x=0,0.2,0.5(%))合金在3.5% NaCl溶液中浸泡3 d的腐蚀速率
图5为Mg-3Al-xMn(x=0,0.2,0.5(%))合金在3.5% NaCl溶液中浸泡3 h后并去除腐蚀产物的SEM形貌图。由前文可知, Mg-3Al合金中白色颗粒为Al-Fe相,Mg-3Al-0.2Mn和Mg-3Al-0.5Mn合金中白色颗粒为γ2-Al8Mn5相。从腐蚀形貌来看,各合金镁基体均发生严重腐蚀,而中间化合物Al-Fe相、γ2-Al8Mn5相尚未发生明显腐蚀,这表明中间化合物与镁基体间存在微观原电池,且镁基体作为阳极优先腐蚀溶解。
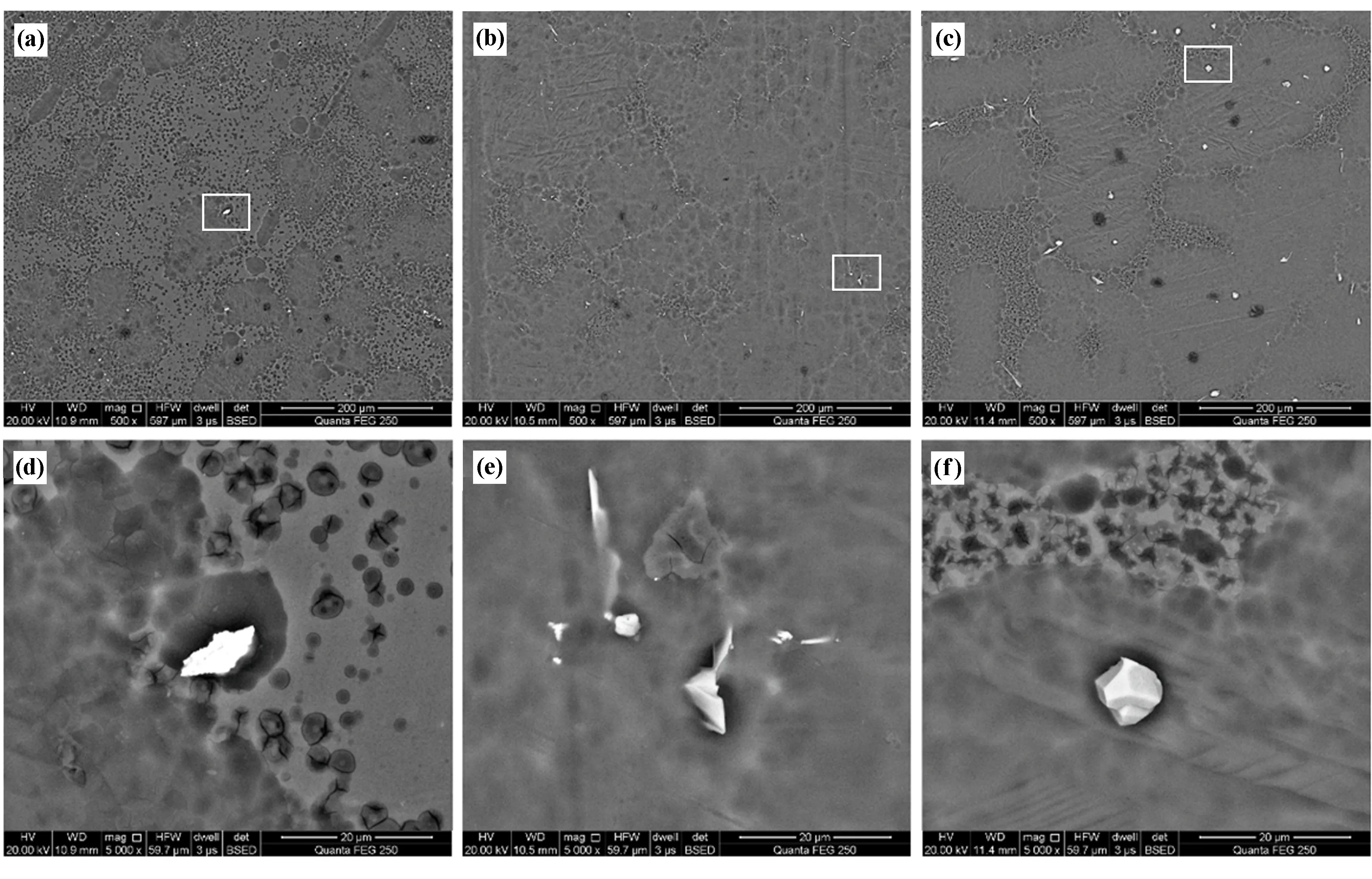
图5 实验合金腐蚀3 h后的SEM形貌
从腐蚀机理来看,有文献报道,Al-Fe相通常与α-Mg基体构成微观原电池,且由于Al-Fe相的电位相对α-Mg基体正很多,因而作为原电池的阴极加速α-Mg基体腐蚀溶解。当合金中添加Mn元素后,合金中会生成γ2-Al8Mn5相,尽管γ2-Al8Mn5与α-Mg基体之间仍然会形成微观原电池,但由于γ2-Al8Mn5相与α-Mg基体间的电位差较Al-Fe相与α-Mg基体电位差小很多,因此微观原电池的加速效应被大大抑制,进而镁合金耐蚀性得到大大改善。
3 结语
随着Mn的添加,Mg-3Al合金中的Al-Fe相转变为γ2-Al8Mn5相,后者数量随着Mn的增加而增加。添加Mn显著改善合金耐蚀性,这与Al-Fe相变为γ2-Al8Mn5相有关,因为中间化合物与镁基体之间的微观原电池效应受到抑制。因此,在含Al镁合金中适当添加Mn元素,能改善耐蚀性,进而扩大镁合金的应用。
