肝移植常见肝脏恶性肿瘤的病理分类及其临床特点
2019-05-08王政禄丛文铭天津市第一中心医院病理科天津300192
王政禄,丛文铭(天津市第一中心医院病理科,天津 300192)
肝移植已成为治疗终末期肝病最为有效的方法之一,与其他器官移植不同,符合标准的肝脏恶性肿瘤也被列为肝移植适应证并可取得很好的疗效。肝移植不仅可以彻底清除肿瘤,还能消除原肝新发肿瘤的风险。肝移植术后肿瘤复发是影响移植效果的主要因素,因此,原发肿瘤准确、详细的病理学诊断和评估有助于指导临床制定合理的治疗方案,降低肿瘤复发风险。根据《消化系统肿瘤WHO分类(第四版)》将肝脏肿瘤分为上皮性肿瘤、混合性或来源不明的恶性肿瘤、间质肿瘤、生殖细胞肿瘤、淋巴瘤和继发性肿瘤,其中恶性肿瘤中以肝细胞癌最为常见,本文将主要介绍肝移植中常见恶性肿瘤的病理学特点,其他少见类型可参考相关病理学专著。
1 上皮性肿瘤:肝细胞性
1.1 肝细胞肝癌(hepatocellular carcinoma,HCC):肝细胞癌的大体分型以癌结节的数目和大小为依据。目前,我国多数采用“中国常见恶性肿瘤诊治规范”中的大体分型标准(表1)。肝细胞癌结节呈球状,边界不清,无明显包膜,但边界尚清,肿瘤周围可有“卫星结节”围绕。切面颜色质地各异,多数呈灰白色实性,质地较软。
镜下显示:① 高分化,癌细胞呈多角形,胞浆丰富,颗粒状,嗜酸或轻度嗜碱性,有时出现胆汁色素。细胞核大,核膜厚,染色质多集中于核膜周围,核仁大,明显嗜酸性(图1)。② 低分化,癌细胞明显间变,细胞异形,胞浆少且嗜碱性,细胞核明显增大,深染,核浆比例增高,有时可见核内嗜酸性包涵体。肝癌细胞常向血管渗透,形成癌栓,以静脉为多。微血管浸润(microvascular invasion,MVI)表现为内皮细胞衬覆的血管腔内的癌细胞巢团(图2)。MVI以癌旁肝组织、门静脉为主,偶可侵犯肝动脉、胆管和淋巴管分支。MVI的组织学类型主要包括小静脉癌栓、小动脉癌栓、小胆管癌栓、包膜血管癌栓、淋巴管癌栓和悬浮癌细胞。MVI是肝癌患者预后的重要预测指标,应将全部组织切片内的MVI进行计数,并根据 MVI的数量和分布情况进行风险分级:① M0未发现MVI;② M1(低危组)肿瘤细胞5个MVI,且发生于近癌旁肝组织区域(≤1 cm);③ M2 (高危组)>5个MVI,或MVI发生于远癌旁肝组织区域(>1 cm)。研究报道MVI是肝癌肝移植术后肿瘤复发风险的独立预测因素,因此,在病理报告中应详细描述MVI情况,有助于临床制定科学的移植术后治疗方案。部分肝细胞癌中可出现其他类型的癌细胞,需注意与其他肿瘤细胞鉴别(表2)。
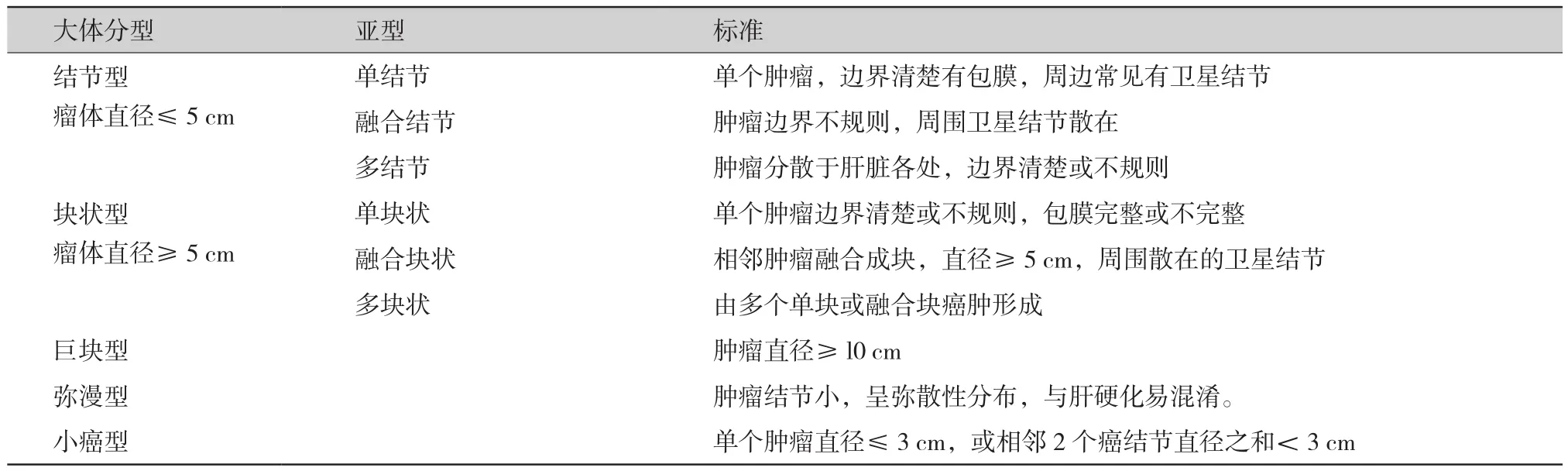
表1 肝癌分型标准
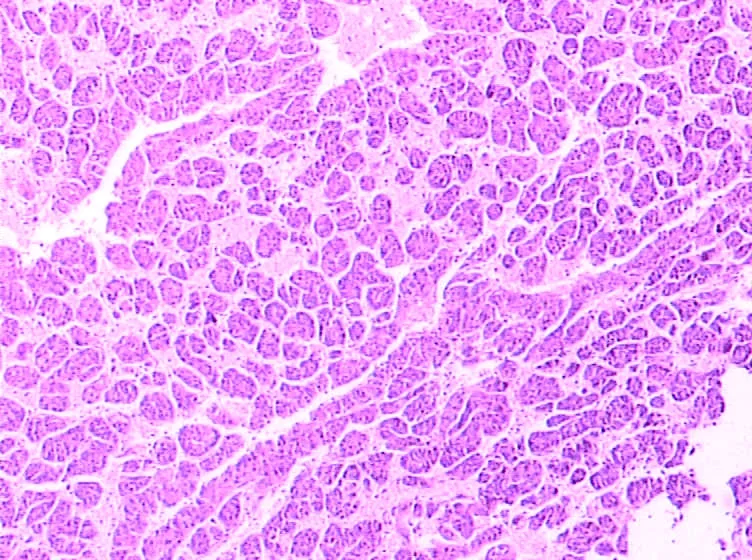
图1 肝细胞癌梁索型
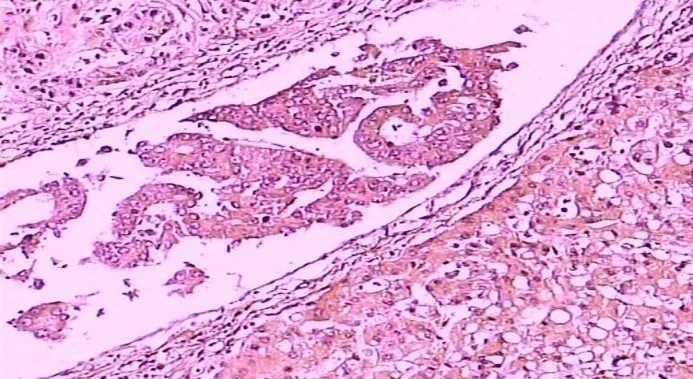
图2 癌细胞巢团(MVI)
HCC的组织学分型包括梁索型(最常见的组织学类型)、假腺管型(又称假腺泡型)、致密型(实体型和团片型)、菊型团型、硬化型、紫癜型和自发坏死型。同一肝癌的各部分组织结构可以不同,故分型应以主要形态为主。目前普遍采用的HCC分化分级标准仍为Edmondson-Stelner四级分级法(表3)。
肿瘤的不同部位往往分级有异质性,一般以级别高者为准。同时也需强调,单凭形态有时难以明确级别。Ⅰ级肝细胞癌应与肝腺瘤、良性反应性增生结节和不典型增生结节(交界性结节)鉴别。对分级难以确定者,可描述为诸如Ⅰ~Ⅱ级、Ⅱ~Ⅲ级或Ⅲ~Ⅳ级。HCC病理分级作为临床治疗、预后的一项参考指标,通常分级越高,预后越差。HCC的生物学行为与预后有直接的关系,HCC的侵袭性生长方式有侵犯包膜、血管和胆管(图3)、神经及周围肝组织。肝癌的转移途径中影响因素甚多,包括年龄(年轻者较多转移)、癌细胞的侵袭性、肿瘤的分化(分化差者多转移)以及是否伴肝硬化(不伴者84%,伴肝硬化者60%有转移)等。转移主要有血道转移(最为常见,其中90%为肺转移,其次为脊椎骨、股骨、肾上腺、肾及脑等)、淋巴道转移(相对较少,主要累及肝门淋巴结)和种植性转移。多结节及多块状型HCC的克隆起源分型与肝转移术后复发具有相关性,其中单中心肝内转移型复发风险明显高于多中心发生型,有条件的单位应进行肿瘤克隆起源分型检测。
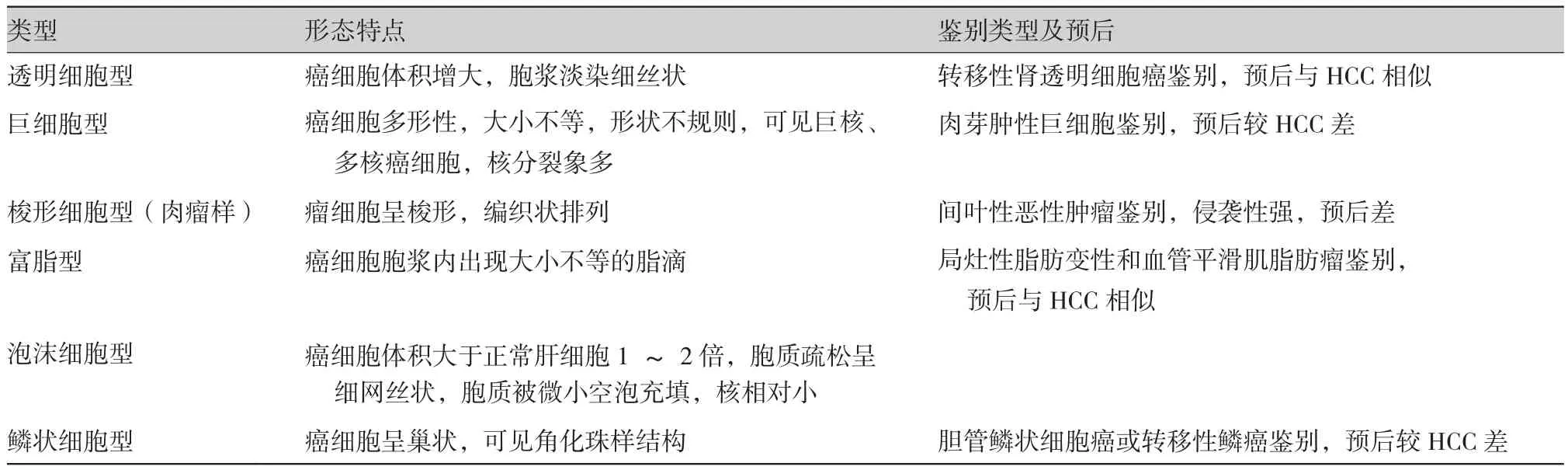
表2 不同细胞类型HCC的形态特点、鉴别诊断及预后特点

表3 HCC分化分级标准(Edmondson-Stelner四级分级法)
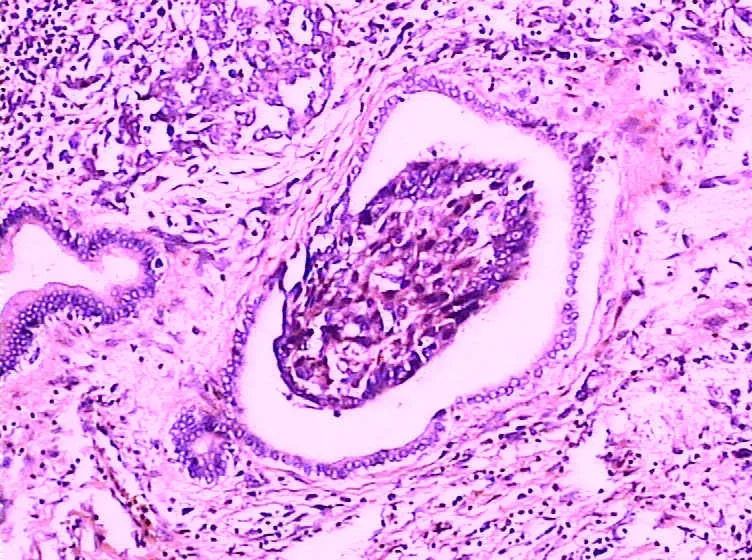
图3 胆管内瘤栓
1.1.1 小肝癌:又称“亚临床肝癌”是指单个癌结节直径或相邻两个癌结节直径之和<3 cm。多以单结节性、膨胀性生长为主,肿瘤多呈球形,边界清楚,约67%有完整的包膜,直径在2.5 cm以下的小肝癌也可无明显包膜或无连续性包膜形成,但边界仍较清晰。切面组织均匀致密,可见纤细的放射状纤维分隔,类似于肝细胞性瘤样结节,可有少量出血坏死,少有肉眼可见的癌栓。小肝癌中仅3%伴卫星结节,在距肿瘤1.5 cm以外的肝组织内很少有卫星结节或转移灶形成。小肝癌的分化多与肿瘤大小有关,约60%的小肝癌呈Ⅰ或Ⅱ级高分化表现,极小的肝癌(75%)以Ⅰ级分化为主。癌细胞可仅有轻度异型,细胞大小较为一致,胞质嗜酸性增强,或可因含有糖原和脂肪而呈空泡状,核染色加深,核/质比值轻度增加,核分裂象少见。癌细胞多排列成细梁型,可有局部假腺管结构,也可有门管区残留。肿瘤间质内可有小巢状生长,但包膜多较完整,其中30%可见包膜中有癌细胞浸润,但包膜突破率仅为大肝癌的20%。邻近肝组织内多无明显侵犯。约30%的小肝癌可见MVI,个别直径仅0.8 cm的小肝癌已显示肿瘤浸润血管和癌栓形成。
1.2 纤维板层型肝细胞癌(fibrolamellar hepatocellular carcinoma,FHC):1980年Craig首次报道,肿瘤生长缓慢、预后较好,多见于青少年及壮年,其中90%发生于35岁以下,女性多见。90%的患者无肝硬化病史,与乙型肝炎病毒(hepatitis B Virus,HBV)感染和乙醇无关,少数患者甲胎蛋白(alpha fetoprotein,AFP)可轻度升高,血清维生素B12、转钴胺素和神经紧张肽可升高。肿物多单发,直径较大(3~25 cm),有包膜。切面结节状,纤维瘢痕或卫星状纤维瘢痕灶为大体特点。镜下肿瘤细胞较大、多边形,胞浆明显嗜酸性,可见嗜酸性小球及胆色素颗粒。核仁明显,鹰眼状,核分裂少见。癌巢被丰富致密的板层状纤维(Ⅰ、Ⅲ、Ⅳ型胶原)组织有规则的围绕、排列(图4)。
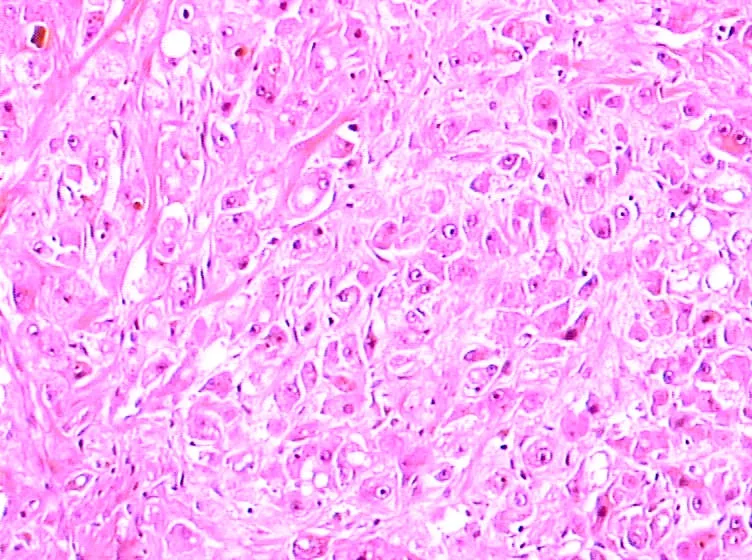
图4 纤维板层肝细胞癌
1.3 肝母细胞瘤(hepatoblastoma,HB):HB是发生于儿童的肝脏常见恶性肿瘤,占儿童肝脏原发恶性肿瘤的52%~62%。平均发病年龄16个月,几乎不发生于青少年。近半数患者伴有先天性异常,如先天性心脏病、肾发育畸形或多发性结肠息肉。血清人绒毛膜促性腺激素、睾酮、AFP可升高,尿中胱硫酶升高。肿瘤通常为单个实性肿块,多位于肝右叶,直径5~25 cm。镜下依据上皮细胞分化的不同分为上皮型和上皮-间叶混合型。其中上皮型又分为胎儿型、胚胎型、粗梁型和小细胞未分化型4个亚型。上皮型最为常见,肿瘤细胞呈梁状、索状、条带状、腺泡状及菊形团状等排列。瘤细胞圆形或立方形,细胞比正常肝细胞小,如6~8周的胎肝细胞。瘤细胞胞浆内嗜酸性增强和富含脂肪或糖原,而导致出现明暗交替的排列(图5)。小细胞未分化型为HB中分化最差的一型,瘤细胞呈松散的片状或巢状分布,细胞边界不清,核分裂易见,有黏液或纤维基质,可出现间叶成分,如骨样基质、软骨、横纹肌、神经、脂肪等,即为上皮-间叶混合性。
2 上皮性肿瘤:胆管性
2.1 肝内胆管癌(intrahepatic cholangio carcinoma,ICC):是肝内胆管上皮最常见的恶性肿瘤,占肝脏恶性肿瘤的5%~25%,年龄通常较肝细胞癌者大。ICC包括发生于肝内胆管的胆管细胞癌和Hering氏管上皮发生的肝内恶性肿瘤,通常被分为外周型和肝门型,前者来自肝内二级分支以下胆管树上皮的腺癌,即通常所称的ICC,后者来自肝门部左、右肝管和肝总管的腺癌。ICC的男女之比为2.3:1,平均年龄51岁。外周型ICC通常呈现出与肝细胞癌相似的临床特点,血清AFP多为阴性,CA 19-9升高,部分患者癌胚抗原升高。ICC有多种分型,Ohashi等(1994年)将ICC分为:① 结节型,形成明显的肿块,边界较清楚;② 管周浸润型,肿瘤沿胆管壁扩展,致管壁明显增厚,不形成明显的结节;③ 结节浸润型,肿瘤呈多结节浸润性生长,边界不清。ICC以肝左外叶多见,瘤体直径2~15 cm,切面灰白色,实性,质硬,具有浸润性边界,癌旁有肝硬化者少见。典型的ICC为分化好至中度分化的腺癌,癌细胞有胆管上皮细胞特点,可呈立方、柱状或多形性,胞浆较透明,但有时可呈颗粒状。核较小,核仁不明显。大多数细胞可证实有黏液分泌现象,但无胆汁形成。癌细胞常排列成明显的腺样结构,其中以管状腺癌最多见(图6)。少数可呈乳头状腺癌,偶尔可见分化差的多形性腺癌、黏液性或印戒细胞癌、腺鳞癌、黏液表皮样癌、类癌或未分化癌。有时部分癌细胞可排列成狭窄的管状结构,呈紧密的团块状结构者罕见。同一肿瘤中,组织学表现常较均一,但少数病例亦可呈现多种分化程度不同的组织学形态。丰富的纤维性间质是胆管细胞癌的一个重要特征。细胆管细胞癌是发生于细胆管或Hering管的一种特殊类型的胆管细胞性肝癌,约占原发性肝癌的1%。癌细胞均一呈小立方形,胞浆稀少,椭圆形核,核仁不明显,类似Hering管上皮。癌细胞排列成实性细索状,或为密集而规则的小腺管状但缺乏明显的腺腔,纤维间质丰富。
2.2 肝外胆管癌:肝外胆管癌按癌细胞类型分化程度和生长方式分为6型:① 乳头状腺癌;② 高分化腺癌;③ 低分化腺癌;④ 未分化癌;⑤ 印戒细胞癌;⑥ 鳞状细胞癌等。最常见的组织学类型为乳头状腺癌、高分化腺癌,占90%以上。典型的肝外胆管癌显示大小不一、不规则的扩张腺体伴黏液合成,细胞多形和核染色质丰富,偶见微乳头结构。常见广泛的肝门浸润和神经周围侵犯。偶见胆管上皮内瘤变。
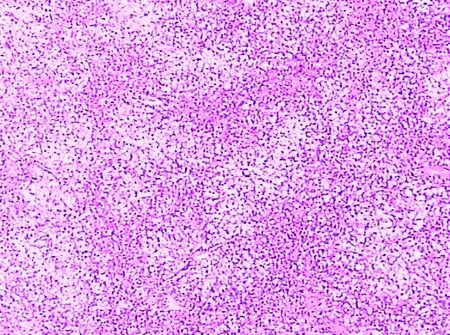
图5 肝母细胞瘤
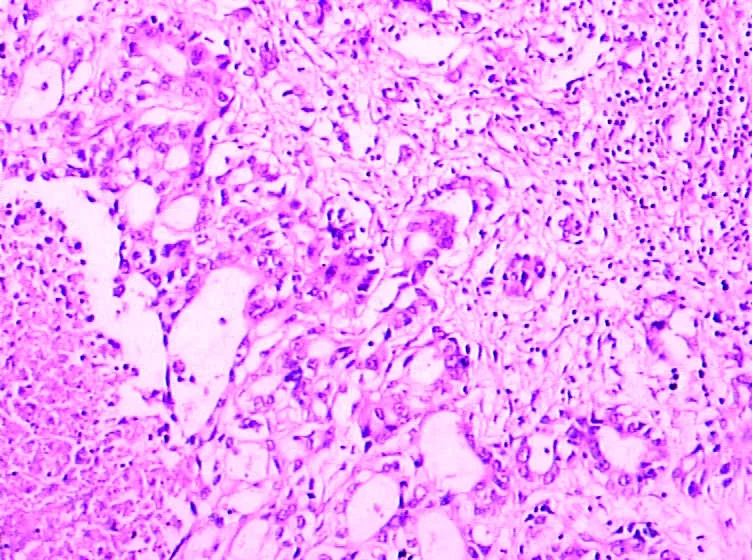
图6 肝内胆管癌
2.3 肝门部胆管癌(hilar cholangio carcinoma,HCCA):肝门部胆管癌也称Klatskin瘤,是胆道系统常见的恶性肿瘤。肝门部胆管癌因其发生部位特殊、呈浸润性生长及与肝门部血管关系密切等特点给手术切除造成极大的困难。肝门部胆管癌的组织病理类型以腺癌居多(占90%以上)。按大体形态可分为:① 硬化型:胆管壁环形增厚,常伴管周组织的弥漫性浸润和纤维化;② 结节型:坚硬不规则瘤结节突入胆管腔,与硬化型特征可伴随出现;③ 乳头型:质软而易碎的息肉样组织占据胆管腔;④ 浸润型:沿胆管壁广泛浸润,管壁增厚、管腔狭窄,管周结缔组织明显炎症反应,与硬化性胆管炎不易区别。美国癌症联合委员会肝门部胆管癌的TNM分期(第七版)如下(表4)。
3.4 胆管囊腺癌:肿瘤多呈球形,表面光滑,有纤维包膜。切面为囊实性或多房性囊性肿块,囊内壁光滑,或呈颗粒状或乳头状嵴,囊腔常含黏液状甚至胶冻状物,或稀薄的黄棕色蛋白液。囊壁内衬胆管型上皮,细胞立方形或柱状,胞质嗜酸性,胞核位于细胞基底部,细胞核异型明显,病理性核分裂象活跃,肿瘤细胞可排列呈乳头状结构,形成囊性乳头状腺癌,囊壁基底膜可衬覆黏液分泌细胞,腺腔扩张,腔内含有黏液和坏死物,呈囊性黏液腺癌特点。
3 混合性或来源不明的恶性肿瘤
3.1 混合型肝细胞和胆管癌(combined hepatocellular and cholangio carcinoma):指同一肿瘤中含有明确的肝细胞癌和胆管细胞癌两种成分混合构成,发生率不到肝脏肿瘤的5%。男性略多于女性,约60%可伴有肝硬化,血清AFP和(或)CA l9-9升高,临床特点和HCC相似,属于高侵袭性肿瘤,术后生存率比单纯性HCC差。根据组织学结构不同,可有3种类型:① 胆管细胞癌和肝细胞癌两种成分截然分开。② 两种成分镶嵌混杂排列。③ 两种成分密切混杂,其中可有过渡的双向分化现象。混合性肝癌的组织发生有以下三种可能性:① 双癌;② 肝细胞或胆管上皮发生癌变后部分恶变细胞向另一种方向转化;③ 来自干细胞的向肝细胞或胆管上皮两种方向分化。混合细胞型肝癌大体特点类似于HCC。镜下显示HCC区域呈梁索状、假腺管状或致密型,癌细胞多边形,间质成分少,梁索间衬覆血窦。胆管癌区域呈腺管样或梁索状结构,癌细胞呈立方形,间质纤维组织丰富(图7)。对于血清AFP水平很高,但瘤组织呈胆管癌特点,或血清CA l9-9水平很高,但瘤组织呈HCC特点,均应再增加取材数量,以确定是否为混合型肝癌。
3.2 癌肉瘤:肝脏上皮性恶性肿瘤成分合并各种间叶性肉瘤成分,也称恶性多形性腺瘤。肿瘤上皮性成分以肝细胞癌为主,也可是胆管癌、神经内分泌癌或未分化癌等,肉瘤成分以骨肉瘤和软骨肉瘤多见,也可为横纹肌肉瘤、平滑肌肉瘤、恶性纤维组织细胞瘤、纤维肉瘤、恶性神经鞘瘤以及未分化梭形细胞肿瘤等成分,上皮和间叶两种成分之间可有移行过渡。
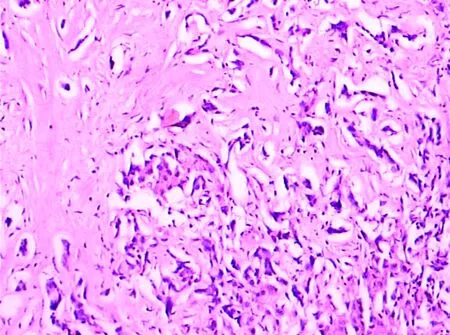
图7 混合细胞型肝癌
4 间质肿瘤
4.1 血管肉瘤:血管肉瘤是一种高度恶性血管性肿瘤,是肝内最常见的肉瘤。多见于老年男性,常迅速转移到脾脏,淋巴结、肺、骨和肾上腺。血管肉瘤形成许多界限不清的大小不一的结节,结节质软、海绵状伴出血和坏死。肿瘤由多形性梭形或上皮样细胞构成,常见怪异或多核细胞及核分裂象,瘤细胞呈“靴钉样”衬于血管壁上,肿瘤无完整包膜,瘤细胞沿血窦、终末肝静脉和门静脉分支的内皮扩散,在肝板上呈支架样或覆盖式生长,致肝板解离,肝细胞萎缩或消失,快速生长的瘤组织内可见残留的肝细胞条索。
4.2 上皮样血管内皮瘤(epithelioid hemangioendothelioma,EHE):是一种低度恶性的血管肉瘤。常见于中年人,2/3为女性。典型的表现为质硬、灰色肿瘤,细胞构成呈条索状,周边或进展前沿细胞较多。中央区细胞减少、硬化或钙化,移行区为黏液样或软骨样。肿瘤细胞呈树突状或上皮样,瘤细胞体积中到大,呈圆形或不规则形,胞质丰富嗜酸性,有大核仁,特征性的形成胞质内空腔,核偏位,类似印戒样细胞形态,具有细胞内血管样腔隙,内可有红细胞。上皮样瘤细胞向周边肝血窦和终末肝静脉内浸润性生长,可于终末肝静脉和门管区门静脉分支内形成瘤栓,可导致血管腔完全机化性闭塞。

表4 肝门部胆管癌的TNM分期标准
4.3 胚胎性肉瘤(未分化肉瘤)〔undifferentiated(embryonal) sarcoma,UES〕:UES 主要发生于儿童和青少年,75%以上为6~15岁,90%<21岁,女性多见。UES肿瘤成分复杂多样,多无包膜,质软,呈明胶状,灰白、灰黄或灰褐色,囊实性,多数有囊性退行性变、出血和坏死。囊腔直径大小不等,囊内含棕色凝胶样内容物。镜下瘤细胞呈梭形、星状或多形性,常可见到怪状核或多核,核畸形深染,核分裂象多见,核仁明显,核/质比值增大;在间质内见到凋亡小体是UES的一个重要诊断特征,PAS染色可见较多大小不等的嗜酸性小体。病变周边常可见到扩张的胆管和肝细胞索。
4.4 恶性纤维组织细胞瘤(malignant fibrous histiocytoma,MFH):肝MFH的组织学形态类似于软组织的MFH,瘤细胞的高度多形性和席纹生长方式是其两个重要的镜下特征。组织学类型分为车辐状-多形性型、黏液型、巨细胞型、炎症型、血管瘤样型。Li等(2008年)将肝脏MFH的分化程度分为3级:Ⅰ级:梭形瘤细胞有轻度多形性细胞核,松散稀疏分布于黏液变性的基质内,核分裂少见(<5/10HPF),无肿瘤坏死;Ⅱ级:梭形瘤细胞有多形性不规则细胞核,呈漫性车辐状生长,局部可见多核巨细胞,核分裂数(10~12)/10HPF,肿瘤坏死范围约20%;Ⅲ级:瘤细胞杂乱排列,多形性多染色质细胞核,核分裂数>20/10HPF,常有异型核分裂,肿瘤坏死范围>20%,怪异巨核细胞多见。
4.5 Kaposi肉瘤(Kaposi sarcoma,KS):KS 多见于后天免疫缺乏综合征(AIDS)患者(>90%)和器官移植后患者。肝KS病灶分布具有特征性,为多发性散在分布、大小不一、棕褐色的海绵状病灶,以门管区为中心,病灶界限不清,直径1~2 cm,类似血肿或血管瘤。KS以梭形瘤细胞增生、不规则的毛细血管腔隙、红细胞外渗、含铁血黄素沉积以及慢性炎性细胞浸润为基本特征。病变主要累及门管区及门管区周围,表现为门管区梭形细胞结节,大多数可见PAS阳性嗜酸性小体,瘤细胞常侵犯门静脉血管壁肌层、周围肝血窦和肝板。
5 继发性肿瘤
在欧美等西方国家,转移性肝癌的发生率明显高于原发性肝癌,而在我国由于后者的发生率较高,导致前者的发生率较低。原则上转移性肝癌患者不适宜接受肝移植手术,但少数低度恶性的转移性肝癌(转移性类癌),移植后仍有较长的生存时间,因此,术前明确肿瘤性质非常重要。转移性肝癌中30%~50%经门静脉转移,多见于直肠癌、胃癌和胰腺癌。乳腺、泌尿生殖系统、甲状腺、支气管等恶性肿瘤可由肝动脉系统转移至肝脏。胆囊癌可经淋巴管或直接蔓延转移至肝脏。转移性肝癌血清AFP多正常,无HBV或HCV等HCC相关病毒感染,肝硬化者少见。肿物多为单个结节,大小不等,也可为弥漫性分布。较大肿物由于中心坏死可在肿瘤表面形成“脐凹”,边界清楚,可有包膜。镜下与其原发部位的肿瘤相似,但分化程度可发生变化,侵犯门静脉者少见。结合病史和免疫组化染色,有助于确诊(图8)。
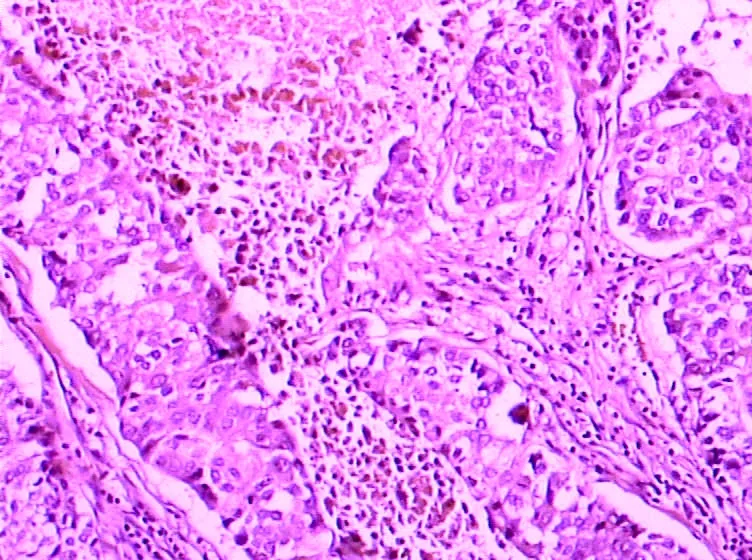
图8 转移性肝癌,结肠腺癌肝转移
