PD-1单克隆抗体成功逆转3例多线治疗失败的难治性霍奇金淋巴瘤
2019-04-25曹婷雍李亚茹贾永前
曹婷雍,李亚茹,吴 俣,刘 霆,贾永前
(四川大学华西医院血液科/血液病研究室,成都 610041)
程序性死亡蛋白-1(PD-1)是表达于活化T细胞表面的抑制性受体,其配体PD-L1和PD-L2主要表达在抗原提呈细胞及各种肿瘤细胞表面,染色位点是9P24.1[1]。生理情况下PD-1/PD-L信号通路抑制T细胞的功能[2]。肿瘤细胞会表达过量的配体PD-L1及PD-L2,通过PD-1/PD-L1 信号通路发生免疫逃逸。经典型霍奇金淋巴瘤(cHL)的特征是霍奇金淋巴瘤肿瘤(Hodgkin reed-sternberg,HRS)细胞染色体9P24.1位点表达增强[3],HRS细胞高表达PD-L1和PD-L2,cHL便通过PD-1/PD-L通路发生了免疫逃逸,而且位于9p24.1 染色位点的另一个JAK2基因也表达增强,该基因通过JAK2/STAT通路也会促进PD-L1和PD-L2表达增多,提示阻断该通路是治疗cHL的有效途径[3-4]。
PD-1单克隆抗体研究最多的有nivolumab和pembrolizumab,两者都是高度选择性人源性IgG4同型性抗体。Checkmate 039是nivolumab(3 mg/kg,2周1次)治疗复发难治性cHL(r/r cHL)最早的Ⅰ期的临床研究[5],纳入23例r/r cHL患者,78%的患者为自体干细胞移植(ASCT)和靶向CD30的抗体(brentuximab vedotin,BV)治疗失败的患者,87%的患者既往化疗方案至少大于3线,结果整体反应率(overall response rate,ORR)87%,完全缓解(complete response,CR)19%,部分缓解(partial response,PR)74%,24个月的无进展生存期(PFS)为46%。严重的药物不良反应(3/4级)为22%,但是大部分药物不良反应是可逆的。
本研究院报道3例r/r cHL经PD-1单克隆抗体治疗获得显著的缓解反应(3例均获得PR),仅有1级药物相关不良反应发生,无严重药物相关不良反应。
1 资料与方法
1.1一般资料 3例患者均为2016年7月至2017年12月在四川大学华西医院诊断为r/r cHL的患者,均签署治疗同意书,患者基线特征见表1。
1.2治疗方案 PD-1单克隆抗体约2 mg/kg,3周1次,常规检测指标为血常规、肝肾功能、甲状腺功能、NK细胞、T细胞亚群和免疫球蛋白,每个月通过CT或超声评估治疗反应。
2 结 果
病例1,男,27岁,诊断cHL(结节硬化型)。PD-1抗体治疗前东部肿瘤协作组(ECOG)3~4分,Ⅳb期。患者对标准ABVD(4)及G-ABVD(2)方案治疗均耐药,再行GemOx(2)及STANFORD V(1)方案同样耐药,后行RD方案姑息治疗,患者病情仍进展,双侧颈部、腹股沟多部位淋巴结持续肿大、融合,最大淋巴结长约6.2 cm,严重压迫气管及脏器、血管等。患者对一线、二线化疗均无效,为多线治疗失败的r/r cHL,充分沟通后行pembrolirumab单克隆抗体单药(100 mg/次,3周1次)治疗。累积用药400 mg时患者获得显著缓解。用药12周后,患者自行购药换为nivolumab单克隆抗体,方法剂量同前,共用药18次。PD-1抗体治疗后全身情况从ECOG 3~4分恢复到ECOG 0分,全身肿大淋巴结缩小大于75%,达到PR,全身淋巴结变化及一般情况见表2。患者输注nivolumab时出现全身轻度皮疹,可自行缓解,偶感气紧,予以盐权异丙嗪片50 mg对症处理后缓解。患者已停药10个月,PFS 21个月,目前从事轻体力劳动,无任何药物依赖。
病例2,女,17岁,诊断cHL(倾向混合细胞性)。PD-1单克隆抗体治疗前ECOG 2分,Ⅲa期。行G-ABVD(6)方案治疗后仅有左侧腋窝残留淋巴结。休息4个月后全身多部位(包括脾脏)肿瘤复发,行DHAP+VCR(3)方案治疗后仍有腹腔淋巴结残留病灶。再行GVD(1)方案及放疗(15)后达CR。遂行自体造血干细胞移植(ASCT)。移植半年后患者再次出现颈部、腹部多部位肿瘤复发,行BV+GDP(3)方案治疗,淋巴结缩小不明显,患者经一线、二线、ASCT、BV+GDP治疗后均复发难治,遂行nivolumab单克隆抗体单药治疗,单药治疗3个周期后长大脾脏缩小超过50%,达到PR,见图1。目前已行nivolumab治疗8个周期,PFS 6个月,ECOG 0分,在家休学,定期用药。

表1 3例复发难治的霍奇金淋巴瘤均予以PD-1单克隆抗体治疗
G-ABVD:吉西他滨+阿霉素+博莱霉素+长春新碱+达卡巴嗪;GemOx:吉西他滨+奥沙利铂;STANFORD V:阿霉素+长春花碱+氮芥+长春新碱+博莱霉素+依托泊苷+泼尼松;RD:雷那度胺+地塞米松;DHAP+VCR:顺铂+阿糖胞苷+地塞米松联合长春新碱;GVD:吉西他滨+长春瑞滨+脂质体多柔比星;GDP:吉西他滨+顺铂+地塞米松;BV:brentuximab vedotin;BEACOPP:博来霉素+依托泊苷+多柔比星+环磷酰胺+长春新碱+甲基苄肼+泼尼松;c:PD-1单克隆抗体治疗获得最佳反应时的分期及ECOG评分
表2 病例1在PD1单克隆抗体治疗前后一般情况及淋巴结大小变化比较
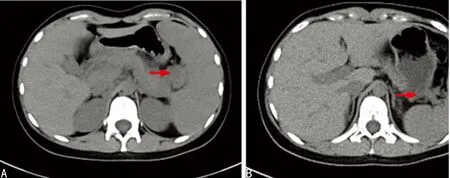
病例3,男,45岁,诊断为霍奇金淋巴瘤(混合细胞型),PD-1抗体治疗前ECOG 2分,Ⅱa期。行标准的ABVD(10)、BEACOPP(8)、放疗(22)方案治疗后获得 CR,无病生存16年。1年前以“右侧腋窝淋巴结肿大、左前胸壁肿大软组织团块”复发,ⅡE期。患者要求行nivolumab治疗,单药治疗3个周期后左胸壁肿大组织缩小大于50%,右侧腋窝淋巴结完全消失,见图2。患者输注nivolumab期间出现轻度疲乏,可自行缓解。目前患者已行nivolumab治疗8个周期,PFS 6个月,ECOG 0分,从事办公工作,定期用药。
A:经nivolumab治疗前脾脏大小;B:治疗3个周期后CT提示腹部淋巴结及脾脏明显缩小
图1 病例2

A:经nivolumab治疗前左前胸壁软组织包块大小;B:治疗3个周期后CT提示左前胸壁软组织包块大小明显缩小
图2 病例3
3 讨 论
霍奇金淋巴瘤是血液系统常见的恶性肿瘤之一,约80%患者经一线治疗能治愈,但仍有15%~20% Ⅰ/Ⅱ期患者及35~40% Ⅲ/Ⅳ或具有危险因素的患者在一线治疗后复发,部分患者原发难治。目前对于复发或难治的患者,主要的治疗措施是大剂量化疗和ASCT、挽救放疗及异基因干细胞移植(allo-SCT)[6]。r/r cHL在过去生存时间只有几周至几个月。近年来,靶向药CD30抗体BV取得较好的临床反应,1项Meta分析纳入903例经BV单药治疗的r/r cHL,整体反应率66.9%(CR 31.8%,PR 35.1%),1年PFS为47.6%及OS 79.5%[7]。对于ASCT及BV治疗失败的患者,目前没有标准的治疗方案,对于这些患者仍然需要探索新的治疗方案。其中PD-1单克隆抗体对霍奇金淋巴瘤的治疗成为新的研究热点[8-9]。
HRS细胞是霍奇金淋巴瘤的肿瘤细胞,分布在由大量的免疫细胞和基质细胞组成的微环境中,免疫细胞主要是CD4+辅助T细胞及调节T细胞,而HRS细胞数只占1%~5%[10],而这些T细胞的表面广泛表达PD-1,与HRS细胞过表达的配体PD-L1及PD-L2结合形成PD-1/PD-L通路,保护HRS细胞的生存。研究也证实HRS细胞的染色位点9P24.1表达增强,而9P24.1编码产物是PD-L1、PD-L2和JAK2,后者活化JAK/STAT通路,也会导致HRS细胞表达过量的PD-L1、PD-L2[3-4]。研究报道40%的cHL患者EB病毒阳性,而EB病毒与HRS细胞表达过量的PD-L1、PD-L2相关[11]。
Checkmate 039[5]、Checkmate 205[12]、Keynote 013[13]和Keynote 087[14]这4个研究均提示PD-1单克隆抗体对r/r cHL有很高的临床反应率,整体反应率依次为87%、66%、65%、70%。Checkmate 039已在前面介绍,Checkmate 205是关于nivolumab(3 mg/kg,2周1次)治疗r/r cHL的1个多中心多队列单臂二阶段试验,80例经ASCT及BV治疗均失败,治疗前患者接受化疗的中位方案数为4种,ORR 为66%(CR 9%,PR 58%),PFS达15个月。最常见(1/2级)的药物相关不良反应(≥15%)包括疲劳、输液相关反应和皮疹,严重的药物不良反应(3/4级)包括脂肪酶增加(8%)、中性粒细胞减少(5%)、转氨酶升高(4%)。Keynote 013研究使用pembrolizumab(10 mg/kg,2周1次)治疗的31例r/r cHL,55%的患者治疗前已经至少尝试4线方案,71%患者行ASCT治疗后复发,所有患者行BV治疗仍不能缓解,PD-1单克隆抗体治疗后结果ORR 为65%(CR 16%,PR 49%),6个月PFS为69%,1年PFS为46%,并且无严重的不良反应及死亡事件,3级药物相关不良事件5例(16%)。Keynote 087研究使用pembrolizumab(300 mg,3周1次)纳入210例r/r cHL患者,根据入组前接受化疗方案的不同分为3组研究,第一组纳入69例经ASCT、BV均治疗失败的cHL患者,98.6%的病例治疗前接受3线以上化疗,结果ORR为73.9%(CR 21.7%、PR 52.2%);第2组纳入81例经化疗、BV治疗不适合做ASCT的cHL病例,结果ORR为64.2%(CR 24.7%、PR 39.5%);第3组纳入60例经ASCT治疗失败,但没有接受BV治疗cHL患者,结果ORR为70.0%(CR 20.0%、PR 50.0%)。该研究总体ORR 为69%(95%CI:62.3%~75.2%),CR为22.4%(95%CI:16.9%~28.6%)。常见药物不良事件(1/2级)为发热(11.0%)、甲状腺功能减退(10.5%)、血小板减少症(1.0%)、腹泻(1.0%);严重的不良事件(3/4级)为中性粒细胞减少(1.4%),血小板减少(1.0%)、腹泻(1.0%)。
因此,PD-1单克隆抗体在治疗r/r cHL患者有明确的临床疗效,尤其是多线化疗、BV治疗、ASCT后仍不缓解及复发的患者,PD-1单克隆抗体具有很高的治疗反应,整体反应率可达65%~87%,无进展生存时间显著提高。其治疗的安全性及患者耐受性良好,大多数不良反应以1/2级药物不良反应事件为主,3/4级药物不良反应非常少见。
本研究病例ORR 100%,不良反应轻微,与文献数据相符。病例1取得显著PR,该患者经5线方案化疗均未缓解,仍有全身多处淋巴结肿大,累及肺部、胸壁乳腺区及T12胸椎,为原发多线治疗失败的r/r cHL,Ⅳb期,患者本身病情重,选择PD-1单克隆抗体,取得非常意外的治疗效果,目前患者已停药10个月,至随访日PFS为21个月。病例2为多线治疗失败、BV及移植后复发的患者,对于这种患者目前尚无有效方案可选,PD-1单克隆抗体提供了一种不良反应轻微,治疗效果却非常显著的选择,因治疗周期较短,已经取得明显的缓解,需要跟进治疗及观察是否能取得CR。病例3为复发的霍奇金淋巴瘤,仅治疗3周期就几乎取得CR,无不良反应,相比于传统的大剂量化疗方案,治疗周期短,不良反应轻微,耐受性好,同样因治疗周期短,需要跟进治疗及观察是否能取得CR。
因考虑患者的经济问题,本研究使用较低剂量PD-1单克隆抗体(2 mg/kg,3周1次),3例患者整体反应率100%,几乎无不良反应。而以上已报道的研究中使用的剂量分别是:3 mg/kg、2周1次,10 mg/kg、2周1次,300 mg、3周1次,反应率为65%~87%,患者的不良反应较多。CHAN等[15]报道了5例r/r cHL在使用较低剂量pembrolizumab(100 mg,3周1次)时获得100%的整体反应率,其中4例经多线化疗及BV治疗失败的cHL患者平均用药在495 mg获得CR,中位治疗周期为16(14~25)个周期,ORR为100%(CR 80%,PR 20%),PFS达18个月(9~18个月),仅有1例患者出现了1级不良反应腹泻及湿疹,证实低剂量的PD-1单克隆抗体在低成本及低不良反应的情况下获得很好的治疗作用。
霍奇金淋巴瘤特有的HRS细胞上PD-L1、PD-L2的基因表达增强,介导了肿瘤细胞的免疫逃逸,PD-1单克隆抗体在r/r cHL中的治疗反应率高,耐受性好。少数研究也证实低剂量的PD-1单克隆抗体治疗效果更好,且不良反应更少,从经济和治疗效果上考虑,低剂量PD-1单克隆抗体可作为r/r cHL的一种选择。
