基于可视化软件eChem的分子立体构型学习
2019-04-22芦瑞刘英涛
芦瑞 刘英涛

摘要:化学是基于原子、分子水平上研究物质的一门基础学科。在高中化学中涉及了大量的分子立体构型,然而,高中学生尚处于具象思维向抽象思维过渡阶段,缺乏对微观粒子构型的空间想象能力,因此,将分子构型可视化显得尤为重要。為学生正确理解分子构型提供帮助,将eChem软件应用于高中化学学习中,通过软件将微观粒子可视化帮助学生树立微粒观,进而建立微观与符号之间的联系。
关键词:eChem;立体构型;可视化
文章编号:1008-0546(2019)02-0007-02 中图分类号:G633.8 文献标识码:B
化学是在原子、分子水平上研究物质的组成、结构、性质、转化及其应用的一门基础学科,其特征是从微观层次认识物质,以符号形式描述物质,在不同层面创造物质[1]。化学将学生的视角从宏观物体带向微观粒子领域,体现物质的宏观性质和微观结构的双重表征,帮助学生理解微观粒子结构与化学符号之间的联系。然而,处于高中学习阶段的学生思维虽已超越了对具体的可感知事物的依赖,但仅能初步从多维度对抽象的性质进行思维[2],这就限制了学生对分子立体构型的空间想象能力,导致其在学习分子立体构型知识过程中遇到困难,这在某种程度上也促进了一些教学辅助软件的发展。同时,2017年版《普通高中化学课程标准》已明确指出信息技术与课程整合的必要性。因此,将软件技术融入教育教学中已成为教学改革的一大趋势。在化学教学中,教师要示范性地指导学生运用化学软件学习化学,让化学软件成为学生学习化学的辅助性工具,进而提升学习化学的兴趣。
一、分子立体构型学习的得力助手——eChem
众多化学软件如Diamond、GaussView5.0、Authorware、Chem3D等都可绘制分子模型进行分子立体构型的学习,但由于这些软件界面复杂,教师在研读使用说明和制作分子模型上会耗费大量时间,学生学习化学软件时也会产生困难。在新课标中,学业要求表明学生要学会分析简单的分子空间构型,人教版选修3《物质结构与性质》一书分子立体构型的章节中就有利用计算机软件制作分子立体模型的实践活动,因此,寻找一款简便、易操作、实用性强的软件是必要的。本文倡导的eChem是一款国外开发的界面简洁、操作简单并可有效地将信息技术融入化学课程中的软件。借助计算机软件模拟的直观手段,可充分发挥学生自己动手搭建分子结构活动的作用,降低教学内容的抽象性,促进学生对分子立体构型相关内容的理解和认识,发展学生“宏观辨识与微观探析”的化学学科核心素养[3]。
二、eChem软件在分子立体构型学习中的应用
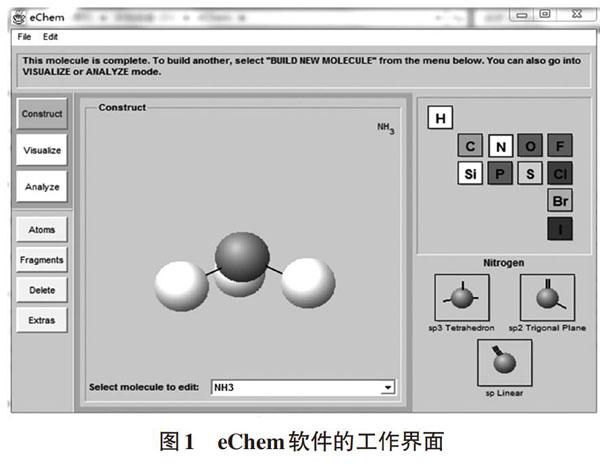
eChem是一个化学软件包,是由密歇根大学教育学院研制和开发的[4],该软件可以创建虚拟的三维分子模型,同时可以实现在一个界面内将多个分子形象化,包含分子的模型构造和分子的性质比较。如图1所示,eChem主要包括三个工具:Construct(构造分子模型)Visualize(形象化比较分子)和Analyze(分析分子性质)。eChem软件有两个版本,即网络版本和应用程序版本,安装时任何一种版本都适用于Windows或Mac操作系统。使用说明详见网址:http://www.hi-ce.org/echem/index.html。
1.辅助无机分子立体构型学习
学习无机分子立体构型时,教师可示范性地应用eChem软件进行教学,指导学生软件的使用方法。学生根据价层电子对互斥理论计算出中心原子孤对电子数和价层电子对数推测出VSEPR模型,进而得知分子的立体构型。要验证某分子的立体构型正确与否,可依据中心原子的杂化轨道类型并在eChem软件中绘制分子的立体构型进行判断。
以中学化学中常见的H2O分子和NH3分子为例,学生在初步学习分子立体构型知识时通常会产生这样的困惑:H2O分子和NH3分子的中心原子的轨道杂化类型都是sp3且VSEPR模型都是四面体,但为何H2O分子的实际立体构型是V型,而NH3分子的实际立体构型却是三角锥型?通过分析可知,H2O分子中存在两对孤对电子,而NH3分子中存在一对孤对电子,导致分子立体构型不同。对此,学生无法将抽象的理论与具象的立体结构联系在一起,从而导致学习分子立体构型遇到困难,其实我们完全可以借助eChem软件进行辅助学习。在H2O分子中,中心原子氧原子的杂化轨道类型为sp3,学生可在eChem软件中找到中心氧原子杂化方式为sp3的氧原子,点击选择,在construct界面单击便绘制出了中心原子氧原子,然后选择氢原子,此时便绘制出了H2O分子的空间构型,即为V型。绘制NH3分子时,中心原子为氮原子,氮原子的杂化轨道类型为sp3,在eChem软件中找到杂化方式为sp3的氮原子,点击杂化方式为sp3的氮原子,在construct界面进行绘制,把氢原子补全,即可得到NH3分子的空间立体构型。学生可将绘制好的H2O分子和NH3分子的立体构型置于同一界面中进行比较学习,推测孤对电子所在位置,如图2(a)所示,同时,也可以将分子模型转动(如图2(b)所示),更加直观地感受微观分子构型与宏观物质之间的联系。除此之外,该软件还可以绘制BallandStick(球棍模型)、Wireframe(线状模型)、SpaceFill(比例模型),对需要的分子模型进行原子数目、沸点、碳原子个数、偶极矩、相对分子质量等数值的分析,也可以将有可比性的分子构型置于两界面、四界面进行对比学习,方便了学生的学习。
2.辅助有机分子立体构型学习
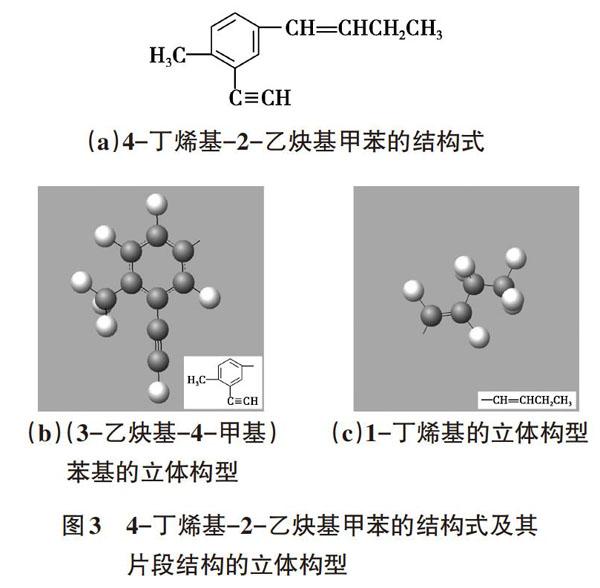
eChem软件不仅可以绘制无机分子立体构型,也可以绘制链状、环状的有机分子立体结构模型,对学生学习空间立体构型产生了积极的促进作用。如问有机分子4-丁烯基-2-乙炔基甲苯(结构式如图3(a)所示)中共平面的碳原子最多有几个,学生也许会很难做出判断,这时可以借助eChem软件绘制分子模型。由于该软件中共价键不能旋转,所以绘制两个片段进行判断,如图3(b)、(c)所示,可以看出该分子最多有13个碳原子共平面。
利用eChem软件,学生可将绘制好的分子立体构型直接在电脑上旋转观看,借助计算机软件模拟的直观手段,降低立体构型的抽象性,充分发挥自己动手搭建分子结构的能力,促进对分子立体构型相关内容的理解,帮助建构微观结构与化学符号间的联系。
三、总结
利用eChem软件可将传统的图片式学习转换为3D立体式学习,借助计算机的力量来帮助学习者积极地解决问题,建立概念上的理解,为化学教育提供便捷。eChem软件以其简洁、干净、小巧的界面及特有的构建分子模型的功能,不仅方便了教师在分子立体构型中的教学,也有利于提高学生动手能力,充分调动学生的视觉及空间想象能力,使抽象问题具体化,增加学生的学习兴趣,帮助学生建立映象表征和符号表征之间的联系,实现宏观映象、抽象符号、微观粒子间的相互转换。但是,该软件在搭建分子模型时也具有一定的局限性。并不是所有的分子都可以建模,可以看到该软件只是包含了少数元素,因此可构建的分子模型较少,例如绘制SO3分子模型,其中中心原子硫原子属于sp2杂化,但该软件sp2杂化方式却是硫双键,因此无法绘制出SO3立体分子模型。另外,分子模型中的共價键不能旋转,这就为分子模型的建立带来了一定的局限性。利用eChem软件可建立大多数有机化合物和部分无机化合物分子模型,该软件是一款很好的计算机模拟软件,性能稳定,为响应《普通高中化学课程标准(2017年版)》要求,可将该软件推广于中学及大学低年级全体师生使用。
参考文献
[1][3]中华人民共和国教育部.普通高中化学课程标准(2017年版)[M].北京:人民教育出版社,2018:1,41-42,84
[2]陈琦,刘孺德.当代教育心理学(第2版)[M].北京:北京师范大学出版社,2007:31-34
[4]沈理明,章建东,田军.eChem——分子结构教与学的辅助工具[J].化学教学,2005(10):42-44
