介孔分子筛SBA-15负载MnO2吸附剂去除水中As(Ⅲ)
2019-04-20高秀坤刘晓胜杜博文王林军姚淑华
高秀坤, 刘晓胜, 杜博文, 王林军, 姚淑华
(沈阳化工大学 应用化学学院, 辽宁 沈 阳 110142)
随着工农业的发展,砷污染已成为全球十分严重的环境污染之一.砷对人体健康和动植物均具有毒性和危害.据报道,全球尤其是亚洲国家,至少有5000多万人正面临着砷中毒的威胁,中国也是面临砷中毒威胁的国家之一.在过去的20多年间,曾发生过30余起砷中毒事件.近几年来,关于重金属污染的话题在环境保护中急剧升温,治理重金属污染,保护生态环境,尤其是砷污染,已经是刻不容缓的事情.砷通常以三价砷As(Ⅲ)和五价砷As(Ⅴ)两种价态存在于自然界中,其中As(Ⅲ)的毒性高于As(Ⅴ)和元素砷.因此,去除As(Ⅲ)显得尤为重要.水中砷污染的治理方法主要有静电沉淀、氧化聚沉、离子交换树脂、吸附、反渗透等[1-6].在实际应用中,以上相关技术具有操作复杂、成本高等缺点,其中一些处理技术甚至需要后续的处理,因此,难以推广应用.而吸附法因其具有高效、节能、环保等特点而较常用[7].锰氧化物对砷有很强的吸附能力,可是单一吸附剂一般呈粉末状,因此,难以用于柱状或床式水处理装置.研究复合材料即由两种或两种以上物理和化学性质不同的物质组成的材料可克服此缺点,即把对砷吸附能力较强的金属氧化物类吸附剂负载在多孔材料上,进而使所得的复合材料拥有更大的除砷容量,可用于水处理装置[8].根据国际纯粹与应用化学联合会(IUAPC)的规定[9],孔径在2~50 nm之间的材料为介孔材料.介孔材料主要的结构和性能是:均一可调的介孔孔径;易于修饰的内表面;高达1 000 m2/g的比表面积;较高的热稳定性和水热稳定性.因而在催化、分离以及吸附等诸多领域有广阔的应用前景[10].1998年,赵东元等首次以三嵌段聚合物P123为模板剂,在强酸性条件下合成了SBA-15介孔分子筛[11-13],该类介孔分子筛具有大孔径和厚孔壁等优点,因而具有很高的水热稳定性.
本文以P123为模板剂,以正硅酸四乙酯为硅源制备介孔分子筛SBA-15,并以其为基质负载MnO2,制成SBA-15/MnO2吸附剂,利用SBA-15/MnO2对含As(Ⅲ)废水进行吸附处理;讨论硅锰摩尔比、吸附剂用量、溶液pH、离子强度对去除率的影响,进行相关数据分析,为相关复合吸附材料的制备、应用提供有益的基础实验数据.
1 实验部分
1.1 实验药品
P123、正硅酸四乙酯、乙醇、高锰酸钾、一水合硫酸锰、硫脲、浓盐酸、抗坏血酸、硼氢化钾等,所有化学试剂除浓盐酸外均为分析纯试剂.所有玻璃器皿使用前均经体积分数为5 %的硝酸浸泡48 h,再用自来水和去离子水冲洗数次后烘干备用.
1.2 实验方法
1.2.1 SBA-15的制备
用分析天平称取4.0 g P123溶解到150 mL 0.4 mol/L的HCl溶液中,量取8.5 g正硅酸四乙酯加入到上述溶液中(溶液放置在308 K恒温水浴中搅拌20 h).将得到的产物在温度为353 K的条件下陈化24 h,将所得固体在室温下过滤、水洗,干燥.再从室温缓慢升温至773 K煅烧14 h,并在773 K的温度下保持6 h,研磨,制得SBA-15.
1.2.2 MnO2的制备
称取4.0 g一水合硫酸锰和2.6 g高锰酸钾,分别溶解到去离子水中,将溶解后的高锰酸钾溶液缓慢滴入不断搅拌的硫酸锰溶液中.滴加结束后,继续搅拌30 min.经抽滤、洗涤,所得固体60 ℃烘干,研磨,制得 MnO2粉末[14-16].
1.2.3 SBA-15/MnO2的制备
将SBA-15和一水合硫酸锰放入烧杯中,并加入去离子水搅拌混匀.用磁力搅拌器搅拌混合液6 h,停止搅拌后把混合液60 ℃烘干.将3.0 g 高锰酸钾固体颗粒放入250 mL烧杯中,加入去离子水使其溶解.将烘干后的SBA-15粉末倒入正在搅拌中的高锰酸钾溶液中并持续搅拌3 h,经洗涤、抽滤,所得固体60 ℃烘干,研磨,制得SBA-15/MnO2.
1.2.4 分析方法
取适量上清液,加入还原剂(质量分数为5 %的硫脲+质量分数为5 %的抗坏血酸),用体积分数为5 %的盐酸定容至刻线,摇匀静置,用氢化物发生-原子荧光分析仪测定其中剩余As(Ⅲ)含量.
1.2.5 表征方法
利用S-3400N型扫描电镜和X射线粉末衍射(XRD)对吸附剂进行表征.
1.2.6 吸附实验
用亚砷酸钠配置质量浓度为1 000 mg/L的含砷模拟水样,实验过程中逐级稀释.具体实验步骤如下:向锥形瓶中加入一定量吸附剂,量取一定体积的As(Ⅲ)溶液,调整pH值等条件,然后放入恒温空气振荡器中.在150 r/min、(25±1) ℃的恒温空气振荡器中振荡.经24 h 的吸附反应后,溶液用0.45 μm滤膜过滤,取上清液,用氢化物发生-原子荧光分析仪测定其中剩余As(Ⅲ)含量.
2 结果与讨论
2.1 表征
图1为样品的SEM图.(a)为SBA-15,形状比较规则,统一为条状,长度在1 μm以上.(b)为MnO2,球状粉末.(c)为SBA-15/MnO2,可以观察到有大量的球形颗粒,未观察到SBA-15的结构,这些球形颗粒小而均匀并且连成一片.


图2为SBA-15的小角XRD图.SBA-15拥有规整的孔道结构以及无定形SiO2组成的孔壁,因此,在XRD谱图上,SBA-15在2θ为1°~8°的小角范围内会出现典型的晶体结构衍射峰.在图2中可明显观察到(100)、(110)、(200)三个晶面衍射峰,表明所制备的样品为典型的SBA-15.
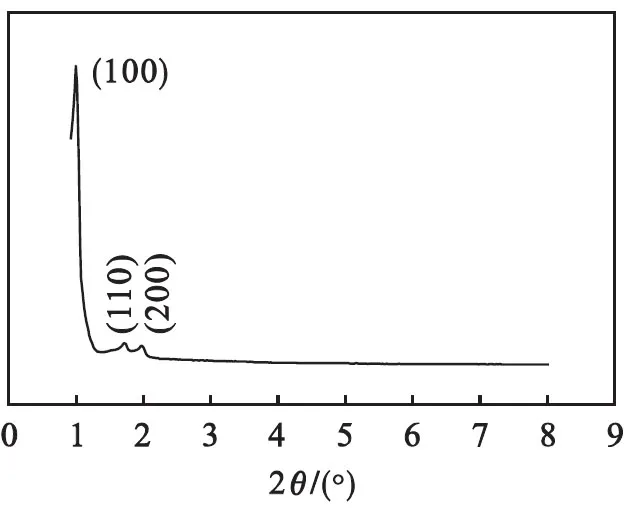
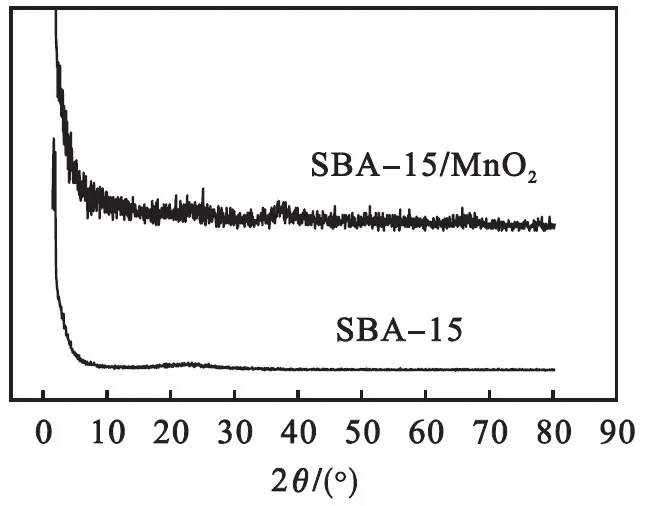
图3为SBA-15和SBA-15/MnO2的广角XRD图,没有发现明显的衍射峰,推测生成的MnO2为无定形化合物或者结晶度低的矿物.
2.2 硅锰摩尔比对As(Ⅲ)去除的影响
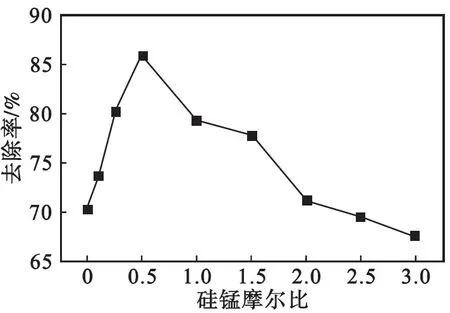
图4为初始砷质量浓度10 mg/L、吸附剂用量1.0 g/L时,合成吸附剂时的硅锰摩尔比对As(Ⅲ)去除率的影响.通过吸附剂硅锰摩尔比的考察,可以确定最佳的吸附剂制备条件.由图4可知:以介孔材料SBA-15为基质负载MnO2所形成的SBA-15/MnO2吸附剂比MnO2对砷的吸附效果好;当吸附剂的硅锰摩尔比为0.5∶ 1时,吸附效果达到最佳;但是,随着硅锰摩尔比的增加,过多的SiO2导致吸附效果下降.其原因可能是SBA-15对砷的吸附效果较差.
2.3 吸附剂用量对As(Ⅲ)去除的影响
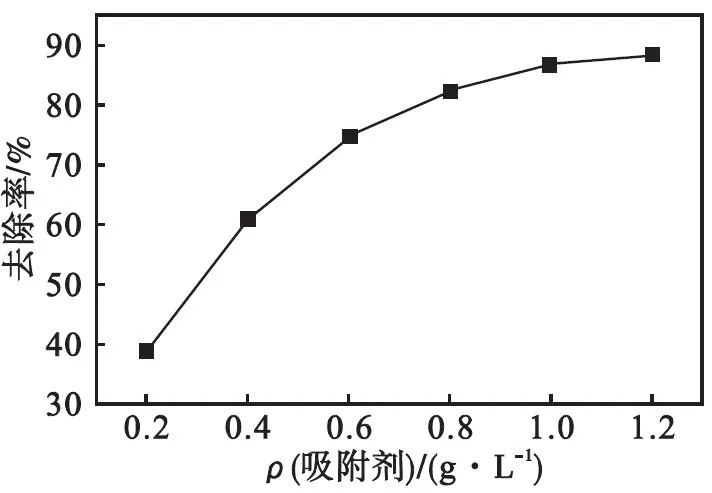
图5为砷初始质量浓度为10 mg/L时,吸附剂用量对As(Ⅲ)去除率的影响.由图5可知:在0.2~1.2 g/L,增加吸附剂投加量,对As(Ⅲ)去除率明显上升.在吸附剂用量1.0 g/L时,去除率为86.36 %,增加吸附剂用量到1.2 g/L,去除率为88.13 %,增长缓慢,因此,接下来的吸附实验吸附剂用量均采用1.0 g/L.
2.4 溶液pH对As(Ⅲ)去除率的影响
初始砷质量浓度为10 mg/L,吸附剂用量为1.0 g/L,采用0.1 mol/L HCl和0.1 mol/L NaOH调节溶液pH分别为2、4、6、8、10,考察溶液pH对As(Ⅲ)去除率的影响,结果如图6所示.对砷进行吸附时,在溶液初始pH为2的情况下表现出较好的吸附效果,去除率达到了96.53 %,而在碱性条件下,吸附效果明显减弱.原因可能有以下几点:(1)二氧化锰在酸性条件下有着较强的氧化能力,和As(Ⅲ)之间发生氧化还原反应,高价的锰变成二价锰离子进入溶液,使得吸附剂表面的吸附位增加.(2)吸附剂表面在溶液中带有负电荷,与亚砷酸根和砷酸根之间存在静电斥力,而随着溶液pH值的减小,其溶液pH值靠近MnO2的等电点,或小于其等电点,使得吸附剂与吸附质之间的静电力发生改变,促进了MnO2对砷的吸附[17].(3)较低的pH值可能增强了二氧化锰的化学活性,特性吸附能力增强.
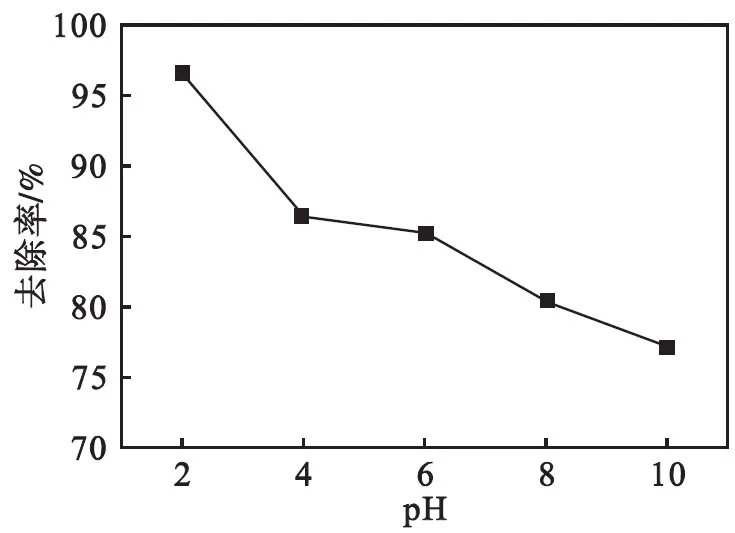
2.5 离子强度对As(Ⅲ)去除率的影响
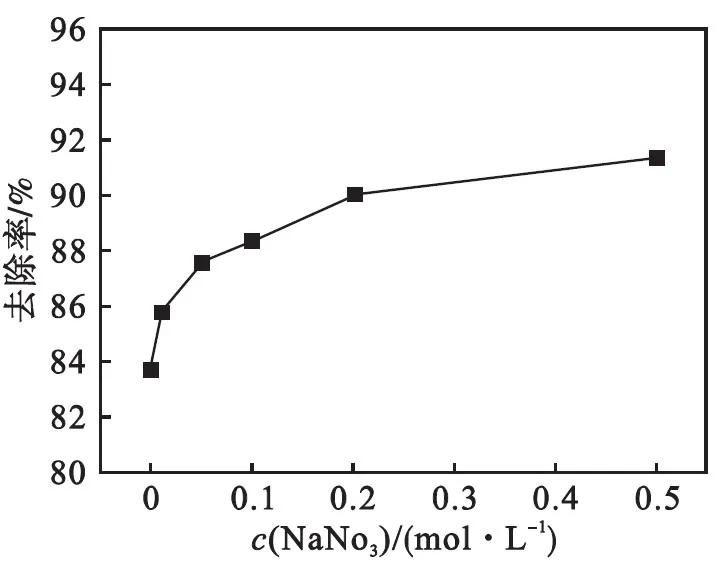
初始砷质量浓度为10 mg/L,吸附剂用量1.0 g/L,通过向溶液中加入不同浓度的NaNO3溶液改变体系离子强度,结果如图7.
由图7可知:随着NaNO3浓度的增加,砷的去除率在不断上升,当硝酸钠浓度为0.5 mol/L 时,对砷的去除率达到91.36 %,而不加硝酸钠时,对砷的去除率为83.74 %.此结果说明增加离子强度能明显促进吸附剂对砷的吸附.其原因可能是电解质的加入压缩了双电层的厚度,削弱了吸附剂与吸附质之间的静电作用,电荷平衡离子包围带相反电荷的吸附点位,部分中和了吸附点位的电荷,削弱了吸附点位与吸附质之间的静电作用,当吸附剂和吸附质之间存在静电吸引作用时,增加离子强度对吸附不利;当吸附剂和吸附质之间存在静电排斥作用时,增加离子强度对吸附有利[18].离子强度对吸附的影响可用来区分吸附质被吸附后形成的络合物类型,当吸附对离子强度不敏感或吸附随离子强度的增加而增加时,可能形成了内层表面络合物; 当吸附随离子强度的增加而减小时,可能形成了外层表面络合物.所以,实验中的吸附剂可能与砷形成了内层表面络合物.
2.6 吸附等温线
在温度为25 ℃,吸附剂用量为1.0 g/L,砷初始质量浓度分别为5、10、20、50、100、250、500 mg/L条件下进行等温吸附实验,实验结果采用Freundlich和Langmuir吸附等温式模型,Langmuir(等温吸附模型)方程可表示为:
qe=qmKLCe/(1+KLCe)
(1)
式中:KL为吸附系数,与温度及吸附热有关;qm为单位吸附剂表面盖满单分子层时的吸附量,即饱和吸附量.其线性形式为:
Ce/qe=Ce/qm+1/(KLqm)
(2)
Freundlich(等温吸附模型)方程可表示为:
qe=KFCe1/n
(3)
式中:KF是Freundlich的吸附系数,与吸附剂的用量和性质、吸附质的性质、温度等因素有关;n是Freundlich常数,取决于吸附体系本身,n值通常大于 1. 一般认为0.1<1/n<0.5 时易于吸附, 1/n>2时难以吸附.其线性形式为:
lnqe=(lnCe)/n+lnKF
(4)
等温吸附实验结果如图8所示.
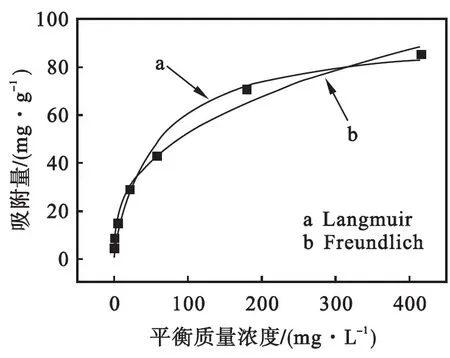
根据方程(2)、(4),用Freundlich和Langmuir模型对实验数据进行线性拟合(见图9),拟合后R2分别为0.993 9和0.978 3,吸附平衡更好地符合Freundlich模型.相关参数在表1中列出.
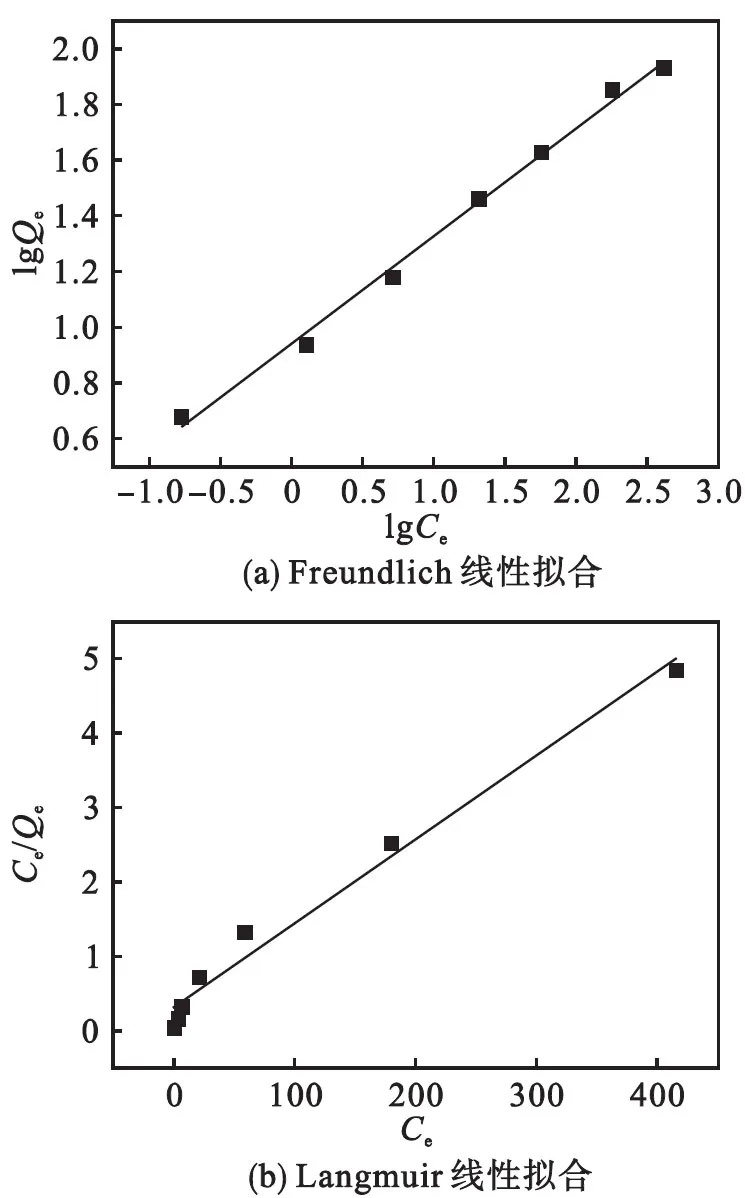

表1 吸附等温线方程参数
2.7 吸附动力学
砷初始质量浓度为10 mg/L,吸附剂用量为1.0 g/L,在吸附时间为2、5、10、15、20、30、60、120、240、720 min时取样,结果如图10.
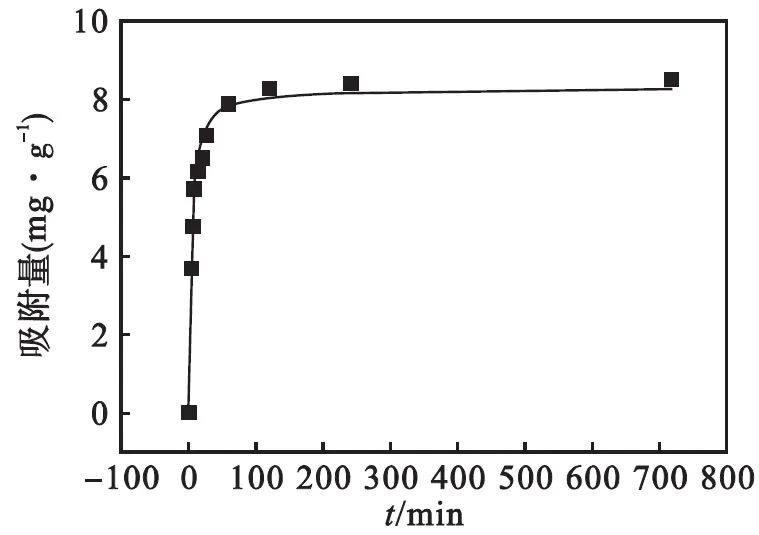
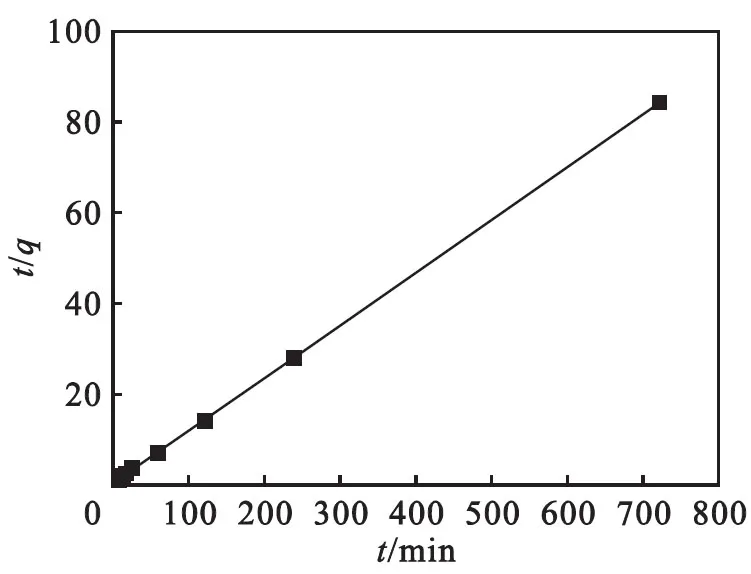
采用准二级动力学方程对动力学实验结果进行拟合(见图11),R2为0.999 9,说明介孔分子筛SBA-15负载MnO2吸附剂对As(Ⅲ)的吸附过程可用准二级动力学描述.由图10可知:在前30 min内SBA-15/MnO2吸附剂对砷吸附的吸附量增长较快;但吸附量随着时间的推移,增长呈下降趋势,当吸附时间达到4 h时,吸附基本达到平衡,最终的平衡吸附量为8.5 mg/g.根据Langmuir等温吸附理论,每个吸附位只能容纳一个吸附质分子;根据Freundlich等温吸附理论,吸附热随着覆盖度增加而指数下降.SBA-15/MnO2吸附剂对砷进行去除时,吸附初期吸附剂表面的吸附位处于不饱和状态,并且此时吸附体系中的砷浓度较高,梯度较大,因此,SBA-15/MnO2吸附剂在前30 min内对砷呈现出较高的吸附去除效果; 随着吸附反应的进行,吸附剂表面的吸附位被大量占据,体系中的砷浓度降低,梯度减小,去除效果减弱.吸附进行一定时间后,吸附剂表面吸附的砷与脱离的砷相等[19],此时,吸附达到平衡.
3 结 论
(1) SBA-15/MnO2吸附剂对砷的去除率明显优于MnO2,当砷初始质量浓度为10 mg/L,吸附剂用量为1 g/L时,去除率达86.76 %;溶液pH对吸附影响较大,酸性条件下吸附较好,增加离子强度能明显促进吸附剂对砷的吸附.
(2) 吸附等温线较好地符合Freundlich和Langmuir模型,尤其是Freundlich模型,其R2为0.993 9,1/n为0.368,在0.1~0.5之间,说明易于吸附;吸附开始30 min内有较快的吸附速率,吸附量达到7.1 mg/g,在随后的一段时间里吸附量缓慢升高,在吸附开始4 h后基本达到了吸附平衡,吸附过程符合准二级动力学模型.
另外,本文提供了一种介孔分子筛SBA-15负载MnO2的方法(已申请专利),可为同类型吸附剂的制备提供借鉴,但介孔分子筛SBA-15造价较高,可以考虑采用膨润土等替代SBA-15作为载体.
