儿童原发塑型性支气管炎的临床及影像学分析
2019-04-17郑州大学附属医院南阳市中心医院儿一科河南南阳473000
郑州大学附属医院(南阳市中心医院)儿一科 (河南 南阳 473000)
朱彩华 孙文武 屈会霞
儿童原发塑形性支气管炎是因肺脏内生异物部分或完全阻塞支气管呼吸道,造成肺内局部或全部通气功能障碍,引起严重呼吸困难的一类儿科罕见疾病[1]。内生异物堵塞支气管后可限制患儿通气功能,若不及时取出易进展为顽固性低氧血症,引起难以纠正的呼吸衰竭,导致患儿死亡[2]。但临床上对该病尚未形成统一诊断标准,且患者临床症状及实验室检查特异性不高,极易将支气管塑型树样异物误诊呼吸道异物,从而延误病情,增加患儿死亡风险[3]。本研究回顾性分析2015年1月-2017年12月在我院确诊为原发塑型性支气管炎的27例患儿的临床资料,总结儿童原发塑形性支气管炎的临床表现及影像学特征。
1 资料与方法
1.1 一般资料 选取2015年1月-2017年12月我院收治的原发塑型性支气管炎患儿27例,其中男19例,女8例;年龄10个月~14岁,平均年龄(6.35±1.74)岁;病程2d~2个月,平均病程(24.37±4.29)d,并发症包括脂肪肝1例、肾病综合征2例、胸腔积液9例、呼吸衰竭8例、心力衰竭2例、中毒性肝炎4例。
1.2 纳入标准 选取患者均采用纤维支气管镜取出内生异物,并经病理学检查确诊;排除其他继发性原因导致的塑型性支气管炎;排除有支气管扩张或支气管哮喘病史者。
1.3 检查项目与方法
1.3.1 实验室检查:采集所有患儿血液标本,进行血常规及血清生化检查检查,记录患儿白细胞计数、中性粒细胞、血小板计数(PLT)、血细胞沉降率(ESR)炎性因子、心肌酶、肝酶等指标。
1.3.2 纤维支气管镜:检查前4h禁食禁水,前30min予以阿托品0.01mg/kg,肌内注射,患儿取仰卧位,予以喉罩全麻,将支气管镜穿过喉罩进入声门,利多卡因作局部麻醉,将支气管镜分别探入左右主支气管,逐级观察支气管结构及黏膜情况,确认黏液栓位置后,予以灌洗液进行反复灌洗,采用活检钳取出阻塞气道黏液栓,同时采集灌洗液送至检验科作病原学培养,黏液栓送至作病理学检查。
1.3.3 CT检查:采用Siemens SOMATOM Spirit64层螺旋CT机,管电压设置为80kV,管电流设为8 0 m A,螺距1.4,扫描层厚3.75mm,患儿取仰卧位,处于平静呼吸状态后行胸部平扫,难以配合检查的患儿可予以5%水合氯醛灌肠,待患者镇静后行胸部扫描,采集数据传送至数据处理工作站,重建层厚0.63mm,将薄层图像进行冠状位多平面重组。
2 结 果
2.1 临床表现 27例患者均伴有不同程度的咳嗽、高热、气促症状,体温在38.5℃~41℃之间,最高体温均达40℃以上,发热持续时间在4~14d之间,平均发热时间(6.71±2.01)d,其中表现为稽留热的患儿16例(59.26%),余患儿发热无规则。患儿发病后均表现为进行性呼吸困难,其中8例(29.63%)患儿出现呼吸衰竭,平均氧分压(PO2)为(61.29±12.55)mmHg;均可闻及中细湿罗音,部分患儿可闻及少许喘鸣音及痰鸣音。
2.2 实验室指标 见表1。
2.3 病原学特征 27例患儿灌洗液培养细菌为阳性者11例,其中金黄色葡萄球菌感染7例(25.93%),肺炎链球菌感染5例(18.52%),草绿色链球菌感染1例(3.70%),大肠埃希菌2例(7.41%),铜绿假单胞菌感染1例(3.70%),肺炎克雷伯杆菌1例(7.41%);肺炎支原体(MP)特异性I g M 抗体滴度阳性者1 9 例(70.37%);腺病毒抗原检测阳性者5例(18.52%),乙型流感病毒抗原检测阳性者2例(7.41%),甲型流感病毒抗原检测阳性者1例(3.70%);白假丝酵母菌培养阳性2例(7.41%);混合感染者12例(44.44%)。
2.4 病理学特征 黏液栓切片固封后检查显示均呈纤维素样改变,均可见大量中性粒细胞及淋巴细胞等炎性细胞浸润,其中有4例(14.81%)患儿黏液栓标本呈大量嗜酸性粒细胞浸润表现。
2.5 纤维支气管镜检查 患儿纤支镜下均可呈气道黏膜充血、水肿表现,黏性分泌物明显增多,其中6例患者可见大量黏膜滤泡增生(图1),段支气管分支均可见灰白色黏液栓,取出黏液栓呈支气管塑型树样改变(图2),长2~6cm,其中阻塞部位于右主支气管者19例(70.37%),阻塞于左主支气管者8例(29.63)。
2.6 CT影像学结果 患儿胸部CT均呈肺部感染征象,肺纹理增多,均示支气管部分或完全阻塞,左侧肺实变3例(11.11%),右侧肺实变7例(25.93%),双侧肺实变17例(62.96%),节段性肺不张5例(18.52%),合并胸腔积液者9例(33.33%),其中6例积液量较少,包裹性气胸2例(7.41%),呈支气管黏液嵌塞症者10例(37.04%),累及胸膜病变者4例(14.81%),见图3、图4。
3 讨 论
随着医学诊疗技术的迅速发展,纤维支气管镜的广泛应用,塑形性支气管炎的检出率不断升高,但该病的发病因素及致病机制尚未明确,诊断标准及治疗原则仍未统一。国外研究认为,塑形性支气管炎的的发病群体主要集中于哮喘、肺囊性纤维病、镰状细胞性贫血、先天性心脏病及Fonton术后儿童,而该类继发性塑型性支气管炎通常不会呈现明显炎性细胞浸润表现[4-5]。2004年,国内首次进行了塑形性支气管炎相关报告[6],表明在我国由致病原感染导致原发性塑形性支气管炎患儿较为常见,而感染可显著增加该病的发生风险,尤其以甲型H1NI流感病毒感染多见,致病菌导致的塑形性支气管炎肺部呈明显炎症反应,取内生黏液栓进行病理检查可见大量中性粒细胞及淋巴细胞[7]。近年相关报道发现,除甲流病毒外,乙型流感病毒与肺炎支原体同样是诱发塑形性支气管炎的高危因素,另外在患儿机体免疫功能严重障碍的情况下,细菌性感染也可造成塑形性支气管炎[8-9]。本研究采集原发性塑型支气管炎患儿灌洗液进行病原学检查,结果显示,70.37%的患儿肺炎支原体特异性抗体滴度>1:160,除此,金黄色葡萄球菌感染患者占25.93%,而乙型流感病毒及甲型流感病毒感染患儿比例较低,分别为7.41%与3.70%。该结果提示肺炎支原体同样是导致儿童原发塑型性支气管炎的关键致病菌,该结果与丁小芳等[10]研究结果一致,而本研究对甲型流感病毒及乙型流感病毒检出率明显较低,考虑原因可能是纳入对象较少,无法进行流行病统计学比较。
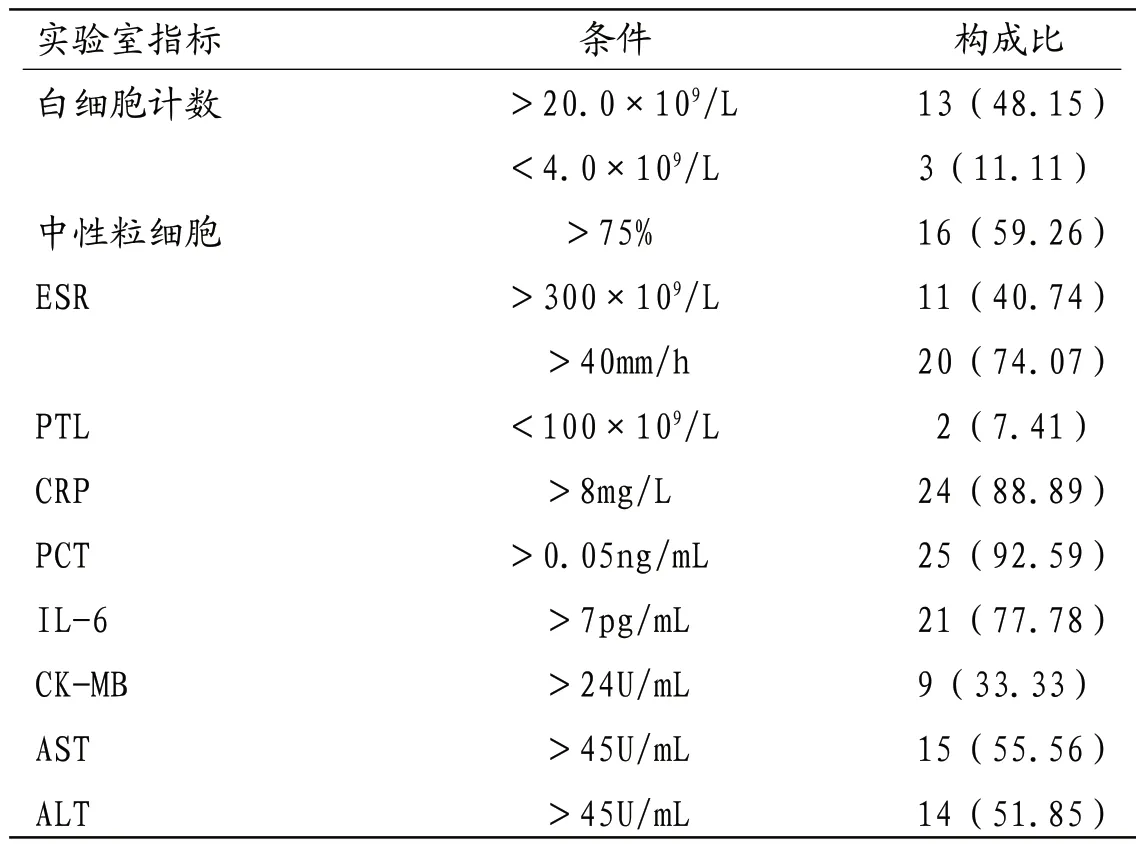
表1 患儿实验室指标[n(%)]

图1 支气管黏膜滤泡增生。

图2 内生塑型树样异物。
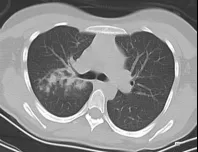
图3 肺部感染、肺实变。
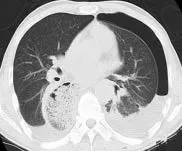
图4 肺不张伴胸腔积液。
原发塑型性支气管炎临床表现与黏液栓阻塞支气管部位有关,患儿通常伴有持续高热、咳嗽、咳痰、气促等表现,同时伴发不同程度的呼吸困难,严重者可有呼吸衰竭表现[11]。本研究结果显示,患儿均表现为高热、咳嗽、气促症状,肺部听诊可闻及湿罗音,29.63%的患儿出现呼吸衰竭,均予以气管插管、呼吸机辅助通气,其中仅1例患儿通气功能明显缓解,余患儿呼吸衰竭症状不能纠正,后行纤支镜取出塑型黏液栓后并反复灌洗后,呼吸功能明显改善,撤机予以促进排痰、抗感染治疗后肺通气功能恢复正常。
Seear分型标准[12]将塑型性支气管炎分为I型和II型,I型又称为炎症型,黏液栓镜下可见大量纤维素及炎性细胞,以中性粒细胞、淋巴细胞及嗜酸性粒细胞浸润为主;II型又称非细胞型,病理图片示黏液栓主要成分为纤维素及黏液蛋白,未见明显炎性细胞浸润表现。本研究塑型性支气管炎病例均为I型,塑型黏液栓主要由纤维素与炎性细胞组成,部分患者可见嗜酸性粒细胞。血常规、生化检查显示48.15%的患儿白细胞计数升高,11.11%患儿计数降低,CRP、PCT、IL-6等炎症因子升高比例超过75%,肝酶异常升高比例超过50%,患儿炎症反应较为严重,同时可能侵犯心、肝等脏器,引起急性心包炎、急性肝炎等并发症。
胸部CT是诊断塑型性支气管炎的重要手段,CT可准确清晰显示支气管腔狭窄及扩张程度,黏液栓阻塞支气管导致阻塞性肺气肿、肺不张等并发症,重度肺部感染造成肺实变,进一步发展可引起炎性胸腔积液,管壁增厚,加重肺不张[13-14]。临床上易将塑型性支气管炎误诊为支气管异物或单纯视作大叶性肺炎[15],通过胸部CT,进行支气管三维重建可显示支气管腔阻塞状态及程度,当影像表现为典型肺部感染、肺实变及肺不张时,应考虑塑型性支气管炎可能[16]。本研究中患儿呈典型肺部感染表现,均有不同程度的肺实变征象,其中病变主要集中于右肺中下叶,胸腔积液发生比例达33.33%,37.04%的患儿表现为支气管黏液嵌塞症。
儿童原发塑型性支气管炎发病急,进展迅速,致死率可达6.0%[17],本研究患儿均采用胸片CT扫描及病理学检查进行早期诊断,予以纤维支气管镜清除支气管塑型黏液栓并反复灌洗,灌洗后给予常规抗感染、祛痰、免疫支持治疗等,患儿临床症状均得到不同程度缓解,未见死亡病例。
