施硅降低碱性土壤铅生物有效性的机制研究
2019-04-08刘鸣达张婧婷王耀晶
刘鸣达,张婧婷,马 聪,王耀晶,2*
(1.沈阳农业大学土地与环境学院,沈阳 110866;2.沈阳农业大学理学院,沈阳 110866)
关于硅缓解重金属元素对作物的胁迫作用已得到各国学者的广泛认同。多数研究集中在其生物学机制方面[1-3]。对此,Liang等[4]做过较为详细的综述,主要归结为激活植物抗氧化系统、抑制重金属元素向植物地上部运转、与重金属在植物根部外层细胞壁发生共沉淀、促进重金属离子的细胞内区室化等作用。
从土壤化学角度探讨硅缓解植物重金属胁迫机制的研究并不多,且多集中在硅与镉的关系方面。普遍认为,硅提高了土壤的pH值,使硅酸根等与重金属形成硅酸盐沉淀,从而抑制其活性[5-7]。但陈怀满[8]认为活性硅本身可能是抑制镉吸收的一个重要因素。也有学者认为施硅酸钙等增加了土壤中硅酸根的浓度,促进了硅酸镉沉淀生成,降低了植物体内镉的含量[9-10]。陈晓婷等[11]则认为,施硅抑制小白菜吸收镉的主要机制是促进土壤吸附镉而降低其有效性。
有关土壤-植物系统中硅与铅关系的研究不多且结论尚存在一定的矛盾。何电源[12]采集湖南省内有代表性的8种土壤进行水稻盆栽试验,设置施无定形二氧化硅和不施硅的2种处理,发现一般施硅都可降低糙米的铅含量;赵明柳等[13]研究证明,施用硅酸钠可降低铅从根到茎(分蘖期)、从茎和叶到糙米(成熟期)的转移;Li等[14]研究发现硅可以将铅固定于土壤中、抑制根向枝叶的转运及抑制抗氧化酶的活性进而提高香蕉幼苗对铅毒性的耐受性。但王凯荣等[15]的研究结果显示施硅对土壤铅有效性影响不显著,也不能抑制水稻对铅的吸收。值得注意的是,上述试验中多加入了高炉渣、硅酸钠等含硅碱性物质,同时还引入了相应的伴随离子;而钙、镁、钾、钠等元素均能抑制植物对重金属的吸收转运[16]或影响重金属的土壤化学行为。因此,未消除pH和伴随离子影响的试验结果未必能反映硅对铅的真正作用。显然,硅对土壤中铅生物有效性的影响机制尚不清楚。
我们前期在消除pH和伴随离子影响的基础上研究了硅对土壤吸附铅的影响,结果表明:加硅促进酸性土壤对铅的吸附,抑制碱性土壤对铅的吸附[17]。初步的推测是:在碱性土壤中,硅和铅形成了不能被水稻吸收的水溶性复合物。但这一推测尚未被生物试验证实。以上研究尚不能明确硅降低碱性土壤铅生物有效性的机制。
为此,本研究拟通过室内模拟试验和生物试验,在消除pH和伴随离子影响的基础上,开展硅对碱性土壤铅化学行为影响及硅抑制水稻吸收铅效应的研究,从土壤化学角度探讨施硅降低碱性土壤铅生物有效性的机制。
1 材料与方法
1.1 试验材料
供试土壤采自辽宁省沈阳市康平县,为种稻多年的水田土壤,采样深度为0~20 cm。土壤pH 8.15,有机质 59.47 g·kg-1,碱解氮 181.73 mg·kg-1,速效磷38.94 mg·kg-1,速效钾 310.36 mg·kg-1,有效硅(SiO2)300.68 mg·kg-1,全铅23.01 mg·kg-1。试验用尿素含N 46%,过磷酸钙含P2O512%,氯化钾含K2O 60%;硝酸铅、硝酸钠和硅酸钠均为分析纯试剂。供试水稻(Oryza sativa L.)品种为沈农265。
1.2 试验方法
1.2.1 盆栽试验
水稻盆栽试验在沈阳农业大学土地与环境学院盆栽试验场进行。试验设3个处理,即无硅无铅的对照处理(CK)、单加铅处理(以Pb计,加铅量为1000 mg·kg-1土,用Pb表示)、加硅加铅处理(以SiO2计,加硅量为120 mg·kg-1土,加铅量为1000 mg·kg-1土,用Pb+Si表示)。
选用体积为15.0 L的塑料桶,首先放入1 kg干净的鹅卵石;然后装入10.00 kg风干的土壤;接着将硝酸铅溶液施入盆栽土壤中,陈化一周后施入硅酸钠溶液,用硝酸中和硅酸钠的碱性,处理间硝酸根和钠离子的差异用硝酸钠补齐。各处理设4次重复,均施入氮(0.15 g·kg-1)、磷(P2O5,0.10 g·kg-1)、钾(K2O,0.15 g·kg-1)。其中磷肥、钾肥和70%的氮肥作为底肥施入,采取与盆栽土壤混匀的方式施入,平衡一周后,种植水稻,每盆一穴,每穴两株,追施的氮肥以水溶液的形式施入。整个生育期定量浇灌蒸馏水,按常规管理。水稻成熟后采集植物和土壤样品,风干脱粒测产后测定糙米铅含量及土壤中不同形态铅含量。
1.2.2 吸附试验
称取1.25 g(烘干质量)过1 mm筛的供试土壤若干份于已知重量的50 mL离心管中,分别加入以0.01 mol·L-1硝酸钠为电解质的不同浓度(0、150、300、450、600、750、900 mg·L-1,以Pb计)的硝酸铅溶液和不同浓度(0、120 mg·L-1,以SiO2计)的硅酸钠溶液(用硝酸中和其碱性)共25 mL。各处理间钠离子和硝酸根的差异用硝酸钠补齐。试验共设14个处理,每个处理3次重复。各处理密闭后在25℃下振荡2 h(振速为200 r·min-1),恒温培养24 h后,离心5 min(4000 r·min-1),用原子吸收分光光度法测定上清液铅浓度(C1),根据吸附平衡前后溶液中铅含量之差计算出吸附量。计算公式如下:

式中:X为土壤对铅的吸附量,mg·kg-1;C0为铅的初始浓度,mg·L-1;C1为铅的吸附平衡浓度,mg·L-1;V为吸附反应溶液的体积,mL;m为土壤质量,g。
1.2.3 解吸试验
在1.2.2试验结束后,称量离心管及样品质量,然后向离心管中加入0.01 mol·L-1硝酸钠溶液(补足到原始溶液质量),然后按照1.2.2中条件重复振荡、培养、离心步骤,取上清液,测定平衡溶液中铅浓度(C2),计算其中的铅含量,公式如下:
Xd=(C2×Vd-C1×Vr)/m
式中:Xd为铅的解吸量,mg·kg-1;C1为铅的吸附平衡浓度,mg·L-1;Vd为解吸反应溶液的体积,mL;Vr为残留液的体积,mL;m为称取的土壤质量,g。根据吸附量和解吸量差值计算铅的剩余吸附量。
1.2.4 土壤溶液中硅铅复合物筛分
称取5.00 g(烘干质量)过1 mm筛的供试土壤于150 mL离心管中,分别加入以0.01 mg·L-1硝酸钠为支持电解质的120 mg·L-1的硅酸钠溶液(以SiO2计)和1500 mg·L-1的硝酸铅溶液(以Pb计)共100 mL,振荡2 h,培养24 h,离心5 min后过滤获得平衡液。
取吸附平衡液,低温真空旋转浓缩后,进行冷冻干燥,得到粉末,加5 mL去离子水溶解,吸取1 mL浓缩后的液体添加到填充Sephadex G-10树脂的分子筛柱中,在确定最佳洗脱条件的基础上,以去离子水洗脱,每组分3 mL,获得100个不同组分;分别测定不同组分中硅、铅的含量。
1.2.5 土壤溶液中硅铅复合物的红外光谱测定
试验共设3个处理,分别为1000 mg·L-1的硝酸铅溶液(以Pb计,用Pb表示),120 mg·L-1硅酸钠溶液(以SiO2计,用Si表示),1000 mg·L-1的硝酸铅溶液和120 mg·L-1的硅酸钠溶液的混合液(以Pb和SiO2计,用Pb+Si表示),混合前用硝酸中和硅酸钠的碱性,各处理间钠离子和硝酸根的差异用硝酸钠补齐。各处理均在常温下200 r·min-1振荡48 h,恒温培养48 h,接着冷冻干燥,最后利用傅里叶变换红外光谱仪(Spectrum GX,美国)测量样品的红外光谱。
1.3 测定方法
1.3.1 土壤基本理化性质
土壤理化性质测定参照鲍士旦的方法[18]。土壤pH值:土水比为1∶2.5,酸度计法;土壤有机质:重铬酸钾-外加热法;土壤碱解氮:碱解扩散法;土壤速效磷:碳酸氢钠提取-钼锑抗比色法;土壤速效钾:醋酸铵提取-火焰光度法;土壤有效硅:醋酸-醋酸钠缓冲液提取-硅钼蓝比色法。
1.3.2 植株中全铅含量测定
取1.000 g植物样品于三角瓶中,加入9∶1的硝酸-高氯酸10 mL静置过夜。放在通风橱内缓慢加热,待大量棕色气体逸出时,适当提高炉温,直至液体清亮,瓶内有高氯酸白色烟雾出现后,取下冷却后转移定容,采用石墨炉原子吸收分光光度计(Spectr AA220,美国)测定铅含量。
1.3.3 土壤中不同形态铅的测定
土壤全铅采用王水高氯酸消煮,土壤不同形态铅应用改进的BCR连续提取法[19],均采用石墨炉原子吸收分光光度计(同上)测定。
1.4 数据分析
试验数据采用SPSS 20.0和Excel 2003软件进行统计分析,用Origin 2016绘图。
2 结果与分析
2.1 铅胁迫下硅对水稻产量及铅含量的影响
2.1.1 铅胁迫下硅对水稻产量的影响
水稻收获后,测定各处理产量,所得结果如图1所示。可以看出,施硅处理水稻产量显著高于单加铅处理(P<0.05)而略低于对照处理;但施硅处理与对照处理间的差异未达到统计学上的显著水平。说明施硅可以缓解铅对水稻的毒害作用,减轻铅胁迫导致水稻减产的影响程度。
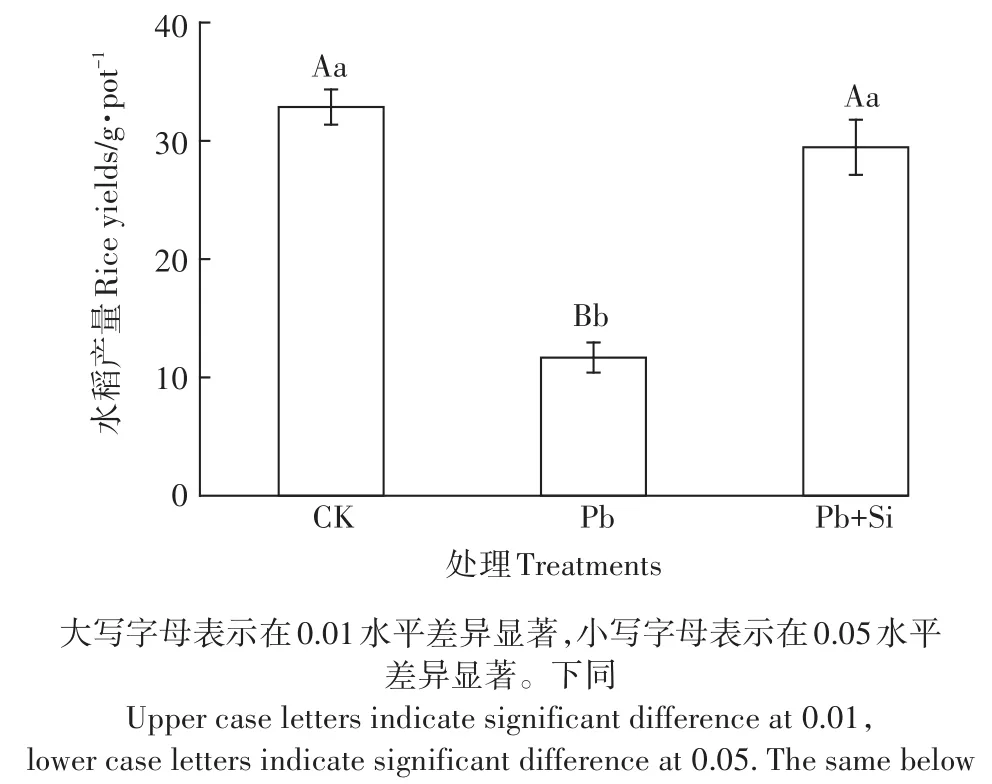
图1 铅胁迫下硅对水稻产量影响Figure 1 Effect of Si application on rice yield under lead stress
2.1.2 铅胁迫下硅对水稻糙米铅含量的影响
测定了不同处理糙米中铅的含量,结果如图2所示。可以看出,与对照处理相比,单加铅处理的糙米铅含量明显升高(P<0.01),施硅则能显著地降低糙米铅含量(P<0.01);尽管施硅处理糙米铅含量仍显著高于对照(P<0.05),但其含量已低于国家规定的糙米中Pb含量的限量标准0.20 mg·kg-1(GB 2762—2017)[20]。说明土壤遭受铅污染条件下,施用适量的硅可以实现水稻安全生产。
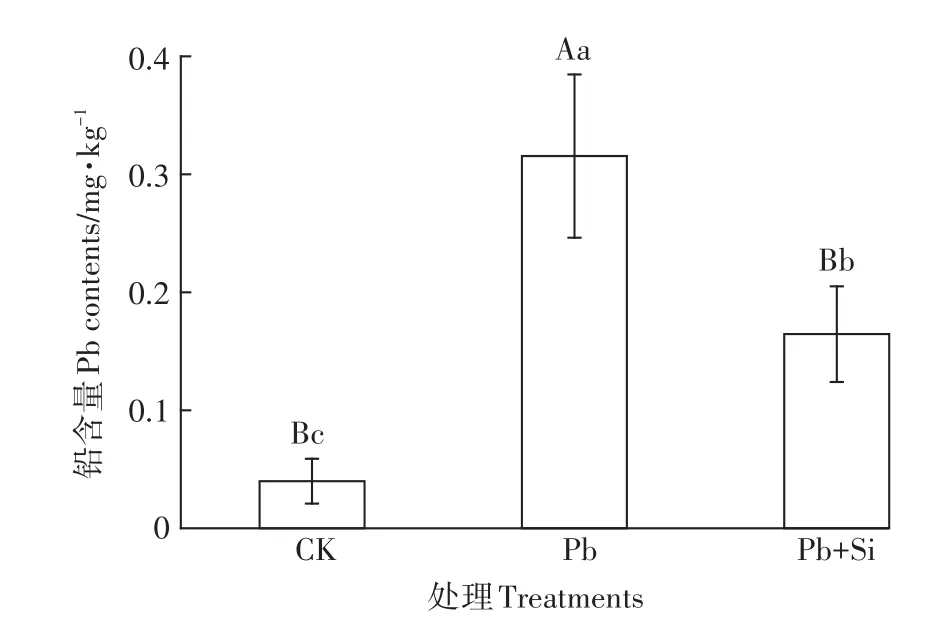
图2 铅胁迫下硅对水稻糙米中铅含量的影响Figure 2 Effect of Si application on Pb content in rice
2.2 硅对碱性土壤铅化学行为的影响
2.2.1 硅对碱性土壤铅吸附-解吸特征的影响
图3为不同硅水平下土壤对铅的吸附-解吸等温线。由图可知,无论加硅与否,铅的吸附量均随平衡浓度增大而增大,吸附量增幅随吸附平衡浓度增大有变缓的趋势;加硅则抑制了碱性土壤对铅的吸附解吸。
采用Langmuir、Freundlich、Temkin模型对试验获得的数据进行拟合,3种方程都能很好地描述不同硅水平下土壤吸附-解吸铅的特征(表1),综合考虑吸附和解吸方程相关系数的显著水平以及硅酸的聚合特性,采用Freundlich模型探讨硅对碱性土壤铅吸附-解吸的影响。
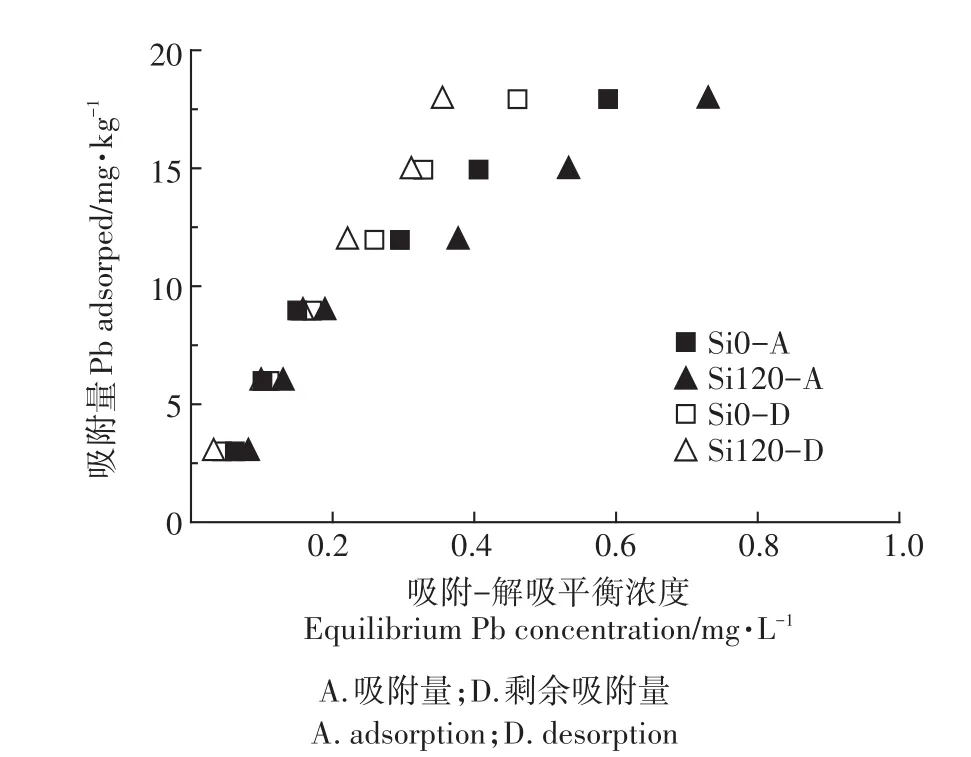
图3 硅对土壤铅的吸附-解吸特征的影响Figure 3 Isotherms of Pb adsorption and desorption in soils at different Si levels

表1 不同硅水平下土壤对铅的等温解吸吸附直线型方程Table 1 The Pb isothermal adsorption equation by soils at different Si level

表2 硅对土壤铅吸附-解吸Freundlich方程常数和滞后系数的影响Table 2 Parameters of Freundlich equation and hysteretic coefficients of soils at different Si levels
表2为硅对土壤铅吸附-解吸Freundlich方程常数和滞后系数的影响。其中na和ka为吸附方程常数;nd和kd为解吸方程常数。k与吸附容量有关,其值越大则吸附容量越大;n表征吸附强度,其值越大则土壤对离子的吸附能力越弱。加硅后ka值变小、na值变大,说明铅的吸附容量和吸附强度降低。Δk=kd-ka和Δn=nd-na可反映土壤对铅吸附-解吸反应的可逆性程度,将Δk+Δn称为滞后系数。滞后系数越大,吸附解吸的可逆性越小[21]。加硅后滞后系数变大,说明铅的解吸受到抑制。
2.2.2 硅铅复合物筛分与红外特征
为探讨土壤溶液中硅、铅的相互作用关系,了解硅对土壤液相中铅形态的影响,将获得的吸附平衡液低温浓缩,然后将浓缩液加入填充有Sephadex G-10树脂的分子筛层析分离柱中,用pH 7.0的去离子水洗脱进行层析分离,共收集100个组分。测定各组分铅和硅的浓度,绘制如图4所示。
可以看出,在第10~20 min之间的组分同一位置都出现铅和硅的洗脱峰,说明吸附平衡液中存在着铅和硅浓度同时升高的组分,推测可能是硅酸和铅以一定的方式结合且具有水溶性的特点。为此利用IR研究溶液中复合物官能团的变化特征,进一步探讨碱性条件下,硅与铅形成水溶性配合物的可能。
图5是纯溶液硅-铅反应傅里叶红外光谱图。图中从上至下分别为Pb处理、Si处理和Pb+Si处理的红外光谱图。其中460 cm-1处的吸收峰为Si-O弯曲振动吸收峰[22],1100~1000 cm-1处的吸收峰为Si-O-Si反对称伸缩振动特征峰。

图5 硅-铅反应产物傅里叶红外光谱图Figure 5 FTIR spectra of Si-Pb reaction product
对比Si处理与Pb+Si处理发现,位于466 cm-1处的Si-O的弯曲振动特征吸收峰向低波数偏移至462 cm-1,位于1086 cm-1处的Si-O-Si的反对称伸缩振动特征峰向低波数方向偏移至1072 cm-1;说明铅的加入影响到Si-O和Si-O-Si特征峰的振动频率,暗示硅酸或聚硅酸与铅可能发生配位反应,形成可溶性复合物。
2.2.3 施硅对碱性土壤固相铅形态的影响
收获水稻后,采取各处理土壤样品,风干处理后应用改进的BCR连续提取法测定了土壤中不同形态铅的含量。结果如图6所示。

图4 吸附平衡液中硅和铅的Sephadex G-10分子筛柱层析图谱Figure 4 The tomographic map of Si and Pb Sephadex G-10 molecular sieve column in the adsorption equilibrium liquid
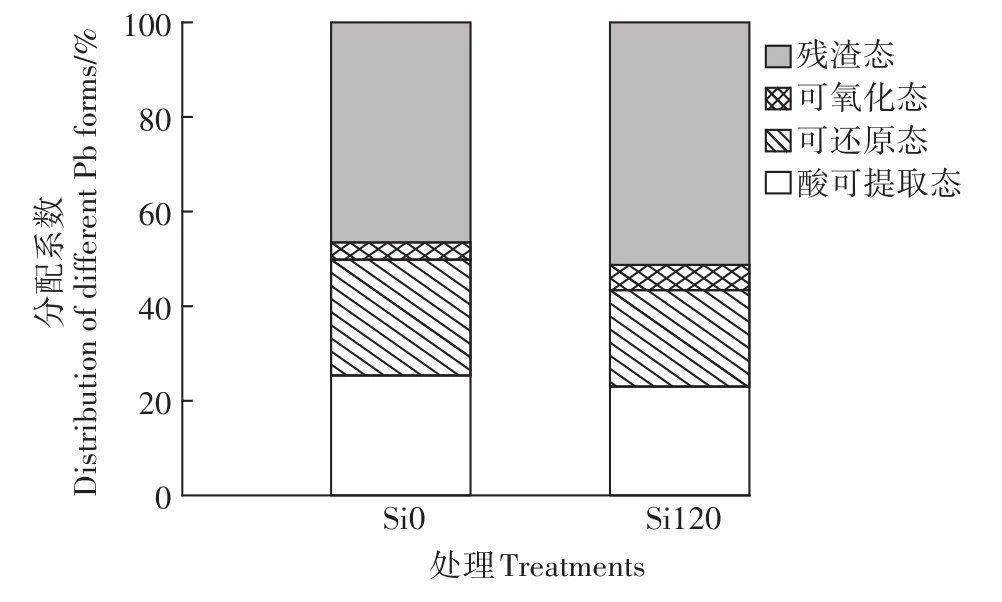
图6 硅对土壤固相不同形态铅含量的影响Figure 6 Effect of Si application on the distribution of Pb in soil
由图可知,施硅后土壤酸可提取态铅、可还原态铅含量分别比单加铅处理降低了11.18%、18.54%,其中酸可提取态铅含量的差异达到了统计学上的5%显著水平;土壤可氧化态铅、残渣态铅分别比单加铅处理升高了42.56%、7.84%,其中可氧化态铅含量达到了统计学上的5%显著水平。这说明施硅有利于土壤中的铅向无效态转化。
3 讨论
硅缓解植物重金属胁迫的机制包括生物学和土壤化学两个方面。从生物学角度来看,通常植物对重金属的吸收和分配有明显的基因型差异[23]。但对于同一品种而言,采取一定的改良措施则是减轻植物重金属毒害的主要原因。研究表明,硅在柳蒿根部淀积可以阻碍铅向地上部分迁移,因此加硅降低了柳蒿地上部铅的吸收量[24];添加硅材料的磷酸盐矿处理显著降低水稻根、茎、叶质外体和共质体中铅的含量[25],说明硅影响了铅的质外体运输过程。也有研究表明,施用硅酸钠可使水稻植株中各种形态的铅含量降低,特别是乙醇和去离子水提取态铅的比例显著下降[26];此外,上述研究中,施硅后生物量都明显增加,故铅胁迫得到缓解也可能是“稀释效应”所致。本研究中,施硅显著降低了水稻植株中的铅,进而提高了稻谷产量,应该与上述机制有关。
本文主要探讨其土壤化学机制。重金属在土壤中的化学形态和行为决定其生物有效性。通常可以从土壤固、液界面的重金属吸附-解吸特征、重金属在土壤固、液相中的赋存形态等方面综合考虑其环境风险。吸附解吸是土壤胶体重要的化学性质之一,是控制土壤溶液中重金属浓度的关键过程。它受制于土壤固相物质的组成、含量、形态和溶液中离子的种类、含量、形态,以及酸碱性、温度、水分状况等条件及其变化情况[27]。研究表明,自由态离子浓度是决定重金属生物有效性和毒性的关键因子[28],离子态铅毒性远大于络合态铅,且络合物越稳定,毒性越低[29]。
本研究是在消除了硅酸钠的碱性和钠离子对吸附的影响基础上进行的,结果表明,加硅抑制了碱性土壤对铅的吸附,导致土壤液相铅浓度升高。但这并不能单纯地看作是自由态铅离子浓度升高。笔者以前推测,碱性土壤中加入的硅可能同铅离子形成了可溶性的配合物,从而造成水溶态铅浓度升高[17];而通常植物主要是以单硅酸的形式吸收硅[30],并不吸收以配合物形态存在的铅,故而不会加剧植物毒害。盆栽试验和硅铅复合物筛分与红外特征研究的结果印证了这种推测。盆栽试验结果显示,铅胁迫下施硅处理水稻产量增加且糙米铅含量降低并达到国家食品安全标准要求,说明水溶态铅浓度升高不但未加剧胁迫,反而是减轻了毒害。从溶液化学角度来看,分离吸附平衡液过程中发现了铅、硅浓度同时升高的组分,进一步应用红外光谱表征溶液中硅铅反应产物,发现Si-O弯曲振动吸收峰和Si-O-Si反对称伸缩振动特征峰均出现了红移。具体来说,硅共价半径为111 pm,而铅的共价半径为147 pm,若铅进入硅氧四面体骨架,由于铅的共价半径大于硅的共价半径,因此振动更加困难,会使Si-O的弯曲振动峰红移[31];伸缩振动是原子沿着价键方向来回运动[32],影响其特征峰的主要因素是键长。Si-O键长为1.61 Å,而Pb-O键长为2.54 Å,若Pb-O形成,会引起键的力常数减少,从而使振动频率降低,导致Si-O-Si反对称伸缩振动特征峰红移。上述红移现象说明了Pb2+与Si-O及Si-O-Si成键的可能,在一定程度上证实了硅酸或聚硅酸与铅生成水溶性复合物的可能。
从解吸的角度来看,加硅后滞后系数变大,说明铅的解吸受到抑制。这可能是因为当土壤溶液中硅浓度较高时,过量的硅酸会发生聚合反应,沉淀在土壤或铁、铝氧化物表面,其结合能力强,解吸困难[33];此外,聚合反应生成的硅凝胶表面有大量的羟基[34],会与铅离子进行配位交换,形成氧与铅结合的双配体螯合物而难以解吸。显然,这种情况对于降低铅生物有效性有积极的意义。
从土壤固相铅形态来看,BCR法中酸可提取态主要是指土壤中可交换的离子和碳酸盐结合的形态,该形态迁移能力较强,在中性和酸性条件下极易被活化释放,是植物最容易吸收的状态。实际上,酸可提取态也包含了水溶态重金属。可还原态铅主要是铁锰氧化物结合的铅,可氧化态铅主要是有机物和硫化物结合的铅,这两种形态都可以被植物吸收利用。残渣态主要是硅酸盐矿物结合态铅,其迁移能力较弱且不易被生物所利用[19]。本研究中施硅显著降低土壤酸可提取态铅、可还原态铅含量,提高可氧化态铅、残渣态铅含量,这在一定程度上降低了铅的生物有效性。
4 结论
(1)铅胁迫下水稻产量显著降低,糙米铅含量明显升高,施硅则显著提高了水稻产量,降低糙米铅含量,并达到了国家标准的安全要求。
(2)加硅降低了碱性土壤吸附铅的容量和强度,增强了铅吸附-解吸过程中的滞后效应;降低了土壤酸可提取态和可还原态铅含量,提高了可氧化态与残渣态铅含量;加硅可使溶液中硅酸或聚硅酸与铅发生配位反应,生成水溶性复合物。
因此,在碱性土壤中,促进土壤液相、固相铅向无效态转化,抑制固相铅解吸是施硅降低铅生物有效性的土壤化学机制。
