溶剂萃取分离废锂离子电池中的钴
2019-04-07鲁桃程洁红
鲁桃 程洁红


摘 要:废锂离子电池中钴金属含量高,具有回收价值。为了提高钴金属的回收率,采用胺类萃取剂甲基三辛基氯化铵(TOMAC)和磷酸类萃取剂Cyanex272,在各自最优条件下对废锂离子电池中的钴进行萃取回收,比较萃取回收率,确定最佳的钴萃取剂。结果表明:在25 ℃反应条件下,萃取剂TOMAC在浓度为0.8 M、O/A=2、初始pH为4及氯离子浓度为5.5 M的条件下,对钴的一级萃取率为98.09%;Cyanex272在浓度为0.56 M、O/A=1、初始pH为4及皂化率为76.7%的条件下,对钴的一级萃取率达99.95%。经反萃后,TOMAC和Cyanex272对钴的回收率分别达到98.00%和98.37%。经成本分析,从废锂离子电池回收1 kg钴,采用TOMAC和Cyanex272的成本分别是26 000元和35 000元。因此,从废锂离子电池中萃取回收金属钴,采用萃取剂TOMAC更经济。
关键词:废锂离子电池;钴金属 ;TOMAC;Cyanex272;溶剂萃取
中图分类号:X705 文献标识码:A 文章编号:2095-7394(2019)06-0022-07
我国是锂离子电池最大的生产、消费及出口国,随着锂离子电池使用数量的上升,报废量也在逐年增加[1]。报废的锂离子电池是一种有效的二次资源,它里面含有多种有价金属,其中钴的含量最高,按质量百分比一般为5%~20%,这一比例高于自然界(矿石)当中的含量(0.002 5%)[2-3],所以,对其进行有效的回收尤为必要。金属钴具有高温下强度高、耐腐蚀性好、铁磁性优异、良好的电化学性能等优点,是制造电池、硬质合金、磁性合金、超级合金以及催化剂和颜料等的重要原料,其中在电池领域的应用率高达46%[4]。所以,从废锂离子电池中回收钴一定意义上能缓解资源短缺的问题。
溶剂萃取法因其具有选择性高、工艺成熟、较高的回收率及操作简单等优点,已被广泛地应用于废锂离子电池中钴金属的回收[5-8]。目前,常用于钴萃取回收的萃取剂大体可以分为两类:酸性萃取剂[9-13](P507、Cyanex272、P5709)和胺类萃取剂[14-18](N235、Alamine336、TOMAC、TIOA)。酸性萃取剂需要皂化,增加了萃取工序,继而延长了操作时间。其中,Cyanex272萃取剂是比较典型的酸性萃取剂,常用于钴矿石的萃取,虽然萃取率高,具备低pH值下实现Ni2+和 Co2+萃取分离[6]的优点,但是負载有机相需在酸性条件下反萃[19],属于进口产品,成本也高。胺类萃取剂中的TOMAC常用于从磁性废料和废磁铁中回收金属[20],其萃取效率也高,并且季铵盐类萃取剂具有在盐酸介质浸液中能够不调节pH直接萃取,并用水反萃回收的优点。
为了简化萃取工艺,得到萃取效率高、成本相对较低、适合工业应用的钴回收萃取剂,试验分别采用胺类萃取剂中的TOMAC和有机磷酸萃取剂中萃取率高、典型的Cyanex272进行比较,考察在最优萃取条件下两类萃取剂的钴萃取效率,并在萃取率、工艺操作、药剂成本方面进行对比,最终确定最佳的钴萃取剂,为今后产业化提供依据。
1 试验部分
1.1 试验材料与方法
1.1.1废锂离子电池及萃原液
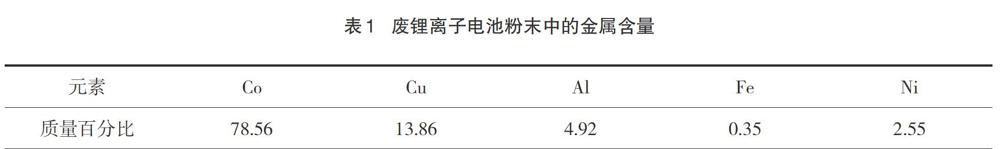
试验用的废锂离子电池属于某型号的华为手机电池。将废锂电池去壳,放电,拆解,并将正负极材料粉粹,测试粉末中的金属含量,见表1。
将上述混合粉末经碱浸出除铝,酸浸出除铁、锰、镁、钙等杂质金属后,再萃取回收铜,得到含钴10.19 g/L、镍1.12 g/L的浸出液,用于本实验的萃原液。
1.1.2试验用萃取剂
甲基三辛基氯化铵(商业名:Aliquat 336)又名TOMAC,它的化学分子式为R4NCl。试验采用磺化煤油做稀释剂,添加5%的异丙醇为改性剂,以改善有机相的流动性。
Cyanex272是一种有机磷酸类萃取剂,主要成分为二(2,4,4-三甲基)戊基磷酸,其分子式为
R2P(O)OH。试验采用磺化煤油做稀释剂,使用前使用4 M氢氧化钠溶液对其进行皂化。
1.2 萃取方法
(1)TOMAC萃取。在萃取前,先向钴、镍的浸出液中投加NaCl从而引入Cl-,由于Co2+与Cl-能生成钴氯络合阴离子(CoCl[2-4]),而Ni2+不与Cl-形成络合物,再用TOMAC萃取CoCl[2-4]进而将钴与镍分离。探讨在不同氯离子浓度、有机相浓度、相比(O/A)和初始pH条件下,钴萃取率的变化,同时分析镍的萃取率(定义为损失率),最终获得最高的钴萃取率,而镍损失率最低。
(2)Cyanex272萃取。在用萃取剂Cyanex272萃取前,采用4 M氢氧化钠溶液进行皂化,然后进行萃取,探讨不同的皂化率、有机相浓度、相比(O/A)和初始pH对钴萃取率的影响,同时分析镍的萃取率(定义为损失率)。最终获得最高的钴萃取率和最低镍损失率的最优条件。
(3)负载有机相的反萃。用稀硫酸作为反萃剂,研究不同反萃条件(反萃的相比O/A、硫酸浓度)对反萃效果的影响。
1.3 分析方法和仪器
溶液中金属离子钴、镍的测定采用PE-2100DV型电感耦合等离子体原子发射光谱仪(ICP-AES,美国Perkin-Elmer 公司)。
1.4 计算公式
2 结果与讨论
2.1 钴的萃取结果
2.1.1TOMAC的萃取
为了研究氯离子浓度对钴萃取结果的影响,改变氯离子浓度从0 M~5.5 M,调节酸浸出液(Co2+10.19 g/L,Ni2+1.12 g/L)pH为4,有机相浓度为0.72 M,以相比(O/A)=2的条件在25 ℃下进行萃取,振荡时间2 min,得到的结果如图1(a)。
从图1(a)中可以看出,随着氯离子浓度的上升,钴的萃取率也随之增加,其中从0 M到4 M的过程中,增加幅度巨大,增加了83.18%。随后缓慢上升,在[Cl-]=5.5 M时达到最大,此时钴的萃取率为98.05%。镍的损失率也随着氯离子浓度的升高而有所上升,但总体变化不大,从0 mol/L的0.1%到5.5 mol/L的0.86%,增加了0.76%,基本可以忽略。因此,5.5 mol/L的氯离子浓度是最佳的钴回收条件,此时钴的萃取率为98.05%,而镍的损失率仅为0.86%。周学玺采用季铵盐也得出当氯离子浓度达到4~5 mol/L后,钴的萃取率为82.6%,但几乎不萃取镍[16]。本试验进一步提高氯离子浓度到5.5 mol/L ,钴的萃取率较周学玺的萃取率上升了15.45%,达到98.05%,此时镍的损失率为0.86%,不到1%,可以忽略不计。
在[Cl-]=5.5 M,其它条件同上的情况下,改变有机相浓度,得到的结果如图1(b)所示。
从图1(b)中可以看出,随着有机相浓度的增加,钴的萃取率和镍的损失率都在逐渐上升,这与文献[21]中作者使用胺类萃取剂萃取时,提高萃取剂的浓度,萃取率也随之上升的结论类似。有机相浓度从0.18 M增加到0.72 M,钴的萃取率上升幅度较大,上升了60.83%。再继续随着有机相浓度增加,钴的萃取率继续增长,但幅度减缓;当有机相浓度达到0.8 mol/L后,增加有机相浓度,萃取率基本不变,且有机相变得粘稠,这给后面的两相分开增加了难度。镍的损失率随着有机相浓度的提高也在逐渐稳步上升,当有机相浓度为0.87 mol/L时,镍的损失率达到了1.06%,超过了1%。所以,有机相浓度0.8 mol/L为钴萃取的最佳条件,此时钴萃取率达到96.87%,镍损失率为0.89%。
在[Cl-]=5.5 M,有机相浓度0.8 M,其它条件同上的情况下改变相比,得到的结果如图1(c)所示。
从图1(c)中看出,在O/A=2.5时,钴的萃取率达到了最大值98.09%。但当O/A=2时,钴萃取率为97.85%,与最大值只相差0.24%,考虑到萃取剂的消耗和镍的损失率,相比为2时的镍的损失率比相比为2.5时的镍的损失率低,所以最佳相比为2,此时钴的萃取率为97.85%,镍的损失率为0.62%。
在[Cl-]=5.5 M,有机相浓度0.8 M,O/A=2,其它条件同上的情况下,改变溶液的初始pH,得到的结果如图1(d)所示。
从图1(d)中看出,pH对钴的萃取率影响较小,呈轻微下降趋势。这是因为在有机相中,TOMAC自身以盐的形式存在,水相pH对金属萃取的影响不大[16]。从开始的98.32%到最后的97.37%,下降了不到1%。镍的损失率随着pH的升高也有所下降,当pH=6时,镍的损失率最低仅为0.46%。因为考虑到钴的萃取率,所以最佳pH为4,此时的钴萃取率为98.05%,镍的损失率为0.86%。周学玺在使用季铵盐对钴和锰的萃取分离中也发现,在料液酸度>1时,钴的萃取率随pH增加略为下降[22]。
在综合考虑各影响因素的基础上,确定使用TOMAC进行钴萃取时的最佳条件:[Cl-]=5.5 M,有机相浓度0.8 M,O/A=2,初始pH=4,振荡时间2 min。在上述条件下,钴的一级萃取率为98.05%,而镍的损失率為0.86%。
2.1.2Cyanex272的萃取
为了研究皂化率对钴萃取结果的影响,使用4 M氢氧化钠溶液对萃取剂进行皂化,改变皂化率,调节酸浸出液pH为4,相比(O/A)=1,振荡时间2 min,有机相浓度为0.69 M,在25 ℃下进行萃取,得到的结果如图2(a)。确定好皂化率后,与上面确定TOMAC萃取的最佳条件的过程相似,依次改变有机相浓度、相比、初始pH值,得到如图2(b)、2(c)、2(d)所示的实验结果。
由图2(a)可以看出,随着皂化率的上升,钴的萃取率也随之上升,当皂化率为77.3%时,钴的萃取率为99.95%,镍的损失率为2.14%,所以确定萃取剂Cyanex272的最佳皂化率为77.3%。彭学斌等采用Cyanex 272 萃取分离硫酸钴溶液中的镍、钴,皂化率为75%,钴萃取率为99.86%[23]。本试验皂化率稍微上升,钴的萃取率也随之上升,结论相似。
从图2(b)可知,随着有机相浓度的增大,钴萃取率和镍损失率也随之增大。当有机相的浓度为0.69 M时,钴的萃取率最大达99.95%,镍的损失率为3.12%。因为当有机相浓度过高时,容易产生第三相(有机相和水相之间形成的不相混溶的第二有机相),第三相的产生易造成水相夹杂有机相,不利于后续的试验操作(如电解)[24]。综合考虑钴与镍的分离效果,有机相浓度0.56 M为萃取剂Cyanex272钴萃取的最佳条件。此时,钴的萃取率为98.38%,镍的损失率为2.28%。
由图2(c)可以看出,相比从0.25提高到1.00的过程中,钴的萃取率和镍的损失率都急剧上升,当相比为1.00时,钴的萃取率最大为99.95%,此时镍的损失率为2.21%。萃取率 E 与相比 R(O/A)的关系为E=D/(D+R)×100%,其中 D 为分配系数。 在 pH 值、萃取剂浓度等保持一定值,其它条件一致时,D 为常数,萃取率 E 随相比 R 减小而增大;若相比过大,使体系粘度增大影响分相效果及分相速度,若相比过小,则钴不能得到有效富集[25]。综合考虑萃取分离效果及钴离子富集等因素,萃取剂Cyanex272最佳相比为O/A=1。
由图2(d)可知,pH对萃取剂Cyanex272的影响较小,整体呈平缓趋势。在pH=4时,稍微上升,镍的损失率随着pH的增加而提高。综合考虑,最佳pH为4,此时钴的萃取率为71.56%,镍的损失率为2.62%。
综合考虑各影响因素后认为,萃取剂Cyanex272萃取钴的最佳条件:25 ℃、初始pH为4、Cyanex272浓度=0.56 M,皂化率75%左右,O/A=1,振荡时间2 min。在此条件下,钴的一级萃取率为98.38%,而镍的损失率为2.28%。
2.2 钴的反萃
在25 ℃、相比O/A=1/2的条件下,对用0.8 M TOMAC和0.56 M Cyanex272一级萃取后的含钴有机相(钴浓度分别为4.22 g/L和10.76 g/L)进行反萃,反萃时间3 min,考察硫酸浓度对反萃效果的影响。结果如图3(a)所示,随着硫酸浓度的上升,两种萃取剂萃取后的钴反萃率增加,变化规律相似。所不同的是,使用萃取剂TOMAC萃取后的钴反萃率在硫酸浓度为0 mol/L时,也就是说用纯水反萃时,萃取率能达到96.72%;在硫酸浓度为0.05 mol/L时,反萃率达到最高99.95%;之后,随着硫酸浓度的增加,反萃率基本保持不变。而使用萃取剂Cyanex272萃取后的钴反萃率在硫酸浓度为0.2 mol/L时达到最高,反萃率为99.99%。
在25 ℃,用0.05 mol/L的稀硫酸对用TOMAC一级萃取后的含钴有机相进行反萃,用0.2 mol/L的稀硫酸对用Cyanex272一级萃取后的含钴有机相进行反萃,反萃时间3 min,考察相比對反萃效果的影响,结果如图3(b)所示。可以看出,随着相比的降低,钴的反萃率上升。当O/A=1/2时,用TOMAC和Cyanex272萃取后的钴反萃率最高,分别为99.95%和99.99%,而镍检测不到。因此,两种含钴有机相的最佳反萃相比O/A=1/2。
综上,在萃取最优条件下,对含钴有机相进行反萃,使用TOMAC萃取后的有机相用0.05 mol/L的稀硫酸反萃,反萃相比O/A=1/2,一次反萃率达99.95%;使用Cyanex272萃取后的有机相用0.2 mol/L的稀硫酸反萃,反萃相比O/A=1/2,一次反萃率达99.99%。
2.3 两种萃取剂的对比
从以上结果可知,萃取剂TOMAC在萃取最佳条件下,钴的一级萃取率为98.05%,一次反萃率达99.95%,钴的最终回收率为98.00%;萃取剂Cyanex272在萃取最佳条件下,钴的一级萃取率为98.38%,一次反萃率达99.99%,钴的最终回收率为98.37%。萃取剂Cyanex272的钴萃取回收率仅高出TOMAC 0.37%。
从萃取成本看,TOMAC萃取剂成本相对较低。以本试验用的废锂离子电池为例,电池重量为36 g,其中所含金属钴为5.4 g左右。萃取回收1 kg的金属钴,需要Cyanex272的用量为25 L,而Cyanex272是进口药剂,其价格平均为700元/500 mL[26],回收1kg的钴成本为35 000元。相应地,回收1 kg的金属钴需要TOMAC的用量36 L,而TOMAC为国产产品,更方便易得,价格为358元/500 mL[26],回收1 kg的钴成本为26 000元。因此,使用萃取剂TOMAC成本更低。
从工艺操作方面看,采用TOMAC萃取剂可以使用纯水反萃,而Cyanex272则不能。另外,Cyanex272是酸性萃取剂,进行萃取操作前需要提前皂化,增加了操作工序以及皂化工序的成本。因此, 从工艺来看,采用萃取剂TOMAC更具优势。
综上所述,从废锂离子电池中萃取回收金属钴时,从成本、工艺操作等方面考虑,适宜采用胺类萃取剂TOMAC。
3 结论
考察了胺类萃取剂TOMAC和磷酸类萃取剂Cyanex272回收钴的萃取效率,得到以下结论。
(1)TOMAC的最佳萃取条件是:初始pH为4,萃取剂浓度0.8 M,[Cl-] =5.5 M,O/A=2,振荡时间2 min。在上述条件下,钴的一级萃取率为98.05%,而镍的损失率为0.86%。用0.05 M硫酸反萃,反萃相比O/A=1/2,一次反萃率均达到99.95%。最终得到钴的回收率是98.00%。
(2)Cyanex272萃取的最佳条件是:初始pH为4,萃取剂浓度0.56 M,皂化率75%左右,O/A=1,振荡时间为2 min。在上述条件下,钴的一级萃取率为98.38%,而镍的损失率为2.28%。用0.2 mol/L的稀硫酸反萃,反萃相比O/A=1/2,一次反萃率达99.99%,钴的最终回收率为98.37%。
(3)综合考虑萃取钴的成本和工艺,采用胺类萃取剂TOMAC较好。
参考文献:
[1] 徐健智,刘梦妹.废旧锂离子电池中的有价金属的回收技术研究[J].化工管理,2019(3):194-195.
[2] 陈欢欢.废旧锂离子电池中有价金属回收工艺的研究进展[J].中国金属通报,2018(5):34-36.
[3] 姚路. 废旧锂离子电池正极材料回收再利用研究[D].新乡:河南师范大学,2016.
[4] 王京,石香江,王寿成,等.未来中国钴资源需求预测[J].中国国土资源经济,2019,32(10):28-33.
[5] TORKAMAN R , ASADOLLAHZADEH M , TORAB-MOSTAE M , et al. Recovery of cobalt from spent lithium ion batteries by using acidic and basic extractants in solvent extraction process[J]. Separation and Purification Technology, 2017, 186:318-325.
[6] 刘美荣, 周桂英, 温建康. P507与Cyanex272协同萃取分离溶液中钴镍离子[J]. 过程工程学报, 2012, 12(3):415-419.
[7] ZOUBI W A, KANDIL F, CHEBANI M K. Solvent Extraction of Chromium and Copper Using Schiff Base Derived from Terephthaldialdehyde and 5-Amino-2-methoxy-phenol [J]. Arabian J. Chem., 2016, 9(4): 526-531.
[8] VIROLAINEN S , FALLAH F M , LAITINEN A , et al. Solvent extraction fractionation of Li-ion battery leachate containing Li, Ni, and Co[J]. Separation and Purification Technology, 2017, 179:274-282.
[9] 胡建锋, 朱云. P204萃取硫酸体系中钒的性能研究[J]. 稀有金属, 2007, 31(3):367-370.
[10] 吴月顺, 宋其圣, 俞海云,等. P5709萃取钴(Ⅱ)、镍(Ⅱ)的动力学研究[J]. 山东大学学报(理学版), 2001, 36(2):210-215.
[11] 鐘盛华, 汪小强, 吕永康, 等. P507分馏萃取分离钴镍的研究[J]. 中国有色冶金, 2012, 41(1):76-78.
[12] 王成彦, 胡福成. Cyanex272在镍钴分离中的应用[J]. 有色金属工程, 2001, 53(3):1-4.
[13] KANG J , SENANAYAKE G , SOHN J, et al. Recovery of cobalt sulfate from spent lithium ion batteries by reductive leaching and solvent extraction with Cyanex 272[J]. Hydrometallurgy, 2010, 100(3):168-171.
[14] 范艳青, 蒋训雄, 汪胜东,等. 富钴结壳浸出液中钴镍的N235萃取分离[J]. 有色金属工程, 2006, 58(3):70-72.
[15]张平伟, 朱屯. 钴镍协同萃取体系[J]. 过程工程学报, 1997(3):282-288.
[16] 周学玺, 朱屯. 季铵萃取分离钴镍的研究[J]. 中国有色金属学报, 1995(3):34-38.
[17] 陈燕飞,季尚军,常宏涛,等.P292与Alamine336协同萃取稀土元素的研究[J].有色金属(冶炼部分),2018(6):45-47.
[18] EYUPOGLU V , SURUCU A , KUNDURACIOGLU A . Synergistic extraction of Cr(VI) from Ni(II) and Co(II) by flat sheet supported liquid membranes using TIOA and TBP as carriers[J]. Polish Journal of Chemical Technology,2015,17(2):32-34.
[19] 易爱飞, 朱兆武, 张健, 等. 废旧三元电池正极活性材料盐酸浸出液中钴锰共萃取分离镍锂[J]. 有色设备, 2018(4):4-9.
[20] FILIZ M,SAYAR N A,SAYAR A A . Extraction of cobalt(II) from aqueous hydrochloric acidsolutions intoalamine 336mxylene mixtures[J].Hydrometallurgy,2006,81:167-173.
[21] TORKAMAN R , ASADOLLAHZADEH M, TORAB-MOSTAEDI M , et al. Recovery of cobalt from spent lithium ion batteries by using acidic and basic extractants in solvent extraction process[J]. Separation and Purification Technology, 2017,186:318-325.
[22] 周学玺, 许新, 马驰骋, 等. 季铵盐对钴(Ⅱ)和锰(Ⅱ)的萃取分离[J]. 中国有色金属学报, 2000, 10(4):542-545.
[23] 彭学斌,田林,翟忠标,等.Cyanex 272萃取分离硫酸钴溶液中镍钴的试验研究[J].矿冶工程,2018,38(6):127-130.
[24] 杨维俊. 萃取过程中第三相产生的原因及解决办法[J]. 新疆有色金属, 2014(4):80.
[25] 陈炎,程洁红. 醛肟萃取剂萃取分离废锂离子电池中的铜[J]. 过程工程学报, 2017, 17(6):1170-1175.
[26] 安平县盛阳金属丝网制品有限公司业务部.30万种化学试剂价格查询[EB/OL].(2012-06-25)[2019-08-09].https://www.chemical/book.com/Supplier News-431.htm.
