基于微波法制备玉米秸秆活性炭及对孔雀石绿的吸附
2019-04-01焦春霞张钢强高楼军
李 哲,焦春霞,张钢强,高楼军
(延安大学化学与化工学院;陕西省化学反应工程重点实验室,陕西延安716000)
染料在纺织业中被广泛使用,其大部分是复杂的芳香烃类化合物,具有复杂的化学结构、稳定性高、难降解、有毒等特点,其中孔雀石绿就是一种有毒、难降解的染料,如果处理不当就会引起严重的环境污染问题,目前处理染料废水的方法有吸附法、膜分离法、离子交换法、化学氧化法、光催化降解法等[1-5]。其中常用的吸附剂活性炭具有较大的比表面积和较高的化学稳定性,对于去除各种污染物具较强的作用,所以被广泛用于工业、医疗、环保等领域[7,8]。近年来,对活性炭研究的热点之一是利用廉价的农林废弃物为原料和简单清洁的工艺来制各经济效益高吸附性能好的生物质活性炭。
本文以玉米秸秆为原料,氯化锌活化-微波法所制得的活性炭,探究其对孔雀石绿的吸附性能,考察了吸附剂用量、吸附时间、介质pH值、染料初始浓度和温度等因素对吸附效果的影响,并研究了其吸附过程的热力学和动力学,为废水中有机染料的处理提供理论基础。
1 实验部分
1.1 仪器与试剂
UV-5100紫外可见分光光度计(上海元析仪器有限公司);XT-9900A型智能微波消解仪(上海—新拓分析仪器科技有限公司)。
玉米秸杆(采自于延安市枣园):采用当年废弃的玉米秸杆,剪成2 cm左右的小段,先用自来水洗去玉米秸杆上面的附着物,再用蒸馏水清洗、浸泡,放入烘箱中,在373 K的高温条件下烘干,粉碎,过筛,得到100目的玉米秸杆粉末,备用。
孔雀石绿溶液(25 mg/L);pH=5.8的HAc-NaAc缓冲溶液;水为二次蒸馏水。
1.2 活性炭制备方法
称取10 g玉米秸秆于100 mL烧杯中,加50 mL 60%的氯化锌溶液,封口,放置12 h后,过滤,放入消解罐内,在微波压力为2.5 MPa下消解360 s,然后在0.1 mol/L稀盐酸中煮沸20 min后,反复用蒸馏水清洗至无Cl-,最后在95 ℃下干燥,备用。
1.3 吸附平衡实验
在19个干燥碘量瓶中分别加入0.01 g的活性炭,以及浓度为25 mg/L孔雀石绿溶液:1 mL、3 mL、5 mL、7 mL、9 mL、11 mL、13 mL、15 mL、17 mL、19 mL、21 mL、23 mL、25 mL、27 mL、29 mL、31 mL、33 mL、35 mL、39 mL,pH=5.8的HAc-NaAc缓冲溶液5 mL,再分别加入蒸馏水使总体积均为50 mL。然后在室温下振荡50 min,离心后取上清液,测定滤液吸光度,计算吸附后孔雀石绿溶液浓度及吸附量。
1.4 吸附热力学和动力学实验
在干燥碘量瓶中分别加入0.01 g活性炭,以及13 mL浓度为25 mg/L的孔雀石绿溶液,各加入蒸馏水32 mL,pH=5.8的HAc-NaAc缓冲溶液5 mL,在不同温度(10 ℃、20 ℃、30 ℃、35 ℃、40 ℃、45 ℃)的恒温振荡器中分别振荡10 min、30 min、50 min、70 min、90 min、120 min、150 min、210 min之后,离心取上清液,测定其吸光度,计算吸附后孔雀石绿溶液浓度及吸附量。
2 结果与分析
2.1 缓冲溶液pH值对吸附量的影响
按照吸附平衡实验,于一系列干燥碘量瓶中分别加入0.01 g的活性炭,5 mL孔雀石绿溶液,不同体积不同pH值的缓冲溶液(pH为3.6、4.0、4.5、5.0、5.8、7.0的HAc-NaAc缓冲溶液和pH为7.5、8.0、8.5、9.0、9.5、10.0、10.5、11.0的NH3-NH4Cl缓冲溶液),再加入蒸馏水使体系总体积为50 mL,在室温下振荡60 min,离心后取上清液,测定滤液吸光度,计算吸附量。结果发现随着体系pH的增加,吸附量先增加后减小,在5 mL pH为5.8的HAc-NaAc缓冲溶液中体系的吸附量最佳,因此本实验选择pH=5.8的HAc-NaAc缓冲溶液5 mL作为吸附介质。
2.2 初始浓度对吸附的影响
按照吸附平衡实验,只改变孔雀石绿的初始浓度,在室温下进行测定,结果发现随着孔雀石绿初始浓度的增加,吸附量先增加,在初始浓度为13.5 mg/L后基本不变。因此实验选择14.0 mg/L为最佳浓度。
2.3 振荡时间对吸附的影响
按照吸附平衡实验,只改变振荡时间进行测定,结果发现在50 min后吸附量较大且基本稳定,达到平衡,因此本实验选择吸附时间为50 min。
2.4 活性炭质量对吸附的影响
按照吸附平衡实验,只改变活性炭量的用量进行实验,结果发现随着活性炭用量的增加,吸附量先增加后减小,在活性炭用量为0.01 g时出现最佳值,因此选择0.01 g作为吸附剂的用量。
2.5 温度对吸附的影响
在不同温度下进行实验,发现随着实验温度的增加,吸附量略有增加,因此选常温(295.15 K)下进行试验。
2.6 吸附平衡分析
按照吸附平衡实验结果,分别用Langmuir等温线模型和Freundlich等温线模型进行数据拟合[1],结果见表1所示:

表1 293.15K时吸附等温线模型
由表1中数据可见,活性炭对孔雀石绿的吸附用Langmuir方程的拟合度相对较好,R2>0.99,说明该吸附基本属于单分子层吸附。
2.7 吸附热力学分析[1]
按照吸附热力学实验,用ln(1/Ce)对1/T作图,如图1所示:
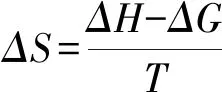
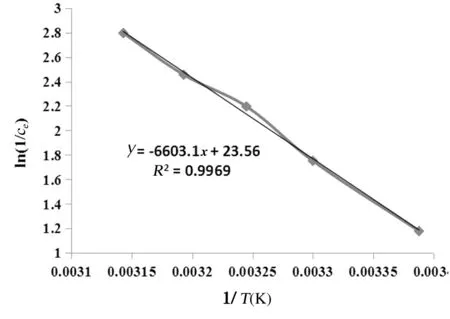
图1 热力学关系图
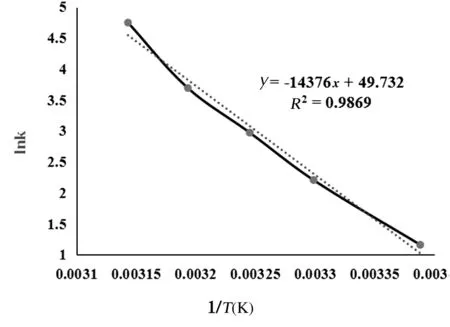
图2 lnk与1/T的关系
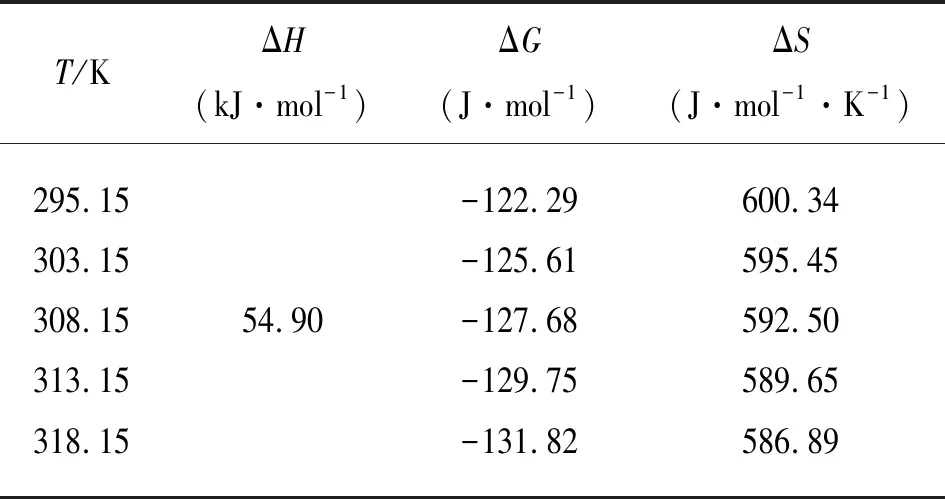
T/KΔH(kJ·mol-1)ΔG(J·mol-1)ΔS(J·mol-1·K-1)295.15303.15308.15313.15318.1554.90-122.29-125.61-127.68-129.75-131.82600.34595.45592.50589.65586.89
由表2可知,ΔH为正值,说明高温有利于吸附;ΔG为负值,说明吸附过程是自发过程;ΔS为正值,表明孔雀石绿从水溶液本体中溶解的自由状态到被吸附的状态是有序增加的过程。
2.8 吸附动力学分析[2]
根据吸附动力学试验分别对数据进行动力学线性拟合,由于反应一定时间后,吸附量不再发生变化,所以其不符合准一级动力学,对二级动力学拟合结果见表3所示。
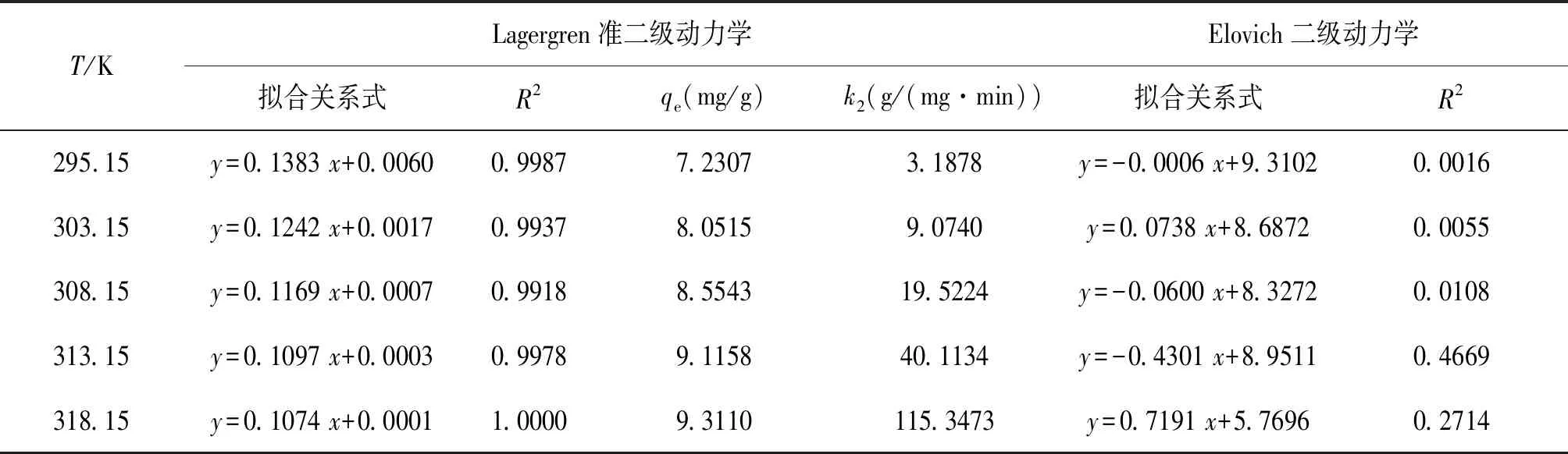
表3 活性炭吸附孔雀石绿的动力学模型及参数
由表3可以看出,活性炭吸附水中孔雀石绿较好的符合Lagergren准二级反应动力学模型,由lnk对1/T作图,如图2所示。根据阿龙尼乌斯公式算的吸附过程的表观活化能Ea=119.52 kJ·mol-1。
3 结论
(1)活性炭吸附孔雀石绿的最佳条件:吸附介质为pH=5.8的HAc-NaAc缓冲溶液5 mL、孔雀石绿初始浓度为14.0 mg/L、振荡时间为50 min、活性炭质量为0.01 g、温度为295.15 K。
(2)活性炭对孔雀石绿随吸附温度的升高吸附量先升高后降低,表明该吸附为一吸热过程;通过计算不同温度下各热力学参数ΔG、ΔH和ΔS,从理论上证实该吸附为一自发的吸热过程。
(3)吸附平衡符合Langmuir模型;Lagergren准二级反应动力学过程能较好地适合活性炭对孔雀石绿溶液的吸附。
