原发性输卵管癌的超声图像特征及误诊分析
2019-03-28欧阳小兰肖秋金
欧阳小兰 肖秋金
中国人民解放军第九四医院特诊科,江西南昌 333000
原发性输卵管癌(PFTC)是女性生殖系统少见恶性肿瘤,发病率约占女性恶性肿瘤的0.18%~1.60%,好发于绝经期女性,患者临床表现特异性有限,仅有约15%的患者存在“输卵管癌三联征”(阴道排液、腹痛、盆腔包块)表现[1]。临床诊断PFTC的方法包括血清CA125检测、细胞学检查、宫腔镜检查、诊断性刮宫等,但其诊断特异性均较为有限,加之该病发病率低、常被忽视,均造成临床PFTC误诊率极高,甚至达到94%~98%[2]。然而,PFTC恶性程度高、预后差,误诊所致治疗时机贻误也是影响患者生存质量的重要原因。越来越多的研究指出,PFTC发病率呈上升趋势,但其早期诊治率仍未得到有效改善[3-4]。此次研究就PFTC的超声图像特征及误诊原因进行了分析,望为临床PFTC的早期诊断提供参考依据。
1 对象与方法
1.1 研究对象
2014年8月至2018年5月于我院接受外科手术,经术后病理组织学检查明确PFTC诊断[5]的患者53例,患者术前超声检查资料保存完整。使用E8彩色多普勒超声诊断仪(美国GE公司),腔内、腹部探头频率分别为6~10 MHz、2~7 MHz。
年龄22~79岁,平均(56.71±11.32)岁,临床表现:阴道排液10例,阴道不规则出血5例,月经量增多3例,下腹痛25例,腹胀15例,盆腔包块35例,肛门坠胀或尿频尿急6例,10例无明显不适症状;月经状态:绝经35例,未绝经18例;病变位置:左侧输卵管24例,右侧输卵管25例,双侧输卵管4例;病理类型:浆液性腺癌40例,移行细胞癌7例,低分化子宫内膜样腺癌4例,肉瘤样癌2例。
1.2 判断标准
根据超声声像图改变判断病变分型[6],I型:附件区可见囊性结构且呈迂曲管状,囊壁可见单发或多发乳头样突起,彩色多普勒血流成像(CDFI)示乳头可见丰富的血流信号。Ⅱ型:附件区可见囊实性肿块,呈腊肠形改变,边界清晰,实性部分边缘或单侧沿输卵管走行方向可见囊性区,CDFI示实性部分可见较丰富或丰富的血流信号。Ⅲ型:附件区可见低回声肿块,呈腊肠形改变,边界清晰,CDFI示实性部分可见较丰富或丰富的血流信号。Ⅳ型:附件区可见单发或多发实性为主低回声肿块,边界欠清晰,CDFI示实性部分可见较丰富或丰富的血流信号;单侧或双侧附件区正常卵巢结构未显示,可见膀胱子宫陷窝腹膜增厚、子宫直肠陷窝腹膜增厚、大网膜增厚和(或)远处其他脏器转移。Ⅴ型:附件区未见异常改变,或仅可见输卵管积液表现。分析不同病变分型PFTC患者的超声图像特征及其误诊情况,总结误诊原因并探讨超声诊断思路。
1.3 统计学分析
对本临床研究的所有数据采用SPSS 22.0进行分析,计数资料以(n/%)表示,并采用χ2检验,计量资料以(x±s)表示,并采用t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 病变分型判断结果
53例PFTC患者中,超声分型Ⅰ型8例,Ⅱ型3例,Ⅲ型17例,Ⅳ型18例,Ⅴ型7例,分别占15.09%、5.66%、32.07%、33.96%、13.22%。
2.2 超声图像特征
超声分型Ⅰ型、Ⅱ型者术前超声准确诊断率均为100.00%;Ⅲ型诊断准确率82.35%,3例患者误诊为浆膜下肌瘤;Ⅳ型患者均误诊为卵巢来源恶性肿瘤,误诊率100%;Ⅴ型术前超声均漏诊。详见表1。

表1 53例PFTC患者术前超声分型表现及诊断结果分析(n/%)
3 讨论
PFTC的生物学行为与卵巢癌有极大相似之处,且临床及形态学特征与上皮性卵巢癌、原发性浆液性腹膜癌相似,加之其发病率低、早期典型表现缺乏,均导致临床漏诊或误诊率处于较高水平[7]。与此同时,较卵巢上皮癌而言,PFTC的预后更差,据报道,Ⅰ期PFTC患者5年生存率不足65%,而Ⅲ~Ⅳ期患者5年生存率仅为10%~20%[8],且多数患者在初始治疗后的3~5年内复发,目前尚无有效的二线治疗方案,故复发患者的预后极差[9]。
术前完善的影像学检查被认为能够提高PFTC诊断的准确性,如CT检查可见盆腔内实性或囊实性包块,特征性表现为包块呈梭形或腊肠型,最具意义的诊断征象为输卵管积水,而未见输卵管积水存在时,CT与MRI往往可见分叶状实性包块[10]。然而,由于设备因素与患者经济因素限制,CT和MRI难以成为PFTC的首选筛查技术。
得益于探头直接与盆腔脏器接触,经阴道彩色多普勒超声能够显示盆腔内细微结构,以及包块内血供、血流动力学特点,有望为PFTC的术前诊断提供一定参考。附件区腊肠状囊性肿块是超声声像图的典型特征(图1~3),进一步总结患者术前超声图像可见1)附件可见腊肠形囊性包块,囊性块壁上可见乳头状突起;2)附件为腊肠形实质性低回声包块;3)附件实质为不均质性包块。PFTC超声图像上述特征的产生原因可能为:肿瘤病灶多起源于输卵管粘膜并位于输卵管壶腹部,常导致伞端闭锁,此时输卵管往往因积水、积血而扩张,故呈腊肠形变化[11-12]。另一方面,随着病灶体积的增加,原有输卵管结构逐渐遭到破坏,实质性包块形成,可导致不均质实质性包块的出现[13]。
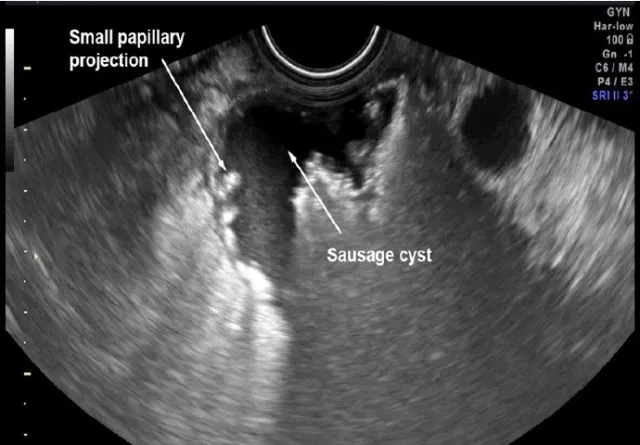
图1 左侧卵巢旁见一不规则长条囊性结构,其内可见乳头状突起,病灶体积1.4×0.9×1.0 mm)(Small papillary projection:小乳头突起;Sausage cyst:腊肠样囊肿)

图2 含富血供实性成分的腊肠样囊肿(Solid part:实性成分)

图3 右卵巢旁见范围约67×43不规则腊肠样囊肿,内见大小约23×16×15mm大乳头突起。盆腔内见范围约89×76mm的腹水(Sausage cyst:腊肠样囊肿;Uterus:子宫;Ascites:腹水;Papillary Projection:乳头状突起)
此次研究统计了术前超声的诊断准确率,结果显示,超声对PFTC的误诊率、漏诊率分别达到39.62%(21/53)、13.21%(7/53),进一步分析不同超声分型PFTC的超声图像特征及诊断结果可见,Ⅰ型、Ⅱ型、Ⅲ型PFTC的声像图改变具有典型性,超声图像往往可清晰显示病变侧卵巢,为临床诊断提供可靠参考,Ⅳ型和Ⅴ型术前超声误诊和漏诊率极高。绝经后卵巢易萎缩,此时超声检查往往难以显示正常卵巢,易误诊为卵巢癌[14],但卵巢癌常伴有中等或大量腹腔积液,而PFTC往往不会导致腹腔积液出现,可作为两种恶性肿瘤的鉴别诊断依据[15]。需要注意的是,本研究17例Ⅲ型PFTC患者中,3例误诊为浆膜下肌瘤,考虑与肿块体积较大且与子宫关系密切有关,两者的鉴别重点在于:浆膜下肌瘤多为球形,其内回声不均匀且可随子宫位置改变而移位,血流信号来源于子宫,而PFTC位于子宫和卵巢之间,走行迂曲不规则并主要沿输卵管方向,CDFI往往可见丰富的血流信号[15-16]。
Ⅳ型PFTC意味着病变已达晚期,此时肿块往往较大且伴有癌组织穿透浆膜,且常与盆腔组织、器官或肠管粘连,呈团块状,卵巢常因受侵所致正常结构损伤[17],虽然超声可见附件区恶性肿瘤,但肿瘤来源难以区分,故该型PFTC误诊率高达100%,其鉴别诊断依据仍有待探索。Ⅴ型PFTC往往较小,超声常难以发现,加之患者临床表现不典型,使其漏诊率达到100%。有学者认为,约有70%的PFTC患者合并慢性输卵管炎,且常伴有附件炎性包块、输卵管伞端闭锁、输卵管积液等病理生理改变[18],因此,对于合并肿瘤标志物升高、输卵管积液[19]、存在PFTC相关临床表现的患者而言,应高度怀疑PFTC并强调超声检查时输卵管仔细扫查,以指导早期诊治,改善患者预后质量。
综上所述,不同超声分型PFTC患者的超声图像特征存在一定差异,Ⅰ型、Ⅱ型、Ⅲ型PFTC的声像图改变具有典型性,超声诊断准确率值得肯定;Ⅳ型PFTC图像的典型性有限、Ⅴ型PFTC病变较小,均是导致临床误诊、漏诊率较高的主要原因。在今后的临床检查中,应强调超声图像内细微结构特征的仔细观察,并结合包块内血流特点及患者临床症状体征做出综合判断,以期为PFTC的鉴别诊断提供更为全面的参考。
