高强度间歇训练对大鼠骨骼肌细胞自噬的影响及其调节机制
2019-03-14李方晖艾竞一
李方晖,艾竞一,李 涛,孙 磊
(1.南京师范大学 体育科学学院,江苏 南京210046;2.华南师范大学 激光运动医学实验室和运动再生医学实验室,广东 广州510006)
1 前言
乙醛脱氢酶 2(acetaldehyde dehydrogenase 2,ALDH2)(Zhang et al.,2017)和去乙酰化酶3(sirtuin 3,SIRT3)(王海涛 等,2011)是线粒体生物发生和自噬的上游调控因子。SIRT3(Lin et al.,2014; Palacios et al.,2009)和 ALDH2(GUO et al.,2015)基因敲除小鼠的骨骼肌和心肌腺苷酸活化蛋白激酶(AMP-activated protein kinase, AMPK)活性降低,进而促使骨骼肌和心肌自噬活性下降(Nakashima et al.,2014);相反,促进骨骼肌 SIRT3(Lin et al.,2014)和ALDH2(Zhang et al.,2017)蛋白表达可激活骨骼肌自噬,改善机体有氧耐力。综上所述,SIRT3和ALDH2在维持骨骼肌线粒体质量控制系统功能过程中发挥重要作用,但HIIT是否能促进骨骼肌SIRT3和 ALDH2蛋白表达鲜见文献报道。
本文拟探讨 10周 HIIT对大鼠股直肌(以快肌纤维为主)和比目鱼肌(以慢肌纤维为主)(Carmeli et al.,2005)两种不同类型肌纤维的自噬相关蛋白和线粒体 SIRT3和ALDH2蛋白表达的影响,揭示 HIIT对骨骼肌自噬的影响及其潜在的作用机制。
2 材料与方法
2.1 实验动物
清洁级Sprague-Dawley(SD)雄性大鼠34只,约8周龄,体重 369.00±24.13 g,广东省医学动物实验中心提供(动物许可证号:SCXK【粤】2013-0002)。国家标准啮齿类动物常规饲料及垫料由广东省医学动物实验中心提供。动物实验内容和方案获得广东省医学动物实验中心使用伦理委员会的批准。所有大鼠保持自由饮食,饲料供给量根据体重增长相应的增加,每周更换垫料2~3次,环境温度20℃~23℃,相对湿度50%~70%,采用自然光照。
2.2 动物分组及运动方案
大鼠在实验室适应性喂养一周后随机分为 3组,即安静组(SC,n =10)、中等强度持续训练组(MICT,n =12)和高强度间歇训练组(HIIT,n =12)。MICT组和HIIT组在正式训练前进行 2周的适应训练。动物实验跑台【型号FD000043】购置于广州飞迪生物科技有限公司。正式训练方案参照 Criswell等(1993)微调。MICT组跑步速度为28 m/min,根据Bedford等(1979)和Liao等(2015)估算约为70% VO2max;HIIT组高强度跑步速度42 m/min约为95%~99% VO2max(洪平 等,2002; Sariret al.,2015),间歇期跑步速度18 m/min约为40%~45% VO2max(洪平等, 2002; Bedfordet al.,1979)。适应训练后进行正式训练(表 1),训练时段为晚间 18:30~22:00,周六和周日停训。

表1 本研究高强度间歇性训练与中等强度持续训练实施方案一览表Table 1 Programs of HIIT and MICT Training
2.3 测定跑步力竭时间和力竭测试前后的血乳酸
在末次训练后的次日对各组大鼠跑步力竭时间进行测定,具体方法参考施曼莉等(2015)文献方法执行。并在力竭时间测试前(pre-EX)、力竭时间测试即刻(IEX)、力竭时间测试后10 min(10 min POST)和力竭时间测试后3 h(3 hPOST)尾静脉取血测定血乳酸浓度(Neves et al.,2017)。
2.4 取材
为了去除力竭测试导致的急性效应的干扰,所有大鼠在力竭时间测试后先静息24 h,随后进行禁食12 h,禁食处理完毕后按照力竭时间测试的顺序对大鼠麻醉处死(施曼莉 等,2015)。步骤:按照4 ml/kg剂量10%水合氯醛麻醉后断颈,随后迅速取出股四头肌、腓肠肌和比目鱼肌称重,分别计算与体重的比值作为骨骼肌质量指数。将股直肌和比目鱼肌(Carmeli et al.,2005)用锡纸包裹投入液氮后置于-80℃冰箱保存。
2.5 蛋白免疫印迹检测蛋白表达
取股直肌和比目鱼肌进行蛋白提取和定量,并将各组蛋白样品在4%浓缩胶80 V恒压30 min,随后在12%分离胶150 V恒压60 min,300 mA恒定电流120 min;5%脱脂奶粉室温封闭 60 min,一抗孵育过夜;后转移于聚偏二氟乙烯膜上,再以1:1 000辣根过氧化物酶标记的羊抗兔IgG抗体(二抗)于37℃孵育60 min,洗涤后置于暗室曝光成像。利用Image J软件读取各条带灰度值,结果以目标蛋白灰度值与甘油醛-3-磷酸脱氢酶(glyceraldehyde-3-phosphate dehydrogenase, GAPDH)灰度值的比值表示。目标蛋白一抗:微管相关蛋白轻链 3A/B(microtubuleassociated protein light chain 3A/B, LC3A/B)、自噬相关蛋白(autophagy related gene,ATG)-5/-3/-7/-12/-16L、Beclin-1、ALDH2、SIRT3、细胞色素C氧化酶亚基IV(cytochrome C oxidase subunitIV, COXIV)和琥珀酸脱氢酶(succinate dehydrogenase,SDH)。ALDH2一抗购于艾博抗公司,其余一抗购于细胞信号技术公司。上述操作详见 QIAO等(2011)文献。
Research on the influence of the opening of residential district on the traffic state of the surrounding road network
2.6 透射电镜观察自噬体和线粒体的超微结构
取比目鱼肌组织在戊二醛固定后放入 1%锇酸固定60 min,并采用丙酮逐级脱水,环氧树脂包埋剂包埋,再置入烤箱中干燥;完成聚合后进行超薄切片,以醋酸铀和枸橼酸铅双染色后透射电镜下观察、拍照。每组 3只,每只 2个标本,选取 6 000倍进行拍摄,观察比目鱼肌自噬体和线粒体超微形态结构。具体方法参考 He等(2012)文献。
2.7 数据分析
采用SPSS 21.0软件分析数据,Graph Pad Prism软件作图。以平均数(Mean)±标准差(SD)表示。对所有指标均采用进单因素方差分析,多重比较采用 Tukey比较法,显著性水平为 P<0.05,非常显著性水平为 P<0.01;采用Pearson相关分析计算各变量间的相关系数,用“r”表示。
3 结果
3.1 各组大鼠体重和骨骼肌质量指数的改变
图 1显示各组大鼠最终体重和骨骼肌质量指数的变化情况。HIIT和MICT组大鼠最终体重降低,与SC组相比有非常显著性差异(P<0.01)(图 1A);MICT组腓肠肌质量指数(图 1C)和股四头肌质量指数(图 1D)分别增加21.80%和 12.10%,HIIT组腓肠肌质量指数(图 1C)和股四头肌质量指数(图 1D)分别增加 14.60%和 10.60%,与SC组相比均有显著性差异(P<0.05);HIIT和 MICT组比目鱼肌质量指数与 SC组相比无显著性差异(P>0.05,图1B)。

图1 各组大鼠的最终体重(A)比目鱼肌(B)腓肠肌(C)和股四头肌(D)质量指数的变化Figure 1. Changes of FinalBody Weight (A) Soleus (B) Gastrocnemius (C) and Quadriceps (D) Muscles MassIndex
3.2 各组大鼠跑步力竭时间和力竭测试前后血乳酸水平的改变
图2A显示各组大鼠跑步力竭时间的变化情况。HIIT和MICT组大鼠跑步力竭时间明显增加(图 2A),与SC组相比有非常显著性差异(P<0.01);HIIT组大鼠跑步力竭时间长于MICT组,与MICT组相比有显著性差异(P<0.05)。
图2B显示各组大鼠力竭测试前后的血乳酸变化。HIIT和MICT组力竭测试后即刻血乳酸均降低,与SC组相比均有非常显著性差异(P<0.01);在力竭测试后 10 min,HIIT组大鼠血乳酸低于SC组,与SC组相比有显著性差异(P<0.05),但MICT组与SC组相比没有显著性差异(P>0.05)。

图2 各组大鼠跑步力竭时间(A)和跑步力竭时间测试前后的血乳酸(B)变化Figure 2. Changes of Time to Exhaustion(A) and Blood Lactate Levels (B) after theExhaustionTest
3.3 线粒体功能蛋白及其调控蛋白表达的改变
图3A显示各组大鼠比目鱼肌COXIV、SDH、SIRT3和ALDH2蛋白表达情况。HIIT和MICT组比目鱼肌COXIV、SDH、SIRT3蛋白表达增加,且分别与SC组相比有非常显著性(P<0.01)和显著性(P<0.05)差异;HIIT组比目鱼肌COXIV蛋白表达高于MICT组,与MICT组相比具有显著性差异(P<0.05)。
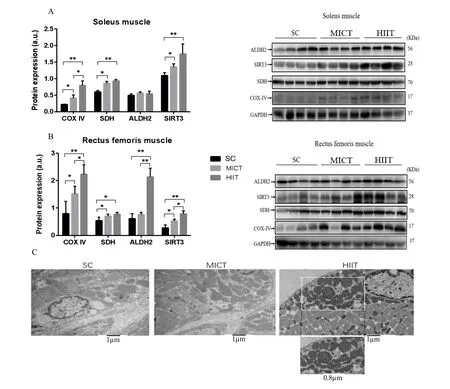
图3 比目鱼肌(A)、股直肌(B)线粒体功能蛋白表达和比目鱼肌线粒体超微结构(C)变化Figure 3. Changes of Mitochondrial Function Protein Expression inthe Soleus (A),Rectus Femoris Muscles(B), andUltrastructure ofSoleusMuscleMitochondria (C)
图 3B显示各组大鼠股直肌 COX IV、SDH、SIRT3和ALDH2蛋白表达情况。HIIT组和 MICT组股直肌 SDH蛋白表达高于SC组,与SC组相比有显著性差异(P<0.05);HIIT组股直肌COX IV和SIRT3蛋白含量高于SC组,与SC组相比有非常显著性差异(P<0.01);MICT组股直肌COX IV和SIRT3蛋白表达高于SC组,但低于HIIT组,且分别与 SC和 HIIT组相比均有显著性差异(P<0.05);HIIT组股直肌 ALDH2蛋白表达高于 SC组和 MICT组,且分别与 SC组和 MICT组相比有非常显著性差异(P<0.01)。
图 3C显示各组大鼠比目鱼肌的线粒体超微结构改变情况。HIIT和 MICT组大鼠比目鱼肌的线粒体体积和内膜嵴密度明显增大。
3.4 骨骼肌自噬相关蛋白表达和自噬体形态的改变
图 4显示各组大鼠比目鱼肌和股直肌的自噬相关蛋白表达和比目鱼肌自噬体形态的变化情况。图 4A显示,HIIT组比目鱼肌 LC3-II/LC3-I比值、LC3-II、Beclin-1、ATG-3、ATG-5、ATG-7和ATG-12蛋白表达高于SC组,且与 SC组相比均有显著性差异(P<0.05);图 4B显示,与SC组相比,HIIT组股直肌Beclin-1、ATG-5和ATG-7蛋白表达高于SC组,与SC组相比有显著性差异(P<0.05);透射电镜显示,HIIT组大鼠比目鱼肌细胞内部出现典型的双层膜结构的自噬体(图4C)。

图4 比目鱼肌(A)和股直肌(B)自噬相关蛋白表达和自噬体形态(C)的改变Figure4. Changes of Autophagy Protein ExpressionintheSoleus(A) and RectusFemorisMuscles (B) andthe Form of Autophagic Vacuole (C)
3.5 相关性分析
图5A显示,大鼠跑步力竭时间与股直肌SDH(r=0.58,P<0.05)、COXIV(r=0.74,P<0.01)、Beclin-1(r=0.63,P<0.05)、ALDH2(r=0.68,P<0.01)和 SIRT3(r=0.63,P<0.05)蛋白含量呈正相关;跑步力竭时间与比目鱼肌SDH(r=0.87,P<0.01)、COXIV(r=0.70,P<0.01)、Beclin-1(r=0.78,P<0.01)和 LC3-II(r=0.63,P<0.05)蛋白含量呈正相关。
图5B显示,股直肌SIRT3蛋白含量与SDH(r=0.74,P<0.01)、COXIV(r=0.87,P<0.01)、Beclin-1(r=0.66,P<0.05)和 ALDH2(r=0.63,P<0.05)蛋白含量呈正相关;股直肌 ALDH2蛋白含量与 Beclin-1(r=0.94,P<0.01)及COXIV(r=0.66,P<0.05)蛋白含量呈正相关。
图 5C显示,比目鱼肌 SIRT3蛋白含量与 SDH(r=0.58,P<0.05)、COXIV(r=0.72,P<0.01)蛋白含量及LC3-II/LC3-I 比值(r=0.61,P<0.05)呈正相关,SDH蛋白含量与LC3-II/LC3-I比值(r=0.58,P<0.05)呈正相关。

图5 各功能参数之间的Pearson相关性分析Figure 5. Pearson Correlation Analysis among Functional Variables
4 讨论
4.1 HIIT对大鼠有氧代谢能力的影响
HIIT是提高有氧耐力省时有效的训练模式(胡国鹏等,2017; Gibala et al.,2009; Little et al.,2010; Pereira et al.,2013;Perry et al.,2008)。与MICT相比,HIIT能更显著提高骨骼肌的线粒体氧化酶活性和脂肪氧化速率(梁春瑜 等,2017;施曼莉 等,2015;王林佳 等,2016;Helgerud et al.,2007; Little et al.,2010; Lkahtani et al.,2013; Weng et al.,2013)。本文也证实,HIIT对提高大鼠跑步力竭时间优于 MICT组(图2A);在对跑步力竭时间测试前后血乳酸测定也显示,HIIT组大鼠机体的血乳酸清除能力也明显增强(图2B);此外,本文也检测了表征线粒体氧化磷酸化活性的COX IV和 SDH蛋白表达(田野,2003)。结果也发现,HIIT和MICT均能上调比目鱼肌和股直肌COX IV和SDH蛋白表达;但 HIIT组比目鱼肌和股直肌 COX IV蛋白表达高于MICT组(图3A和B);采用TEM观察线粒体超微结构也发现了HIIT组大鼠比目鱼肌的线粒体体积和内膜嵴密度增大的现象(图 3C),这与已有文献报道一致(Criswell et al.,1993; Macinnis et al.,2017)。本文相关性分析也显示,比目鱼肌和股直肌COX IV和SDH蛋白含量均与跑步力竭时间呈正相关(图 5A)。已有文献也表明,骨骼肌线粒体正向重塑与自噬活性的改变有关(梁春瑜 等,2017; Lira et al.,2013; Little et al.,2010; Sin et al.,2016; Webster et al.,2013)。本文发现的 HIIT组大鼠骨骼肌线粒体功能增强是否与细胞自噬活性上调有关?
4.2 HIIT对骨骼肌细胞自噬的影响
细胞自噬是在自噬相关蛋白调控下利用溶酶体降解自身受损的细胞器和大分子物质过程。自噬的启动源于 LC3蛋白翻译,随后被胞浆中的 ATG-4酶切转变为 LC3-I形式;LC3-I在ATG-7、ATG-3及ATG-5—ATG-12—ATG-16复合物的作用下与磷脂酰乙醇胺(phosphatidylethanolamine,PE)结合,形成具有膜结合能力的 LC3-II(漆正堂 等,2013; Laker et al.,2017)。因自噬泡闭合过程中仅LC3-II定位于吞噬泡膜上,故可将 LC3-II蛋白表达水平和 LC3-II/LC3-I比值分别用于表征自噬体形成和自噬活性水平(Ogura et al.,2011)。在自噬体的形成过程中,哺乳动物第III类 PI3激酶(PI3K-III)与 Beclin-1及 ATG-14L形成Beclin-1复合物(Beclin-1 complex),加速自噬信号的传递,从而正向调控自噬体形成(Laker et al.,2017)。
本研究中,HIIT组大鼠比目鱼肌LC3-II/LC3-I比值、LC3-II、Beclin-1、ATG-3、ATG-5、ATG-7 和 ATG-12 蛋白表达均明显升高(图 4A)。提示:HIIT可能加速了自噬体的延伸和闭合过程,进而促进自噬体的形成过程(图6)。本文图 4C透射电镜也观察到了比目鱼肌典型双层膜结构的自噬体。已有研究表明(祖靓 等,2013; He et al.,2012;Ogura et al.,2011),耐力运动和急性运动均能上调骨骼肌、心肌、肝脏、脂肪和大脑皮质等组织的自噬活性,进而促进细胞对运动刺激的代谢性适应;然而,特异性敲除骨骼肌ATG-3基因的小鼠在急性运动过程更易引发氧化损伤,导致骨骼肌线粒体氧化功能失调和耐力下降(Lira et al.,2013)。细胞研究进一步证实,增强自噬活性可促进线粒体生物发生信号通路的激活(Sin et al.,2016; Webster et al.,2013)。本文相关性结果显示:比目鱼肌 LC3-II/LC3-I比值与SDH蛋白含量呈正相关(图5C);说明,HIIT改善比目鱼肌线粒体功能可能与自噬活性上调有关。
本文也发现,MICT与SC组相比,股直肌和比目鱼肌的自噬相关蛋白表达均无明显变化。这与 Lira等(2013)文献报道一致。Lira等(2013)在检测 C57BL/6小鼠持续耐力运动 28天后比目鱼肌 LC3-II/LC3-I比值也未发生改变。Schwalm等(2015)研究进一步表明,耐力运动对骨骼肌自噬活性的影响依赖于运动强度。推测,本文中MICT组大鼠采用的运动强度可能不足以促进骨骼肌的自噬相关蛋白表达。然而,HIIT组股直肌 LC3-II/LC3-I比值及LC3-II、ATG-3、ATG-12蛋白表达并未明显增加(图4B),说明 HIIT对骨骼肌自噬活性和自噬相关蛋白表达的影响也可能与肌纤维类型有关。
4.3 HIIT对骨骼肌自噬的机制探讨
作为细胞内的能量感应器,AMPK被认为是自噬的调控因子(漆正堂 等,2013)。AMPK通过抑制雷帕霉素靶蛋白(mammalian target of rapamycin,mTOR)活性及增加ATG-1激酶同源蛋白 ULK1磷酸化水平来启动自噬过程(漆正堂 等,2013)。作为 AMPK途径的上游调节因子,SIRT3既能通过调控 AMPK活性间接上调自噬活性,也能对自噬相关蛋白乙酰化修饰直接促进自噬体的形成(Palacios et al.,2009; Shi et al.,2015)。此外,定位于线粒体基质的ALDH2也能通过调控AMPK/mTOR通路实现对骨骼肌自噬的正向调节作用,进而保护急性运动诱导的骨骼肌氧化损伤(Zhang et al.,2017)。而 SIRT3(Palacios et al.,2009)和 ALDH2(Nakashima et al.,2014)基因敲除小鼠的骨骼肌 AMPK/mTOR途径及自噬活性明显下调。总之,在调控自噬过程中,线粒体 SIRT3(Palacios et al.,2009; Shi et al.,2015)和 ALDH2(Guo et al.,2015)是AMPK/mTOR途径的上游调控因子。尽管文献报道了HIIT可激活骨骼肌AMPK(梁春瑜 等,2017; Gibalaet al.,2009),但SIRT3和ALDH2在HIIT激活骨骼肌自噬过程中的作用尚不清楚?
在本研究中,HIIT和 MICT均能促进大鼠股直肌和比目鱼肌SIRT3蛋白表达(图3A和B)。这与前人研究一致(Hokari et al.,2010;Palacios et al.,2009)。矛盾的是,Edgett等(2016)和 Casuso等(2017)研究却发现,6周冲刺训练无法上调受试者股外侧肌 SIRT3蛋白表达;提示,运动对骨骼肌 SIRT3蛋白表达的影响可能与运动方式和骨骼肌类型有关。文献表明(Lin et al.,2014),小鼠骨骼肌特异性过表达 SIRT3可提升小鼠耐力水平;而这与骨骼肌 SDH和 COX IV活性增加有关(Finley et al.,2011;Vassilopoulos et al.,2014)。本文也证实,比目鱼肌和股直肌SIRT3与SDH和COX-IV蛋白含量均呈正相关(图5B和C);同时,比目鱼肌SIRT3蛋白含量也与LC3-II/LC3-I比值呈正相关(图5 C);推测,比目鱼肌SIRT3可能通过正向调控自噬活性来提升线粒体功能。
与SC组大鼠相比,MICT组股直肌和比目鱼肌ALDH2蛋白含量均无显著性差异,尽管 HIIT组大鼠股直肌ALDH2蛋白表达增加并具有显著性差异,但在比目鱼肌中无显著性差异(图 3A、B)。值得注意的是,股直肌ALDH2蛋白含量与跑步力竭时间呈正相关(图 5B),提示:股直肌 ALDH2蛋白表达上调可能与大鼠耐力水平提升有关。Zhang等(2017)研究证实,骨骼肌过表达ALDH2小鼠的跑步力竭时间明显增加。该课题组另一项研究进一步发现,ALDH2能通过上调SIRT3蛋白表达来促进线粒体氧化磷酸化蛋白表达(Hu et al.,2016)。本文也证实,股直肌ALDH2与SIRT3及COX IV蛋白含量均呈正相关(图 5B)。综上可知,尽管 ALDH2并未参与 HIIT对比目鱼肌自噬的调控,但可能介导了HIIT对股直肌线粒体功能改善的过程。然而,HIIT是如何通过 ALDH2调控线粒体氧化功能仍有待深入研究。
图6总结了HIIT上调比目鱼肌自噬活性的可能机制。尽管文献报道了 HIIT上调骨骼肌 AMPK磷酸化活性(梁春瑜 等,2017; Gibala et al.,2009);但遗憾的是,本文并未论证10周HIIT能上调比目鱼肌AMPK磷酸化水平及其下游mTOR活性。因此,今后的研究应在证实HIIT激活比目鱼肌 AMPK/mTOR信号通路的基础上,进一步探究 HIIT对SIRT3基因敲除小鼠比目鱼肌自噬的影响,进而明确SIRT3调控AMPK/mTOR通路介导了HIIT激活骨骼肌自噬的过程。

图6 HIIT调控骨骼肌细胞自噬潜在机制示意图Figure 6. Schematic of HIITRegulatedAutophagyand Relevant Mechanisms
5 小结
10周 HIIT能上调比目鱼肌细胞自噬活性及自噬相关蛋白表达,但并未上调股直肌自噬活性,线粒体 SIRT3可能参与了HIIT对比目鱼肌细胞自噬的调控过程。
洪平,赵鹏,杨奎生,2002.不同强度运动时大鼠骨骼肌能量代谢产物的变化[J].中国运动医学杂志,21(3):261-267.
胡国鹏,郑阳,孟妍,等,2017.大强度间歇训练与中等强度持续训练对耗氧量动力学特征影响的比较研究[J].体育科学,37(3):58-67.
黎涌明,2015.高强度间歇训练对不同训练人群的应用效果[J].体育科学,35(8):59-75.
梁春瑜,王林佳,倪震,等,2017.不同时长高强度间歇训练与中等强度持续运动对大鼠骨骼肌 AMPK、PGC-1α表达量及最大摄氧量的影响[J].中国运动医学杂志,05(36):390-399.
漆正堂,丁树哲,2013.运动适应的细胞信号调控:线粒体的角色转换及其研究展望[J].体育科学,33(7):65-69.
施曼莉,朱荣,2015.高强度间歇运动对骨骼肌糖原含量的影响及机制研究[J].体育科学,35(4):66-71.
田野,2003.运动生理学高级教程[M].北京:高等教育出版社.
王海涛,刘玉倩,赵焕彬,等,2011.运动对骨骼肌线粒体去乙酰化酶3(SIRT3)的影响[J].体育科学,31(1):85-88.
王林佳,苏浩,梁春瑜,等,2016.不同时长HIIT与中等强度运动后大鼠VO2max及血液心血管风险指标的变化[J].中国体育科技,52(6):81-85.
祖靓,朱荣,2013.力竭运动对小鼠骨骼肌细胞自噬的影响及相关调节机制研究[J].体育科学,33(9):77-84.
BEDFORD TG, TIPTON CM, WILSON NC, et al.,1979. Maximum oxygen consumption of rats and its changes with various experimental procedures[J]. J Appl Physiol Respir Environ Exerc Physiol, 47(6):1278-1283.
CARMELI E, MOAS M, LENNON S, et al.,2005. High intensity exercise increases expression of matrix metalloproteinases in fast skeletal muscle fibres[J]. Exp Physiol, 90(4):613-619.
CASUSO RA, PLAZA-DÍAZ J, RUIZ-OJEDA FJ, et al.,2017. Highintensity high-volume swimming induces more robust signaling through PGC-1α and AMPK activation than sprint interval swimming in m. triceps brachii[J]. PLoS One, 12: e0185494.
CRISWELL D, POWERS S, DODD S, et al.,1993. High intensity training-induced changes in skeletal muscle antioxidant enzyme activity[J]. Med Sci Sports Exerc,25(10):1135-1140.
EDGETT BA, BONAFIGLIA JT, BAECHLER BL, et al.,2016. The effect of acute and chronic sprint-interval training on LRP130,SIRT3, and PGC-1α expression in human skeletal muscle[J]. Physiol Rep, 4: pii: e12879.
FINLEY LW, HAAS W, DESQUIRET-DUMAS V, et al.,2011.Succinate dehydrogenase is a direct target of sirtuin 3 deacetylase activity[J]. PLoS One, 6: e23295.
FOX EL, BARTELS RL, BILLINGS CE, et al.,1973. Intensity and distance of interval training programs and changes in aerobic power[J]. Med Sci Sports, 5(1):18-22.
GARBER K,2012. Autophagy. Explaining exercise[J]. Science,335(6066):281-281.
GIBALA MJ, MCGEE SL, GARNHAM AP, et al.,2009. Brief intense interval exercise activates AMPK and p38 MAPK signaling and increases the expression of PGC-1alpha in human skeletal muscle[J].J Physiol, 106(3):929-934.
GUO Y, YU W, SUN D, et al.,2015. A novel protective mechanism for mitochondrial aldehyde dehydrogenase (ALDH2) in type I diabetesinduced cardiac dysfunction: Role of AMPK-regulated autophagy[J].Biochim Biophys Acta, 1852(2):319-331.
HE C, RHEA SUMPTER J, LEVINE B,2012. Exercise induces autophagy in peripheral tissues and in the brain[J]. Autophagy,8(10):1548-1551.
HELGERUD J, HØYDAL K, WANG E, et al.,2007. Aerobic highintensity intervals improve VO2maxmore than moderate training[J].Med Sci Sports Exerc, 39(4):665-671.
HOKARI F, KAWASAKI E, SAKAI A, et al.,2010. Muscle contractile activity regulates Sirt3 protein expression in rat skeletal muscles[J]. J Appl Physiol (1985), 109:332-340.
HU N, REN J, ZHANG Y,2016. Mitochondrial aldehyde dehydrogenase obliterates insulin resistance-induced cardiac dysfunction through deacetylation of PGC-1α[J]. Oncotarget,7:76398-76414.
LAKER RC, DRAKE JC, WILSON RJ, et al.,2017. AMPK phosphorylation of Ulk1 is required for targeting of mitochondria to lysosomes in exercise-induced mitophagy[J]. Nat Commun, 8(1):548.
LAURSEN PB, MARSH SA, JENKINS DG, et al.,2007. Manipulating training intensity and volume in already well-trained rats: Effect on skeletal muscle oxidative and glycolytic enzymes and buffering capacity[J]. Appl Physiol Nutr Metab, 32(3): 434-442.
LIAO J, LI Y, ZENG F, et al.,2015. Regulation of mTOR pathway in exercise-induced cardiac hypertrophy[J]. Int J Sports Med,36(5):343-350.
LIN L, CHEN K, ABDEL KHALEK W, et al.,2014. Regulation of skeletal muscle oxidative capacity and muscle mass by SIRT3[J].PLoS One, 9:e85636.
LIRA VA, OKUTSU M, ZHANG M, et al.,2013. Autophagy is required for exercise training-induced skeletal muscle adaptation and improvement of physical performance[J].FASEB J, 27(10):4184-4193.
LITTLE JP, SAFDAR A, WILKIN GP, et al.,2010. A practical model of low-volume high-intensity interval training induces mitochondrial biogenesis in human skeletal muscle: potential mechanisms[J]. J Physiol, 588(Pt 6):1011-1022.
LKAHTANI SA, KING NA, HILLS AP, et al.,2013. Effect of interval training intensity on fat oxidation, blood lactate and the rate of perceived exertion in obese men[J]. Springerplus, 2:532.
LOVERSO F, CARNIO S, VAINSHTEIN A, et al., 2014. Autophagy is not required to sustain exercise and PRKAA1/AMPK activity but is important to prevent mitochondrial damage during physical activity[J]. Autophagy, 10(11):1883-1894.
MACINNIS MJ, ZACHAREWICZ E, MARTIN BJ, et al.,2017.Superior mitochondrial adaptations in human skeletal muscle after interval compared to continuous single-leg cycling matched for total work[J].J Physiol, 595(9):2955-2968.
NAKASHIMA Y, OHSAWA I, NISHIMAKI K, et al.,2014.Preventive effects of Chlorella on skeletal muscle atrophy in musclespecific mitochondrial aldehyde dehydrogenase 2 activity-deficient mice[J]. BMC Complement Altern Med, 14:390.
NEVES CH, TIBANA RA, PRESTES J, et al., 2017.Digoxin induces cardiac hypertrophy without negative effects on cardiac function and physicalperformance in trained normotensive rats[J]. Int J Sports Med, 38(4):263-269.
OGURA Y, IEMITSU M, NAITO H, et al.,2011.Single bout of running exercise changes LC3-II expression in rat cardiac muscle[J].Biochem Biophys Res Commun, 414(4):756-760.
PALACIOS OM, CARMONA JJ, MICHAN S, et al.,2009. Diet and exercise signals regulate SIRT3 and activate AMPK and PGC-1alpha in skeletal muscle[J]. Aging (Albany NY), 1(9):771-783.
PEREIRA F, MORAES RD, TIBIRIÇÁ E, et al.,2013. Interval and continuous exercise training produce similar increases in skeletal muscle and left ventricle microvascular density in rats[J]. Biomed Res Int, (3):752817.
PERRY CG, HEIGENHAUSER GJ, BONEN A, et al.,2008. Highintensity aerobic interval training increases fat and carbohydrate metabolic capacities in human skeletal muscle[J]. Appl Physiol Nutr Metab, 33(6):1112-1123.
QIAO S, DENNIS M, SONG X, et al.,2011.A REDD1/TXNIP prooxidant complex regulates ATG4B activity to control stress-induced autophagy and sustain exercise capacity[J]. Nat Commun, 6:7014.
SARIR H, EMDADIFARD G, FARHANGFAR H, et al.,2015. Effect of vitamin E succinate on inflammatory cytokines induced by highintensity interval training[J]. J Res Med Sci, 20(12):1177-1181.
SCHWALM C, JAMART C, BENOIT N, et al.,2015.Activation of autophagy in human skeletal muscle is dependent on exercise intensity and AMPK activation[J]. FASEB J, 29(8):3515-3526.
SHI L, ZHANG T, ZHOU Y, et al.,2015.Dihydromyricetin improves skeletal muscle insulin sensitivity by inducing autophagy via the AMPKPGC-1α-Sirt3 signaling pathway[J]. Endocrine, 50(2):378-389.
SIN J, ANDRES AM, TAYLOR DJ, et al.,2016.Mitophagy is required for mitochondrial biogenesis and myogenic differentiation of C2C12 myoblasts[J]. Autophagy, 12(2):369-380.
VASSILOPOULOS A, PENNINGTON JD, ANDRESSON T, et al.,2014.SIRT3 deacetylates ATP synthase F1 complex proteins in response to nutrient- and exercise-induced stress[J]. Antioxid Redox Signal, 21:551-564.
WEBSTER BR, SCOTT I, HAN K, et al.,2013.Restricted mitochondrial protein acetylation initiates mitochondrial autophagy[J]. J Cell Sci, 126(Pt 21):4843-4849.
WENG TP, HUANG SC, CHUANG YF, et al.,2013.Effects of interval and continuous exercise training on CD4 lymphocyte apoptotic and autophagic responses to hypoxic stress in sedentary men[J]. PLoS One, 8(11): e80248.
ZHANG Q, ZHENG J, QIU J, et al.,2017.ALDH2 restores exhaustive exercise-induced mitochondrial dysfunction in skeletal muscle[J].Biochem Biophys Res Commun, 485:753-760.
