雷公藤新碱对LPS诱导小鼠骨髓树突状细胞成熟分化过程及炎症因子分泌的影响
2019-03-13闫越颖王政洁
张 伟 闫越颖 王政洁
(菏泽市立医院皮肤科,菏泽274000)
自1936年首次发现雷公藤红素以来,人们在卫矛科雷公藤属植物雷公藤中已分离得到生物碱、萜类及多糖等有效成份100余种[1,2]。既往研究表明雷公藤具有抗炎及免疫抑制作用,在类风湿关节炎、器官移植、肿瘤等疾病治疗中具有显著疗效[3,4]。近期研究发现,雷公藤能够阻止淋巴细胞增殖,诱导活化的淋巴细胞凋亡,对T细胞具有显著的抑制作用[5,6],但详细机制不明;树突状细胞(Dendritic cells,DCs)是调控免疫系统最强细胞之一,其成熟后在T细胞激活过程中发挥关键作用,是机体激活T细胞的最重要因素[7]。
雷公藤生物学成份复杂,其生理活性成份主要为二萜内酯、生物碱、三萜等。其中生物碱包括雷公藤精碱(Wilforgine)、雷公藤新碱(Euonine)、卫矛碱(Euonymine)等[8]。雷公藤新碱分子式为C38H47NO18,作为雷公藤重要的活性成分之一,是否具有与雷公藤相似的药理学作用及其详细作用机制,有待进一步探讨。本研究通过流式细胞术与抗体芯片技术检测雷公藤新碱对LPS诱导树突状细胞(Dendritic cells,DCs)成熟过程中表面分子变化、抗原吞噬能力及细胞因子分泌的变化,以探明雷公藤新碱对DCs成熟过程影响的具体作用机制,为临床应用雷公藤治疗自身免疫性等炎症相关疾病找到理论依据。
1 材料与方法
1.1材料 流式细胞仪购自BD公司(Aria2,BD,USA),雌性C57BL/6小鼠购自山东大学动物实验中心,RPMI1640培养基购自Gibco公司,无钙镁的Hank′s平衡盐溶液购自Hyclone公司,rmGM-CSF购自瑞典ProSpec公司(#cyt-720),rmIL-4购自美国R&D公司(# 404-ML-010),LPS购自Sigma公司(#L2630),MHCⅡ、CD80、CD86等流式抗体购自BD公司,抗体芯片购自Abcam公司(#Ab133995),雷公藤新碱购自南京景竹生物科技有限公司(# 37239-48-8)。
1.2方法
1.2.1小鼠骨髓DCs的获取 将C57BL/6小鼠颈椎脱位法处死,取出股骨与胫骨浸泡在RPMI1640培养中,用1 ml培养基冲洗骨髓腔中的骨髓,收集骨髓悬液,离心弃上清;加入细胞沉淀体积3倍量Tris-NH4Cl溶液室温裂解红细胞,离心弃上清,PBS洗涤2~3次;使用RPMI1640培养基重悬细胞,以细胞密度2×106ml-1接种于75 cm2培养瓶中,依次加入 rmIL-4 、mGM-CSF(工作液浓度为10 ng/ml),37℃、 5%CO2培养48 h,每隔一天半量换新鲜培养基,培养5 d,流式细胞仪检测树突状细胞纯度。
1.2.2DCs成熟过程中MHCⅡ、CD80、CD86分子标志检测 获取小鼠骨髓DCs后,以6×105ml-1细胞浓度分别接种于无菌的A、B培养板中;A培养板加入终浓度1 μg/ml LPS,37℃、5%CO2培养48 h;B培养板加入终浓度1 μg/ml LPS与雷公藤新碱(工作浓度为40 ng/ml)混合液,37℃、5%CO2培养48 h;常规消化细胞后,向流式管中加入50 μl细胞悬液与1 μl抗小鼠MHCⅡ、CD80、CD86标志的荧光抗体,另取一支流式管加入50 μl细胞悬液作为空白对照;轻柔混匀后室温避光静置45 min,PBS洗涤2次;流式细胞术检测DCs表面相关分子表达量变化。
1.2.3DCs抗原吞噬能力检测 取上述A、B两板中约一半细胞加入浓度为1 mg/ml的FITC-dextran,继续培养1 h后收集细胞,调整细胞浓度至1×105ml-1,800 r/min离心5 min,弃上清后PBS洗2遍,流式细胞仪检测DCs吞噬能力变化,同时以未处理细胞作为阴性对照。
1.2.4抗体芯片检测 收集A、B两板DCs细胞培养上清液;取出抗体膜置于反应盒中,向反应盒中缓慢加入2 ml 1×封闭液,室温孵育30 min;弃去封闭液,轻轻加入1 ml 样品液,室温孵育1~2 h;去除样品液,依次用2 ml 1×洗液Ⅰ、2 ml 1×洗液Ⅱ,各洗膜3次×5 min;用2 ml 1×封闭液溶解抗体管中的生物素,配成一抗反应液备用;向反应盒中加入1 ml上述一抗反应液,室温孵育1~2 h;洗掉多余抗体;用1×封闭液稀释辣根过氧化物酶(HRP)标记的抗链酶生物素抗体,向反应盒中加入上述稀释液2 ml,室温孵育2 h;洗膜;各取ECL试剂盒中A、B液250 μl,混合均匀备用;将反应盒中的膜取出,置于保鲜膜上,加入染色液并采集数据。
1.3统计学方法 本实验使用Graphpad Prism7.0软件进行统计学分析(GraphPad Software,San Diego,CA,USA)。数据采用t检验,当P<0.05表示差异有统计学意义。
2 结果
2.1雷公藤新碱影响LPS诱导DCs成熟过程 加入雷公藤新碱组中DCs表面的协同刺激分子MHCⅡ、CD80、CD86的表达量与对照组相比明显降低。结果如图1所示,MHCⅡ分子实验组55.3%,对照组66.7%;CD80实验组36.4%,对照组62.4%;CD86实验组36.5%,对照组60.2%,每组分别进行3次独立实验。以上结果表明雷公藤新碱可降低LPS诱导DCs成熟过程。
2.2雷公藤新碱增强 DCs抗原吞噬能力 实验结果如图2所示,与对照组相比,雷公藤新碱组吞噬FITC-Dextran的DCs比值增多,结果有统计学意义(P<0.01)。
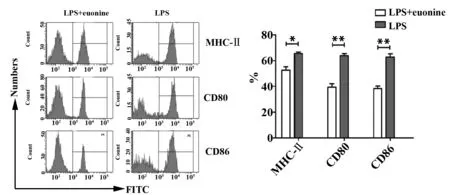
图1 雷公藤新碱降低LPS诱导DCs表面MHCⅡ、CD80、CD86表达量
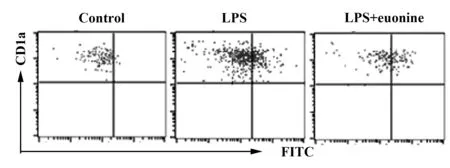
图2 雷公藤新碱增强DCs吞噬能力
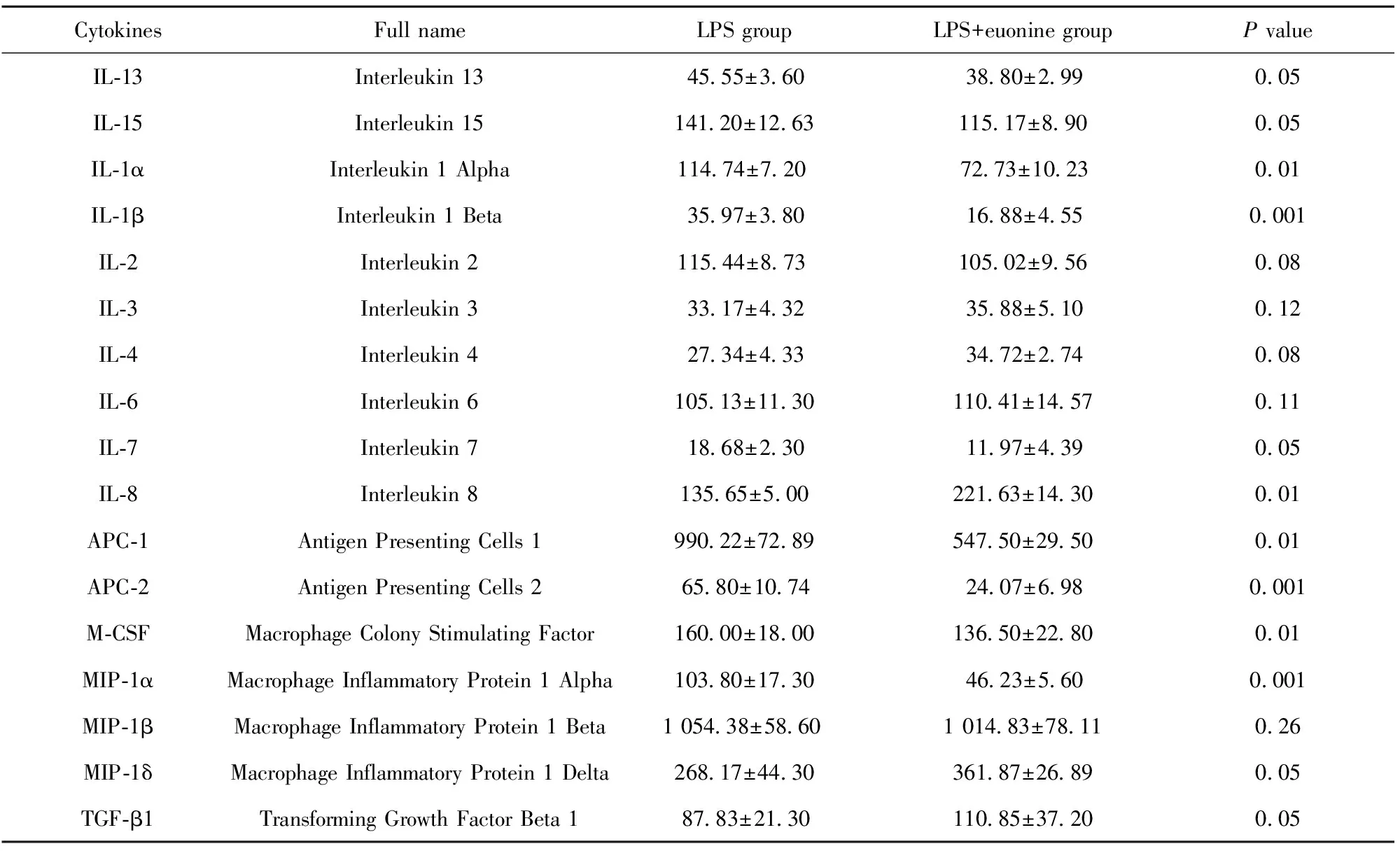
表1雷公藤新碱作用后细胞因子分泌变化
Tab.1Changesofcytokinesecretionaftereuonineadministration
CytokinesFull nameLPS groupLPS+euonine groupP valueIL-13Interleukin 1345.55±3.6038.80±2.990.05IL-15Interleukin 15141.20±12.63115.17±8.900.05IL-1αInterleukin 1 Alpha114.74±7.2072.73±10.230.01IL-1βInterleukin 1 Beta 35.97±3.8016.88±4.550.001IL-2Interleukin 2 115.44±8.73105.02±9.560.08IL-3Interleukin 333.17±4.3235.88±5.100.12IL-4Interleukin 4 27.34±4.3334.72±2.740.08IL-6Interleukin 6 105.13±11.30110.41±14.570.11IL-7Interleukin 7 18.68±2.3011.97±4.390.05IL-8Interleukin 8 135.65±5.00221.63±14.300.01APC-1Antigen Presenting Cells 1990.22±72.89547.50±29.500.01APC-2Antigen Presenting Cells 265.80±10.7424.07±6.980.001M-CSFMacrophage Colony Stimulating Factor160.00±18.00136.50±22.800.01MIP-1αMacrophage Inflammatory Protein 1 Alpha103.80±17.3046.23±5.600.001MIP-1βMacrophage Inflammatory Protein 1 Beta1 054.38±58.601 014.83±78.110.26MIP-1δMacrophage Inflammatory Protein 1 Delta268.17±44.30361.87±26.890.05TGF-β1Transforming Growth Factor Beta 187.83±21.30110.85±37.200.05
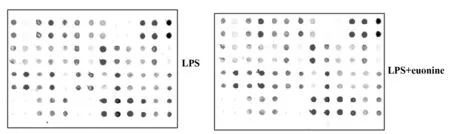
图3 小鼠抗体芯片检测结果
2.3雷公藤新碱降低LPS诱导DCs上清中细胞因子分泌水平 检测结果如表1和图3所示,与对照组相比,雷公藤新碱实验组可降低大部分细胞因子分泌水平,特别是APC-2、MIP-1α及IL-1β的表达水平较对照组明显降低。实验重复3次,结果显示差异有统计学意义。
3 讨论
DCs主要有DC1、DC2两种亚型,其中DC1主要由细菌LPS、病毒等诱导产生,DC2则主要由IL-1、肿瘤坏死因子(TNF-α)诱导产生[9]。DCs的起源、表型以及亚型的异质性与多样性决定了它复杂的生物学特性,体内多以不成熟DCs存在,不成熟的DCs具有较强的胞饮、吞噬及受体介导摄取抗原的能力,但几乎没有抗原递呈的能力,且不能激活T淋巴细胞和免疫应答,其表面低表达共刺激分子、限制性标志分子与MHC分子等。当不成熟DCs由中枢淋巴器官、初级淋巴器官向外周、次级淋巴结迁移时,伴随着DCs形状、细胞表面分子数目及细胞因子受体形态的改变,逐渐演变为成熟的DCs。成熟的DCs高表达上述分子,同时上调趋化受体,大量分泌IL-1α、IL-1β、IL-8、IL-12等细胞因子[10]。成熟的DCs具有极强的抗原呈递能力、可刺激淋巴T细胞活化增殖,启动免疫应答,参与T细胞介导的特异性免疫应答[11]。DCs是唯一能激活初始T细胞(naive T cell,Tn)的抗原呈递细胞,Tn活化以后分化成Th1、Th2、Th7以及调节性T细胞,Th1/Th2动态平衡是维持正常免疫状态的关键,Th1/Th2比例失衡将会诱导炎症性疾病的发生,因此DCs可通过该途径参与多种疾病的发生发展进程[12]。
本研究发现小鼠骨髓DCs在加入雷公藤新碱后与单独LPS诱导组相比,其表面分子MHCⅡ、CD80、CD86均明显降低。LPS作为抗原成份刺激DCs成熟,使其共刺激分子、表面分子表达上调,从而有效激活T细胞诱导免疫应答[13]。以上结果表明雷公藤新碱能够抑制DCs成熟,随后我们又对DCs进行了抗原吞噬能力检测,同样发现雷公藤新碱干预后,DCs吞噬能力比未干预组显著增强,该结果进一步表明雷公藤新碱可抑制LPS诱导DCs成熟作用,提示雷公藤可能通过抑制DCs成熟进而抑制T细胞参与机体免疫应答过程。
同时,本实验利用抗体芯片技术发现雷公藤新碱干预组与对照组相比,IL-4、IL-8、MIP-1δ等细胞因子表现为细微上调现象,其他因子相对于对照组表达水平均有所下降。DCs细胞成熟一般需要共刺激分子的表达及细胞因子表达的上调[14],LPS则主要通过与TLR4受体结合促进细胞分泌细胞因子。本研究中雷公藤新碱调控大部分TLR4通路细胞因子表达下调,表明雷公藤新碱可能通过TLR4信号通路调控DCs成熟过程,但详细机制需进一步进行研究。与对照组相比APC-2、MIP-1α及IL-1β减少量尤为明显,APC-2、MIP-1α及IL-1β等细胞因子主要激活CD4+Th1细胞亚群,导致炎症的产生;而IL-4、IL-8、MIP-1δ等细胞因子主要激活CD4+Th2细胞亚群从而抑制炎症。因此,我们的结果进一步表明雷公藤新碱影响DCs的成熟过程,也提示雷公藤新碱具有有效地抗炎作用。
DCs具有极强的抗原提呈能力,在免疫应答及免疫耐受中具有重要的作用。相信随着研究的不断深入,DCs终将成为治疗皮肤病等各种炎症性疾病、自身免疫病等疾病的重要作用靶点。雷公藤是临床应用中非常重要的免疫抑制药物,对免疫调节具有明显的抑制作用及抗炎作用,已在临床应用取得了可喜的成果。但雷公藤成分复杂,免疫调控机制尚不明确以及毒副作用较强,在如何取得单一有效的成分、降低毒副作用的发生等领域仍存在许多值得深入探讨的问题。本研究发现雷公藤新碱作为雷公藤的重要组成分之一,可以有效抑制DCs的成熟过程,提示可能在DCs及T细胞参与的免疫性疾病中发挥关键作用,因此,本研究具有十分重要的理论与实践意义。
