以非编码RNA为靶点的中药活性成分研究现状*
2019-03-06姚魁武刘咏梅
董 艳,姚魁武,刘咏梅,张 云,陈 光,2,王 阶**
(1.中国中医科学院广安门医院 北京 100053;2.北京中医药大学广安门医院 北京 100029)
非编码RNA(ncRNA)是不编码蛋白质的RNA,参与调控多种疾病的发生与发展[1-3]。作为占真核细胞总RNAs 95%以上[4]的功能RNA,其在药物靶点领域也受到越来越多研究者的重视。而一直以来中药的肯定疗效和模糊作用机理促成了其在矛盾中寻求自我发展。尽管中药提取物被认为具有更高纯度和相对明确的活性成分,但将其代替传统中药的有效性和安全性仍然受到质疑。ncRNA的出现从表观遗传学角度为中药活性成分研究提供了新方向,有助于从上游基因调控层面明确作用靶点,揭示其多靶点多层次治疗疾病的本质,促进“中药成分—靶点—分子机制—疾病”的精准医疗模式的实现。目前,有关中药活性成分干预ncRNAs 的研究已如雨后春笋,故本文对相关内容进行综述,以梳理发展现状并阐述尚存在的问题。
1 以多种ncRNAs为靶点的抗肿瘤中药活性成分
越来越多的研究发现某些中药活性成分可通过调节miRNA 的表达而发挥抗肿瘤作用。而lncRNA 和circRNA 作为内源性竞争性非编码RNA(ceRNA),能通过miRNA 识别元件,竞争性结合miRNA,从而诱导基因沉默[5]。因此,这些ceRNAs 同样具有成为中药靶点的潜能,进而发挥抗肿瘤作用(表1)。
1.1 小檗碱下调miRNAs,诱导肿瘤细胞凋亡和周期停滞
小檗碱(分子式C20H19NO5)是一种季铵生物碱,为黄连、黄柏及三颗针等中药的活性提取物,具有抗炎、抗肿瘤、降血糖、降血脂及抗心律失常等作用[6]。越来越多的研究发现其抗肿瘤机制与多种miRNAs 相关。通过下调3 个miRNA 簇(miR-99a-125b、miR-17-92和miR-106-25),以 及RAC1、NFκB1、MYC、JUN 和CCND1 等多个靶基因,小檗碱调控p53、Erb 和MAPK信号通路,抑制多发性骨髓瘤[7]。另一项研究[8]则显示,它至少部分通过调节IL6/STAT3,下调miR-21,增加程序性细胞死亡蛋白4(PDCD4)表达,阻滞p53信号通路,从而抑制多发性骨髓瘤细胞生长,且该作用可被PDCD4 沉默所逆转。进一步实验证实[7,8],小檗碱具有类似mir-99a-125b 簇和miR-21 抑制剂的作用,通过诱导细胞凋亡、G2期细胞周期停滞和集落抑制从而发挥抗肿瘤作用。因此,小檗碱调节多种基因表达,其主要的调控通路为p53 信号通路,参与的细胞功能为抑制肿瘤细胞周期和诱导凋亡,而这种治疗作用的潜在上游靶点为mir-99a-125b簇和miR-21。
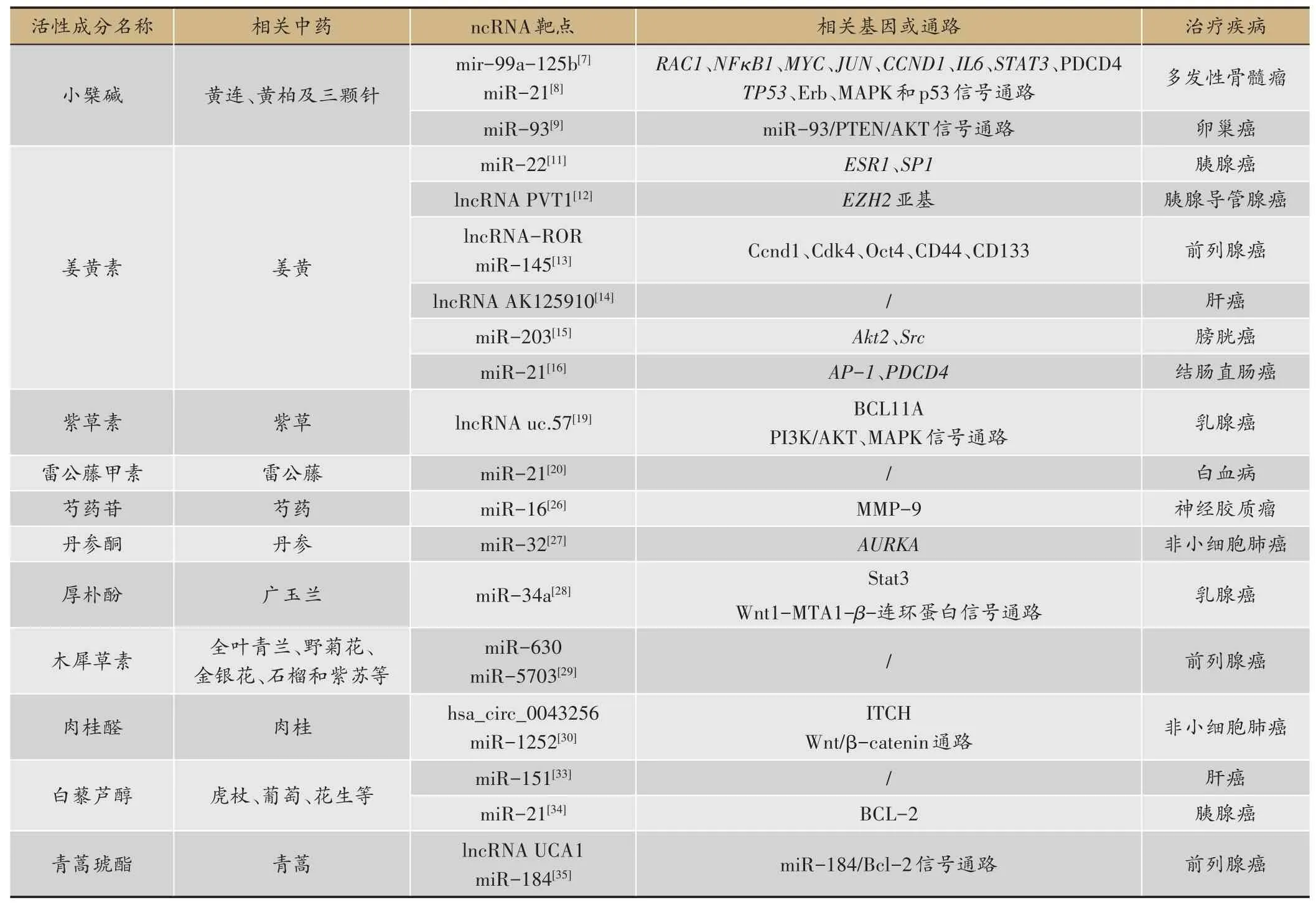
表1 以多种ncRNAs为靶点的抗肿瘤中药活性成分
此外,小檗碱还能与抗肿瘤药物联合作用,减弱西药耐药性,增强临床疗效。顺铂耐药细胞系中miR-93 水平高于顺铂敏感细胞系,小檗碱可以抑制miR-93 在卵巢癌中的表达和功能,增加肿瘤抑制因子PTEN表达,调节miR-93/PTEN/AKT 信号通路,从而增强顺铂的促细胞凋亡作用,并诱导G0/G1 细胞周期停滞,增强顺铂对卵巢癌细胞的敏感性[9]。
1.2 姜黄素靶向调节lncRNA-miRNA,诱导肿瘤细胞凋亡,抑制肿瘤侵袭
姜黄素(分子式C21H20O6)是从姜黄中提取的酚类化合物,具有抗肿瘤、抗炎、抗氧化及抗纤维化等作用[10]。其抗肿瘤作用与调节多种lncRNAs 和miRNAs相关。姜黄素上调胰腺癌相关miR-22,下调靶基因雌激素受体1(ESR1)和转录因子SP1,抑制胰腺癌细胞生长和侵袭[11];并能抑制EZH2 亚基及其相关lncRNA PVT1 的表达,增强化疗耐药胰腺导管腺癌细胞的敏感性[12]。它还能抑制lncRNA-ROR,上调miR-145 表达,降低细胞周期蛋白Ccnd1和Cdk4,以及Oct4、CD44和CD133 等干细胞标记物,进而抑制人前列腺癌干细胞的体外增殖、侵袭和细胞周期停滞[13]。通过上调lncRNA AK125910 表达,姜黄素还能诱导肝癌细胞凋亡[14]。它抑制miR-203 启动子甲基化,上调miR-203表达,下调Akt2 和Src,进而抑制膀胱癌细胞增殖,并诱导凋亡[15]。通过抑制激活蛋白1(AP-1)与启动子的结合,它以剂量依赖性方式降低miR-21 启动子活性和表达,并诱导肿瘤抑制因子PDCD4 表达,从而抑制结肠直肠癌细胞生长,侵袭和体内转移[16]。
由此可见,姜黄素能从miRNAs 和lncRNAs 两个层面发挥不同的抗肿瘤作用,它们之间构成了潜在的ceRNA 交互网络。通过干预lncRNA-ROR/miR-145/细胞周期蛋白/干细胞标记物调控网络,姜黄素表现出抗前列腺癌作用。而在胰腺癌中,lncRNA PVT1 和miR-22/ESR1 被发现参与姜黄素的抗肿瘤作用,它们之间亦或存在直接或间接的调控关系,值得进一步深入研究。
1.3 紫草素、雷公藤甲素分别调节lncRNA和miRNA,恢复靶向药物敏感性
紫草素(分子式C16H16O5)是一种天然茶醌类衍生化合物,存在于中药紫草根中,具有抗炎、抗病原微生物、抗肿瘤,以及抑制脂肪和雌激素形成等作用[17]。雷公藤甲素(分子式C20H24O6)则是从雷公藤中提取的环氧二萜内酯化合物,具有抗肿瘤、抗炎和免疫调节等作用[18]。随着肿瘤化疗药的普遍使用,耐药现象越来越广泛,显著降低了其临床疗效;而中药活性成分能增强药物敏感性,降低耐药性而发挥独特的协同作用。研究[19]显示抗他莫昔芬的MCF-7R 乳腺癌细胞中存在lncRNA uc.57 低表达和BCL11A 高表达。紫草素能通过上调lncRNA uc.57,下调BCL11A,抑制PI3K/AKT 和MAPK 信号通路,从而增强他莫昔芬的敏感性。而雷公藤甲素联合阿霉素则能促进K562/A02 细胞的凋亡指数,其潜在机制可能为雷公藤甲素抑制miR-21表达,增强白血病细胞对阿霉素的敏感性[20]。
1.4 芍药苷、丹参酮、厚朴酚、木犀草素、肉桂醛上调保护性miRNA 和circRNA,抑制肿瘤细胞增殖并诱导凋亡
芍药苷(分子式C23H28O11)是芍药根的主要活性成分,具有舒张平滑肌、抗氧化、抗肿瘤及免疫调节等作用[21]。丹参酮(分子式C18H12O3)为丹参的脂溶性菲醌类提取物,包括丹参酮I、丹参酮IIA、丹参酮IIB 等多种活性成分,具有抗氧化、抗炎、抗血小板聚集、抗肿瘤及性激素样等作用[22]。厚朴酚(分子式C18H18O2)源于广玉兰的生物活性多酚,具有抗氧化、抗炎、抗肿瘤及抗动脉粥样硬化等作用[23]。木犀草素(分子式C15H10O6)是全叶青兰、野菊花、金银花、石榴和紫苏等植物的黄酮类成分,具有抗炎、抗氧化、抗肿瘤及神经保护等作用[24]。肉桂醛(分子式C9H8O)是肉桂的醛类提取物,具有抗肿瘤、抗炎、抗氧化和保护缺血再灌注损伤等作用[25]。研究显示miR-16、miR-32、miR-34a及miR-630 等在多种肿瘤细胞中低表达,具有抑制肿瘤的作用。中药活性成分通过上调这些保护性基因,进而发挥抗肿瘤功效。
MiR-16 在神经胶质瘤组织中下调,而芍药苷通过上调miR-16,下调MMP-9,发挥抑制肿瘤细胞增殖并诱导凋亡的作用[26]。丹参酮则通过上调miR-32,下调AURKA,抑制细胞增殖,促进细胞凋亡,从而抗非小细胞肺癌[27];且进一步实验证实,沉默AURKA 基因能获得与上述观察一致的结果。厚朴酚抑制Stat3 磷酸化,阻止其向miR-34a启动子募集,诱导miR-34a活化,阻滞瘦素诱导Wnt1-MTA1-β-连环蛋白信号通路,进而抑制肥胖状态下乳腺癌细胞生长、侵袭、迁移,以及瘦素诱导的乳腺-肿瘤-异种移植物生长[28]。在前列腺癌细胞中,木犀草素能上调miR-630和miR-5703,抑制肿瘤细胞生长[29]。此外,肉桂醛靶向上调非小细胞肺癌细胞中hsa_circ_0043256 表达,抑制Wnt/β-catenin 通路,减弱细胞增殖并诱导细胞凋亡[30]。而hsa_circ_0043256 诱导的Itchy E3 泛素蛋白连接酶(ITCH)表达能被miR-1252 部分消除,表明其与miR-1252 存在相互调节关系。由此可以推测,肉桂醛介导的抗肿瘤作用与hsa_circ_0043256/miR-1252 交互网络相关。
1.5 白藜芦醇、青蒿琥酯下调促肿瘤miRNA 和lncRNA,抑制细胞增殖和迁移,诱导凋亡
白藜芦醇(分子式C14H12O3)是一种多酚类化合物,为虎杖、葡萄、花生等植物的活性提取物,具有抗炎、抗氧化和抗肿瘤等作用[31]。青蒿琥酯(分子式C19H28O8)是青蒿叶的倍半萜内酯提取物,具有抗疟、抗肿瘤及免疫调节等作用[32]。研究表明,miR-151、miR-21和lncRNA UCA1在多种肿瘤细胞中上调,具有促肿瘤作用;而中药活性成分通过下调这些ncRNAs 而发挥抗肿瘤功效。其中白藜芦醇下调miR-151 表达,抑制肝癌HepG2 细胞株增殖,并诱导细胞凋亡[33]。而在胰腺癌中,它通过下调miR-21,调控BCL-2 表达而诱导细胞凋亡[34]。青蒿琥酯则下调lncRNA UCA1 水平,参与下游miR-184/Bcl-2 信号通路,抑制细胞增殖和侵袭,诱导凋亡,从而改善前列腺癌患者的不良预后;且这种作用能被lncRNA UCA1 高表达所逆转[35]。由此可见,青蒿琥酯能从lncRNA-miRNA-mRNA 的网络层面发挥抗肿瘤机制。
2 以miRNAs、lncRNAs为靶点的抗炎性中药活性成分
炎症参与多种疾病的病理过程,与冠心病、哮喘及炎症性肠病等的发生发展密切相关。但目前无论是非甾体类抗炎药还是免疫抑制剂都存在较大的副作用,因此作为疾病基础病理改变的炎症反应尚缺乏有效的药物治疗。而中药在这方面表现出显著的治疗优势,其活性成分可通过调节miRNA 或lncRNA,抑制多种炎症因子,进而在炎症相关性疾病中发挥重要的基础治疗作用(表2)。
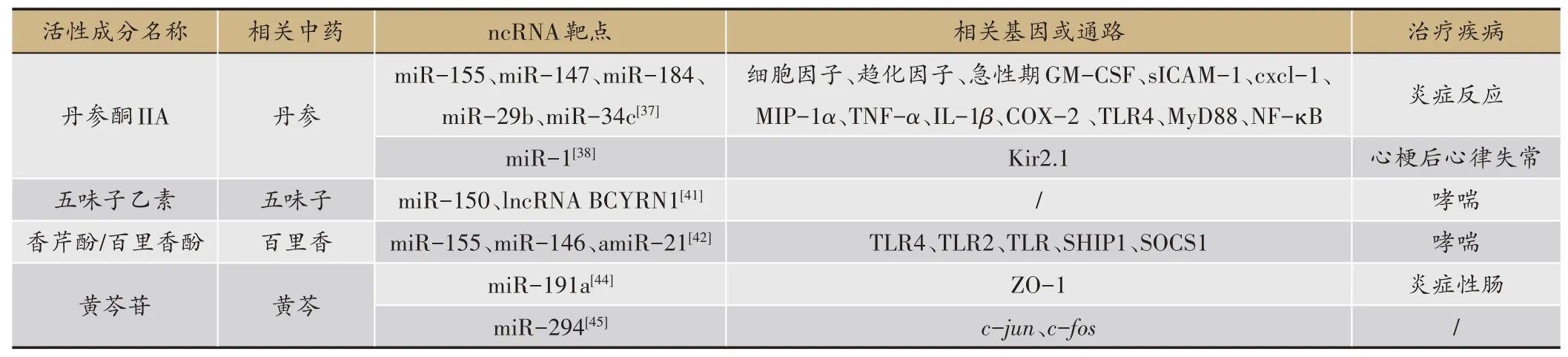
表2 以miRNAs、lncRNAs为靶点的抗炎性中药活性成分
2.1 丹参酮ⅡA双向调节miRNAs,抗炎抗心律失常
丹参酮ⅡA(分子式C19H18O3)为丹参酮的主要组成部分,也是其发挥药效的成分之一,具有抗氧化和抗动脉粥样硬化等作用[36]。研究[37]发现丹参酮ⅡA 还具有抗炎功效,且这种作用与多种miRNAs 密切相关。通过下调miR-155、miR-147、miR-184、miR-29b 和miR-34c表达,它能降低细胞因子,趋化因子和急性期GM-CSF、sICAM-1、cxcl-1、MIP-1α 水平,抑制LPS 诱导的NF-κB 活化,降低肿瘤坏死因子α(TNF-α)、IL-1β、COX-2、TLR4 和MyD88 等[37]。另有报道则显示,丹参酮ⅡA 增加心梗后miR-1 表达,抑制其基因转录激活因子SRF,恢复大鼠心室肌细胞中低IK1 电流和Kir2.1 蛋白,进而降低急性心肌缺血诱发的心律失常及心梗3 个月后大鼠的死亡率[38]。由此可见,丹参酮ⅡA 作为传统活血化瘀中药的主要活性成分,其抗炎和抗心律失常的心脏保护作用与双向调节miRNAs 密切相关。但遗憾的是,它的miRNAs 靶点并不能直接作为其发挥活血化瘀功效的客观依据,因此进一步针对性的开展活血化瘀相关的靶基因研究,对于揭示中药传统功效的作用机理有重要的现实意义。
2.2 五味子乙素、香芹酚调节miRNA、lncRNA,抗细胞增殖及炎症因子,抑制哮喘的炎症反应
五味子乙素(分子式C23H28O6)为五味子的木脂素提取物,具有保肝、抗衰老及心脏、神经保护作用[39]。香芹酚(分子式C10H14O)及其异构体百里香酚是百里香的主要单萜酚成分,具有调节细胞内钙离子平衡、舒张血管、保肝、抑菌、抗真菌及抗氧化等作用[40]。通过上调miR-150,下调lncRNA BCYRN1 表达,五味子乙素能抑制哮喘大鼠气道平滑肌细胞增殖和迁移[41]。香芹酚及百里香酚则通过下调miR-155、miR-146a 及miR-21,降低炎症因子TLR4 和TLR2 的蛋白水平,增加TLR 的负调节剂SHIP1 和SOCS1 水平,进而抑制哮喘炎症反应[42]。以上研究表明,哮喘的炎症反应受miRNA 和lncRNA 的调节,而中药活性成分靶向调控这些ncRNAs 进而发挥治疗作用。值得注意的是,在五味子介导的miR-150/lncRNA BCYRN1 调控网络中,miR-150 为lncRNA BCYRN1 的上游调控基因,这种交互作用与常规的ceRNA 网络并不相同,表明了miRNA和lncRNA之间存在着复杂的双向调节关系。
2.3 黄芩苷下调miR-191a,改善细胞活力,治疗炎症性肠病
黄芩苷(分子式C21H18O11)是从黄芩中提取的黄酮苷类活性成分,具有抗菌、抗病毒及保肝等作用[43]。它可逆转TNF-α诱导的小肠内皮细胞ZO-1 减少和miR-191a增加,显著改善细胞活力和迁移。进一步实验表明,抑制miR-191a 能增强黄芩苷对ZO-1 蛋白表达的恢复作用,保护TNF-α诱导的细胞损伤,进而为炎症性肠病治疗提供新思路[44]。由此可见,黄芩苷与miR-191a低表达之间存在协同增效的作用,一方面黄芩苷能下调miR-191a 表达,另一方面miR-191a 低表达又能促进黄芩苷的细胞保护作用。此外,黄芩苷还可以抑制小鼠胚胎干细胞增殖,增加G1 期细胞,减少S 期或G2/M 期细胞。这种作用可能通过下调miR-294,降低c-jun 和c-fos表达实现,且该作用能被miR-294过表达所逆转[45]。
3 靶向调节lncRNA 或miRNA 的抗动脉粥样硬化性中药活性成分
冠状动脉粥样硬化是冠心病和脑梗塞的重要病理改变,因此抗动脉粥样硬化也成为了缺血性心脑血管疾病的基础治疗。目前循证依据较多的具有稳定粥样斑块的药物是他汀类,但该药需长期服用,且具有损害肝功能和肌溶解的风险,尤其对于老年患者,其副作用更加明显。有鉴于此,寻找具有抗动脉粥样硬化的药物对于防治心脑血管疾病具有重要意义。而目前已有研究显示,某些中药活性成分可以通过调控lncRNA 和miRNA 的异常表达,发挥抗动脉粥样硬化的作用(表3)。

表3 靶向调节lncRNA或miRNA的抗动脉粥样硬化性中药活性成分

表4 以miRNAs为靶点的抗感染中药活性成分
3.1 芥子酸下调lncRNA-MALAT1,抑制细胞焦亡,抗糖尿病性动脉粥样硬化
芥子酸(分子式C11H12O5)是白芥子、黄芥子的主要活性成分之一,具有保护高糖诱导的血管平滑肌损伤及同型半胱氨酸诱导的血管内皮损伤等作用[46,47]。研究[48]显示,lncRNA-MALAT1 在糖尿病性动脉粥样硬化大鼠的巨噬细胞中显著上调;而低剂量芥子酸能降低lncRNA-MALAT1 水平,抑制血清内皮素1(ET-1)和白细胞介素-1β(IL-1β)含量,抑制骨髓来源巨噬细胞的细胞焦亡以及ASC、NRLP3 和Caspase-1 等焦亡相关蛋白的表达,从而抗糖尿病性动脉粥样硬化。
3.2 虎杖苷靶向调节miR-214,抗动脉粥样硬化合并肝功能不全
虎杖苷(分子式C20H22O8)是虎杖根茎的提取物,亦称为白藜芦醇苷,具有抗氧化、保护心肌缺血再灌注损伤、改善血管内皮功能及降脂等作用[49]。一项动物研究[50]显示,虎杖苷能显著改善血糖,血清ALT、AST、TC、TG、LDL-C 和HDL-C 水平,以及肝组织中MDA 和SOD 含量,发挥抗动脉粥样硬化和保护肝功能的作用。此外,它还能调控肝组织中miR-214 表达,而该ncRNA 或为虎杖苷调节血糖、血脂和肝功能的上游靶点,但它们之间的调节关系仍需进一步更深入的研究。
4 以miRNAs为靶点的抗感染中药活性成分
抗菌素和抗病毒药物是治疗感染性疾病的基础用药,然而随着抗菌素滥用、耐药菌及病毒变异等问题的逐渐凸显,人们开始关注感染性疾病的其他治疗药物,而中医药在这发面表现出显著的优势。研究表明,某些中药活性成分能调控miRNA 的异常表达,进而改善机体感染过程中的病理改变(表4)。
4.1 淫羊藿苷下调miR-34c,促成骨分化和矿物结节形成,治疗细菌性骨丢失病
淫羊藿苷(分子式C33H40O15)是从淫羊藿中分离出的主要活性类黄酮葡萄糖苷,具有抗骨质疏松、促进造血及调节神经内分泌系统等作用[51]。研究[52]显示,淫羊藿苷可通过下调miR-34c表达,抑制JNKs、p38和NF-kB通路,恢复LPS诱导的骨丢失,从而治疗细菌性骨丢失病。此外,它的这种促成骨分化和矿物结节形成的作用能被miR-34c 过表达所逆转,进一步证实了miR-34c作为淫羊藿苷靶点的潜能。该研究从转录后调控层面揭示了淫羊藿苷治疗细菌性骨丢失病的作用靶点,也在一定程度上为传统中药淫羊藿治疗骨关节疾病提供了客观依据。
4.2 人参皂苷上调miR-15b,对抗H9N2 流感病毒诱导的细胞凋亡,促进细胞活力
人参皂苷是从人参中提取的固醇类化合物,含有人参皂甙Re、Rg、Rh、Rb 及Rc 等多种活性成分,具有抗病毒、增强免疫力、抗炎、抗氧化、抗衰老及抑制血管内皮细胞凋亡等作用[53]。研究[54]显示,其代谢物原人参三醇通过上调miR-15b 表达,抑制H9N2/G1 感染后IP-10 的生成,促进细胞活力;而人参皂甙Re 则可抑制H9N2/G1 诱导的细胞凋亡和DNA 损伤。由此可见,miR-15b 或可成为人参皂苷抗病毒的重要靶点。该研究结果丰富了人参的传统治疗功效,扩大了其临床运用范围,为研究中药治疗急性感染性疾病提供新的靶点和思路。
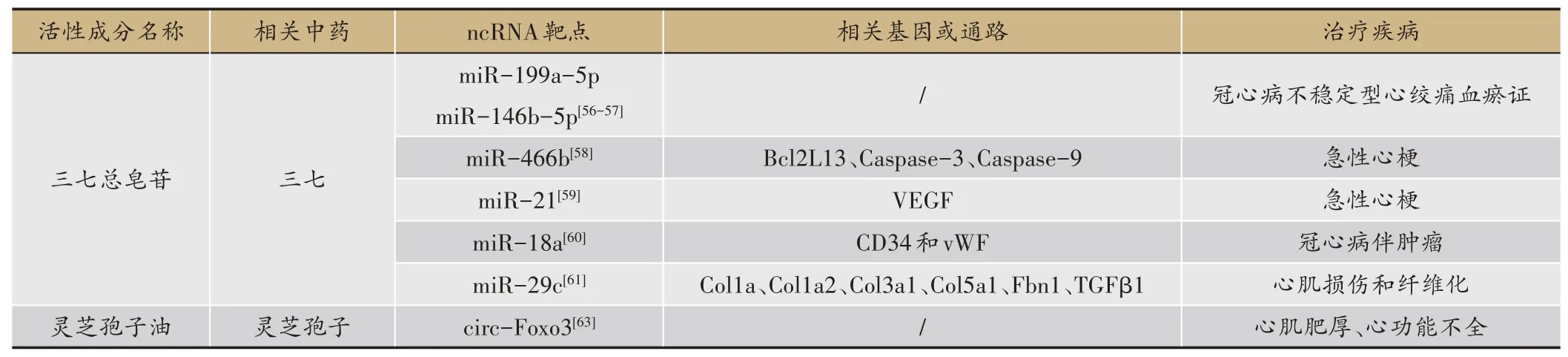
表5 靶向调节miRNA或circRNA的抗结构重构性中药活性成分
5 靶向调节miRNA 或circRNA 的抗结构重构性中药活性成分
结构重构是许多疾病发展至后期的难逆性病理改变,与组织器官的功能失调密切相关,目前针对结构重构尚缺乏有效的治疗方法。中药活性成分被证实能靶向调节某些circRNA 或miRNA(表5),从而逆转结构重构,恢复机体正常功能,改善疾病预后。
5.1 三七总皂苷多靶点双向调节miRNAs,抑制细胞凋亡,促进血管生成,抗心肌纤维化
三七总皂苷(分子式C47H80O17)是三七根的主要活性成分,具有抗炎、抗动脉粥样硬化、抑制心肌肥厚及保护缺血再灌注损伤等作用[55]。研究[56]显示三七总皂苷能改善冠心病不稳定型心绞痛血瘀证患者症状,其机制可能与下调miR-199a-5p 和miR-146b-5p 相关。进一步研究证实,三七总皂苷可通过下调miR-146b-5p表达,抑制细胞凋亡,对抗H2O2诱导的细胞氧化损伤[57]。且通过上调miR-466b,下调Bcl2L13、Caspase-3和Caspase-9 蛋白,它还能抗急性心梗大鼠心肌细胞凋亡[58]。同时,它促进心梗后VEGF 和miR-21 表达,促进血管新生,从而缩小梗死面积[59]。有趣的是,另一项研究发现,三七总皂苷中的Rg1、Rb1 和R1 成分对血管生成表现出组织特异性调节,能减轻心肌缺血,同时抑制肿瘤生长。其潜在的机制可能是上调心脏中miR-18a、CD34 和vWF 表达,但下调肿瘤中这些基因及蛋白表达[60]。此外,它能上调心脏中抗纤维化miR-29c的表达,下调Col1a、Col1a2、Col3a1和Col5a1,以及Fbn1 和TGFβ1,从而减弱ISO 诱导的心肌损伤和纤维化[61],改善结构重构。由此可见,三七总皂苷以多个miRNAs 为作用靶点,调控凋亡、血管生成及胶原蛋白相关分子,抑制细胞凋亡,促进血管新生,抗心肌缺血和心肌纤维化。其中三七总皂苷靶向下调冠心病血瘀证的miR-146b-5p 表达,或能为三七的活血化瘀功效提供生物学基础。
5.2 灵芝孢子油降低circRNA-Foxo3 表达,抗动脉粥样硬化,抑制心室重构
灵芝孢子油是从破壁的灵芝孢子中提取的油状脂质物,含有多种脂肪酸及不饱和脂肪酸等成分,具有抗肿瘤、提高免疫力、抗氧化、抗衰老及神经保护等作用[62]。研究[63]显示,口服灵芝孢子油还能使心脏射血分数恢复正常,校正由横向主动脉缩窄所致的分数缩短,并抑制左心室肥大。其潜在机制可能为灵芝孢子油浓度和时间依赖性降低circ-Foxo3水平。该研究揭示了circ-Foxo3 的心脏保护作用,但遗憾的是并未报道circRNA 的靶基因;且以灵芝孢子油为研究对象,其活性成分并不明确。因此,该研究作为一个探索性的试验,值得更深入和系统的研究。
随着以miRNA、lncRNA 及circRNA 为代表 的ncRNAs 在中药活性成分研究领域的日渐增多,明确中药的作用靶点及调控机制,促进中医药的精准医疗将指日可待。尽管目前已有多种ncRNAs,尤其是miRNAs,被研究发现参与了中药活性成分的治疗过程,但是现有研究仍然存在以下几点问题:①研究数量逐渐增多,但并不深入,未能构建circRNA、lncRNA、miRNA 及mRNA 之间存在的复杂调控关系,因此不能系统的揭示中药活性成分的作用机制;②大多数研究揭示了中药的现代药理作用和潜在治疗靶点,但并未基于传统中医药理论,因此难以构建中药传统功效与客观作用靶点之间的关系;③细胞研究是探索中药活性成分作用ncRNA 靶点的主要方法,通过基因敲除或过表达,能发现它们与药物之间存在的调节关系。但是这种在单细胞中存在的关系能否在人体的复杂系统里实现,仍需要进行临床试验进行验证。因此,ncRNAs 的出现为中药活性成分作用靶点研究提供了一个可预见的方向,但实践中的研究之路仍任重而道远。
