麒麟丸对弱精子症大鼠生殖系统的保护作用及调控机制探讨Δ
2019-02-19刘胜京郭博达余国今高庆和张继伟
刘胜京 郭博达 郭 军 晏 斌 王 福 余国今 高庆和** 张继伟
1. 北京中医药大学(北京 100029);2. 中国中医科学院西苑医院男科(北京 100091)3.北京协和医学院研究生院(北京 100730);4.北京医院泌尿外科(北京 100730)
弱精子症指精液中前向运动精子比例低于32%或前向运动与非前向运动精子之和的比例低于40%的病症,主要特征表现为精子的前向运动能力低下。目前西医治疗效果不甚理想,中医药治疗弱精子症历史悠久,经验丰富,具有独到优势[1,2]。麒麟丸是由制何首乌、墨旱莲、淫羊藿、菟丝子等15 味中药组成的上市中成药,在治疗弱精子症方面的疗效已在临床中得到广泛证实[3-6]。 本实验采用奥硝唑所致弱精子症大鼠模型,拟通过L-肉碱相关通路探讨麒麟丸对生殖系统保护作用及其可能机制。
材 料
一、主要实验药物及试剂
麒麟丸(广东太安堂药业股份有限公司,批号:国药准字Z10930034),左卡尼汀口服溶液(东北制药集团沈阳第一制药厂,批号:国药准字H19990372),奥硝唑胶囊(西安万隆制药股份有限公司, 批号: 国药准字H20031257),左旋肉碱标准品(上海源叶生物科技有限公司提供, 批号:JJ0731RA14),TRIZOL(10296028,Invitrogen),无水乙醇(10009218,国药集团化学试剂有限公司),异丙醇(10009218,国药集团化学试剂有限公司),DEPC (MD911875,MDL),UltraPure Agarose(165 00100,ABI-invitrogen),SuperScript III RT 逆 转 录kit(11752050,ABI-invitrogen),Sybr qpcr mix (4472920,ABI-invitrogen)。
二、实验动物
SD 雄性大鼠,体质量(250±20)g,均由中国中医科学院西苑医院实验动物中心提供,合格证号:SCXK(京)2018-00090, 共计40 只。 大鼠饲养于SPF 级环境中,均自由采食、饮水,室温(25±2)℃,12h/12h 光暗周期。
三、主要仪器设备
Waters e2695 型高效液相色谱仪 (配备2998 型PDA 检测器),荧光定量PCR 仪(StepOne Software,Applied biosystems),电子天平(十万分之一,Mettler Toledo),台式冷冻离心机(MIKRO 22R,Hettich),台式高速冷冻离心机(Legend micro 21R,Thermo Fisher),光学显微 镜(DM3000,Leica),移液器(0.5~10 μL,2~20 μL,100~1000 μL,Eppendorf),涡旋混合仪(XW-80A,其林贝尔),分光光度计(Nanodrop lite,Thermo Fisher)。
方 法
一、造模并分组
适应性饲养1 周后, 将40 只雄性SD 大鼠随机分为4 组,每组10 只,称量后记录体质量并进行编号。 根据文献采用奥硝唑(ORN)所致的大鼠生殖功能损伤机制建立弱精子症小鼠模型[7]。 通过预实验选定ORN 灌胃剂量为400mg/(kg·d),连续灌胃28 d。 因ORN 水溶性差,故ORN 用0.5%的羧甲基纤维素钠(CMC2Na)配制,均为每日新鲜配制。麒麟丸给药剂量为1.62 g/(kg·d),相当于麒麟丸产品说明书中每人每日口服剂量(18 g/d)。(具体分组见表1)。
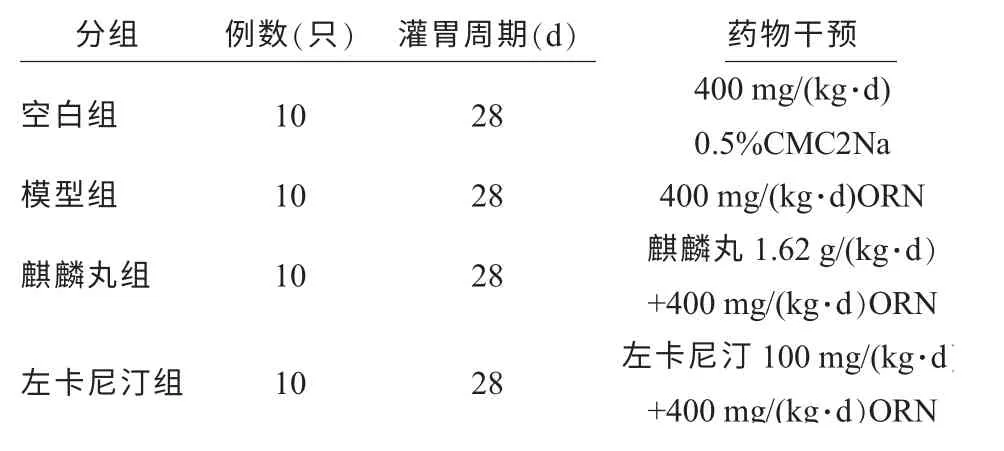
表1 实验分组
二、大鼠精液质量检测
大鼠灌胃连续4 周,于末次给药24h 后,用戊巴比妥钠麻醉大鼠,取出实验大鼠双侧附睾后称量,取左侧附睾尾,放入生理盐水清洗后(37℃预热),迅速放入M199 培养基(1 mL,37℃),剪开附睾尾使精子流出,放入培养箱(5%CO2,37℃),孵育3 min。孵育结束后吹打混匀,选取血细胞计数板进行人工计数。 血细胞计数板取5 μL 精子悬液加入到100 μL M199 培养基中,按照1∶20 的比例进行稀释,吸取10 μL 稀释后的精子悬液,滴于计数板盖玻片的边缘使精子悬液自动渗进计数池计数,并用计算机辅助精液分析系统(CASA)进行精子活力分级检测。
三、高效液相色谱法测定附睾L-肉碱含量
采用高效液相色谱法测定附睾中的L- 肉碱含量。色谱条件为:色谱柱为Waters SunFireTMC18(250 mm×4.6 mm,5μm);检测波长210 nm;柱前预处理,甲醇:0.3 g/L 十二烷基磺酸钠 (SDS) 的磷酸缓冲液(pH2.4)=5:95, 以1.0 mL/min 的流速冲柱子40 min;流动相,甲醇:磷酸 缓冲 液(pH2.4)=20∶80,流速1.0 mL/min,柱温30℃。 取适量左旋肉碱对照品,精密称定后,加入50%乙腈水溶液,制成每1 mL 含左旋肉碱1 mg 的溶液。
取上述对照品溶液,用50%乙腈水溶液逐级稀释,得 浓度 为1000、500、250、125、62.5、31.25 mg/L 6 个 不同浓度的对照品溶液,并按上述色谱条件测定峰面积。以对照品溶液浓度(mg/L)为横坐标,以峰面积为纵坐标绘制标准曲线, 得回归方程为Y=354 X + 726,r2=0.9997。表明左旋肉碱浓度在31.25~1000 mg/L 范围内与峰面积具有良好的线性关系。
四、RT-PCR 技术检测附睾OCTN2 mRNA 表达
迅速从液氮中取出大鼠右侧附睾头、体、尾组织各400mg,加入Trizol(1 mL/100 mg)冰浴研磨,形成组织匀浆。 在组织匀浆中加入氯仿, 振荡混匀, 静置5min后,4℃12000×g离心10min, 取 上 清加 异 丙 醇 提 取RNA,弃上清,经75%乙醇洗涤后,溶于DEPC 水,获得RNA 原液。 用紫外分光光度计检测吸光度 (A 值),A260/A280 值为1.82,纯度符合实验要求。 按照superscript III (invitrogen) 试剂盒步骤进行RNA 反转形成cDNA 第 一链。 用ABI 7900 qPCR 仪 按95℃、94℃、60℃、72℃,2min、20s、20s、30s 条件, 按表2 中引物序列,进行40cycle 扩增。

表2 引物序列
五、睾丸病理切片
取大鼠左侧睾丸,进行称量、脱水、透明、浸蜡、包埋、切片操作后进行HE 染色,在光镜下进行病理形态学观察睾丸结构。
六、统计学处理
采用SPSS 20.0 进行单因素方差分析, 采用LSD进行组间比较。数据采用±s表示,以P<0.05 为具有统计学意义。
结 果
一、精子浓度及总活力
由表3 可见,模型组与空白组相比,精子浓度差异无统计学意义(P>0.05),精子总活力明显下降(P<0.01)。麒麟丸组和左卡尼汀组与模型组相比, 精子浓度差异无统计学意义(P>0.05),精子总活力明显上升(P<0.05)。
表3 各组治疗前后精子浓度及总活力比较(n=10,±s)

表3 各组治疗前后精子浓度及总活力比较(n=10,±s)
注:与空白组比,*P<0.05,**P<0.01;与模型组比,#P<0.05,##P<0.01
组别 精子浓度(106/mL) 总活力(%)空白组 37.29±11.41 60.25±8.02模型组 34.72±10.73 45.01±6.7**麒麟丸组 47.82±15.18 60.28±5.27#左卡尼汀组 46.95±5.68 58.44±5.47#
二、附睾肉碱含量
高效液相色谱法测定左旋肉碱出峰时间2.96 min,各组代表性图谱见图1,定量结果见表4。 与空白组比较,模型组肉碱含量明显降低(P<0.01);与模型组比较,麒麟丸组和左卡尼汀组肉碱含量明显增高(P<0.01)。
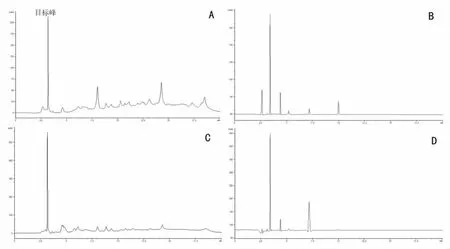
图1 各组附睾L-肉碱代表性图谱
表4 各组附睾L-肉碱含量比较(n=10,±s)

表4 各组附睾L-肉碱含量比较(n=10,±s)
注: 与空白组比,*P<0.05,**P<0.01; 与模型组比,#P<0.05,##P<0.01
组别 左旋肉碱含量(mg/L)空白组 4091.2±176.2模型组 2990.2±179.5**麒麟丸组 8681.3±118.9##左卡尼汀组 7659.4±142.6##
三、OTCN2 RNA 的表达
与空白组组比较, 模型组OTCN2 mRNA 表达量无显著差异(P>0.05);左卡尼汀组和麒麟丸组OTCN2 mRNA表达量高于模型组,差异有统计学意义(P<0.01),见图2。
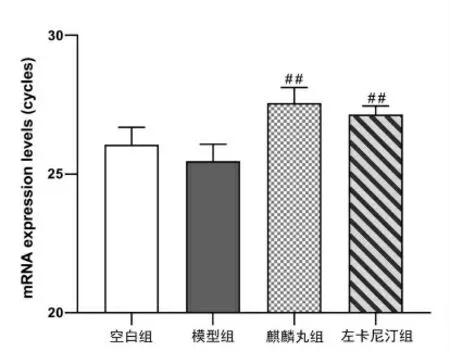
图2 干预后各组OTCN2 mRNA 表达情况比较
四、对睾丸组织病理的影响
用光学显微镜对HE 染色后的大鼠睾丸形态组织进行观察,可见空白组的大鼠睾丸组织结构正常,生精小管形态正常,其管腔明显,为正常类圆形,排列整齐紧密, 基底膜完整, 管腔内可见丰富的精子及精子细胞,层次清晰,各级细胞分裂活跃;间质细胞在小管间均匀分布。 模型组可见大量变性、萎缩等异常结构的不规则分布的生精小管, 可见狭小或部分完全闭合的管腔,管腔内精子及生精细胞数量少,排列不整齐,异常形态数量增多,各级生精细胞分裂不活跃;间质明显减少,上皮细胞变薄并伴有脱落。 麒麟丸组和左卡尼汀组大鼠睾丸组织, 与模型组相比, 生精小管结构基本完整,管腔内生精细胞和精子细胞数量显著增多,且分裂较为活跃,排列紧密;间质细胞分布较均匀,生精上皮细胞可见较为明显恢复(图3)。

图3 光镜下观察各组大鼠睾丸组织结构变化(×200)
讨 论
弱精子症是导致男性不育的重要原因之一, 其病因复杂,与内分泌因素、生殖道感染、染色体异常、隐睾、精索静脉曲张或全身性疾病等有关。 目前弱精子症的机制研究主要涉及蛋白表达异常、能量代谢异常、线粒体功能以及信号转导异常等[8,9]。
精子在睾丸中产生, 在附睾中精子成熟并获得运动和受精能力。 而附睾内的L-肉碱(L-Carnitine),又称左旋肉碱,在附睾中浓度最高,作为转运脂肪酸进入线粒体的重要载体,具有启动精子运动、促进精子成熟及提高精子受精能力的重要作用[10,11]。 目前,已经有多项多中心临床试验发现应用肉碱治疗少弱精子症可明显提高精子的浓度及总活力[12-14]。 在男性生殖系统中, 肉碱的主要获取方式是肉碱转运蛋白通过主动转运从血液中摄取。有机阳离子转运子2(organic cation/carnitine transportor 2,OCTN2) 是附睾转运肉碱的主要转运蛋白,主要分布于附睾、肾脏、心脏等组织。 人类附睾可能依赖OCTN2 转运肉碱进入附睾管, 为精子提供能量,促进精子成熟[15]。
中医学无弱精子症病名,一般将其归纳为精薄、精冷、难嗣等范畴,目前中医药认为在少弱精子症中,肾精亏虚仍是主要病因[16]。 麒麟丸是补肾类中成药的代表,具有补肾填精、益气养血的作用。 本实验主要基于L-肉碱通路, 对麒麟丸生殖系统保护作用及其可能机制进行探讨。 实验结果发现: 在精子浓度及总活力方面:与空白组相比,模型组精子浓度差异无统计学意义(P>0.05),总活力明显下降(P<0.01)。 与模型组相比,麒麟丸组和左卡尼汀组精子浓度差异无统计学意义(P>0.05),精子总活力明显上升(P<0.05)。 附睾L- 肉碱的含量方面:与空白组比较,模型组肉碱含量明显降低(P<0.01);与模型组比较,麒麟丸组和左卡尼汀组肉碱含量明显增高(P<0.01)。 附睾OCTN2 mRNA 的表达方面:与空白组比较,模型组OTCN2 mRNA 表达量无显著差异(P>0.05);左卡尼汀组与麒麟丸组OTCN2 mRNA 表达量高于模型组,差异有统计学意义(P<0.01)。
综上,本实验发现,麒麟丸具有明显提高奥硝唑造模致弱精子症大鼠模型精子活力的作用, 其作用机制可能与其提高附睾L-肉碱的含量和OCTN2 mRNA 的表达有关,更详细的作用机制有待进一步研究。
