胶体金免疫层析法快速检测桔青霉素的研究
2019-02-14陈尔净崔海峰张明洲
陈尔净,徐 影,马 骉,崔海峰,张明洲
(中国计量大学 生命科学学院,浙江 杭州 310018)
霉菌毒素是由霉菌引起的有毒代谢产物,可通过饲料或食品进入人和动物体内,对人和动物造成严重损害[1]。据统计每年约有25%的粮食作物受到霉菌毒素污染,这造成了不可估量的经济损失[2]。而CIT作为霉菌毒素的一种,近年来也受到了广泛关注。
CIT是青霉属,曲霉属和红曲霉属中的丝状霉菌代谢产生的一种霉菌毒素[3]。CIT最初于1931年由Hetherington等[4]从青霉属中的桔青霉中分离得到,在临床中被用作实验性抗生素。许多研究表明CIT经常存在于储存的农产品中,如小麦、玉米、苹果及其他农产品[5-7]。
众所周知,它是导致几种严重疾病的主要霉菌毒素之一[8]。桔青霉素作用的靶器官是肾脏,人和动物如果摄入过量被桔青霉素污染的食物,可能会引起肾脏肿大、尿量增多、肾小管扩张和上皮细胞变性坏死等症状,甚至会导致畸形和肿瘤突变[9,10]。据国际癌症研究机构报道,没有足够的科学证据证明CIT具有致癌性,且目前尚未明确报道桔青霉素的特定毒性机制[11]。因此,桔青霉素被归类为第三类致癌物。这意味着出于安全考虑,防止和控制桔青霉素污染物非常重要。迄今为止,我国尚未建立有关谷物样品中CIT的法律最高限制[12]。但是,日本红色发酵产品中的柑桔素的限量为200 μg/kg,在欧盟为100 μg/kg[13]。2016年,我国食品药品监督管理局在新颁布的食品中桔青霉素的测定方法中规定了大米、玉米、辣椒粉样品的检出限和定量限分别为8 μg/kg和25 μg/kg[14]。
目前大型仪器的CIT检测分析方法主要有薄层色谱(Thin Layer Chromatography,TLC)[15],高效液相色谱(High Performance Liquid Chromatography,HPLC)[16],液相色谱串联质谱(Liquid chromatography-tandem mass spectrometry,LC-MS/MS)[17]等。这些色谱方法是最常规的检测方法,其优点是精度高,重复性好,但是设备昂贵、耗时等缺点限制了它们在实际场景中的应用。为此许多免疫分析方法,如酶联免疫吸附试验[18]和化学发光免疫分析方法[19-20]被开发出来。然而,大多数免疫分析方法不适用于现场测试,这归因于它们的多重洗涤步骤和过长的反应时间。因此,开发快速、稳定、可靠且价格合理的现场检测方法很有必要。免疫胶体金技术是以胶体金作为示踪标志物,应用于抗原抗体的一种新型的免疫标记技术[21]。最初该方法仅用于免疫电镜技术,现在已经发展到光镜染色、免疫印迹以及免疫层析技术等[22]。目前已广泛应用于临床诊断,尤其是在医学临床检验中的应用,如早孕、乙肝和病毒的检测[23]。该方法最大特点是单份测定、简单快速、特异灵敏。如层析试纸条技术,不需任何仪器设备和试剂,几分钟就能得出实验结果。免疫胶体金层析技术现已成为当今最快速灵敏的免疫学检测技术之一,此技术具有快速、简便、稳定性好以及利于现场检测等优点,特别适合于广大基层单位、医院、野外作业人员以及大批量时间紧的检测和大面积普查等[24,25],因此该技术具有巨大的发展潜力和应用前景。近年来,已开发出许多使用免疫试纸条来检测霉菌毒素,如黄曲霉毒素B1[26]、赭曲霉毒素A[27]、玉米赤霉烯酮[28]等。
在这项研究中,我们开发了一种用于快速检测桔青霉素的胶体金免疫层析检测方法。结果表明,该研究方法具有快速且灵敏检测CIT的分析能力,实验结果与HPLC具有良好的一致性。
1 材料与方法
1.1 材料与试剂
桔青霉素(Citrinin,CIT)、黄曲霉毒素B1(Aflatoxin B1,AFB1)、赭曲霉毒素A(Ochratoxin A,OTA)、玉米赤霉烯酮(Zearalenone,ZEA)、呕吐毒素(Vomiting toxin,DON)购自上海邦景实业有限公司;牛血清白蛋白(Bovine serum albumin,BSA)、人血清白蛋白(Human serum albumin,HSA)购自美国Sigma公司;聚乙二醇、弗氏完全佐剂、弗氏不完全佐剂和胎牛血清购自美国Sigma公司;Balb/c小鼠购自上海斯克莱实验动物有限责任公司;SP2/0骨髓瘤细胞系在本实验室前期培养;Tween-20和二甲基亚砜(Dimethyl sulfoxide,DMSO)购自美国Sigma公司;硝酸纤维素膜(Millipore 180)、结合垫、样品垫、吸收垫购自美国Millipore公司;所有试剂均为分析纯。
磷酸盐缓冲液(Phosphate buffer saline,PBS,0.01 mol/L)称取0.2 g NaCl,1.55 g NaH2PO4,0.25 g KH2PO4,超纯水定容至1 L,并调节pH至7.4;硼酸盐缓冲液(Borate buffer,BB,0.05 mol/L)称取0.81 g 硼酸,0.67 g NaB4O7·10H2O,超纯水定容至1 L,并调节pH至8.2;碳酸盐缓冲液(Carbonate Buffer,CB,0.05 mol/L)称取1.59 g Na2CO3,2.94 g NaHCO3,超纯水定容至1 L,并调节pH至9.6。
1.2 CIT人工抗原的合成
精确称取10 mg CIT溶于1 mL甲醇溶液中,并缓慢滴加入9 mL HSA溶液(8 mg/mL,pH 4.0,溶解于乙酸-乙酸钠缓冲溶液)中进行反应,同时滴加入0.195 mL 37%甲醛,37 ℃避光搅拌加成反应24 h。反应产物CIT-HSA用PBS(0.01 mol/L,pH 7.4)4 ℃透析72 h后收集产物并储存在-20 ℃备用[29]。用相同的方法制备CIT-BSA。
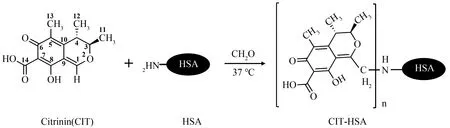
图1 甲醛加成法合成CIT-HSA人工抗原的方案
1.3 单克隆抗体的制备
选取8周龄雌性Balb/c小鼠进行免疫,将CIT-HSA与等量佐剂(首免采用弗氏完全佐剂,次免采用弗氏不完全佐剂)乳化后进行皮下注射[30]。免疫剂量100 μg/只,每两周皮下注射加强免疫一次。从第3次加强免疫后进行小鼠眼部采血,通过酶联免疫吸附试验(ELISA)检测血清效价。当血清效价不再上升时,用免疫原对小鼠进行脾脏冲击免疫,冲击剂量10 μg/只并取脾脏与SP2/0细胞进行融合。将融合好的杂交瘤细胞系经过亚克隆及间接竞争ELISA鉴定筛选出单克隆细胞株[31]。将单克隆细胞株扩大培养进行小鼠腹腔注射使其产生腹水,利用辛酸-硫铵法纯化腹水获得CIT的单克隆抗体。
1.4 胶体金-mAb探针制备
根据林少华[32]描述的方法制备胶体金-单克隆抗体(CG-mAb)探针。我们优化了抗体的标记量,分别优化2.5,5,10,20 μg/mL,实验结果表明10 μg/mL的效果最好,将10 μg/mL作为后续试验标记量。将溶解在0.1 mL BB缓冲液(0.05 mol/L,pH 8.2)中的20 μg CIT抗体溶液逐滴加入到2 mL金纳米粒子溶液中,室温搅拌反应1 h;再加入200 μL BSA(2 mg/mL,用pH 7.0、0.05 mol/L PBS缓冲液溶解)反应30 min。反应结束后离心(15,000 r/min,30 min)弃上清液,并用200 μL的BB缓冲液(0.05 mol/L,pH 8.2,含0.05% Tween-20)重悬并储存在4 ℃备用。
1.5 免疫层析试纸条的构造
免疫层析试纸条由样品垫、缀合物释放垫、吸收垫、NC膜和PVC板组成[33]。将缀合物释放垫与样品垫浸泡于PBS溶液(0.05 mol/L,pH 7.4,含1% BSA与0.05% Tween-20)中30 min并在37 ℃干燥箱中过夜烘干。将一定浓度的胶体金探针铺在已处理好的缀合物释放垫上真空干燥2 h,保存至干燥袋备用。将CIT-BSA和羊抗鼠IgG喷在硝酸纤维素膜上,分别作为检测线和对照线,经真空干燥2 h后并保存至干燥袋备用。最后按吸收垫、NC膜、缀合物释放垫、样品垫的顺序由顶部依次粘贴于PVC板上,裁成2.5 mm保存备用。
将特定量的胶体金-mAb探针与50 μL BB缓冲液(0.05 mol/L,pH 8.2)混合,轻轻摇动使溶液混合均匀,随后将混合溶液滴加到样品垫上,5 min后试纸条上就会出现红色条带,表明混合溶液在条带上成功移动,并胶体金试纸条读数仪读取此时测试线和控制线上的发光强度值。
1.6 免疫试纸条参数优化
1.6.1 最佳检测时间的确定
将待测样品用BB缓冲溶液(0.05 mol/L,pH 8.2)稀释成一定浓度并滴在试纸条上进行检测,分别在反应5、10、15、20、25、30、35、40、45、50 min时用金标读数仪检测,每个时间段测试3遍并记录保存数值。
1.6.2 最佳缓冲液的选择
将待测样品用ddH2O、PBS缓冲液(0.05 mol/L,pH 7.4)、BB缓冲液(0.05 mol/L,pH 8.2)、CB缓冲液(0.05 mol/L,pH 9.6)稀释成一定浓度并滴在试纸条上进行检测,在最佳检测时间内用金标读数仪读取数值并记录保存。
1.7 样品分析
为了验证ICA的适用性,分别通过HPLC和ICA的方法对加标的阴性样品以及实际样品进行分析。首先,根据国家标准中描述的方法进行HPLC测定,以鉴定谷物样品中是否存在CIT残留。通过向阴性样品中加入不同浓度的CIT,使其溶液中CIT的终浓度为10,20,40,80,160 ng/mL来进行回收测试。样品提取方法与KONG[34]等人描述的方法类似,并参考国家标准提取方法。取1 g研磨样品若干份,分别与20 mL甲醇-水(7∶3,体积比)提取液并充分混匀,用高速均质器提取2 min后收集提取液。于振荡器上振荡提取5 min,用滤纸过滤,或者8 000 r/min离心10 min,取上清液备用。通过ICA分析所有样品并通过HPLC分析确认。
从超市随机购买谷物样品,包括玉米、大豆、大米和小麦。用上述方法进行提取,通过胶体金免疫层析法进行检测分析并将结果与HPLC获得的结果进行比对。
2 结果和讨论
2.1 免疫层析试纸条检测原理
本研究中胶体金免疫层析试纸条的检测是基于抗原抗体竞争反应的原理[35]。如图2(a),当样品滴加到样品垫上时,样品溶液通过毛细管力快速流过条带,反应后用便携式读数仪读取结果。固定化抗原与样品溶液中目标分析物之间存在竞争关系,共同竞争CG-mAb探针。当目标分析物与探针特异性结合后,便会形成CG-mAb-分析物复合物,此时测试线上所能捕获的探针量就少,结果呈阳性如图2(b),如果样品溶液中不存在目标分析物或其含量低于检测范围时,所有的CG-mAb探针都会与测试线结合,而多余的CG-mAb探针会继续流过膜与控制线结合,此时结果呈阴性如图2(c)。
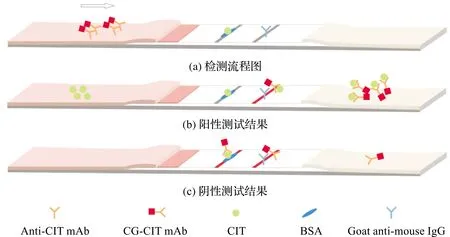
图2 免疫条带检测原理图
2.2 抗原抗体的表征
制备的CIT-BSA和CIT-HSA分别通过紫外-可见光谱扫描鉴定。如图3(a),在253 nm和305 nm处发现CIT的特征峰。在275 nm处发现BSA的特征峰。然而,如图3(b),CIT-BSA的特征峰在275 nm和315 nm处发现。上述性质可表明CIT成功地与BSA载体蛋白偶联,也表明CIT与HSA载体蛋白成功偶联。SDS-PAGE结果显示抗原条带与载体蛋白条带之间存在着明显的滞后现象,表明CIT成功地与载体蛋白结合,结果如图3(c)与3(d)。该鉴定结果与紫外-可见光谱扫描鉴定结果一致。
通过细胞融合筛选出四株稳定的细胞株,使用间接竞争ELISA测定抗体亲和力,详细过程如下。将包被CIT-BSA(包被浓度为250 ng/mL)的96孔板在4 ℃下封闭24小时。反应完成后,将CIT标准品(终浓度为0.1,0.3,1,3,9,27,81 ng/mL)以50 μL/孔添加到封闭的96孔板中。然后,将抗CIT单克隆抗体和酶标抗体稀释并以50 μL/孔的浓度添加到封闭的96孔板中。该反应在25 ℃下进行30 min。反应完成后,将板用PBST洗涤3次。然后,将TMB以100 μL/孔添加到96孔板中。反应在25 ℃下进行10 min。将终止溶液以50 μL/孔添加到平板中,并使用酶标仪在450 nm处测量OD值。从中选出最佳的细胞株2D3使产生腹水纯化后得到抗体,并计算其结合亲和力为7.17×108L/mol,IC50为4.73 ng/mL,结果如图4(a)。用5种不同的霉菌毒素评估抗体的特异性,如图4(b)。结果表明,抗CIT mAb只对桔青霉素体现出强的结合率,而其余4种霉菌毒素并没有体现出明显的交叉反应。抗CIT mAb显示出良好的特异性。
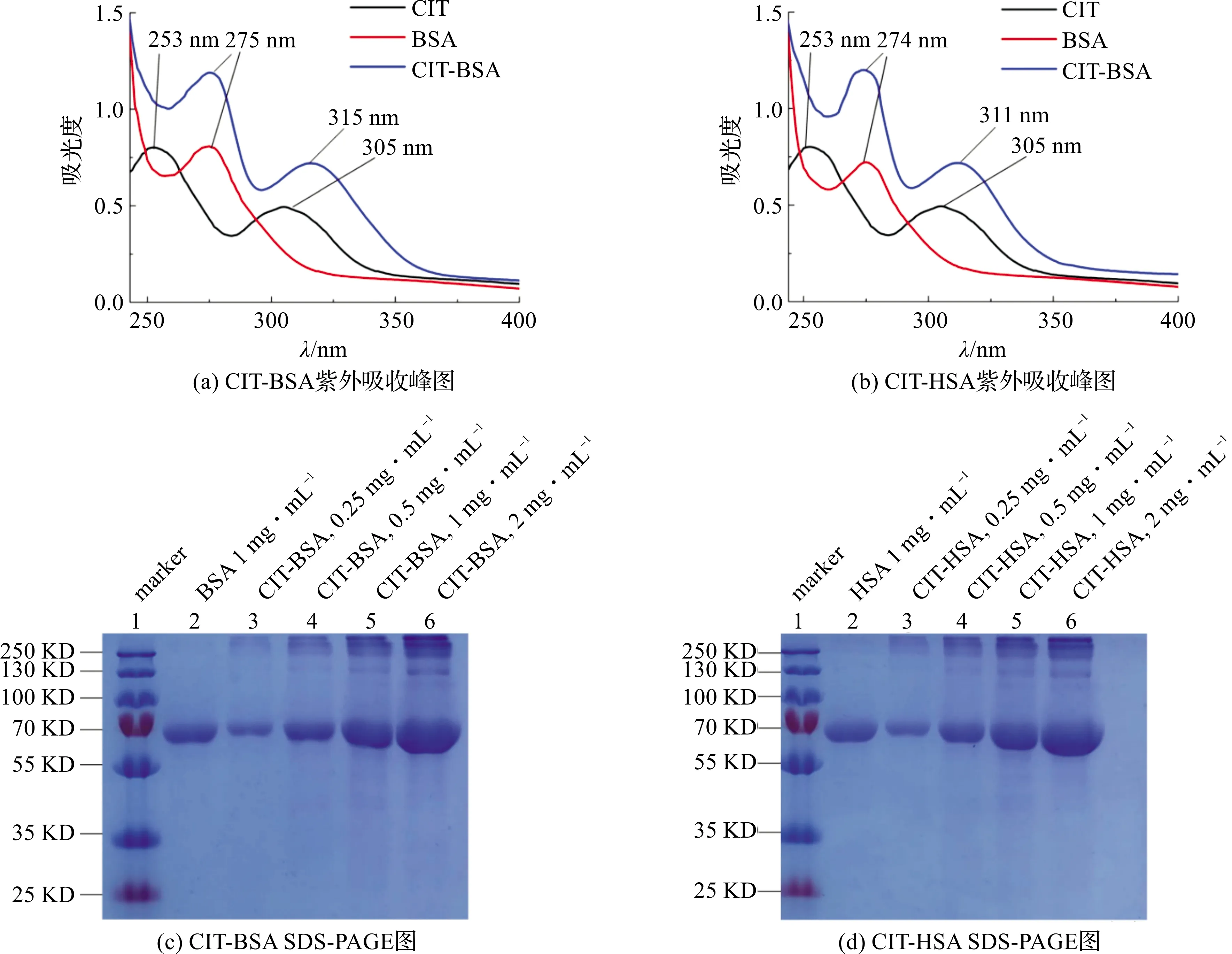
图3 CIT-BSA/CIT-HSA抗原表征图

图4 CIT抗体亲和力鉴定及交叉反应结果
2.3 免疫试纸条参数优化
研究了免疫反应时间对该方法发光强度响应的影响。图5(a)显示了ICA对不同免疫反应时间的发光强度反应,其中T值和C值在前20 min内随着免疫反应时间的增加而急剧增加,然后轻微波动至25 min时趋于稳定。因此,25 min被认为是最佳免疫反应时间。同时,研究了不同缓冲体系对该研究方法发光强度响应的影响。如图5(b),用BB缓冲液(0.05 mol/L,pH 8.2)做缓冲体系时,检测到的发光强度最强。因此,采用BB缓冲液(0.05 mol/L,pH 8.2)作为该研究的稀释缓冲体系。

图5 胶体金免疫层析法优化结果
2.4 免疫条带分析谷物中的CIT
2.4.1 灵敏度及特异性评估
将含有不同CIT标准品浓度(0、0.05、0.1、0.25、0.5、1、2.5、5、10、20、40 ng/mL)的样品溶液滴在试纸条上进行测试。从图6(a)可以看出,随着CIT浓度的增加,T线逐渐消退,在CIT质量浓度为5 ng/mL时完全消失。图6(c)是根据其灵敏度建立的标准曲线,IC50为0.79 ng/mL,检测限(LOD)为0.11 ng/mL。从图中可以看出,抑制率与CIT浓度之间具有良好的线性关系,R2≥0.97。
为了确定免疫测定的特异性,研究了4种霉菌毒素,包括黄曲霉毒素B1、赭曲霉毒素A、玉米赤霉烯酮和呕吐毒素。通过建立的ICA测定法测试稀释至终质量浓度为500 ng/mL的标准溶液的四种毒素。结果显示在图6(b)中,表明测定选择性与先前工作中表征的抗CIT mAb特异性一致。
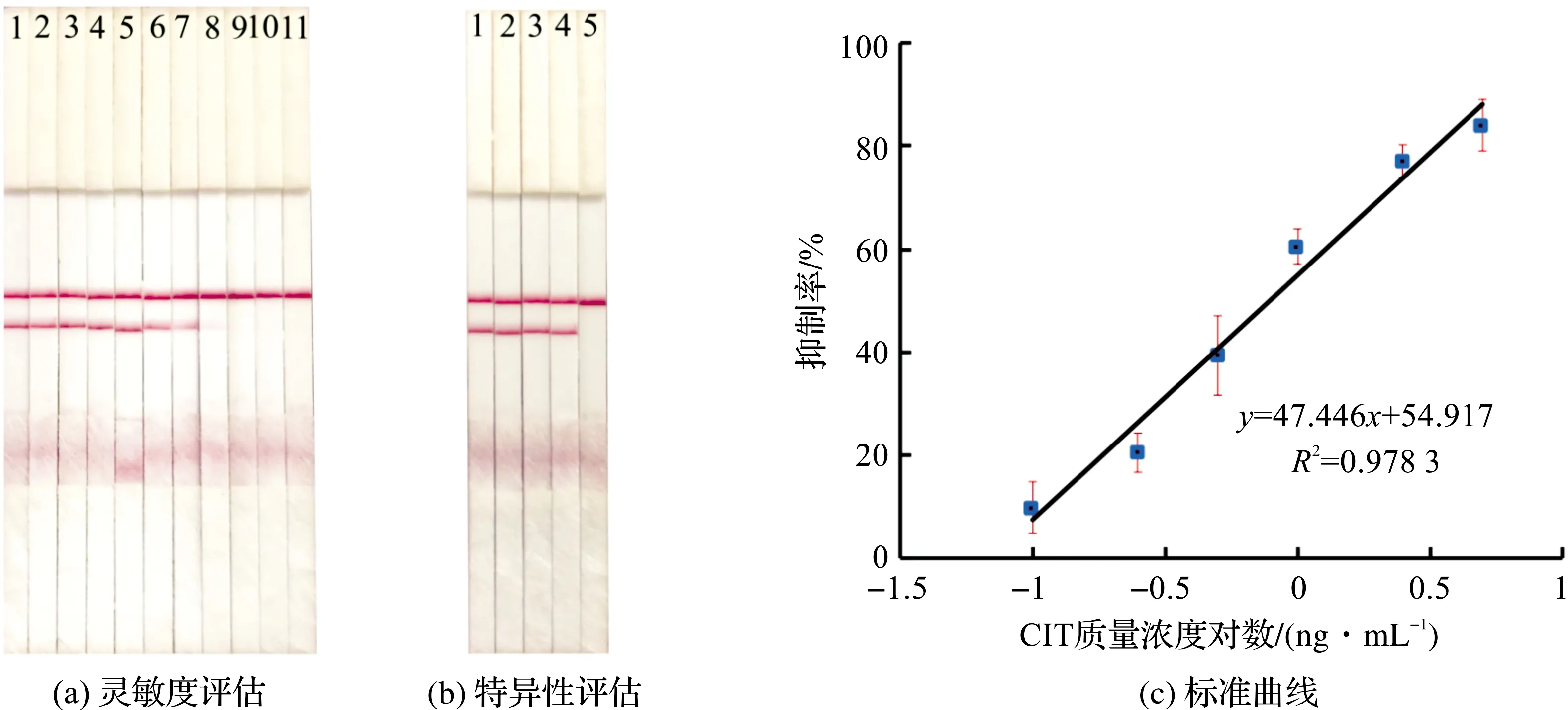
图6 抗CIT mAb灵敏度及特异性评估
2.4.2 样品分析
为了评估开发的胶体金免疫层析检测方法的精密度和准确度,该研究在测定的检测范围内进行了加标回收实验,一式3份,重复6次(n=6)。在阴性样品(玉米和小麦)中,分别加入不同质量浓度的CIT标准品(10,20,40,80,160 ng/g)。表1结果表明玉米样品的回收率在86.93%~110.04%的范围内,相对标准偏差(RSD)在0.47%~2.58%之间;小麦样品的回收率在89.60%~110.34%的范围内,相对标准偏差在0.47%~2.59%之间。检测结果与高效液相色谱法作为参考方法进行比较,图7结果显示胶体金免疫层析检测方法与HPLC结果具有良好的一致性。从当地市场随机购买12份谷物样品进行测试,一式三份,重复6次(n=6),表2结果表明胶体金免疫层析检测方法与HPLC结果较为相符。其中一份山西小麦中桔青霉素在HPLC中无法检出,但在ICA的检测范围内被准确的检测出来。分析其原因,可能由于该ICA检测技术的灵敏度过高,且由于小麦的基质存在干扰而引起的假阳性结果。对于谷物食品的基质影响分析,有待进一步研究。因此,胶体金免疫层析检测技术具有良好的精密度和准确度,可用于谷物中桔青霉素的定性和半定量分析。
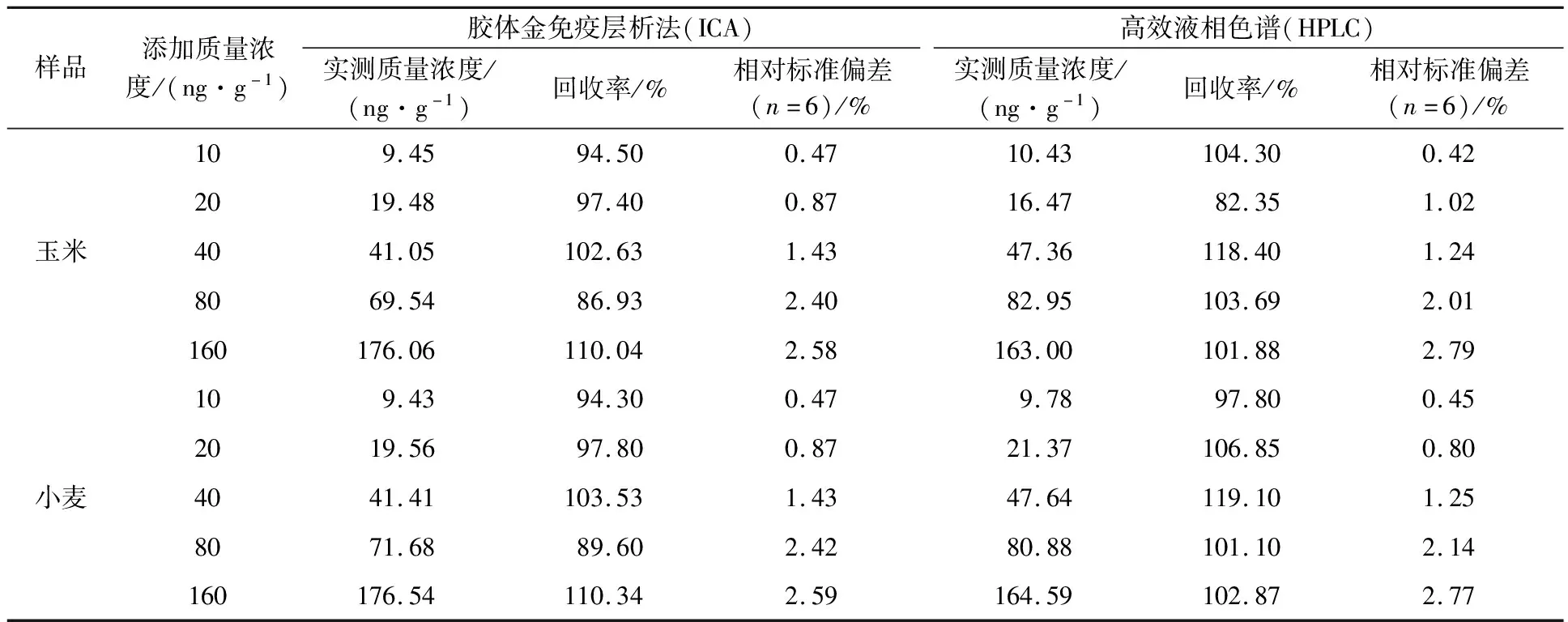
表1 加标玉米和小麦样品对开发的ICA进行精密度和准确度评估
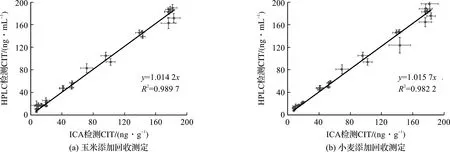
图7 ICA与HPLC检测方法添加回收对比试验结果
3 结 论
食用桔青霉素污染的食物会影响人体健康,为了避免有污染食物在市场中流淌,开发用于桔青霉素的快速检测手段变得非常重要。此项研究的重点为胶体金免疫条带的开发。CIT是分子量为250的半抗原,不具有免疫原性,必须与载体蛋白偶联才表现出免疫原性。为了检测玉米中的CIT残留,将CIT与BSA和HSA缀合,使其成为产生CIT特异性抗体的有效抗原。随后成功制备并表征了具有7.17×108L/mol亲和力的抗CIT mAb 2D3,并将mAb 2D3用于开发CIT残留检测的ICA。在最优条件下,ICA测试可用作定性和半定量工具,在25 min内检测CIT残留物,视觉检测限为5 ng/mL,与其他霉菌毒素无交叉反应。ICA试验的结果与HPLC分析结果具有良好的一致性。总之,这种ICA分析可以达到在实验室和非实验室场所中方便、快速、灵敏和半定量检测桔青霉素残留的目的。

表2 谷物样品中CIT的ICA和HPLC分析
注:“-”表示未检出
