T1期肾肿瘤个性化“缩短热缺血时间”技术辅助腹腔镜肾部分切除术的方案选择及临床应用研究
2019-02-13潘秀武叶剑青陈佳鑫吕建敏杨启维干思舜崔心刚
潘秀武,李 霖,叶剑青,陈佳鑫,徐 达,吕建敏,杨启维,干思舜,崔心刚,
(1.第二军医大学第三附属医院,上海,201805;2.第二军医大学附属公利医院)
肾癌是泌尿系常见的恶性肿瘤,发病率位居第二位[1]。2015年中国癌症统计数据显示,中国肾癌年发病6.68万例,年死亡2.34万例,严重危害民生健康[2]。根据欧洲泌尿外科协会及美国国立综合癌症网络指南推荐,对于T1期肾肿瘤,在技术可行的前提下优选肾部分切除术[2]。对于肾部分切除术,热缺血时间控制在30 min内是术后肾功能恢复的关键影响因素,超过30 min可引起肾脏不可逆的缺血损伤[2]。因此减少热缺血时间成为肾部分切除术的焦点,常见减少热缺血时间的术式包括肾动脉无阻断、肾动脉早期开放、肾动脉分支阻断等。但上述术式操作复杂,如果不能根据肿瘤特征选择个性化术式,可导致手术并发症风险增加(术中出血、损伤动静脉、切缘阳性等),因此迫切需要一种能根据肿瘤特征进行客观判断,并制定个性化术式的选择标准。本研究通过标准化选择流程,拟为患者制定个性化“缩短热缺血时间”的腹腔镜肾部分切除术,取得了良好的临床疗效,现将体会报道如下。
1 资料与方法
1.1 临床资料 本研究回顾性收集2014年1月至2018年1月海军军医大学东方肝胆外科医院与海军军医大学附属公利医院泌尿外科接受腹腔镜肾部分切除术的189例肾肿瘤患者,其中男112例,女77例,平均(56.51±14.31)岁,肿瘤直径平均(3.80±1.68)cm,内生型78例,外生型111例,平均R.E.N.A.L评分(7.45±1.78)分。入组患者均为单发肿瘤,排除双肾肿瘤、多发肿瘤、孤立肾肿瘤。术前患者行肾脏CTA或MRA,明确肾肿瘤无局部进展及淋巴结转移;术前行胸部CT、头颅MRI或全身PET-CT明确无远处转移病灶。术后随访1年以上,术后第1个月、第3个月、第6个月、第9个月及第12个月常规复查血常规、尿常规、肝肾功能、胸部X线或CT、腹部CT平扫或增强等。根据患者术后症状,必要时行头颅MRI、全身骨扫描或PET-CT等检查。均告知手术相关风险并签署知情同意书,经医院伦理委员会备案并批准同意。
1.2 手术方法 传统组:术前行CTA或MRA评估肿瘤及肾脏动静脉特征,患者均行肾动脉全阻断下腹腔镜肾部分切除术。手术步骤:全身麻醉,患者取健侧卧位,于腰部(经腹膜后入路)或侧腹部(经腹入路)穿刺3~4枚Trocar。充分暴露肾动脉,根据肿瘤位置及缝合需要,充分游离肾周脂肪,显露肾肿瘤。用血管阻断钳阻断肾动脉,沿肿瘤边缘0.5 cm锐性与钝性分离相结合法切除肾肿瘤。用3-0可吸收倒刺线连续缝合关闭肾脏创面破损的血管及集合系统,用2-0可吸收倒刺线连续缝合肾实质创缘1~2层。个性化组:患者行肾脏CTA或MRA检查后,进一步利用三维智能定性定量分析系统进行三维重建、个性化手术方案设计及术前手术模拟切除,个性化方案选择流程见图1。个性化组术式包括:(1)标准无阻断技术(个性化亚组1):在肾动脉无阻断的情况下,切除肾肿瘤瘤体,使用倒刺线连续缝合关闭肾实质创面与创缘。(2)预留缝线无阻断技术(个性化亚组2):在肾动脉无阻断的情况下,距肿瘤边缘1 cm正常肾实质处预缝合一根倒刺线,如果出血较多,牵拉或收紧止血,出血仍无法控制时,利用该缝线直接对已切除创面进行缝合止血。如果出血尚可,待肿瘤瘤体完整切除后,利用该缝线缝合肾创面。(3)术前DSA超选栓塞无阻断技术(个性化亚组3):术前1~15 h由同一介入科医师对供应肿瘤的超选动脉行介入栓塞,术中在无阻断的情况下,切除肿瘤瘤体,使用倒刺线连续缝合关闭肾实质创面与创缘。(4)早期序贯开放血流法(个性化亚组4):序贯阻断供应肾肿瘤的肾段动脉与肾动脉主干,在切除肾肿瘤、缝合肾创面破损的血管及集合系统后,开放肾动脉主干。在快速大间距缝合对合肾创缘后,开放供应肾肿瘤的肾段动脉。在无阻断的情况下,仔细连续缝合关闭肾创缘。(5)肾动脉阻断(2+1缝合法,个性化亚组5):在肾动脉阻断的情况下,切除肾肿瘤瘤体、缝合肾创面破损的血管及集合系统,快速大间距缝合对合肾创缘后,开放肾动脉,仔细连续缝合关闭肾创缘。见图2~图6。
1.3 数据收集 观察指标主要包括患者信息(性别、年龄、ASA评分)、肿瘤特征(肿瘤直径、分期、位置、复杂性评分)、围手术期信息(手术时间、热缺血时间、术中出血量、术后住院时间、切缘阳性、手术相关并发症、术前、术后血红蛋白)、术后随访(肾小球滤过率)。
1.4 统计学处理 应用SPSS 21.0软件进行数据分析。计数资料以[n(%)]表示,采用χ2检验;计量资料以均值±标准差表示,采用独立样本t检验,等级资料的比较采用Mann-Whitney U检验。P<0.05为差异有统计学意义。
2 结 果
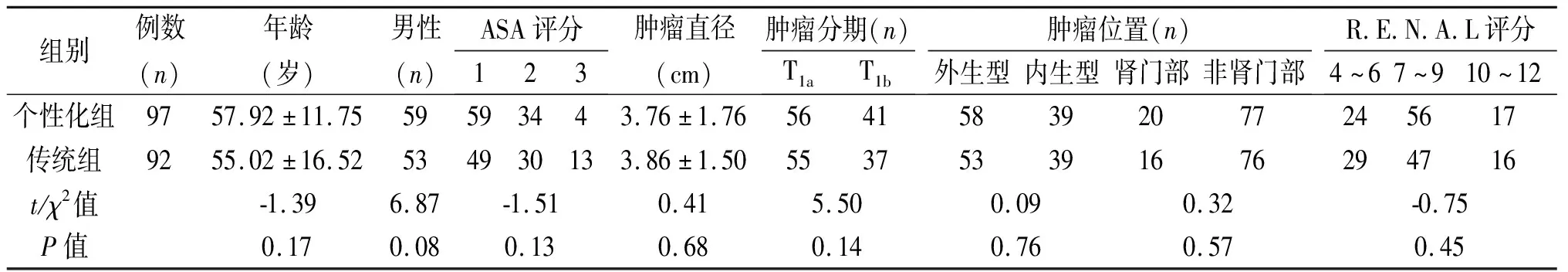
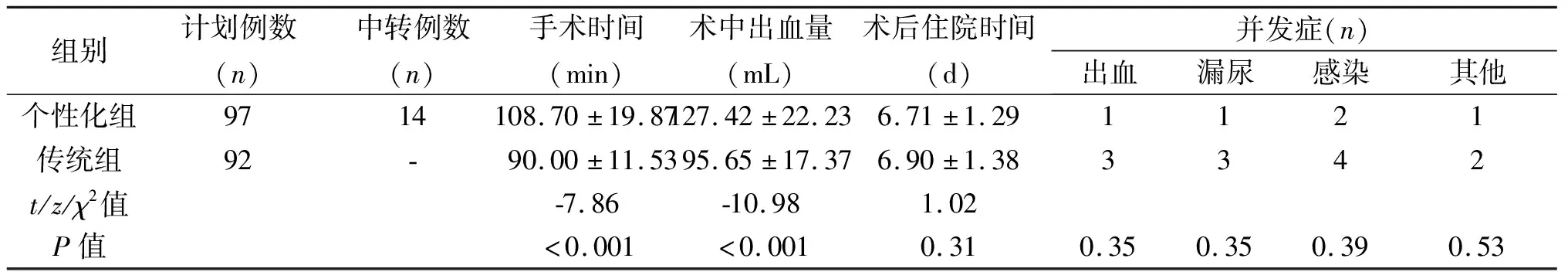
97例肾肿瘤患者施行了个性化”缩短热缺血时间”方案设计,其中83例(85.6%)按个性化方案行个性化肾部分切除术(个性化组);个性化亚组1(标准无阻断肾部分切除术)中,17例(17/20,85.0%)患者完成手术,3例由于术中出血多,转变为肾动脉阻断(2+1缝合法);个性化亚组2(预留缝线无阻断技术)中,15例(15/19,78.9%)患者完成手术,4例中转为2+1缝合法,其中2例肿瘤位置为完全内生型,2例术中出血多;个性化亚组3(术前DSA超选栓塞无阻断技术)中,12例(12/17,70.6%)患者完成手术,5例中转为2+1缝合法,其中3例术前介入未能精确寻及供应肿瘤的超选靶血管,2例肿瘤位置为完全内生型;个性化亚组4(早期序贯开放血流法)中,18例(18/20,90%)完成手术,2例中转为2+1缝合法,其中2例肾门部粘连严重,导致肾动脉分支解剖层次不清晰;个性化亚组5(肾动脉全阻断“2+1缝合法”)中,21例入组患者均完成个性化设计的手术方案,另有14例完成“2+1”。传统组中92例患者均顺利完成肾动脉阻断下腹腔镜肾部分切除术。个性化组与传统组患者基线特征及肿瘤特征(包括年龄、性别、ASA评分、肿瘤直径、肿瘤分期、肿瘤位置、R.E.N.A.L评分)差异无统计学意义,见表1。个性化组患者均在无阻断或早期开放的情况下完成手术,热缺血时间不统一,未与传统组进行相应的比较。个性化组手术时间较传统组长(P<0.001),见表2;可能原因是:(1)无阻断及早期开放较传统无阻断出血多,影响手术视野,进而影响手术操作;(2)部分手术需要精细操作,如“早期序贯开放血流法”需要游离肾动脉分支。虽然个性化组术中出血量多于传统组(P<0.001),见表2,但两组术后血红蛋白差异无统计学意义(P=0.79),见表2。两组术后住院时间、围术期手术相关并发症、术后病理差异均无统计学意义,见表2;且两组患者均未出现切缘阳性。

图1 个性化”缩短热缺血时间”肾部分切除术技术方案选择流程图
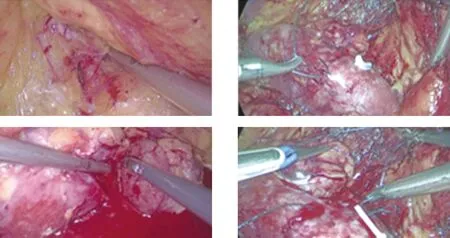
图2 标准无阻断技术 图3 预留缝线无阻断技术
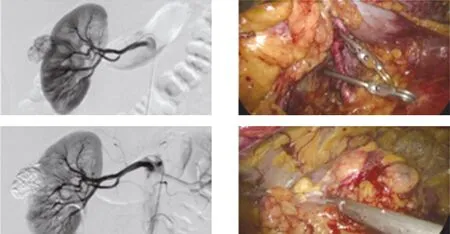
图4 术前DSA超选栓塞无阻断技术 图5 早期序贯开放血流法
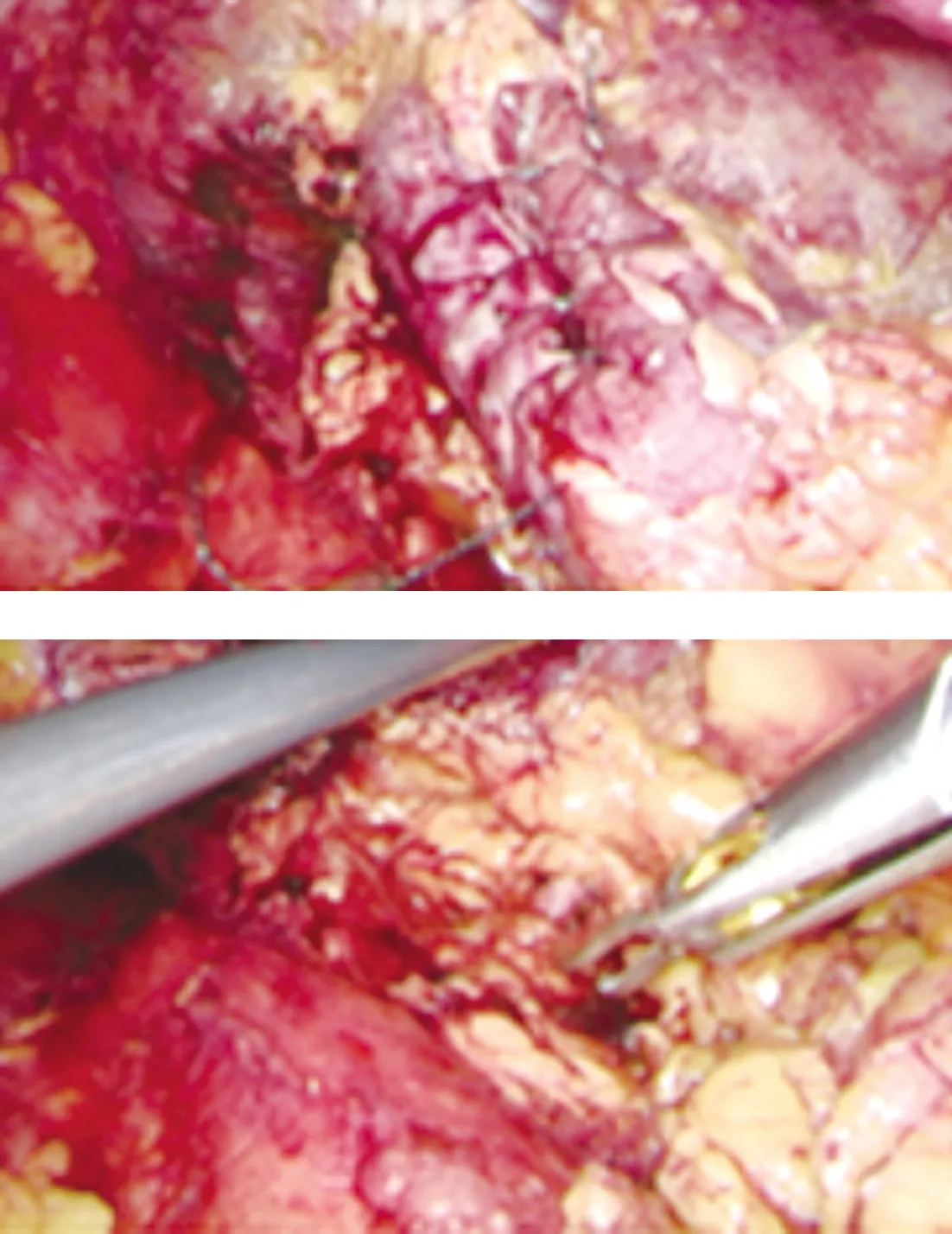
图6 “2+1”缝合法
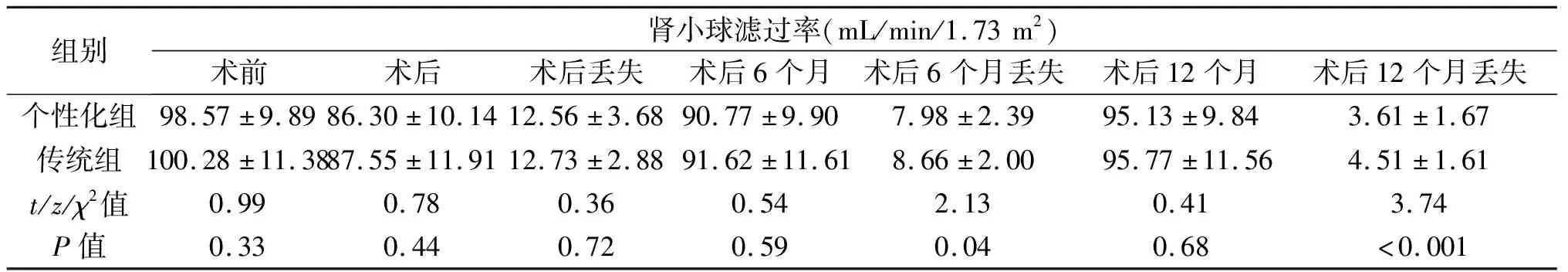
个性化组与传统组术前肾功能评估差异无统计学意义(P=0.33),见表2。术后第2天,个性化组与传统组肾功能丢失情况差异无统计学意义。随着术后时间的推移,个性化组肾功能恢复明显好于传统组。术后6个月、12个月,个性化组肾功能恢复情况占优势,差异有统计学意义(6个月P=0.04,12个月P<0.001),见表2。为了进一步明确个性化组中各亚组之间的差异,我们对比分析了各组间肿瘤直径、R.E.N.A.L评分、手术时间、热缺血时间、术中出血量、术前与术后12个月肾功能情况,见表3。
3 讨 论
随着肾肿瘤手术技术的快速发展,大量研究显示[3-4],对于T1期肾肿瘤,肾部分切除术与肾癌根治性切除术具有相似的肿瘤学结果,但具有更优异的非肿瘤相关生活质量及术后生存率,因此各大指南推荐肾部分切除术为T1期肾肿瘤的优选治疗方案[3-4]。在保留肾单位手术中,如何尽可能地保留肾功能已成为肾部分切除术的关注焦点。肾动脉阻断引起的缺血性损伤是引起肾功能损失的重要因素,将术中热缺血时间控制在30 min甚至20 min内,对肾功能的保护至关重要。
研究表明[5-6],肾动脉无阻断能显著保留患者术后肾功能,但与其他肾部分切除术相比,其术中出血量显著增加,导致此术式目前主要适于外生型小肿瘤(≤2)[5-6]。应进一步探索无阻断肾部分切除术的创新技术,减少术中出血量,降低手术难度,扩大无阻断技术的适用范围。目前常见的无阻断辅助技术包括水刀辅助无阻断技术、预留缝线无阻断技术、术前DSA超选栓塞无阻断技术等,一定程度上提高了无阻断肾部分切除术的安全性及适应证[7-9]。此外,2007年Baumert等学者在国际上首先提出“早期开放血流法”,此术式将热缺血平均时间从27.2 min减至13.7 min[10]。我们在临床实际应用中发现,“早期开放血流法”术中出血明显,影响手术操作视野,早期开放血供后肾脏张力过大,肾创缘对合不佳。因此,在此基础上,我们进一步提出早期开放技术(2+1缝合法),既弥补了上述不足,又显著缩短了热缺血时间[11]。肾动脉分支阻断技术,精确阻断供应肿瘤的动脉分支,造成肾脏区域性缺血状态,保证剩余肾实质正常供血。但在T1b期或解剖位置复杂的肾肿瘤,分支阻断技术往往会增加出血风险,尤其处理肾实质创面时[12-13]。因此我们结合分支阻断与早期开放技术,创新性提出“早期序贯开放血流法”[14],此术式通过肾动脉全阻断下处理肾脏创面,分支阻断下快速对合肾创缘,无阻断下修补缝合肾创缘,降低了手术风险,缩短了热缺血时间。
组别例数(n)年龄(岁)男性(n)ASA评分123肿瘤直径(cm)肿瘤分期(n)T1aT1b肿瘤位置(n)外生型内生型肾门部非肾门部R.E.N.A.L评分4~67~910~12个性化组9757.92±11.7559593443.76±1.76564158392077245617传统组9255.02±16.52534930133.86±1.50553753391676294716t/χ2值-1.396.87-1.510.415.500.090.32-0.75P值0.170.080.130.680.140.760.570.45
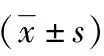
组别计划例数(n)中转例数(n)手术时间(min)术中出血量(mL)术后住院时间(d)并发症(n)出血漏尿感染其他个性化组9714108.70±19.87127.42±22.236.71±1.291121传统组92-90.00±11.5395.65±17.376.90±1.383342t/z/χ2值-7.86-10.981.02P值<0.001<0.0010.310.350.350.390.53
续表2

组别术后病理(n)透明细胞癌乳头状细胞癌嫌色细胞癌其他血红蛋白术前术后个性化组811240112.87±14.43104.60±16.59传统组791111111.87±16.56102.24±13.38t/z/χ2值-0.440.27P值0.530.660.79
续表2
组别肾小球滤过率(mL/min/1.73m2)术前术后术后丢失术后6个月术后6个月丢失术后12个月术后12个月丢失个性化组98.57±9.8986.30±10.1412.56±3.6890.77±9.907.98±2.3995.13±9.843.61±1.67传统组100.28±11.3887.55±11.9112.73±2.8891.62±11.618.66±2.0095.77±11.564.51±1.61t/z/χ2值0.990.780.360.542.130.413.74P值0.330.440.720.590.040.68<0.001
表3 个性化“零缺血”组各亚组患者的相关指标
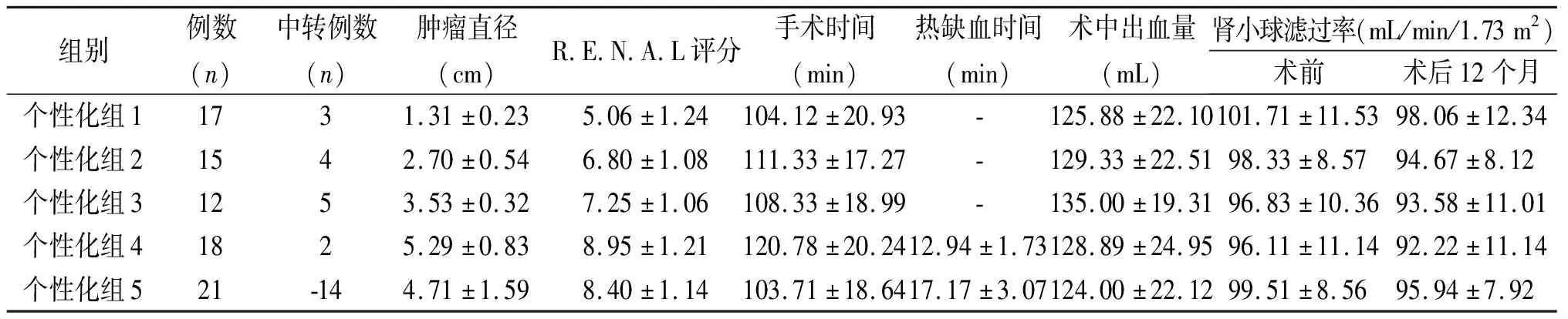
组别例数(n)中转例数(n)肿瘤直径(cm)R.E.N.A.L评分手术时间(min)热缺血时间(min)术中出血量(mL)肾小球滤过率(mL/min/1.73m2)术前术后12个月个性化组11731.31±0.235.06±1.24104.12±20.93-125.88±22.10101.71±11.5398.06±12.34个性化组21542.70±0.546.80±1.08111.33±17.27-129.33±22.5198.33±8.5794.67±8.12个性化组31253.53±0.327.25±1.06108.33±18.99-135.00±19.3196.83±10.3693.58±11.01个性化组41825.29±0.838.95±1.21120.78±20.2412.94±1.73128.89±24.9596.11±11.1492.22±11.14个性化组521-144.71±1.598.40±1.14103.71±18.6417.17±3.07124.00±22.1299.51±8.5695.94±7.92
如何个性化选择腹腔镜肾部分切除术的方式,目前主要取决于术者的主观决策,这种决策建立在丰富的手术经验及肾肿瘤特性上,对于年轻术者而言,缺少根据客观指标选择肾部分切除方式的标准流程[15-16]。本研究所选的标准流程既能缩短热缺血时间、保护肾功能,又能降低手术操作难度、减少手术并发症,为合理设计个性化肾部分切除术的方式提供依据。通过三维智能定性定量分析系统,融入了肿瘤位置、大小及分支血流分布情况,并依据患者临床资料、结合术者手术经验制定个性化手术方案。尽管有研究报道,标准无阻断肾部分切除术适于T1b或更大的肾肿瘤[17],但我们的临床研究发现,对于较大(>2 cm)或复杂肾肿瘤,标准无阻断技术显著增加了术中出血量及不可控的并发症风险。因此我们在方案中设定了肾肿瘤≤2 cm,并属于外生型,适合标准无阻断肾部分切除术。虽然是小肿瘤(≤2 cm),但肿瘤位置较深(内生型),术中出血多,视野不清增加了切缘阳性的风险,因此我们进一步细化方案,≤2 cm内生型肾肿瘤应用预留缝线技术。同时对于2~4 cm的外生型肾肿瘤,适合应用预留缝线无阻断技术(适时而动,应对出血):出血较多时,收紧预置缝线止血;出血量大时,边切边缝;出血可控时,切完再缝[8]。2~4 cm的内生型肾肿瘤,则于术前应用DSA超选栓塞无阻断技术进行提前干预,降低出血量及出血相关风险,显著提高此类型肿瘤的无阻断手术安全性[9]。肾门部肾肿瘤,其肿瘤与肾盂及主要脉管系统关系密切,不论肿瘤大小,无阻断肾部分切除术的风险极大[18-19],因此我们将≤4 cm的肾门部肾肿瘤进行相应分流。对于>4 cm的肾肿瘤,与单支供应血管阻断相比,多血管分支阻断的阻断热缺血区域更大,阻断效果与全阻断相似,且游离多支肾动脉手术难度极大,术中血管损伤的风险增加[9]。因此对于供应肿瘤肾段动脉1~2支的患者,我们应用早期序贯开放血流;>2支的患者,直接应用全阻断(2+1缝合法)。
本研究中,个性化组与传统组围术期大部分相关指标差异无统计学意义,虽然手术时间、出血量增多,但均在可控范围内。值得注意的是个性化组术后肾功能恢复随着时间推移明显优于传统组。我们认为,个性化组各亚组均可一定程度上缩短热缺血时间,尽可能保留肾功能。
综上所述,个性化“缩短热缺血时间”技术根据肿瘤的解剖特征个性化地缩短热缺血时间,降低患肾缺血性肾损伤的风险,极大地保留了术后肾功能,临床应用安全、可行。
