糖尿病视网膜病变合并糖尿病肾病的危险因素及其预测价值
2019-02-13浦丹凤王霞娟马坚邵耀明刘国萍
浦丹凤,王霞娟,马坚,邵耀明,刘国萍*
(南京医科大学附属无锡市人民医院:1内分泌科,2检验科,无锡 214023)
糖尿病视网膜病变(diabetic retinopathy,DR)是2型糖尿病(type 2 diabetes mellitus,T2DM)患者最常见的微血管并发症,20%~40%的T2DM患者会出现DR[1]。研究数据显示,2030年全球DR患者人数将达1.9亿,是20~60岁人群致盲的首要原因[2]。糖尿病肾病(diabetic nephropathy,DN)也是糖尿病患者主要的慢性并发症,DN导致的慢性肾功能衰竭是糖尿病患者死亡的重要原因。我国T2DM患者DN的患病率已超30%,是导致终末期肾脏病的第二大病因[3]。DR和DN均属于微血管并发症,二者之间存在一定的关联,DR患者合并DN并不少见,本研究针对DR患者合并DN的危险因素进行了分析,并对相关指标的预测价值进行了探讨。
1 对象与方法
1.1 研究对象
回顾性分析2017年5月至2018年5月南京医科大学附属无锡市人民医院内分泌科收治的T2DM患者1 969例,其中DR合并DN患者609例,单纯DR患者746例,未并发DN和DR患者614例。纳入标准: T2DM诊断标准参考中华医学会糖尿病学分会2013年制订的《中国2型糖尿病防治指南》[4]。DR诊断标准参考中华医学会眼科学会眼底病学组2014后制订的《我国糖尿病视网膜病变临床诊疗指南(2014年)》[5],DN诊断标准参考中华医学会内分泌学分会2015年制订的《中国成人糖尿病肾脏病临床诊断的专家共识》[6]。排除标准:合并有恶性肿瘤、急性冠脉综合征、自身免疫疾病、血液病、妊娠期或哺乳期患者;合并有除糖尿病外其他全身代谢疾病患者;临床资料不完整患者。
1.2 检测指标
详细询问病史,检测3组患者的收缩压(systolic blood pressure,SBP)、舒张压(diastolic blood pressure,DBP)、白蛋白(albumin,ALB)、空腹血糖(fasting blood glucose,FBG)、餐后血糖(postprandial blood glucose,PBG)、空腹C肽(fasting C-peptide,FC)、餐后2h C肽(postprandial 2h C-peptide,PC)、甘油三酯(triglycerides,TG)、总胆固醇(total cholesterol,TC)、高密度脂蛋白胆固醇(high-density lipoprotein cholesterol,HDL-C)、低密度脂蛋白胆固醇(low-density lipoprotein cholesterol,LDL-C)、总胆红素(total bilirubin,TBIL)、直接胆红素(direct bilirubin,DBIL)、血红蛋白(hemoglobin,Hb)、糖化血红蛋白(glyco-sylated hemoglobin A1c,HbA1c)、血尿酸(blood uric acid,BUA)、血尿酸氮(blood urea nitrogen,BUN)、血肌酐(serum creatinine,SCr)和胱抑素C(cystatin C,Cys C)水平。根据慢性肾脏病流行病合作工作组(chronic kidey didsease epidemiology collaboration,CKD-EPI)方程计算肾小球滤过率(glomerular filtration rate,GFR)。依据中华医学会眼科学会第3次全国眼科学术会议制订的《糖尿病视网膜病变分期标准》对眼底病变分期和评分,分值1~6分,评分越高,病变程度越重。
1.3 辅助检查
CV650型心脏彩色多普勒超声仪(飞利浦公司)检测患者的室间隔和左室后壁厚度,并判定是否存在室间隔增厚。应用C9型便携式颈动脉彩色多普勒超声分析仪(KONTED公司)检测患者左侧和右侧颈动脉内膜中层厚度(intima-media thickness,IMT),并判定是否有颈动脉粥样斑块形成。
1.4 统计学处理

2 结 果
2.1 3组患者检测指标比较
除HDL-C水平和左侧颈动脉IMT外,3组患者其余检测指标差异均具有统计学意义(P<0.05;表1)。
2.2 多因素logistic回归分析DR合并DN的相关因素
以DR合并DN为因变量,3组患者有统计学差异的检测指标为自变量,进行多因素logistic回归分析。结果显示年龄、ALB、服用他汀类药物是DR合并DN的保护因素,高血压病程、SBP、FBG、TG、LDL-C、BUN、Cys-C、眼底评分、左室后壁厚度和颈动脉粥样斑块形成为危险因素(表2)。
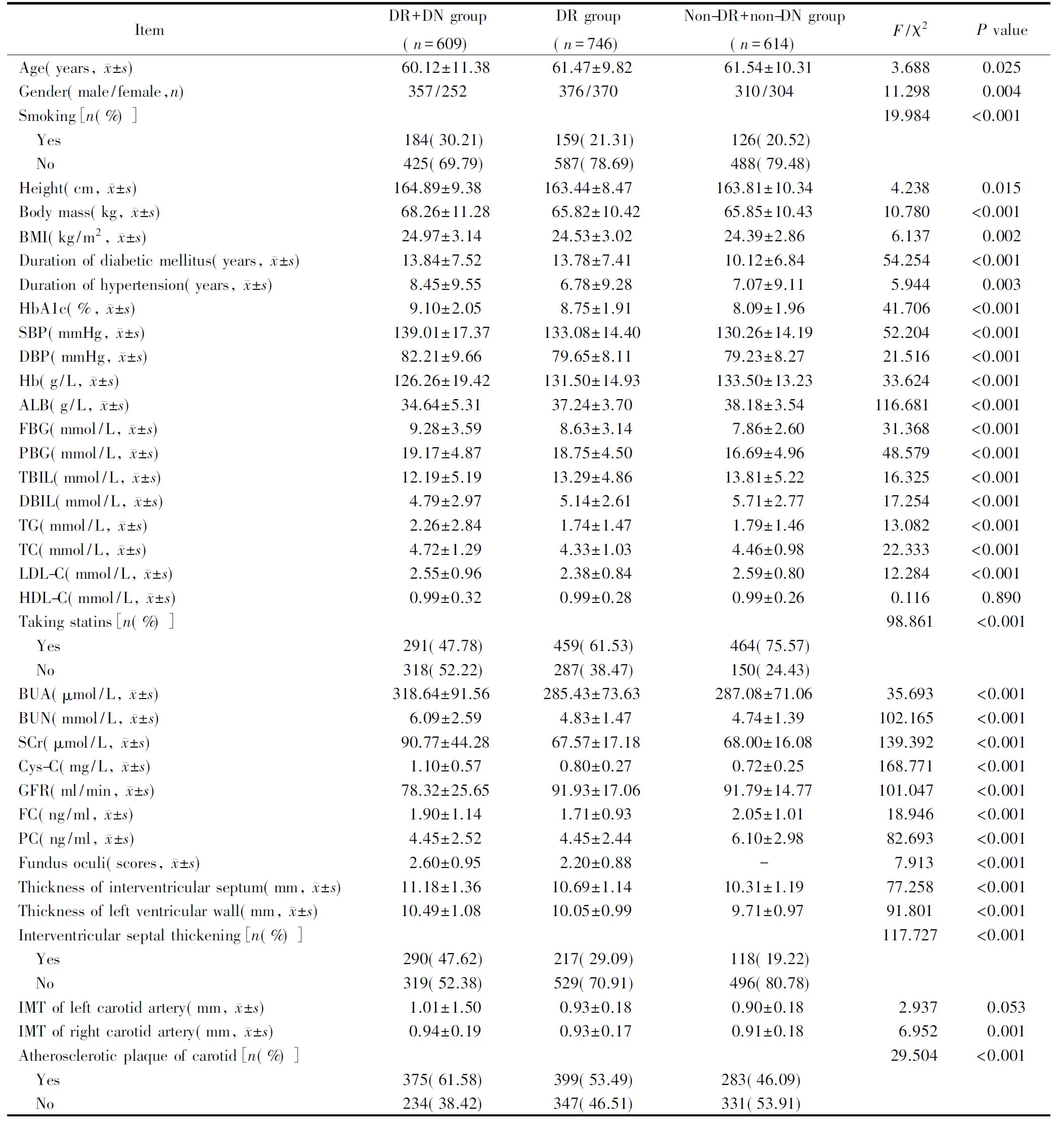
表1 3组患者检测指标比较
DR: diabetic retinopathy; DN: diabetic nephropathy; BMI: body mass index; HbA1c: glycosylated hemoglobin A1c; SBP: systolic blood pressure; DBP: diastolic blood pressure; ALB: albumin; FBG: fasting blood glucose; PBG: postprandial blood glucose; FC: fasting C-peptide; PC: postprandial 2h C-peptide; TG: triglycerides; TC: total cholesterol; HDL-C: high-density lipoprotein cholesterol; LDL-C: low-density lipoprotein cholesterol; TBIL: total bilirubin; DBIL: direct bilirubin; Hb: hemoglobin; HbA1c: glycosylated hemoglobin A1c; BUA:blood uric acid; BUN: blood urea nitrogen; SCr: serum creatinine; Cys C: cystatin C; GFR: glomerular filtration rate; IMT: intima-media thickness. 1 mmHg=0.133 kPa.
2.3 各因素预测DR合并DN的价值
ROC曲线分析结果显示,在应用各相关因素单独预测DR合并DN时,其AUC均较小,Cys C的预测价值最高,AUC为0.677(表3,图1)。
3 讨 论
本研究1 969例T2DM患者中,DR患者1 355例,占68.82%;DR合并DN患者609例,占全部DR患者的44.94%,占全部T2DM患者的30.93%,说明DR合并DN在T2DM患者多见。研究结果表明高血压病程、营养、血糖、血脂、服用他汀类药物、肾功能、眼底病变、心血管病变等指标均与DR合并DN相关。文献报道糖尿病病程、高血压病史、HbA1c、SBP、FBG、BUA与DR合并DN有关,而血脂指标与其相关性较小,体脂肪率和内脏脂肪面积等与其有一定相关性[7],肱三头肌皮褶厚度、Hb、前白蛋白、总蛋白、ALB等营养指标也与DN发生密切相关[8]。还有文献报道,即使接受了相关干预治疗,随着病程延长,T2DM患者DR及DN的病情也仍在进展,SBP、TG、HbA1c是DR的重要危险因素,而年龄、HbA1c、SBP是DN的重要危险因素[9]。结合本研究结果,笔者认为HbA1c、FBG等血糖指标,SBP等血压指标,及ALB,TG等与DR合并DN相关。
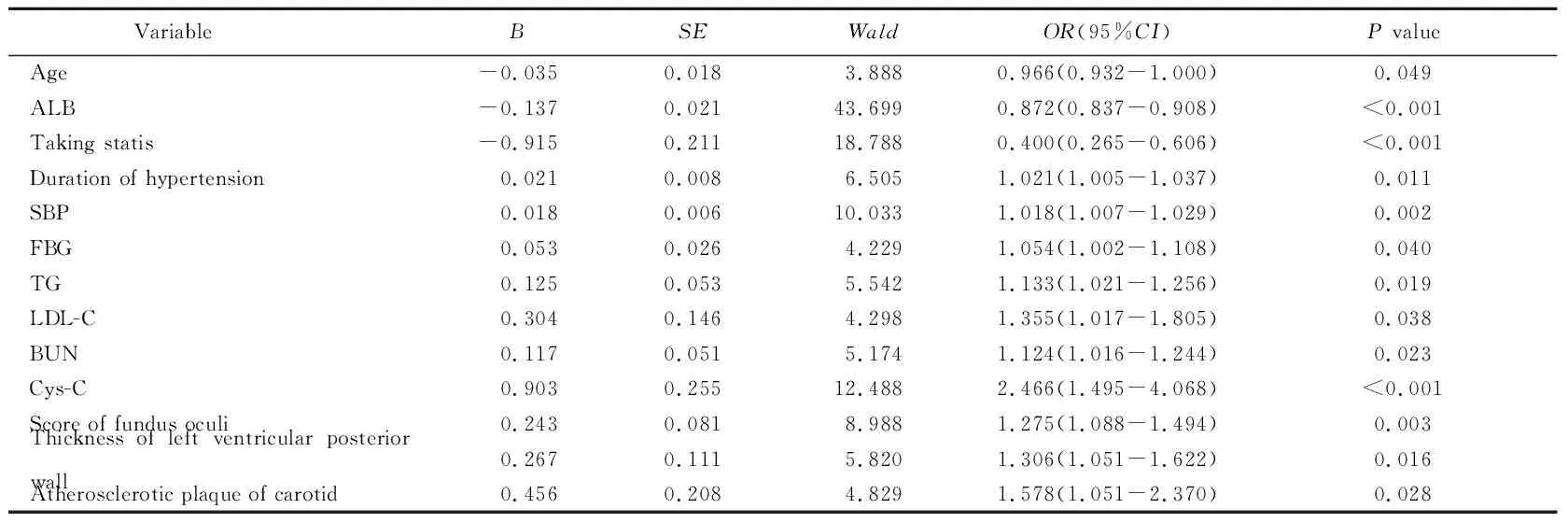
表2 多因素logistic回归分析DR合并DN的危险因素
DR: diabetic retinopathy; DN: diabetic nephropathy; ALB: albumin; SBP: systolic blood pressure; FBG: fasting blood glucose; TG: triglycerides; LDL-C: low-density lipoprotein cholesterol; BUN: blood urea nitrogen; Cys C: cystatin C.
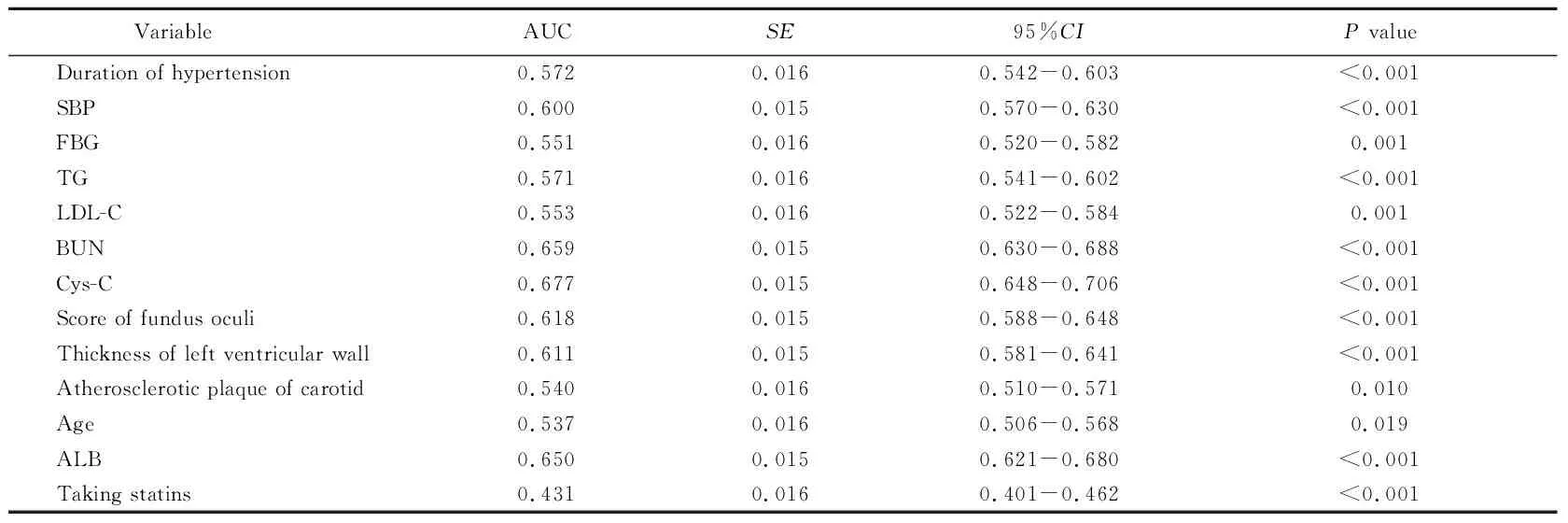
表3 各相关因素预测DR合并DN的价值
DR: diabetic retinopathy; DN: diabetic nephropathy; SBP: systolic blood pressure; FBG: fasting blood glucose; TG: triglycerides; LDL-C: low-density lipoprotein cholesterol; BUN: blood urea nitrogen; Cys C: cystatin C; ALB: albumin.
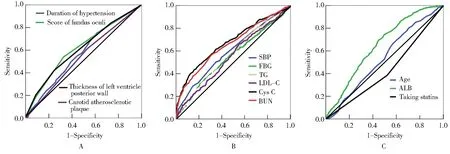
图1 各因素预测DR合并DN的ROC曲线
ROC: receiver operating characteristic; DR: diabetic retinopathy; DN: diabetic nephropathy; SBP: systolic blood pressure; FBG: fasting blood glucose;TG: triglycerides; LDL-C: low-density lipoprotein cholesterol; Cys C: cystatin C; BUN: blood urea nitrogen; ALB: albumin. A and B: risk factors;C: protective factors.
本研究结果还表明眼底病变程度也与DR合并DN相关,说明DR病情也可作为预测DN发病风险的参考依据。部分研究表明随着DR病情由非增殖性视网膜病变向增殖性视网膜病变发展,SCr和BUN水平也会随之升高,SCr、BUN水平与视网膜神经纤维层厚度呈负相关,DR病情进展可预测DN患者肾功能损伤的程度[10,11]。
本研究表明服用他汀类药物为DR合并DN的保护因素,而且OR值达0.4,说明应用他汀类药物可使DR合并DN的风险降低,这反映了有效调节血脂水平对预防糖尿病微血管并发症的发生可能具有显著意义。因此对血脂异常的DR患者一般推荐应用他汀类或贝特类调脂药辅助治疗[12]。本研究还提示左室后壁厚度、粥样斑块形成等心血管病变指标也与DR合并DN相关,可能的原因在于DR、DN等微血管并发症加重了心血管系统的器质性损害,患者通常血糖控制效果差,HbAlc等血糖指标水平较高,而较高的血糖水平是此类患者发生心血管事件的独立因素[13]。
本研究表明各种因素中Cys C预测DR合并DN价值最高。DN患者的主要临床表现是蛋白尿增加和肾功能改变,因此临床诊断DN的主要依据是尿白蛋白排泄率、尿微量白蛋白等尿蛋白指标,但部分DN患者在病程早期尿白蛋白水平正常,依靠尿白蛋白排泄率只能诊断Ⅱ~Ⅲ期DN[14]。近年研究表明,早期DN患者的血清Cys C阳性率和诊断的灵敏度、特异度、准确度均高于BUN、SCr和尿β2微球蛋白等传统肾功能损害指标[15],而且随着DR患者病情加重,血清Cys C水平也逐渐上升,其水平与HbA1c、24h尿白蛋白排泄率均呈正相关,提示Cys C可有助于预测DR患者合并发生DN的风险[16]。本研究结果也表明Cys C预测DR合并DN价值最高,但其AUC未达0.7,仅为0.677。
综上所述,T2DM患者中DR合并DN患病率较高,其发生与多种因素相关,其中,Cys C预测DR合并DN的价值最高。
