LC-MS/MS法测定人血浆中4种非典型抗精神分裂药物及2种代谢物
2019-01-21刘文荣庄绪慧孙合园朱丽萌康毅敏王文艳
刘文荣,庄绪慧,孙合园,朱丽萌,康毅敏,王 帆,王文艳
(1.烟台大学新型制剂与生物技术药物研究山东省高校协同创新中心、分子药理和药物评价教育部重点实验室(烟台大学),山东 烟台 264005;2.内蒙古医科大学精神医学研究室,呼和浩特 010110;3.北京大学北京回龙观医院,北京 100096)
精神分裂症是一种慢性、致残性、终生性的疾病,需要长期维持治疗[1].非典型抗精分裂药物如利培酮(risperidone)、氯氮平(clozapine)、奥氮平(olanzapine)和阿立哌唑(aripiprazole)等是精神分裂症的主要一线治疗药物.精神分裂症的主要治疗策略是抗精神病药物单药治疗(AMP)和抗精神病药物多药治疗(APP,同时联用至少2种抗精神分裂药物).尽管精神分裂症治疗指南推荐采用AMP[1],临床上常采用APP来增加疗效并改善非典型抗精神病药治疗的服药依从性问题[2-3],但是多药联用可能引起临床上的药物-药物相互作用(DDI)[4-5].据报道,利培酮、阿立哌唑、氯氮平和奥氮平可经CYP2D6、CYP3A4或CYP1A2代谢且均为P-糖蛋白的底物[6-8],可能发生竞争性抑制引起临床相关的DDI.
目前,有许多研究报道了同时测定血浆中抗精神分裂药物浓度的液相色谱串联质谱(LC-MS/MS)方法[9-12],这些方法主要应用于常规分析和AMP的治疗药物浓度监测(TDM)研究,很少涉及APP.本研究的目的是建立一种LC-MS/MS方法,用于同时测定接受AMP或APP的治疗稳定期精神分裂患者血浆中的利培酮、氯氮平、奥氮平、阿立哌唑和活性代谢物9-羟基利培酮(9-hydroxyrisperidone)、脱氢阿立哌唑(dehydroaripiprazole)的稳态浓度(cps),并从药代动力学的角度探讨APP潜在的DDI.
1 实验材料
1.1 主要仪器
TSQ Quantum Access型三重四级杆串联质谱仪(美国Thermo公司),配备有ESI离子源和Lcquan数据处理器;Aglient 1100系列高效液相色谱仪(美国安捷伦公司),配有四元输液泵、自动进样器、柱温箱;HSC-24A氮吹仪(天津恒奥科技有限公司);XS-105生物分析天平(瑞士METTLER TOLEDO公司).
1.2 药品与试剂
利培酮(99.9%)和氯氮平(>98%)购自中国药品生物制品检定所(北京);阿立哌唑(99.8%)从永诺制药公司获得(宜昌);脱氢阿立哌唑(≥98%)从呈贡生物制品公司获得(昆明);脱氢阿立哌唑-d8(98.8%)购自多伦多研究化学品公司(多伦多,加拿大);9-羟基利培酮(≥98%)、奥氮平(≥98%)、利培酮-d4(98.6%)、9-羟基利培酮-d4(>99.9%)和奥氮平-d8(99.8%)均购自Sigma公司(美国);色谱纯的甲醇、乙腈、异丙醇购自Merck公司(德国);其余所用试剂为分析纯.
2 实验方法
2.1 色谱质谱条件
色谱条件: 色谱柱为Agilent XDB-C18柱(150×2.1 mm,3.5 μm);流速:0.3 mL/min;柱温箱:30 ℃;进样体积:5 μL;流动相:A相:乙腈(含0.01%冰乙酸),B相:水(含0.01%冰乙酸).采用梯度洗脱的方式,梯度洗脱条件(流动相A线性增加)如下:0~1.5 min,20%~90%A;1.5~2.0 min,90% A;2.0~2.1 min,90%~20% A;2.1~6.5%,20% A.
质谱条件: 电喷雾离子化电离源(ESI),喷雾电压为4 000 V;毛细管温度为350 ℃;鞘气和辅助气压力分别为30和5 psi;碰撞气压力为1.5 minni-Torr.每种分析物的选择性反应监测参数和保留时间见表1.

表1 6种分析物和4种同位素内标的LC-MS/MS参数Tab.1 The optimized LC-MS/MS parameters of six analytes and four isotope Internal standard
2.2 储备液和标准工作液的制备
储备液的配制:分别精密称取利培酮、9-羟基利培酮、阿立哌唑、脱氢阿立哌唑、氯氮平、奥氮平约5 mg,用甲醇稀释至10 mg/mL,作为储备液.利培酮-d4、9-羟基利培酮-d4、奥氮平-d8、脱氢阿立哌唑-d8为100 μg/mL的甲醇溶液.取每种分析物的储备液适量,混合,用甲醇连续稀释以制备所需浓度的标准工作液和质控工作液.同法制备混合的内标工作液.所有储备液和工作溶液均置于4 ℃冰箱中备用.
2.3 血浆样品处理
精密移取25 μL血浆样品置于干净的10 mL玻璃管中,加内标工作液5 μL和0.1 mol/L氢氧化钠溶液25 μL,涡旋30 s,加3 mL混合提取液(正己烷∶二氯甲烷∶异丙醇=2/1/0.1,v/v/v),涡旋震荡3 min,混合物以2 000×g离心10 min,将有机相转移至干净的玻璃管中并于35 ℃空气流吹干,加入200 μL流动相A∶B(50∶50,v/v)复溶并在16 200×g下离心10 min,取5 μL进样分析.
2.4 方法学验证
根据《中国药典》(2015版)生物样品定量分析方法验证的指导原则进行了方法学验证,验证的内容主要包括专属性、残留效应、线性范围、精密度准确度、基质效应、稳定性和稀释可靠性[18].
2.5 样品来源
共收集到46位患者的血浆样品,28人接受AMP,18人接受APP(利培酮与阿立哌唑、利培酮与氯氮平、氯氮平与奥氮平联用各6人).所有患者均服用抗精神分裂药至少1个月且无酗酒、吸毒或重大器质性疾病.稳态下的血液样品收集时间为早上8点(除阿立哌唑组取血时间是服药后24 h外,其余用药组均为服药后12 h).离心分离血浆并保存于-20 ℃待测.本研究经内蒙古第三医院伦理委员会批准,参加本次研究的患者在入组前本人或其家属均已签署知情同意书.
2.6 数据分析
C/D ratio的结果用Mean±SD进行描述性统计分析.采用独立样本t检验(SPSS 17.0)比较AMP和APP的C/D ratio的差异.P<0.05即认为有统计学意义.
3 结果与讨论
3.1 方法开发
在该方法中,使用25 μL血浆进行分析,能达到文献报道200 μL血浆体系的相似的灵敏度[13].采用液-液萃取(LLE)方法,用混合溶剂正己烷-二氯甲烷-异丙醇(2/1/0.1)纯化样品,该方法比文献报道的固相萃取经济快速[14],且提取回收率约90%.此外,同位素内标具有与分析物相似的电离和提取效率,确保了测定结果的准确可靠.
3.2 方法学验证
3.2.1 专属性 通过分析来自6个不同供体的空白血浆来考察方法的专属性.结果表明,在测定条件下,血浆中内源性物质不干扰分析物的测定,所有分析物和内标均无相互干扰,代表性色谱图如图1所示.

1—10分别为奥氮平-d8、奥氮平、9-羟基利培酮-d4、9-羟基利培酮、利培酮-d4、利培酮、氯氮平、脱氢阿立哌唑-d8、脱氢阿立哌唑、阿立哌唑
3.2.2 线性范围、定量下限和残留效应 将5 μL系列标准溶液加至25 μL空白血浆中制备相当于血药浓度氯氮平、奥氮平、阿立哌唑和脱氢阿立哌唑为4、10、20、40、100、200、400、1 000 ng/mL;利培酮和9-羟基利培酮为0.4、1、2、4、10、20、40、100 ng/mL的标准曲线,同时,制备一个空白样品和一个零浓度样品(含内标).在标准曲线最高浓度样品进样后分析空白样品来考察残留效应.结果表明所有标准曲线线性关系良好,相关系数大于0.995 8.此外,在最高浓度样品进样后,空白样品中所有分析物和内标的保留时间处无明显色谱峰,表明无残留.制备定量下限样品每分析6批样本,连续3个分析批考察定量下限,结果如表2所示,每个分析物定量下限的批内批间精密度(用CV表示)均小于12.0%,准确度(用RE表示)在±13.4%以内.
3.2.3 精密度和准确度 配制氯氮平、奥氮平、阿立哌唑、脱氢阿立哌唑低(10 ng/mL)、中(100 ng/mL)、高(800 ng/mL),利培酮和9-羟基利培酮低(1 ng/mL)、中(10 ng/mL)、高(80 ng/mL)浓度质控样品,按照2.3项下方法处理,每浓度点6平行,连续3个分析批进行批内批间的精确度和准确度.结果如表2所示,6种分析物的CV值小于13.8%,RE值在±12.5%之内.该方法精密度和准确度符合要求.
3.2.4 基质效应 基质效应的考察通过将内标和低或高浓度标准工作液加入到6个不同来源的经预处理的空白血浆中,配制成相当于低、高质控浓度的样品,并制备相应浓度的不含基质的标准工作溶液,比较含基质样品中每种分析物和内标的峰面积比与相应工作溶液中的峰面积比.基质效应的结果表明,6种分析物经内标归一化的平均基质效应在低浓度下为94.0%~112.4%,在高浓度下为83.9%~91.9%,并且各浓度下的CV值均低于13.7%,无明显基质效应.

表2 LC-MS/MS法测定人血浆中六种分析物方法的精密度和准确度Tab.2 Precision and accuracy of LC-MS/MS method for determination of six analyzes
3.2.5 稳定性和稀释可靠性 配制低、高浓度质控,分别考察室温放置2 h、自动进样器放置6 h、3次冻融循环和-20 ℃放置6个月的稳定性,每种条件下每浓度3样本平行.此外,制备高于定量上限2倍的血浆样品并在预处理时用空白血浆稀释2.5倍来考察稀释可靠性.各分析物在不同放置条件下稳定性考察的结果见表3,所有分析物在上述条件下RE%在-5.9%至11.6%之间,CV均低于12.5%.表明,所有分析物在上述条件下稳定.稀释2.5倍后每种分析物的RE在±7.5%内且CV小于12.4%,表明稀释稳定性良好.
3.3 临床样品分析

表3 不同条件下6种分析物在人血浆中的稳定性(Mean±SD) (n=3)Tab.3 Stability of six analytes in human plasma under different conditions (Mean±SD) (n=3)
该方法已成功应用于采用AMP或APP的治疗稳定期精神分裂症患者血浆样品分析.6.5%(3/46)患者的Cps超过TDM指南制定的实验室警戒水平[15].WANG等报道中国患者氨磺必利的Cps明显高于警戒水平[12].因此,有必要开展中国抗精神病药物的TDM研究,制定相应的TDM指南.
C/D ratio广泛用于直接比较受试者内部和受试者之间的差异,而不考虑服药剂量的变化,故本实验采用C/D ratio比较AMP和APP之间的差异[16].因利培酮主要经CYP2D6和CYP3A4代谢为9-羟基利培酮,该代谢物具有与母体化合物相似的药理活性[17],故分别比较了利培酮、9-羟基利培酮和总活性物质(利培酮与9-羟基利培酮之和)的C/D ratio.利培酮AMP组(n=14)利培酮、9-羟基利培酮、总活性物质的C/D ratio分别为1.34±1.20、13.17±6.52、17.17±9.84 ng/(mL·mg-1),APP组(n=12)分别为1.92±1.37、6.69±3.14、8.62±4.33 ng/(mL·mg-1),9-羟基利培酮和总活性物质的C/D ratio显著低于AMP(P分别为0.006和0.014)而利培酮无显著性差异(P=0.284),结果见图2.无论利培酮与氯氮平还是与阿立哌唑联用,对利培酮、9-羟基利培酮和总活性物质C/D ratio的影响趋势相同.这可能是因为CYP2D6和CYP3A4是利培酮、阿立哌唑和氯氮平共同的代谢酶,氯氮平和阿立哌唑竞争抑制利培酮的代谢,体外实验也有报道氯氮平对CYP2D6有抑制作用[18].此外,利培酮的消除半衰期(约3 h)远低于其代谢物9-羟基利培酮(约24 h)[19].对于氯氮平组,AMP组(n=14)C/D ratio为2.77±1.04 ng/(mL·mg-1),APP组(n=12)为2.81±1.92 ng/(mL·mg-1),无统计学差异,结果如图2所示,表明APP治疗方式对氯氮平无影响.
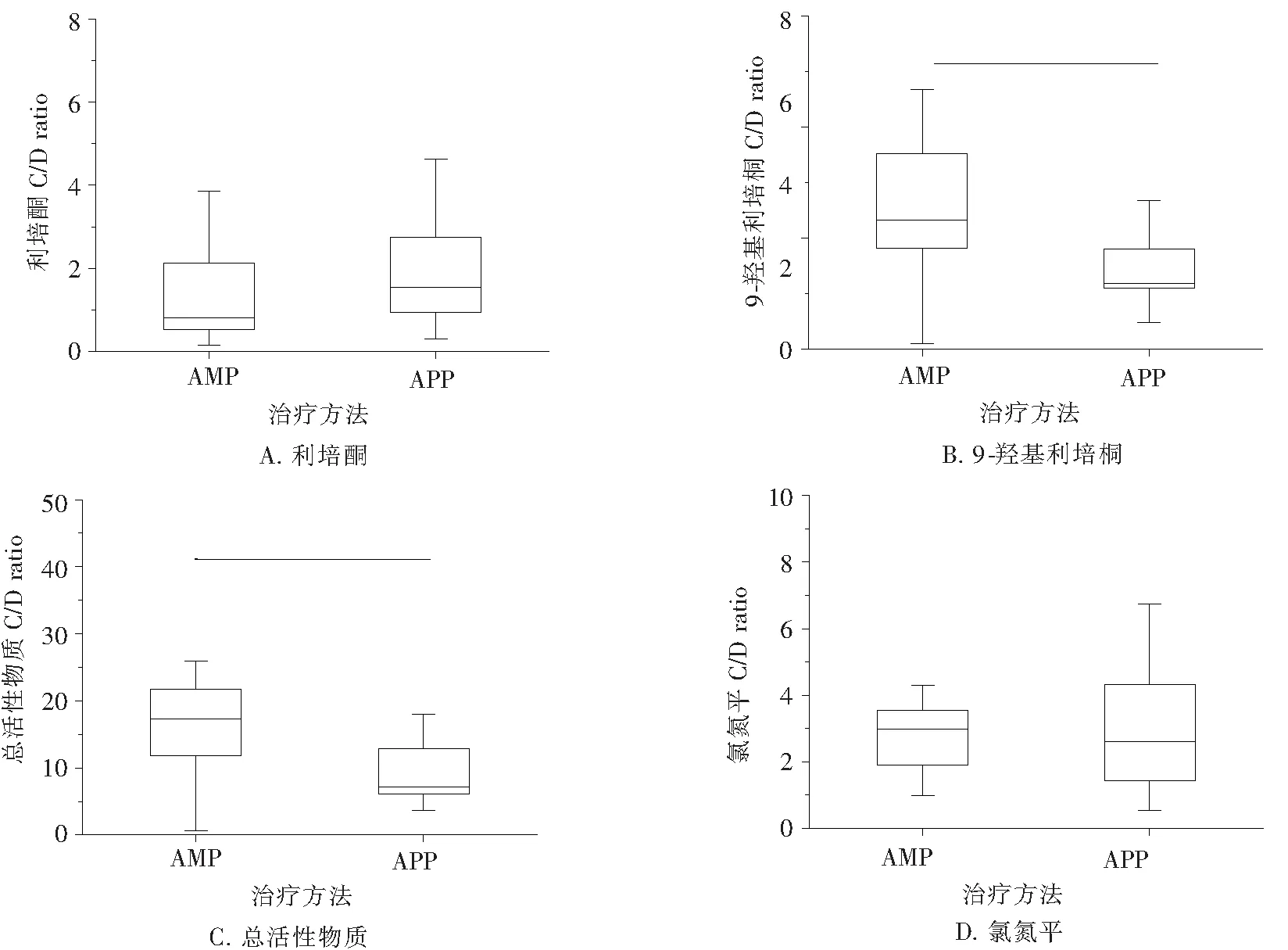
图2 AMP和APP组C/D ratio箱式图比较Fig.2 The box figure of C/D ratio in AMP and APP medations
4 结 论
本实验建立了快速、灵敏、可靠的LC-MS/MS方法用于同时测定精神分裂患者血浆中4种抗精神分裂药物和2种代谢物浓度,并进行了方法学验证.结果表明,当利培酮与氯氮平或阿立哌唑合并用药时可能发生DDI.有必要进一步研究阿立哌唑,利培酮和氯氮平体内和体外的竞争性抑制,并探讨APP的可行性.
