美国血管外科学会2018年腹主动脉瘤诊治指南解读
2019-01-09王磊潘柏宏杨璞王伟黄建华
王磊,潘柏宏,杨璞,王伟,黄建华
(中南大学湘雅医院 血管外科,湖南 长沙410008)
腹主动脉瘤(abdominal aortic aneurysm,AAA)是指腹主动脉呈瘤样扩张,且直径增大超过50%以上。针对AAA患者的诊治,特别是治疗和管理抉择较为复杂。为此,美国血管外科学会(Society for Vascular Surgery,SVS)在系统性回顾的基础上,于2018年1月发布了AAA治疗指南[1],针对AAA的诊断评估、治疗方式、麻醉及围术期处理、术后管理及随访、经济效益学分析5个方面做了重点阐述,并给出111条具体的推荐建议,并按GRADE法给出了推荐强度及证据级别。为方便读者更好的理解该指南,本文对该指南中涉及的新的观点或推荐意见、以及与临床诊疗过程中的密切相关点作一解读。
1 关于AAA的筛查方式及筛查对象
指南肯定了多普勒超声在AAA患者筛查中的地位。多普勒超声作为一种简便和无损的检查方式,同时具有精准性,重复性和有效性的优点,是AAA筛查及术后随访复查的首选方法。超声的灵敏度和特异度均接近100%,只有1%~3%的患者其动脉瘤因肠道气体或者肥胖因素干扰而漏诊[2-3]。关于AAA的筛查对象,鉴于AAA好发于伴有吸烟史的老年男性,女性发病率并不高;同时USPSTF(美国预防服务工作组)在2014年推荐超声筛查对象为年龄在65~75岁伴或不伴有吸烟史的男性,而对于65~75岁的女性,其推荐证据不足[4]。因而,传统观点认为AAA的筛查对象不应该涵盖女性。但是,新指南指出,女性也应纳入超声筛查对象(推荐等级:1;证据质量:A)。这是基于研究发现相较于男性,女性患者虽然其发病率更低,但动脉瘤破裂的比例较男性明显偏高,所以对于女性患者,常规超声筛查在实际临床工作中尤为重要[5]。
2 对于收治AAA患者医疗中心资质的要求
指南推荐,对于收治AAA患者的医院或者医学中心,每年至少应该实施10例以上的AAA手术,且围术期病死率及EVAR中转开腹率不应超过2%。笔者认为,手术应当由专业的血管外科医师团队完成,同时配备杂交手术室以应对各种术中存在的问题以及是否需要及时中转开腹。研究[6-7]表明,医疗中心每年行8~10例以上EVAR是保证其围术期生存率的起码要求。医疗中心每年施行的手术数量与围术期病死率直接相关,当每年施行的手术数量达到30例以上时,其围术期生存率才较为满意。
3 动脉瘤破裂患者治疗时间窗
AAA破裂是一种极其凶险的外科急腹症,病死率高达80%。如何系统规范的处理AAA破裂或者先兆破裂的患者,一直是血管外科医师讨论的重点。指南指出,对于AAA破裂的患者,从出现破裂到干预治疗的时间不应超过90 min,基于此,推荐了一个“30-30-30 min”的时间框架。第1个30 min指与AAA破裂患者或者怀疑破裂的患者第1次医学接触的时间,在这个时间段内,需要对患者做出初步诊断。其中年龄>50岁伴既往动脉瘤病史或有高血压病史的患者出现腹痛或背痛时,需要高度警惕。如果时间允许,可行急诊CT或超声进行初步诊断。第2个30 min指迅速转移到区域中心所需要的时间。这个区域中心是指能够熟练的处理及治疗AAA的医疗机构。第3个30 min指血管外科医生团队评估手术方式所需时间,包括手术入路以及球囊放至位置等。指南特别强调,对于破裂的AAA患者其术前花费时间直接影响结果。通过有组织的区域转移系统,95%的AAA破裂患者能够手术修复,67%能够存活[8]。笔者认为,“30-30-30 min”框架的提出,对于AAA破裂的规范化系统化处理和诊治,起着极大的推进作用,应当全面推广(图1)。
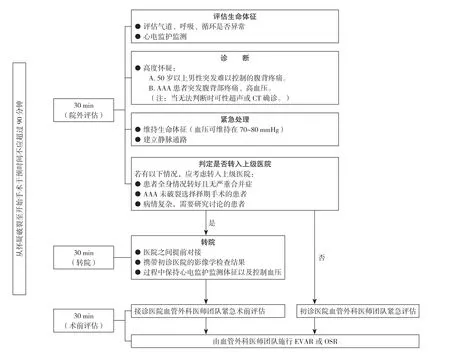
图1 怀疑破裂AAA急诊处理流程Figure 1 Emergency treatment process for suspected AAA rupture
4 AAA患者术前心脏评估
AAA好发于长期吸烟的老年男性,通常伴有COPD或者冠心病。研究[9]发现,AAA术后患者的5年生存率不到70%,心肺相关并发症是导致OSR或EVAR术后早期和晚期病死率的首要原因。所以对于AAA患者,不管是行EVAR或者OSR,术前常规心脏评估都至关重要。 整个心脏评估分为3步。第1步,首先判定是否有现存的活动期心脏疾病存在,包括不稳定冠脉综合征,不稳定或者严重心绞痛,近1个月内心梗发作史,失代偿性充血性心力衰竭,严重的心律失常,严重瓣膜疾病。如果存在上述疾病,应当取消或者延迟手术,直到心脏疾病稳定。第2步,如果没有上述疾病,应当测其主观功能量(表1)来判定是否需要改变治疗计划。第3步,如果患者代谢当量(MET)<4,应当行非侵袭性压力试验。其结果对于心血管疾病并发症具有预见性,通过试验结果,来调整治疗计划,可降低动脉瘤术后早期或晚期病死率。同时,所有接受EVAR或OSR手术的患者在围术期间应做12导联心电图,并且术后行ST段监测以早期发现或诊断围术期心梗。12导联心电图对于预见围术期心梗的发生有独特的优势。在心梗超急性期,急性冠脉血流中断后,最早出现的心肌缺血性改变(T波改变),继而出现心肌损伤性改变(ST段改变),通过12导联心电图能够敏感的抓住这一变化,如果能够识别心肌缺血阶段(T波改变)并且早期干预,可避免其向急性期演变。(推荐等级:1;证据质量:B)。需要注意的是,除非是患者出现了胸痛,或者心电图出现改变怀疑急性心梗,否则不必常规检测肌钙蛋白。因为肌钙蛋白确诊心肌梗死具有延迟性,且研究[10]发现,常规测量肌钙蛋白并没有改善其临床结果(推荐等级:1;证据质量:A)。

表1 AAA患者术前心脏评估表Table 1 Preoperative heart assessment for AAA patients
5 他汀类药物和β受体阻滞剂在AAA中的应用
曾经有小范围实验和临床应用表明了普萘洛尔对AAA有影响,部分学者认为β受体阻滞剂可用于制止患者主动脉根部的扩张。然而最近的临床试验[11]证明,普萘洛尔的血流动力学对于动脉瘤的进程并无影响。由于β受体阻滞剂在全身系统中的副作用,不建议AAA患者常规使用β受体阻滞剂,但若伴有心血管疾病,应当加用β受体阻滞剂以改善心脏情况。
指南推荐围术期常规使用他汀类药物。其原因并非他汀类药物对于限制AAA患者的瘤体增长有一定的作用,而是因为他汀类药物可通过稳定斑块,改善稳定心血管疾病,带来明显益处,且其副作用相对较小[12]。
6 术中副肾动脉的保留与否
术中决策是否保留副肾动脉,应当充分考虑动脉瘤直径、副肾动脉血供,以及现存的肾脏疾病等相关因素。副肾动脉隔绝后导致的肾梗死很常见,可高达84%的发生率[13]。急性肾梗死常表现为氮质血症、水电解质和酸碱失衡以及全身各系统症状,可伴有少尿(<400 mL/24 h或17 mL/h)或无尿(<100 mL/24 h)。虽然大部分患者可耐受,对远期效果无显著影响,但是指南仍然推荐:若副肾动脉直径≥3 mm,或供应了超过1/3肾组织,则行EVAR或者OSR的时候应保留副肾动脉,尤其对于已经存在肾功能不全的患者而言更应如此(推荐等级:2;证据质量:C)。此外,指南推荐术前对肾功能不全的非透析依赖患者用盐水或者碳酸氢钠水化,也可以减少急性肾损伤发生率。
7 血栓的预防
AAA术后血栓的预防,一直是血管外科医师的重中之重。目前公认:对于所有行OSR或者EVAR的患者术后应常规行间歇性气压治疗,以及鼓励早期下床活动等血栓预防措施。(推荐等级:1;证据质量:A)。至于肝素或低分子肝素的运用,目前尚无统一明确的答案,对于接受OSR的患者使用肝素或低分子肝素还缺乏安全性有效性的证据。指南指出,对于ORS术后充分评估后为中危或高危血栓风险同时为低危出血风险的患者,可谨慎使用低分子肝素。笔者结合实际临床,推荐对于接受EVAR的患者,当没有肝素抗凝绝对禁忌证时,在EVAR术后应当使用普通肝素或者低分子肝素以预防支架内血栓或深静脉血栓形成。用药应从小剂量开始,个体化用药。大多数接受动脉瘤修复术的患者静脉血栓风险为中危或者高危,同时相对于OSR,EVAR对机体创伤小,其腹膜后血肿等出血并发症发生率小,使用肝素抗凝可获得较高收益。最近的研究[14]表明,肝素个体化用药并且定期监测其抗凝作用,可明显降低动脉手术术后血栓并发症的风险。
8 移植物感染的诊断与预防
移植物感染是血管移植术后少见并发症,目前报道其发生率约为1~6%。虽然术后移植物感染发生率不高,但其危害极大,可导致器官功能丧失、截肢、甚至危及生命。移植物感染的诊断一般通过临床表现与实验室诊断,如果患者术后出现不明原因疼痛,脓毒症,腹股沟渗液,假性动脉瘤形成,同时实验室检查结果为非特异性的炎症表现:白细胞计数升高、血沉增快、C-反应蛋白(CRP)升高等,应当重点怀疑移植物感染。(推荐等级:1;证据质量:A)。研究[15]发现,在动脉重建手术中,术前预防性用抗生素可有效降低伤口感染及早期移植物感染的风险。一般推荐静脉注射第一代头孢,如果患者对青霉素过敏时,可术前30 min用万古霉素。需要注意的是,预防性抗生素应用不应超过24 h。同时,伴有糖尿病与营养不良的患者,术前应当积极控制血糖与营养支持等对症治疗。
9 内漏的处理
内漏为AAA行EVAR常见的术后并发症,其发生率约为20%~47%,可分为四型 。研究[16-17]表明,I型内瘘会逐渐进展,其囊腔压力会逐渐增高,破裂风险也逐渐增大,所以指南推荐:对于I型内瘘,应当积极进行干预(推荐等级:1;证据质量:B)。对于II型内瘘,50%的II型内瘘会逐渐自愈,不需要干预且II型内瘘结局不唯一,25%患者囊腔逐渐减少,50%~70%患者囊腔保持稳定,25%患者其囊腔直径增大。所以指南推荐:仅当其瘤体逐渐增大时,需要主动进行干预,而对于无扩张的患者,定期监测即可。III型内瘘多为置入移植物时,因输送器械误伤支架或织物所致,对于所有的III型内瘘,都应积极干预,方式首选腔内治疗(推荐等级:1;证据质量:B)。对于IV型内瘘,可不必积极干预,定期观察监测即可,因为IV型内瘘织物上的裂孔可由于血液凝块堵住小孔后自行消失,患者可自愈,但若裂孔较大时,应当主动干预。需要特别注意的是,对于I型内瘘或者瘤体进行性增大的III型内瘘型腔内干预失败时,需及时转开放手术治疗(推荐等级:1;证据质量:B)。
此次SVS在2018版的指南中,针对AAA的诊断评估、治疗方式、麻醉及围术期处理、术后管理及随访、经济效益学分析等五个方面做了重点阐述,并针对性的给出了推荐意见,其目的是为了规范AAA患者的诊治,提高AAA患者的疗效。同时,我们也应当认识到,指南仅仅提供了原则性的、规范化的指导意。但在临床工作中,充分考虑患者的个体情况,选择有针对性的治疗抉择亦是极为必要的。
