初始温度对丙酮爆炸下限的影响
2018-12-18高志崇
高志崇
(泰山学院 化学化工学院,山东 泰安 271000)
可燃气体与空气或氧气混合时并不是在任何浓度范围内均可以发生爆炸,而必须是在一定的浓度范围内才能够发生爆炸。其中,能够发生爆炸的最低浓度为爆炸下限,能够发生爆炸的最高浓度为爆炸上限。不同的可燃气体有不同的爆炸极限,即使是同一种可燃气体在不同的情况下也有不同的爆炸极限,也就是说,多种因素会影响爆炸极限。其中,初始温度是影响爆炸极限的重要因素。在之前的研究中曾计算了不同初始温度下甲烷爆炸后体系的温度与压力,从计算结果可以看出,不同初始温度下甲烷爆炸后体系的温度是很接近的[1]。下面讨论丙酮在不同初始温度、爆炸下限时爆炸后的温度与压力,以期对该问题有进一步的认识。
1 恒容热效应ΔU与光子的波长、数量之间的关系
光是一种非体积功。假设某爆炸反应发出n mol波长为λ的光子,那么,爆炸反应的内能的变化与光子的量及波长之间的关系为[1-5]:

下面利用该公式讨论不同温度下丙酮爆炸反应的极限。
2 丙酮燃烧反应机理
根据丙酮燃烧反应的温度,提出了丙酮在空气中燃烧反应的机理[6]。丙酮在空气中不完全燃烧,形成黑烟,在空气中燃烧反应的机理为:

丙酮在空气中不完全燃烧的反应式为:
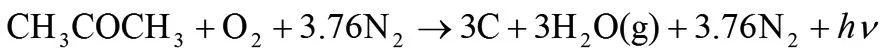
由反应式可以看出,1mol丙酮在空气中不完全燃烧发出1mol光子。
3 不同温度下丙酮在爆炸极限时爆炸产生的温度与压力
3.1 丙酮在0℃爆炸下限时爆炸产生的温度与压力

表1 不同初始温度下丙酮爆炸的极限[7]及爆炸后温度与压力的计算值
0℃ 丙酮爆炸下限为4.2%。取丙酮的量为1mol,则反应前总的气体的量为n1=mol=23.81mol,空气的量为22.81mol。按21%O2计算,则nO2=4.79mol,nN2=18.02mol。因而,丙酮在0℃ 爆炸下限时的反应式为:CH3COCH3(g ) +4.79O2+18.02N2=3C(s)+3H2O(g)+3.79O2+18.02N2+hv.反应后气体物质的量为n2=24.81mol,反应前后气体物质的量的差值△n(g)=1mol。为方便计算起见,现将某些物质的热力学性质列于表2。

表2 298.15K、101.325kPa下某些物质的热力学性质[8]
为计算丙酮爆炸反应的温度与压力,设计途径见图1。假设本文中所有其他均为理想气体.对于理想气体和纯固体而言,内能和焓仅仅是温度的单值函数,因而,
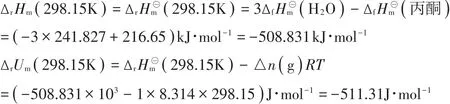
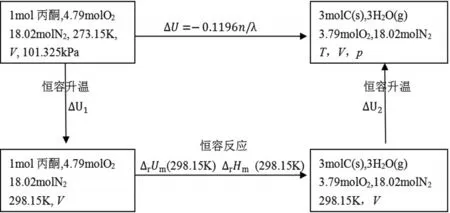
图1 丙酮在0℃、爆炸下限时设计途径

∆U与温度T之间的关系式为:

丙酮在空气中爆炸反应的火焰为红色,红色的波长为650-750nm,取λ=750nm进行计算。根据(1)式,则有:
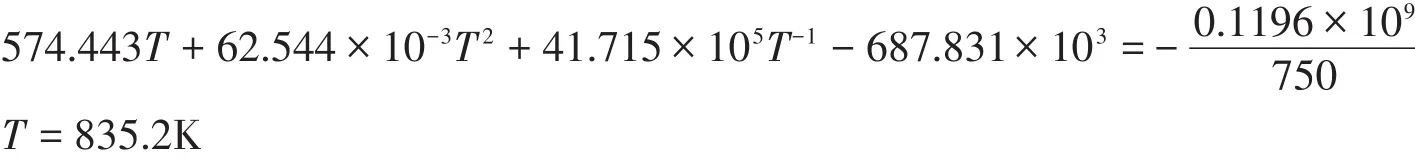
爆炸反应在恒容的条件下进行,因而,爆炸后的压力为:
即丙酮在0℃、爆炸下限时的爆炸温度为835.2K,爆炸时产生的压力为322.83kPa。
3.2 其他温度下丙酮在爆炸极限时爆炸产生的温度与压力
利用相同方法计算丙酮在50℃、100℃爆炸下限时∆U与温度T之间的关系式,进而计算了爆炸后形成的温度与压力。取丙酮的量为1mol,不同温度下丙酮爆炸时∆U与温度T之间的关系式见表3,爆炸后形成的温度与压力见表1。

表3 1mol丙酮不同初始温度、爆炸下限时∆U与温度T之间的关系式
