临床病理讨论:乳腺侵袭性纤维瘤病
2018-12-13王懋莉吴克瑾张明迪孙艺华马凤华王雪梅陈宏亮
王懋莉 吴克瑾 丁 昂 张明迪 孙艺华 马凤华 王雪梅 陈宏亮
(1复旦大学附属妇产科医院乳腺外科,2病理科,3放射科,4超声室 上海 200011)
病史摘要
入院病史 患者,女性,33岁,因“发现右乳肿块1年半,增大4月余”于2017年9月就诊于复旦大学附属妇产科医院乳腺外科。患者诉1年半前曾因右乳内下肿块于外院行右乳肿块切除术,术后病理提示右乳纤维腺瘤。术后1个月于原手术瘢痕下方再次出现肿块,直径约1.5 cm,未予治疗,随访,期间肿块无变化。4个月前患者自觉肿块逐渐增大,要求进一步诊治。起病以来,患者精神睡眠可,二便无殊,体重无明显改变。
家族史 无家族性腺瘤性息肉病,无乳腺癌、卵巢癌等家族史。
体格检查 右乳肿块位于原手术瘢痕下方,近右乳内下乳腺边缘处,大小约3.5 cm×1.5 cm,梭形,质地韧至硬,边界尚清,活动度尚可,无皮肤及胸肌粘连。双侧乳头无溢液,左乳未扪及肿块,双腋下未扪及肿大淋巴结。
辅助检查 乳腺彩超:右乳4~5点处腺体层内探及低回声区,大小8 mm×11 mm×10 mm,边界欠清晰,形态不规则,彩色血流不明显。提示右乳内下象限混合结构。乳腺MRI:右乳内下象限可见条片状异常信号灶,T1WI呈低信号,T2WI脂肪抑制呈高信号,DWI呈略高信号,ADC值无明显降低,局部皮肤增厚,范围约1.4 cm×3.2 cm (图1),动态增强曲线呈逐步上升型(图2)。双侧乳后间隙未见异常信号影。双侧腋下未见明显肿大淋巴结影。MRI提示右乳内下象限条片状明显强化灶,局部皮肤增厚,BI-RADS 4A。

图1 MRI提示右乳内下象限条片状明显强化灶Fig 1 The obvious enhancement in the inner and lower quadrant of the right breast hinted by MRI
入院诊断 右乳肿块,分叶状肿瘤不除外。
手术治疗 患者拒绝行右乳肿块空芯针穿刺活检,于局麻下行右乳肿块切除活检。术中见肿块与胸壁胸大肌似有粘连,切除粘连部分胸大肌肌肉。腹直肌肌肉及腱膜无受累。冰冻病理提示(右乳肿块)镜下见梭形细胞增生。
病理报告 (右侧乳腺肿块)灰白脂黄色组织1块,大小4 cm×3.8 cm×3 cm,肿块切面灰白色,脂黄色相间,质韧稍硬,界不清。病理诊断(右侧乳腺肿块)乳腺侵袭性纤维瘤病,累及横纹肌组织,切缘见病变累及(图3)。免疫组化结果:AE1/AE3(-),Desmin(局灶+),SMA(+),S-100(-),P63(-),β-Catenin(+),Ki-67(2%+),CD34(-)(图4)。
临床与病理讨论
王懋莉主治医师(乳腺外科) 侵袭性纤维瘤病,又称韧带样肿瘤,是一种成纤维细胞单克隆增殖性疾病[1],属良性病变,生长缓慢,局部侵犯,易复发,但无远处转移风险。既往文献报道,侵袭性纤维瘤病复发率约25%~60%[2]。发病年龄、部位、肿瘤大小以及切缘状态与预后相关[3],原发病变预后优于复发病变[4]。一项包括22个研究的Meta分析显示[5],侵袭性纤维瘤病单纯接受手术治疗,切缘阴性、阳性组的局控率分别为72%、41%,总生存率为61%;接受手术联合放疗治疗,切缘阴性、阳性组的局控率分别为94%、75%,总生存率为75%。局部复发及邻近器官受累是该病发病和死亡的主要原因[6]。该病发病率每年为2~4 例/百万人[7],84%~93%[8-9]为散发型,10%~20%与家族性腺瘤性息肉病相关。侵袭性纤维瘤病病因未明,30%病例既往有创伤史[10],与高雌激素状态可能有关[11],20~35岁[12]的年轻女性好发。常见发病部位为前腹壁,腹外部位少见,可累及胸壁、肩部、盆腔、大腿部位肌肉[13]。乳腺侵袭性纤维瘤病罕见,约占乳腺肿瘤的0.2%[14],主要临床表现为孤立性、无痛、异常质硬乳腺肿块。该患者为年轻女性,发病部位曾有乳房肿块手术史,初步诊断右乳肿块术后局部复发。结合辅助检查进行鉴别诊断,应考虑乳腺侵袭性纤维瘤病可能,同时要排除乳腺癌可能。
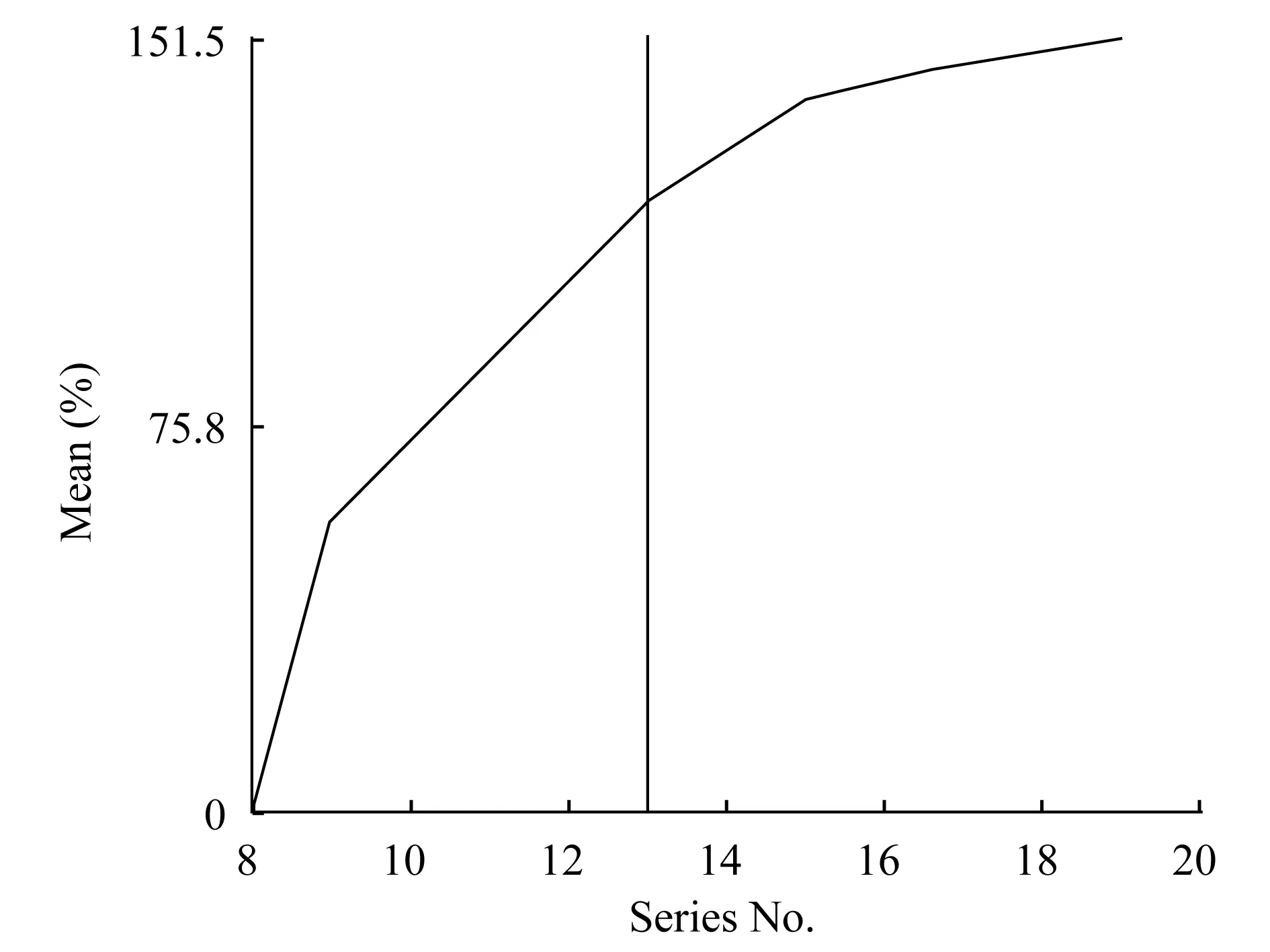
图2 MRI逐步上升型动态增强曲线Fig 2 The gradually rising dynamic enhancement curve of MRI

图3 乳腺侵袭性纤维瘤病,累及横纹肌组织病理Fig 3 Aggressive fibromatosis of the breast involved striated muscle in this case diagnosed by pathology

图4免疫组化提示β-Catenin(+)
Fig4Immunohistochemicalstainingsuggestedβ-Catenin(+)
王雪梅副主任医师(超声室) 乳腺侵袭性纤维瘤病超声表现为边界不清、形态不规则、呈分叶状的低回声肿物,胸肌和肋间肌可受累。乳腺癌相关的超声表现如后方声影、高回声晕和微钙化等少见。乳腺侵袭性纤维瘤病常呈横向生长,可与乳腺癌鉴别。超声弹性成像的5分法和应变比常提示为恶性病变。
马凤华主治医师(放射科) 乳腺侵袭性纤维瘤病钼靶检查缺乏特异性,常提示为BI-RADS 4或5类。增强CT检查侵袭性纤维瘤病密度类似于肌肉,无法与其他软组织来源肿瘤进行区分。MRI能够评估肿瘤范围以及和周围神经血管的关系,是评估病变对胸壁浸润程度的最佳检查方法,有助于病灶的完全切除。但MRI无法判断肿瘤切缘的性质。PET扫描对本病的诊断价值尚待研究[15]。乳腺侵袭性纤维瘤病影像学检查缺乏特异性表现,诊断及切缘的判断仍有赖于病理。
孙艺华主治医师(病理科) 追溯患者既往外院手术病理切片,经我院病理科会诊,诊断为乳腺纤维腺瘤病。本次术后病理诊断为复发性乳腺侵袭性纤维瘤病。相关鉴别诊断包括:(1)瘢痕。纤维瘤病与外伤(包括手术)后瘢痕组织学改变相似。当病变中有含铁血黄素沉积、脂肪坏死、组织细胞和异物巨细胞反应,并缺乏长束状结构与外周埋陷的导管和小叶,倾向于诊断瘢痕。既往外伤或手术史有助于明确诊断,对于曾行手术切除的纤维瘤病患者,区分瘢痕或是纤维瘤病残留或复发,则非常困难。(2)纤维瘤病样化生性癌。纤维瘤病样化生性癌由温和的梭形细胞构成,与纤维瘤病非常相似,需要认真寻找是否出现上皮样细胞巢或导管内癌成分,CK免疫组化能够帮助诊断。化生性癌CK、p63阳性,纤维瘤病CK、p63多阴性,β-catenin多为阳性。(3)脂肪瘤样肌纤维母细胞瘤。该病镜下可见指状浸润生长,类似纤维瘤病,70%以上病例细胞表达ER、PR和AR,而乳腺纤维瘤病细胞3种激素受体均阴性。(4)结节性筋膜炎。该病界限相对清楚,无指状浸润性边缘,核分裂象多见,炎细胞散在分布于病灶内,与纤维瘤病炎细胞呈灶性集聚性分布不同。
丁昂副主任医师(乳腺外科) 小结该例患者诊断,几点思考:(1)对于既往手术部位再次出现肿块的病例应病理会诊既往病变,有助诊断。(2)乳腺复发性肿块,应考虑侵袭性纤维瘤病可能。结合影像学、临床表现、病理进行诊断与鉴别诊断。(3)建议优选空芯针穿刺活检,明确病变性质。空芯针穿刺活检用于纤维瘤病早期诊断的报道不多[20],但结果提示该技术能够提供足够的组织标本进行有效诊断。细针穿刺活检也能够识别纤维瘤病[21],但存在一定比例过度诊断和误诊[22]。开放手术活检,术后局部形成炎症微环境,炎症因子可能促进病变发展,故推荐空芯针穿刺活检。(4)对于病程较为复杂的病变早期推荐多学科诊疗模式,有助于更全面地评估病情,更准确地进行诊断,提供更合适的处理意见。病理会诊能够提示本次病变与既往病变的相关性。临床表现结合影像学检查,能够诊断具有特征性表现的疾病,同时能评估病变范围,指导治疗。鼓励临床医师、影像科医师、病理科医师在早期诊断阶段即开始多学科合作,有助于明确诊断。
陈宏亮副主任医师(乳腺外科) 侵袭性纤维瘤病自然病程多样,未接受任何治疗的侵袭性纤维瘤病患者连续随访,观察到肿瘤生长“自我限制”现象。但并不推荐所有侵袭性纤维瘤病患者仅接受随访,一旦病情出现迅速进展,可能造成严重后果。乳腺侵袭性纤维瘤病尚未形成治疗规范。基于侵袭性纤维瘤病局部浸润、易复发、无远处转移的疾病特点,临床以手术、放疗等局部治疗为主;随着对疾病生物学特性的认识,内分泌治疗、抗炎药物和酪氨酸激酶抑制剂治疗等全身治疗也尝试用于该病。目前,根治性手术切除仍被认为是标准治疗,通过扩大切除范围,取得阴性切缘[22],达到根治目的,类似肉瘤的治疗。患者病灶位于右乳内下,一旦病变范围较广,术后美观不能保证,可联合整形外科医师,在治疗的同时进行塑形。根据国际抗癌联盟(UICC)R分类标准,对术后切缘状态进行分类[23],镜下切缘阴性为R0切除,镜下切缘阳性为R1切除,肉眼切缘阳性为R2切除。乳腺侵袭性纤维瘤病切缘阳性的临床意义及处理方式存在争议[24-25]。大多数专家建议在肿瘤不可切除、肉眼或镜下肿瘤残留、肿瘤复发时,进行放疗[26]。有关乳腺侵袭性纤维瘤病放疗治疗的研究多为小样本临床研究,结果显示手术联合放疗能够取得临床获益。手术切缘阳性的患者,术后放疗使局部复发率由59%下降到25%[27]。手术切缘阴性患者,也存在较高的局部复发风险[16],术后10年局部复发率约25%~77%。联合放疗,局部复发风险可减少至20%~35%[22]。但预防性放疗的运用一直存在争议。随着放疗技术的进步,胸部放疗心肺毒性逐步可控,但对于年轻女性乳腺的影响仍然值得关注。既往报道霍奇金淋巴瘤患者,不同部位不同剂量的放疗,可能增加乳腺癌、乳腺肉瘤的发病风险[28-29]。控制放疗剂量,可能降低乳腺癌的发生风险。该患者术后切缘阳性,推荐再次手术,放疗可考虑。应在充分告知的前提下,结合患者意愿,谨慎选择。
吴克瑾主任医师(乳腺外科) 建议采用多学科模式进行治疗决策。乳腺原发性侵袭性纤维瘤病初始治疗,以根治性手术治疗为主,必要时联合整形外科技术,以最大可能争取阴性切缘。对于切缘阳性以及复发的侵袭性纤维瘤病,除选择再次手术治疗外,可探索性尝试放疗或其他替代治疗,以控制疾病进展。文献报道,多种药物(如他莫昔芬、抗炎药物以及细胞毒性药物)尝试用于不能切除和复发的侵袭性纤维瘤病[25],疗效不一。越来越多的证据表明,无论受体状态,他莫昔芬可明显抑制侵袭性纤维瘤病生长[30]。有报道20例乳腺侵袭性纤维瘤病患者服用他莫昔芬,65%的患者出现了肿瘤大小的稳定甚至完全缓解[31]。另有报道复发性侵袭性纤维瘤病在他莫昔芬治疗后完全缓解,避免进一步手术或放射治疗[32]。意大利的一项研究[33],共94例年龄≤21岁侵袭性纤维瘤病患者,分为3组:手术切缘阴性组,手术切缘阳性组、大体标本残留组。49名患者接受一线或二线全身治疗,治疗反应率分别为47%和50%。然而,尚缺乏大规模的随机试验证明他莫昔芬在侵袭性纤维瘤病手术切除后的疗效。考虑到他莫昔芬自身的药物不良反应和缺乏明显治疗获益的证据,目前不主张手术治疗后常规使用他莫昔芬。酪氨酸激酶抑制剂(如伊马替尼[34])以及冷冻消融[35]等也曾尝试用于侵袭性纤维瘤病的替代治疗。
部分未接受治疗的侵袭性纤维瘤病在随访过程中,肿瘤呈现惰性生长。一项研究更显示,约50%侵袭性纤维瘤病患者在初始治疗时可能存在过度治疗可能[35]。对侵袭性纤维瘤病治疗做减法观点的提出,使优化侵袭性纤维瘤病治疗更显重要。最近提出侵袭性纤维瘤病治疗算法[35],即在疾病初始阶段进行仔细的临床基线评估,随访2个月,根据肿瘤生长速度,肿瘤临床生物学行为特点,提供合适的治疗建议。对于那部分惰性生长的侵袭性纤维瘤病,可建议影像学与临床表现相结合的密切随访,一旦疾病进展,转为积极治疗;对于那部分生长迅速的侵袭性纤维瘤病,建议采用包括手术在内的多学科治疗手段,治疗前应充分评估肿瘤的复发风险、治疗获益以及治疗不良反应,制定获益最大化、不良反应最小化的适宜治疗方案。监测侵袭性纤维瘤病复发,建议患者至少术后2年内应定期进行乳房检查。
该患者既往曾接受右乳肿块切除,术后复发心理压力大。4个月前病灶增大,患者拒绝空芯针穿刺活检,要求肿块完全切除,故选择开放手术。对于术后病理提示切缘受累,患者在明确侵袭性纤维瘤病为良性病变的基础上,理解局部复发风险,其考虑自身年龄、放疗不良反应、内分泌治疗不良反应,选择随访,暂不行再次扩大范围手术或放疗等其他治疗,嘱其随访。
总结本文报道了1例33岁女性乳腺侵袭性纤维瘤病患者临床病史、影像学表现、病理特点及治疗选择。乳腺侵袭性纤维瘤病极为罕见,自然病程多样,易复发,无远处转移风险。影像学检查缺乏特异性,空芯针穿刺活检能够明确诊断。治疗缺乏共识,以手术治疗为主,可联合整形外科技术,在肿瘤R0切除的同时,取得更好的外形。切缘阳性的侵袭性纤维瘤病,除选择再次扩大范围切除外,可尝试放疗等其他治疗。多种类型药物尝试用于治疗本病,疗效不一。侵袭性纤维瘤病治疗算法评估[35],可协助制定获益最大化、不良反应最小化的适宜治疗方案。多学科诊疗模式已广泛用于乳腺恶性疾病诊治,鼓励拓宽用于乳腺侵袭性纤维瘤病这类具有恶性生物学行为风险的良性肿瘤,以更好地优化临床诊疗。
