基于灰度的生物炭pH值与N和K离子吸附研究
2018-11-28王明峰杨璐菡张争艳吴西文蒋恩臣
王明峰,杨璐菡,张争艳,吴西文,钟 旋,蒋恩臣
基于灰度的生物炭pH值与N和K离子吸附研究
王明峰,杨璐菡,张争艳,吴西文,钟 旋,蒋恩臣*
(华南农业大学材料与能源学院,农业部能源植物资源与利用重点实验室,广东 广州 510642)
通过固定床石英管热解装置将稻壳、木薯秸秆及玉米秸秆在350、450、500、550、600℃进行充分热解制备生物炭,利用图像识别技术获得生物炭的RGB值(红、绿、蓝三个通道的颜色)及相应的灰度值,研究了生物炭灰度值与其水溶液中的pH值及阳离子(NH4+-N及K+-K)吸附性能的关系.结果表明:3种生物炭的pH值随着灰度值的增加呈现“S”型增长趋势,并符合DoseResp模型,回归方程的决定系数(R)分别为0.9766、0.9592和0.9219,残差平方和(RSS)均小于0.01;除玉米秸秆炭的K+-K吸附量与灰度值的关系为线性负相关外,3种生物炭的NH4+-N和K+-K吸附量与灰度值之间满足一元高次非线性模型,R范围在0.8595~0.9999.本研究为快速预测生物炭在水溶液中的pH值和阳离子吸附性能提供了理论基础.
生物炭;RGB;灰度;pH值;阳离子吸附
生物炭是一种高碳素多孔物质[1-2],可作为肥料载体减缓所携带营养成分的释放速率,并可以减轻由于肥料淋湿导致的地下水污染、温室气体氧化亚氮排放等环境问题[3-4].目前,利用掺混法、粘结剂造粒法和吸附法等多种方法制备的生物炭基复合肥料,由于其优良的缓释效果,及改良土壤的优点,将有效解决减少农田养分投入量与缓解水体富营养化的难题[5-7].
为了使生物炭作为肥料载体承载更多的养分,许多学者重点研究了生物炭对铵盐与钾盐的吸附性能.研究结果表明,在200℃下由普通农业废弃物制备的生物炭在吸附NH4+21d后,还保留有90%以上[8];在400℃下由玉米秸秆制备的生物炭,其NH4+-N的吸附量为4.22mg/g[10];在600℃下炭化沼渣、城市废物和温室废物制备的生物炭,其NH4+-N吸附量为105.8~146.4mg/g[9];因此,不同原料及炭化温度制备的生物炭都表现出了优异的养分固持能力.目前,普遍认为生物炭吸附主要有3个方面的原因:第一,生物炭表面具有能够电离产生电荷的化学官能团,使其具有较高的离子吸附交换量,让其能通过静电作用吸附养分离子[11];第二,生物炭比表面积大,孔隙度高,具有较大的吸附能力,使其能在表面吸持一定的养分;第三,生物炭表面含有一些官能团,如羟基、羧基等,它们都较为活跃,能够和肥料发生化学反应从而负载一定的养分[12].
近年来,计算机图像处理分析技术使得农业生产领域的研究越来越便捷与迅速[13-14].但是,将图像识别技术应用于生物炭吸附方面的研究较少.本文利用固定床石英管热解装置对稻壳、木薯秸秆和玉米秸秆进行热解炭化,利用colorpix软件获得炭样的(red)、(green)、(blue)值并作灰度化处理,开展吸附实验获得3种生物炭的NH4+-N及K+-K吸附量.分析不同热解温度下3种生物炭的pH值和NH4+-N、K+-K吸附量与其灰度值之间的内在关系,构建相关数学模型,为生物炭pH值及吸附性能的快速检测提供理论基础.
1 材料与方法
1.1 试验材料及制备
本试验选用稻壳(梅州)、玉米秸秆(辽宁)和木薯秸秆(广州)作为热解原料,粉碎后通过20目筛,在60℃鼓风干燥箱内烘干24h后密封保存.参照国标GB/T 28731-2012《固体生物质燃料工业分析方法》[39]和GB/T22923-2008《肥料中氮、磷、钾的自动分析仪测定法》[40],利用全自动工业分析仪(长沙友欣公司,型号:YX-GYFX 7701型)和元素分析仪(北京吉天仪器有限公司,型号:NPK-100型)进行3种生物质的工业分析和元素测定,结果如表1所示.
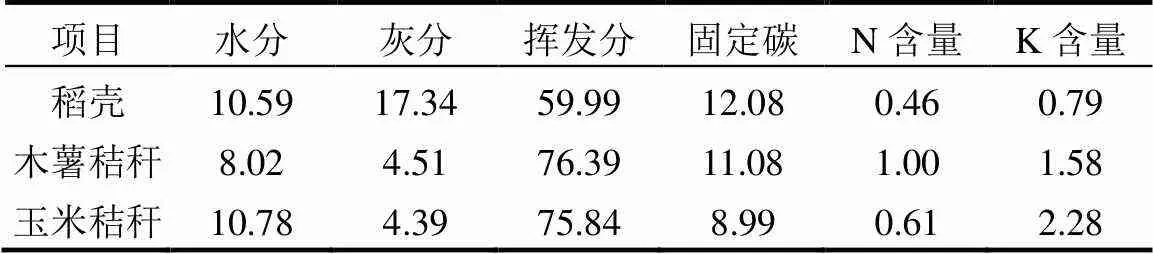
表1 原料的工业分析及元素分析结果(%)
1.2 试验方法
1.2.1 生物炭的制备 利用固定床石英管热解装置,在氮气流速为50mL/min,炭化温度及驻留时间分别为350℃(120min)、450℃(90min)、500℃(60min)、550℃(30min)及600℃(30min) 的条件下,充分热解3种原料.获得的稻壳炭、木薯秸秆炭和玉米秸秆炭分别标记为RHB、CSB和CNB.
1.2.2 pH值的测定 准确称量不同热解温度的RHB、CSB以及CNB各1g,按照水与样品质量20:1的比例加入去离子水混合均匀,经过12小时充分振荡后离心过滤,使用pH计(METTLER TOLEDO公司,型号:FiveEasyPlus)测试3种生物炭的pH值,设3次重复,结果取平均值.
1.2.3 RGB值的采集及灰度化处理 利用白光扫描仪获取3种生物炭粉末的扫描图像(JPG格式,分辨率为600dpi),使用取色软件colorpix对图像随机采集40点,取平均值作为炭样的RGB值.在随机点提取过程中,不考虑巨型亮斑区域以保证特征值的可靠性.采用公式(1)将值转化成相应的灰度值[15]:

式中:分别代表图像中红色、绿色及蓝色成分,范围均在0~255.
1.2.4 NH4+-N和K+-K最大吸附量 将3种生物炭样品研磨后过100目筛(颗粒直径<0.15mm),准确称量0.1000g研磨后的生物炭加入具塞碘量瓶内,分别加入30mL质量浓度为50mg/L的NH4Cl溶液和80mg/L的KCl溶液,并转移至双层恒温摇床(上海智城公司,型号:ZWY-2102C)中,在转速1800rpm及温度25℃的环境下,振荡24h后取出样品.样品过滤后,取上清液,利用离子色谱仪(Metrohm 850Professional ICeAnCat)分别测定NH4+-N以及K+-K离子的浓度,设3次重复,结果取平均值.采用公式(2)计算生物炭对2种阳离子的最大吸附量[16]:
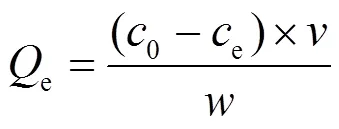
式中:e为平衡时单位生物炭吸附溶液中离子的量, mg/g;0为初始溶液的离子浓度,mg/L;e为平衡时溶液的离子浓度,mg/L;为消耗的溶液体积,L;为生物炭干燥质量,g.
1.3 数据分析方法
利用Origin 9.0和RStudio软件进行建模和数据分析,并利用决定系数(2)判定线性及非线性模型的拟合优度,其值越大,代表自变量对因变量的解释程度越高,模型越合理.为了明确随机误差的效应,使用残差平方和(RSS)检验模型精度.
2 结果与讨论
2.1 生物炭的pH值、NH4+-N及K+-K吸附性能和灰度值
pH值是生物炭的重要性质之一,可反映其在水体中溶解性固体和离子变化,研究发现生物炭一般呈碱性[17].如表2所示,在本实验中,RHB、CSB与CNB的pH值范围分别为7.5~8.0、8.2~8.5和8.2~8.8.3类生物质的pH值均随着热解温度的增加而增加,原因一方面是3种生物炭的灰分含量较高,促使了pH值的提高[18],另一方面是表面碱性官能团的增多[19].分别比较3种生物炭在不同热解温度下水溶液中的pH值发现,350~450℃炭化的生物炭pH值比较相近,变化幅度小于0.05个pH值单位,而500℃炭化的生物炭其pH值较450℃显著增加,增幅分别为0.31、0.21与0.32个pH值单位,500~600℃炭化的生物炭,其pH值变化趋于平稳,只有小幅增长.研究表明[20-21],在相同条件下热解的生物炭由于原料的不同其pH值差异较大,本实验结果与之相符,在同一热解温度下,属于秸秆类生物质的CSB与CNB,2者的pH值接近,变化趋势也相似,并且碱性明显比软壳类的RHB强.
由表2可知,炭化温度为350~600℃时,3种生物炭的NH4+-N吸附能力均先减小后增大.研究表明[22-23],随着热解温度的升高(<500℃),生物炭极性基团不断损失,导致NH4+-N的吸附量减少,因此炭化温度较低的生物炭表现出更好的吸附性能[24].在350℃下,3者对NH4+的吸附量差异最大(1.56mg/g),在600℃下,3者对NH4+的吸附量差异最小(0.15mg/ g).350℃炭化的RHB与CSB和600℃炭化的CNB对NH4+-N的吸附能力最强(分别为1.15,2.00和0.88mg/g).
3种生物炭的K+-K吸附量均为负数,即生物炭释放的K+比吸附的K+多,研究发现,低温(<500℃)热解有利于K、Mg、S等可利用态的矿质养分在生物炭中的保留[25].本实验所用的3种生物炭本身含有大量的K元素,无需进行K+的吸附就有成为缓释钾肥的应用潜力,根据蒋敏等人[26]的研究,按土壤质量施加相应生物炭可以提高土壤有效态钾含量水平,且生物炭中所含有的钾素将直接进入土壤引起理化性质、解钾菌数量等的变化.同时从表中数据可知,随着热解温度的升高,3类生物炭释放K+的量也呈现逐步增长的趋势.
由表2的灰度值可知,随着热解温度的上升,生物炭的灰度值也相应增加.在350~600℃,RHB的灰度值总是大于CNB与CSB.炭化温度的升高利于生成具多微孔及灰分的生物炭[27],因此当扫描仪照射高温炭化的生物炭时,由于其孔隙较多,反射回成像仪的光源较少,导致RGB值与灰度值较高[28].生物炭的炭化程度与孔隙结构是影响其pH值与吸附性能的主要因素,因此利用RGB值转化的灰度值可表征生物炭,进而反映其pH值与离子吸附能力.
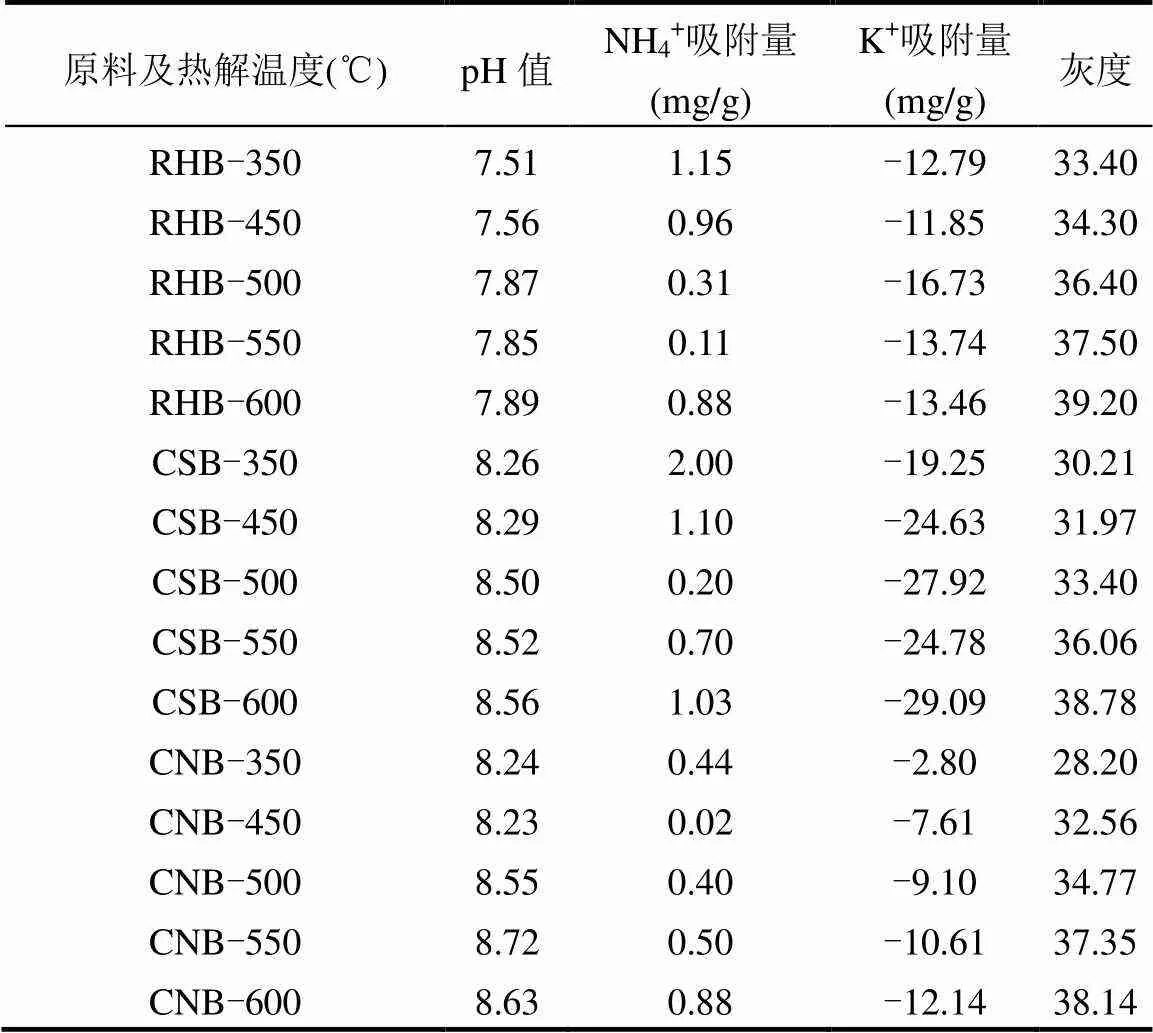
表2 3种生物炭的pH值、NH4+、K+吸附量和灰度值
2.2 灰度值与pH值
3种生物炭在水中的pH值随灰度值的变化如图1所示,pH值在某个灰度节点前变化较为平缓,而在某个灰度范围内有突越现象,且突越后pH值变化又再次趋于平缓,灰度-pH值的变化曲线形似S型函数,符合Growth/Sigmoidal类别下的DoseResp模型(3)[29],

式中:为生物炭在水溶液中的pH值;为生物炭的灰度值;1为生物炭在水溶液中的最低pH值;2为生物炭在水溶液中的最高pH值.
由表3的拟合系数及优度可知,RHB的预测精度最高,CSB次之,CNB最低,但3者的决定系数(R)都大于0.9219,即灰度值可以在超过90%的程度上解释生物炭pH值的变化,同时3个模型的残差平方和(RSS)都小于0.01,因此利用DoseResp模型可以精确地根据生物炭的灰度值预测出相应pH值.

图1 3种生物炭的灰度值与pH值之间的拟合曲线
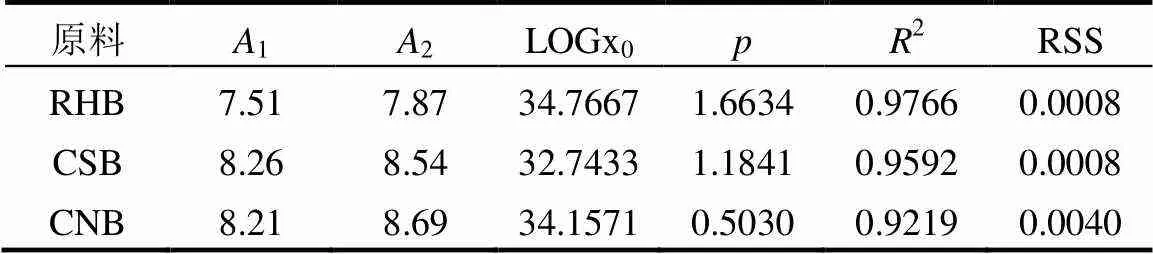
表3 3种生物炭的灰度值与pH值间的拟合系数及优度
2.3 灰度值与阳离子吸附特性
pH值是决定生物炭吸附阳离子能力的重要因素[30-32].一方面,pH值影响生物炭的零电荷点(pHpzc),另一方面,pH值影响吸附质的离子化程度及存在状态[33].当pH
3种生物炭的NH4+-N、K+-K吸附量与灰度值的关系如图2和图3所示.参考生物炭物性关联的相关研究[37-38],根据生物炭NH4+-N及K+-K的吸附能力随灰度值增加的变化趋势,可发现两者满足线性或一元高次非线性模型=0+1´+2´2+3´3+4´4,拟合系数如表4所示.其中,灰度值与NH4+-N吸附量模型的拟合优度中,RHB最高,CSB次之,CNB最低,R分别为0.9972、0.9172和0.8595,并且3者均为一元三次方程;而灰度值与K+-K吸附量间的模型,3者的拟合优度均非常高(2>0.9754),其中RHB与CSB的模型为一元四次方程,CNB为线性方程.因此,可以利用图像识别技术获得生物炭的灰度值,并辅以相关方程,预测出生物炭对NH4+与K+阳离子的吸附能力,精确度较高.

图2 灰度值与NH4+吸附量的拟合曲线

图3 灰度值与K+吸附量的拟合曲线
3 结论
3.1 生物炭图像的RGB/灰度值与其在水溶液的pH值及NH4+-N和K+-K吸附性能存在关联关系,可利用图像识别技术并辅以相关模型,实现生物炭pH及阳离子吸附性能的快速测定.

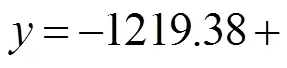
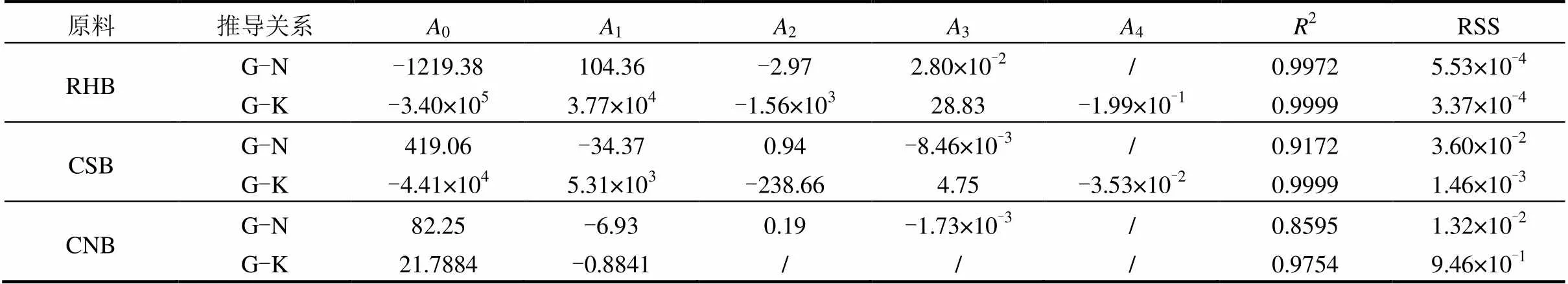
表4 3种生物炭灰度值与NH4+-N、K+-K吸附量间的模型拟合系数及优度
[1] Cao Xinde, Harris W. Properties of dairy-manure-derived biochar pertinent to its potential use in remediation [J]. Bioresource Technology, 2010,101(14):5222-5228.
[2] 周 凤,许晨阳,金永亮,等.生物炭对土壤微生物C源代谢活性的影响 [J]. 中国环境科学, 2017,37(11):4202-4211.
[3] 李飞跃,谢 越,石 磊,等.稻壳生物质炭对水中氨氮的吸附 [J]. 环境工程学报, 2015,9(3):1221-1226.
[4] Nielsen S, Minchin T, Kimber S, et al. Comparative analysis of the microbial communities in agricultural soil amended with enhanced biochars or traditional fertilisers [J]. Agriculture Ecosystems & Environment, 2014,191(6):73-82.
[5] Steiner C, Garcia M, Zech W. Effects of charcoal as slow release nutrient carrier on N-P-K dynamics and soil microbial population: Pot experiments with ferralsol substrate [M]. Netherlands:Springer, 2009: 325-338.
[6] 刘 冲,刘晓文,吴文成,等.生物炭及炭基肥对油麦菜生长及吸收重金属的影响 [J]. 中国环境科学, 2016,36(10):3064-3070.
[7] 俞映倞,王悦满,侯朋福,等.生物炭负载氮还田对水稻生长、根系形态及氮素利用的影响 [J]. 环境科学, 2018,11:1-14.
[8] Yanxue Cai, Hejinyan Qi. Sorption/Desorption Behavior and Mechanism of NH4+by Biochar as a Nitrogen Fertilizer Sustained- Release Material [J]. Journal of Agricultural and Food Chemistry, 2016,64:4958-4964.
[9] Takaya C A, Fletcher L A, Singh S, et al. Phosphate and ammonium sorption capacity of biochar and hydrochar from different wastes [J]. Chemosphere, 2016,145:518-527.
[10] 武丽君,王朝旭,张 峰,等.玉米秸秆和玉米芯生物炭对水溶液中无机氮的吸附性能 [J]. 中国环境科学, 2016,36(1):74-81.
[11] Mukherjee, Atanu, Zimmerman, et al. Organic carbon and nutrient release from a range of laboratory-produced; biochars and biochar- soil mixtures [J]. Geoderma, 2013,193(2):122-130.
[12] 何绪生,张树清,佘 雕,等.生物炭对土壤肥料的作用及未来研究 [J]. 中国农学通报, 2011,27(15):16-25.
[13] 王明峰,陈晓堃,蒋恩臣,等.基于扫描图像RGB分析的生物炭吸附特性研究 [J]. 农业机械学报, 2015,46(12):212-217.
[14] 仇瑞承,张 漫,魏 爽,等.基于RGB-D相机的玉米茎粗测量方法 [J]. 农业工程学报, 2017,33(z1):170-176.
[15] 张铭钧,李 煊,王玉甲.基于灰度化权值调整的水下彩色图像分割 [J]. 哈尔滨工程大学学报, 2015,36(5):707-713.
[16] Takaya C A, Fletcher L A, Singh S, et al. Phosphate and ammonium sorption capacity of biochar and hydrochar from different wastes [J]. Chemosphere, 2016,145:518-527.
[17] Yuan J H, Xu R K. The amelioration effects of low temperature biochar generated from nine crop residues on an acidic Ultisol [J]. Soil Use and Management, 2011,27(1):110-115.
[18] 罗 煜,赵立欣,孟海波,等.不同温度下热裂解芒草生物炭的理化特征分析 [J]. 农业工程学报, 2013,29(13):208-218.
[19] 袁金华,徐仁扣.生物炭的性质及其对土壤环境功能影响的研究进展 [J]. 生态环境学报, 2011,20(4):779-785.
[20] Nguyen BT, Lehmann J, Hockaday WC, et al. Temperature sensitivity of black carbon decomposition and oxidation [J]. Environmental Science and Technology, 2010,44:3324-3331.
[21] Novak JM, Lima I, Xing B, et al. Characterization of designer biochar produced at different temperatures and their effects on a loamy sand [J]. Annals of Environmental Science, 2009,3:195-206.
[22] Zeng Z, Zhang S D, Li T Q, et al. Sorption of ammonium and phosphate from aqueous solution by biochar derived from phytoremediation plants [J]. Journal of Zhejiang University Science B Biomedicine & Biotechnology, 2013,14(12):1152-1161.
[23] Wang Z, Guo H, Shen F, et al. Biochar produced from oak sawdust by lanthanum (La)-involved pyrolysis for adsorption of ammonium (NH4+), nitrate (NO3-), and phosphate(PO43-) [J]. Chemosphere, 2015a, 119:646-653.
[24] Jassal R S, Johnson M S, Molodovskaya M, et al. Nitrogen enrichment potential of biochar in relation to pyrolysis temperature and feedstock quality [J]. Journal of Environmental Management, 2015,152(24): 140-144.
[25] Chan K Y, Van Zwieten L, Meszaros I, et al. Agronomic values of green waste biochar as a soil amendment [J]. Soil Research, 2008, 45(8):629-634.
[26] 姜 敏,汪 霄,张润花,等.生物炭对土壤不同形态钾素含量的影响及机制初探 [J]. 土壤通报, 2016,47(6):1433-1441.
[27] 郭 平,王观竹,许 梦,等.不同热解温度下生物质废弃物制备的生物质炭组成及结构特征 [J]. 吉林大学学报(理学版), 2014,52(4): 855-860.
[28] 黄国祥.RGB颜色空间及其应用研究 [D]. 中南大学, 2002.
[29] 王中慧,陈德珍,王 海.污泥裂解过程的形貌学特征参数研究 [J]. 环境工程学报, 2011,5(11):2610-2614.
[30] 马锋锋,赵保卫,刁静茹.小麦秸秆生物炭对水中Cd2+的吸附特性研究 [J]. 中国环境科学, 2017,37(2):551-559.
[31] 韩鲁佳,李彦霏,刘 贤,等.生物炭吸附水体中重金属机理与工艺研究进展 [J]. 农业机械学报, 2017,48(11):1-11.
[32] Halim A A, Latif M T, Ithnin A. Ammonia removal from aqueous solution using organic acid modified activated carbon [J]. World Applied Sciences Journal, 2013,24(1):1-6.
[33] Li M, Liu Q, Guo L, et al. Cu (II) removal from aqueous solution by Spartina alterniflora derived biochar [J]. Bioresource Technology, 2013,141(4):83-88.
[34] Abdel-Fattah T M, Mahmoud M E, Ahmed S B, et al. Biochar from woody biomass for removing metal contaminants and carbon sequestration [J]. Journal of Industrial and Engineering Chemistry, 2015,22:103-109.
[35] Tan X F, Liu Y G, Zeng G M, et al. Application of biochar for the removal of pollutants from aqueous solutions [J]. Chemosphere, 2015, 125:70-85.
[36] 郜礼阳,邓金环,唐国强,等.不同温度桉树叶生物炭对Cd2+的吸附特性及机制 [J]. 中国环境科学, 2018,38(3):1001-1009.
[37] Lei T, Zhou J, Xu C, et al. Soil Biochar Quantification via Hyperspectral Unmixing [C]. Digital Image Computing: Techniques and Applications (DICTA), 2013International Conference on IEEE, 2013:1-8.
[38] Sadaka S, Sharara M A, Ashworth A, et al. Characterization of biochar from switchgrass carbonization [J]. Energies, 2014,7(2):548-567.
[39] GB/T 28731-2012 固体生物质燃料工业分析方法[S].
[40] GB/T22923-2008 肥料中氮、磷、钾的自动分析仪测定法[S].
Research on pH and adsorption properties of N and K cations of biochar based on gray value.
WANG Ming-feng, YANG Lu-han, ZHANG Zheng-yan, WU Xi-wen, ZHONG Xuan, JIANG En-cheng*
(Key laboratory of Ministry of Agriculture Energy Plant Resources and the Use, College of Materials and Energy, South China Agricultural University, Guangzhou 510642, China)., 2018,38(11):4141~4146
According to statistics of the past 40years, average fertilizer use efficiency is only about 50%. The low fertilizer efficiency not only causes energy loss but also causes environmental pollution and ground and surface water contamination. A new fertilizer using biochar as carrier has a great potential to solve this issue. In this research, the biochars made from rice husk, cassava straw and corn stover were obtained by a horizontal fixed bed quartz tube pyrolysis reactor with varied temperatures (350, 450, 500, 550, and 600℃). The RGB values and corresponding gray value of these biochars were analyzed by image recognition technology. The relationship between pH and gray value and the relationship between adsorption capacities of N and K cations (NH4+-N and K+-K,) and gray value were studied. In general, the pH value of biochar increased as gray value increased withRof 0.9766, 0.9592, and 0.9219, respectively, and the trend fitted well with the DoseResp model. NH4+-N and K+-K adsorption capacity of those three biochars followed the one-dimensional high-order nonlinear models with2ranged from 0.8595 to 0.9999, except the negative linear correlation between K+-K adsorption capacity and gray value for corn stover. This study provides theoretical basis for development of rapid method to predict pH and cation adsorption properties of biochar, and also has a potential to develop portable equipment for online testing.
biochar;RGB;gray value;pH;cation adsorption
X703.1
A
1000-6923(2018)11-4141-06
王明峰(1982-),男,辽宁鞍山人,讲师,博士,主要从事生物质资源化、能源化综合利用研究.发表论文40余篇.
2018-04-08
国家自然科学基金资助项目(51706074);广东省科技计划项目(2015B020237010,2016A020221028)
* 责任作者, 教授, ecjiang@scau.edu.cn
