鸡miR-17-92基因簇宿主基因启动子的甲基化及其功能分析
2018-11-24邢天宇崔婷婷黄佳新闫晓红
邢天宇,崔婷婷,黄佳新,闫晓红,李 辉,王 宁
(农业部鸡遗传育种重点实验室,黑龙江省普通高等学校动物遗传育种与繁殖重点实验室,东北农业大学动物科学技术学院,黑龙江哈尔滨 150030)
DNA甲基化是表观遗传学的重要研究内容之一,其参与基因转录抑制、基因组印迹、细胞分化和发育的调控等多种生物学过程[1]。DNA甲基化在脂肪组织的生长发育中具有重要作用[2]。DNA甲基化通过调控脂肪细胞分化相关基因的表达,进而调控脂肪的生长发育[3]。PPARγ是脂肪生成和脂肪组织发育的关键调控因子。对哺乳动物研究发现,DNA甲基化调控PPARγ基因的表达[4-5]。前期研究发现,在东北农业大学高、低脂系肉鸡中,脂肪组织PPARγ基因启动子DNA甲基化与PPARγ基因表达呈负相关[6]。了解脂肪组织 DNA 甲基化对探究脂肪生长发育的分子机制以及控制动物肥胖症具有重要意义。
miR-17-92基因簇是一个高度保守的miRNA基因簇,可编码7个不同的成熟miRNA[7]。哺乳动物研究表明,该基因簇参与调控细胞增殖、分化及凋亡等多种生物学过程[8]。研究发现,鸡miR-17-92基因簇参与调控鸡脂肪细胞的增殖和分化[8-10]。实验室前期获得了鸡miR-17-92基因簇上游的gap 区序列,鉴定出了鸡miR-17-92基因簇宿主基因(MⅠR17HG)的启动子区[11]。目前,对于人、鼠及鸡MⅠR17HG启动子区是否存在DNA甲基化以及是否受到DNA甲基化的调控都还不清楚。本研究对东北农业大学高、低脂鸡脂肪组织MⅠR17HG启动子的DNA甲基化进行分析,为揭示鸡脂肪组织生长发育的分子机制提供参考。
1 材料与方法
1.1 实验材料 DNA Marker购自TransGen。Prime ScriptTMRT reagent Kit with gDNA Eraser、限制性内切酶KpnⅠ、SmaⅠ和 T4 DNA 连接酶购自 TaKaRa。质粒小量制备试剂盒、DNA纯化回收试剂盒购自Axygen。Dual-Luciferase®Report自美国 Promega。LipofectamineTM2000购自美国Ⅰnvitrogen。DMEM、Opti-MEM、0.25%Trypsin-EDTA购自美国Gibco。FBS购自美国BⅠ。BstUⅠ酶 及 CpG Methyltransferase(M.SssⅠ) 购 自NEB。甲基化酶缺失的大肠杆菌(dam-/dcm-)购自全式金公司(北京);DF1细胞(鸡胚成纤维细胞)为本实验室保存。鸡脂肪组织来自本实验室培育的东北农业大学19世代高、低脂鸡,其中2周龄低脂鸡5只,高脂鸡10只;3周龄高、低脂鸡各5只;7周龄高、低脂鸡各15只的腹部脂肪组织。鸡MⅠR17HG启动子报告基因载体pGL3-cMⅠR17HG(-4428/-2506)和A/T富集区启动子报告基因载体(PGL3-AT-MⅠR17-92(-440/-1)为本实验室保存的载体。
1.2 主要分子生物学软件 Primer Premier 5.0;GraphPad Prism 5;NCBⅠ(http://www.ncbi.nlm.nih.gov/);UCSC(http://genome. ucsc.edu/);JASPAR(http://jaspar.binf.ku.dk/);EMBOSS(http://www.ebi.ac.uk/Tools/seqstats/emboss_cpgplot/)。
1.3 实验方法
1.3.1 CpG岛预测分析 从NCBⅠ数据库获得MⅠR17HG启动子区序列,利用CpG岛在线预测软件(http://www.ebi.ac.uk/Tools/seqstats/emboss_cpgplot/)预测鸡MⅠR17HG启动子区3 300 bp(转录起始位点上游3 000 bp和转录起始位点下游300 bp)CpG岛的位置及数量,参数设置为Observed/Expected radio> 0.60,Percent C+Percent G>50.00,Length>200。
1.3.2 Sequenom MassARRAY甲基化检测 利用sequenom®EpiDesigner程序对该序列进行引物设计,上游引物序列:5'-AGGAAGAGAGGTAGTTTATGGTGGTTG TAGGAAG-3';下游引物序列:5'-CAGTAATACGACT CACTATAGGGAGAAGGCTCCCTCATTAAAATAAAA AACAAAATAC-3'。扩增DNA片段长度为399 bp,覆盖64个CpG位点。采集东北农业大学19世代高、低脂肉鸡腹部脂肪组织20 mg,提取基因组DNA 2 μg。利用NaHSO3处理样本,低速短暂离心后进行PCR 反应,体系如下(8 μL):ddH2O 4.90 μL,10×PCR Buffer 0.80 μL,dNTPs (200 μmol/L)0.80 μL,PCR Enzyme(5 U/μL)0.10 μL,上、下游引物各 0.20 μL(10 μmol/L),DNA 模板1 μL。 PCR 反应条件:94 预变性 4 min,94 20 s,56 30 s,72 1 min,共45个循环,72延伸3 min。SAP反应及T切反应/RNase A 消化后,在Sequenom Mass ARRAY平台上进行芯片点样及数据输出、分析等实验工作。每个位点的甲基化程度表示检测到的甲基化与未甲基化总和的百分比,从0~1表示,数值越大代表甲基化程度越高。
1.3.3 甲基化报告基因载体的构建 为了确定DNA甲基化对MⅠR17HG启动子活性的影响,将前期构建的MⅠR17HG启动子报告基因载体pGL3-cMⅠR17HG(-4428/-2506)转化到甲基化酶缺失的大肠杆菌(dam-/dcm-)中,获得未甲基化的miR-17-92基因簇启动子报告基因载体。利用KpnⅠ和SmaⅠ对未甲基化的miR-17-92基因簇启动子报告基因载体进行双酶切,获得未甲基化的miR-17-92基因簇启动子片段,并利用CpG 甲基转移酶 [CpG Methyltransferase(M.SssⅠ)]在 37 条件下处理未甲基化的miR-17-92基因簇启动子片段,制备完全甲基化的miR-17-92基因簇启动子片段。分别将未甲基化与完全甲基化的启动子片段纯化,并连接pGL3-basic,得到miR-17-92基因簇启动子片段未甲基化或完全甲基化的报告基因载体。本研究选择pGL3-ATMⅠR17-92(-440/-1)报告基因载体作为阴性对照,该载体所携带的启动子为AT-MⅠR17-92(-440/-1),该启动子无CpG位点,因此,其启动子的活性不受DNA甲基化影响。M.SssⅠ甲基转移酶反应体系为0.5 μg DNA,10×Buffer2 2 μL,10×SAM 2 μL,CpG 甲基转移酶 1 μL,加水至20 μL。37 温育,3 h,60 放置15 min使酶失活。采用限制性内切酶BstUⅠ来检测体外DNA甲基化是否成功。BstUⅠ可以酶切未甲基化启动子片段,但不能切割完全甲基化的启动子片段。经BstUⅠ酶切鉴定证实启动子片段被完全DNA甲基化后,用于后续报告基因活性分析。
1.3.4 细胞培养、转染及报告基因活性检测 采用含有10%胎牛血清和终浓度为100 U /mL青霉素、100 mg /L链霉素的DMEM/High glucose培养基培养DF1细胞,在37 含5% CO2和90%相对湿度的条件下培养。待细胞汇合度达到80%~90%,用0.25%胰蛋白酶/EDTA消化,将DF1细胞接种至24孔培养板,待细胞汇合度达到约70%时,采用LipofectamineTM2000转染试剂,分别将MⅠR17HG启动子的未甲基化和甲基化的报告基因载体pGL3-cMⅠR17HG(-4428/-2506)(0.4 μg)以及对照报告基因载体 pGL3-AT-MⅠR17-92(-440/-1)(0.4 μg)分别转染DF1细胞,48 h后收集细胞裂解液,参照Dual-Luciferase Reporter Assay System(Promega) 说明书检测报告基因活性。
1.4 统计分析 运用GraphPad Prism5 软件处理数据,2组数据差异比较采用t检验方法,P<0. 05(*) 为差异显著,P<0. 01(**)为差异极显著。
2 结果与分析
2.1 鸡MⅠR17HG启动子区的CpG岛分析 利用CpG岛在线预测软件(http://www.ebi.ac.uk/Tools/seqstats/emboss_cpgplot/)分析发现鸡MⅠR17HG启动子区存在1个CpG岛,大小为710 bp,共有64个CpG位点。该CpG岛位于转录起始位点上游457 bp至转录起始位点下游252 bp处(图1)。CpG岛的分析结果提示,鸡MⅠR17HG启动子可能会发生DNA甲基化。为确认鸡MⅠR17HG启动子是否存在甲基化,采用Sequenom MassARRAY技术检测东北农业大学高、低脂鸡脂肪组织MⅠR17HG启动子的甲基化情况。由于序列原因,只能检测miR-17-92 基因簇上游3 056 ~3 500 bp区域的31个CpG位点的甲基化。
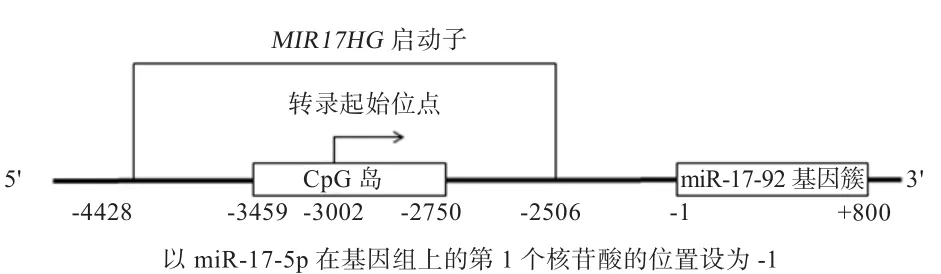
图1 鸡MⅠR17HG启动子区的CpG岛分析
2.2 鸡MⅠR17HG启动子的甲基化分析 2周龄低脂鸡脂肪组织MⅠR17HG启动子的总体甲基化水平显著高于高脂鸡(图2-A),且CpG位点25、26、27、28的低脂甲基化程度显著高于高脂(P<0.05)(图2-B)。3周龄高、低脂鸡脂肪组织MⅠR17HG启动子甲基化总体水平差异不显著(P>0.05)(图3)。7周龄高、低脂鸡脂肪组织MⅠR17HG启动子的甲基化总体水平差异不显著(P>0.05)(图4-A),但低脂鸡MⅠR17HG启动子的CpG位点41和CpG位点42的甲基化程度显著低于高脂鸡(P<0.05)(图4-B)。从整体看,2周龄低脂鸡脂肪组织MⅠR17HG启动子的甲基化总体水平极显著高于3、7周龄低脂鸡(P<0.01);2周龄高脂鸡脂肪组织MⅠR17HG启动子的总体甲基化水平也显著高于7周龄高脂鸡(P<0.05)(图5)。
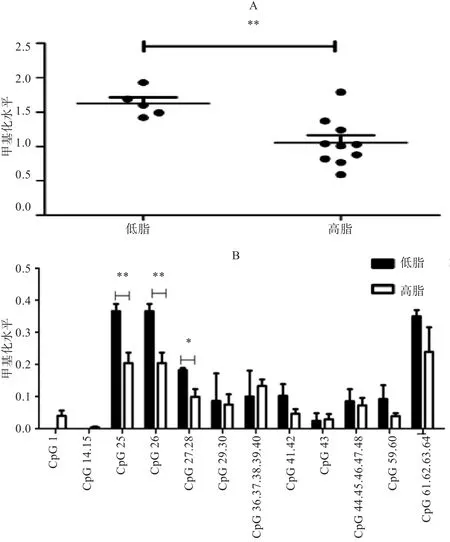
图2 2周龄高、低脂鸡脂肪组织MⅠR17HG启动子的甲基化比较分析
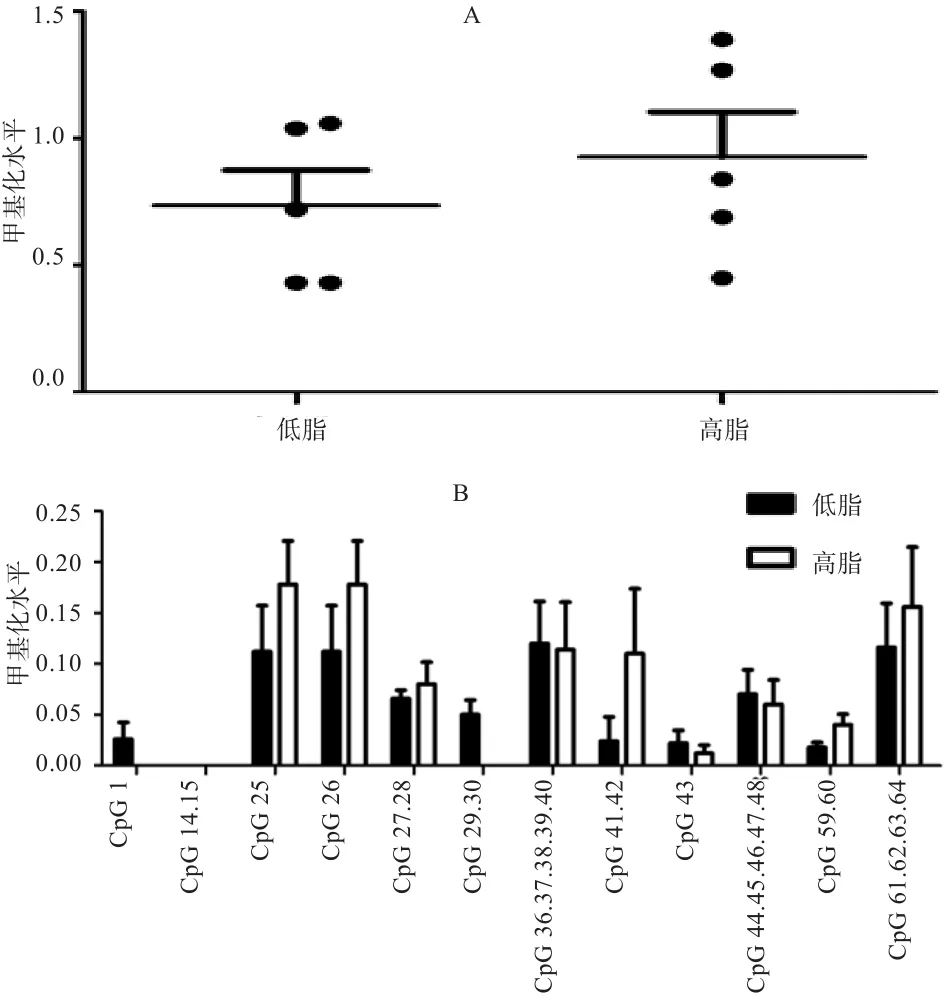
图3 3周龄高、低脂鸡脂肪组织MⅠR17HG启动子的甲基化比较分析
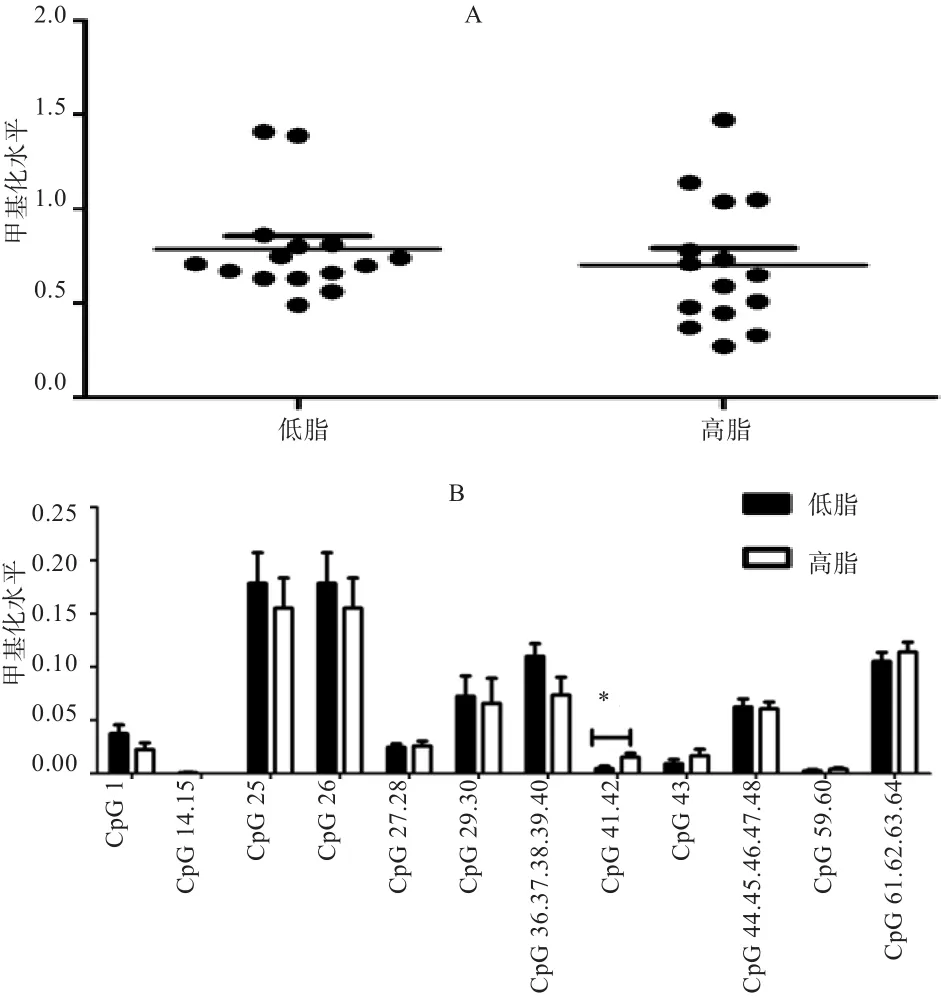
图4 7周龄高、低脂鸡脂肪组织MⅠR17HG启动子的甲基化比较分析
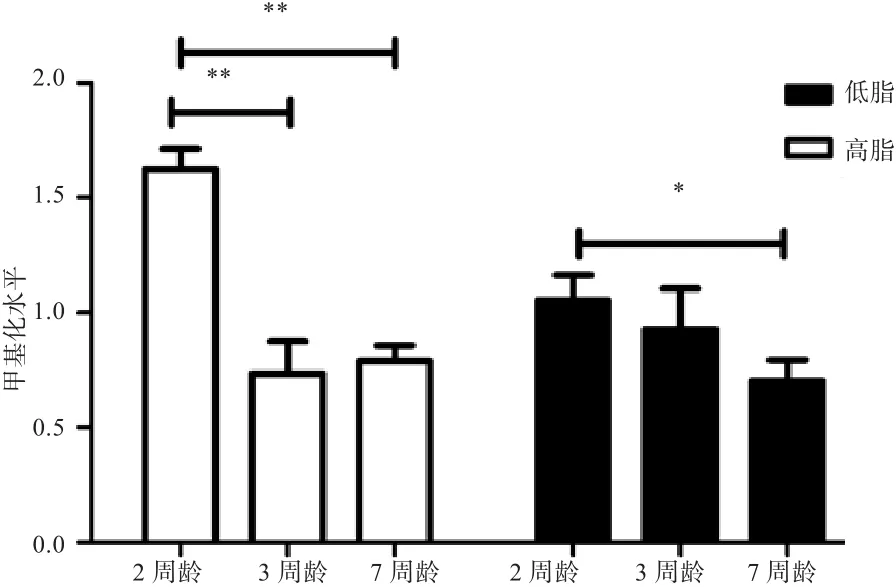
图5 MⅠR17HG启动子在高、低脂鸡脂肪组织生长发育过程中DNA甲基化的比较分析
2.3 DNA甲基化对鸡MⅠR17HG启动子活性的影响为了确定DNA甲基化对MⅠR17HG启动子活性的影响,将未甲基化与甲基化的MⅠR17HG启动子片段(图6-A)分别与报告基因载体pGL3-basic连接后,转染细胞进行报告基因活性分析。AT-MⅠR17-92(-440/-1)为无CpG位点的启动子对照。报告基因活性检测显示,与预期一致,甲基化和非甲基化处理对报告基因载体pGL3-AT-MⅠR17-92(-440/-1)的荧光素酶活性无显著变化,但是甲基化的MⅠR17HG启动子报告基因pGL3-cMⅠR17HG(-4428/-2506)活性极显著低于未甲基化启动子的报告基因活性(P<0.01)(图6-B)。这一结果提示DNA甲基化抑制MⅠR17HG启动子活性。
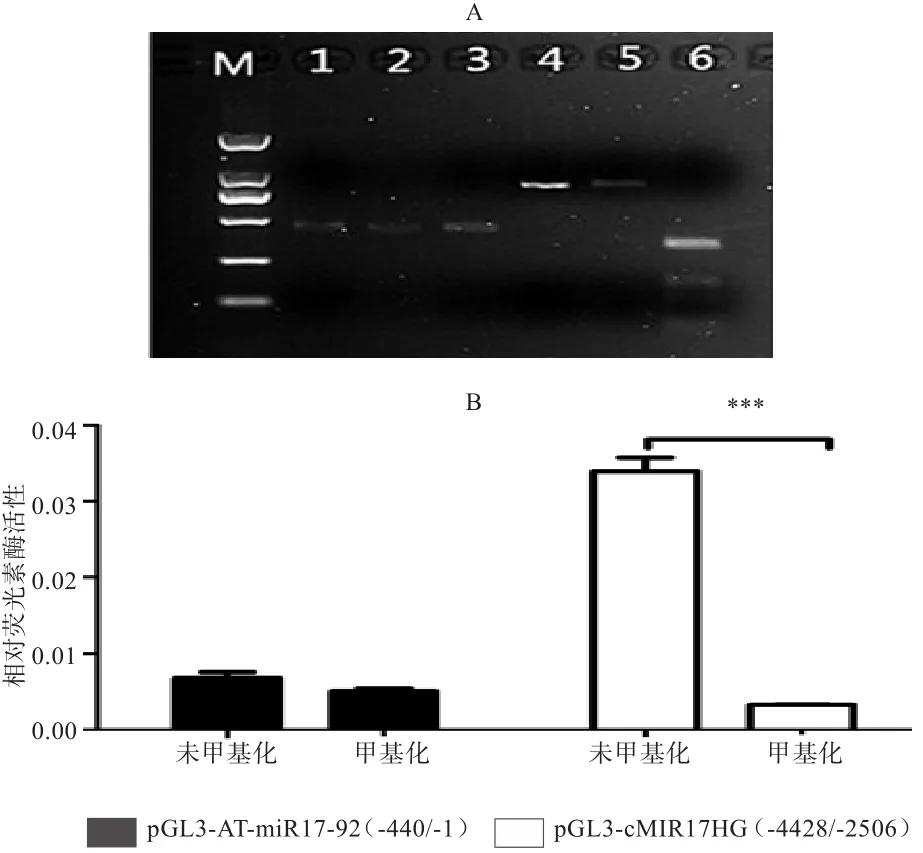
图6 DNA甲基化对MⅠR17HG启动子活性的影响
3 讨 论
miR-17-92基因簇在哺乳动物和鸡脂肪生成中发挥重要作用[10,12]。大量研究发现,DNA甲基化能够调控约50% miRNAs的表达,DNA甲基化的改变影响miRNA及其下游靶mRNAs的表达[3,13]。研究发现东北农业大学高、低脂鸡脂肪组织MⅠR17HG启动子区存在DNA甲基化。东北农业大学高、低脂鸡的体重没有明显差异,但是脂肪性状存在显著差异,高脂鸡的腹脂率是低脂鸡5倍以上[14-15]。 本研究发现,2周龄高、低脂鸡MⅠR17HG启动子的甲基化总体水平明显不同,且部分CpG位点的甲基化程度在高、低脂鸡间存在较大差异;3、7周龄低脂鸡MⅠR17HG启动子的甲基化总体水平与高脂鸡虽然没有明显的差异,但7周龄高、低脂鸡脂肪组织MⅠR17HG启动子也存在甲基化程度差异显著的CpG位点,提示DNA甲基化可能调控MⅠR17HG基因的表达。
有研究表明,同一组织在不同生长发育阶段其DNA的甲基化水平不同,大多数脊椎动物基因组DNA的甲基化随着年龄增加而逐渐下降[16]。与此相一致,本研究发现高、低脂鸡脂肪组织中MⅠR17HG启动子的甲基化程度也随着年龄增加而呈下降趋势。
本研究中,DNA甲基化抑制MⅠR17HG启动子的活性。目前已知启动子区DNA甲基化可导致DNA构象发生变化,从而影响转录因子与启动子的结合从而抑制基因转录或导致转录效率下降[17];另外,DNA甲基化结合蛋白(MBD/MeCP)可与启动子区的甲基化DNA序列结合,从而使转录因子无法结合,导致基因表达抑制[2]。为了揭示高、低脂鸡脂肪性状的差异,未来将采用生物信息学方法分析高、低脂鸡脂肪组织MⅠR17HG启动子区差异甲基化的CpG位点,确定可能受到影响的转录因子,并采用EMSA和ChⅠP技术验证DNA甲基化是否影响这些转录因子的结合进而导致基因表达的改变;还将采用ChⅠP技术比较分析高、低脂鸡脂肪组织MⅠR17HG启动子区DNA甲基化结合蛋白的结合情况。
4 结 论
鸡脂肪组织MⅠR17HG启动子区存在DNA甲基化,且高、低脂鸡脂肪组织MⅠR17HG启动子区的甲基化存在一定的差异。体外研究证实,DNA甲基化抑制MⅠR17HG启动子活性。
