Na2S2O·35H2O-CH3COONa·3H2O 相变储能材料的性能及改性
2018-11-15乔英钧张志宏付振海
乔英钧 ,张志宏 ,付振海 ,王 敏
(1.中国科学院青海盐湖研究所,青海西宁810008;2.青海省盐湖资源化学重点实验室;3.中国科学院大学)
水合盐相变储能材料作为一种行之有效的能源存储方式,近年来得到广泛研究。相比于其他类型的相变储能材料,水合盐相变储能材料有着相变温度低、相变潜热高以及导热系数大等优点,但同时也普遍存在过冷和相分离现象,这2个问题在很大程度上限制了水合盐相变储能材料的发展,因而也成为该领域研究的重点之一[1-3]。目前,有着更多丰富性和可控性的低共熔相变储能材料是相变储能材料的研究热点,水合盐低共熔混合物也备受关注[4]。低共熔物一大重要特征是在其融化-凝固过程中的无相分离现象,迄今已有大量的有机、无机、有机-无机低共熔相变储能材料被报道[5-6]。其中,有机低共熔物的研究相对更为广泛和深入,特别是脂肪酸类和多元醇类,其低共熔体系类型多样,也常常具有较宽的相变温度范围和较高的潜热[7]。无机低共熔物同样有其自身的优点,具有高的导热性、高的储热密度以及不可燃性等。但是针对此类材料的研究较少,且不够深入[8]。笔者选用五水硫代硫酸钠-三水醋酸钠体系,制备了有效的相变储能材料,并针对其结构和热性能做了研究,以期为此类无机低共熔相变储能材料的制备及分析工作提供指导。
1 实验部分
1.1 实验试剂
试剂:五水硫代硫酸钠、结晶乙酸钠、十水碳酸钠、焦磷酸钠、十二水磷酸氢二钠、二水硫酸钙、羧甲基纤维素,以上试剂均为化学纯。
1.2 Na2S2O3·5H2O-CH3COONa·3H2O 的制备
由该体系相图[9]可知,低共熔点出现在五水硫代硫酸钠质量分数为72%的组分,依据该配比称量试剂,在70℃下加热并搅拌,直至固相完全熔化为均匀液相。将试剂放置于室温冷却,凝固后取出粉碎,制得所需材料。此外,在加入改性剂后,需要对样品在50℃条件下超声分散20 min,确保成分均匀。
1.3 分析与表征
采用X′Pert PRO型XRD衍射仪对材料物相结构进行表征;采用Nexus 670型FT-IR光谱仪表征材料官能团结构;采用TA Q20型差式扫描量热仪对材料分析样品的热性能;利用Gaussian 09W软件进行密度泛函理论计算,基组为B3LYP/6-311++G(d,p)。
1.4 改性及热稳定性测试
通过步冷曲线选取合适的成核剂,以CMC作为增稠剂对材料进行改性。利用均匀设计方法分析成核剂与低共熔物的质量比(因素A)、CMC与低共熔物的质量比(因素B)对体系过冷度的影响。采用2因素8水平的U8*(85)均匀设计方案做冷却实验,以体系过冷度作为评价指标。冷却实验中将样品加热至50℃溶解后,置于常温下冷却,过冷度由其步冷曲线得到。对所得实验数据做拟合处理,得到回归方程并获得最优方案。
将优化改性后的材料做融化-凝固循环测试50次,对比分析其热性能变化,考察该相变储能材料的热稳定性。
2 结果与讨论
2.1 低共熔物结构研究
2.1.1 XRD分析
图 1 是 Na2S2O3·5H2O、CH3COONa·3H2O 以及Na2S2O3·5H2O-CH3COONa·3H2O(质量比为 72∶28)低共熔物的XRD衍射谱图。从图1可以看出,Na2S2O3·5H2O 中(040)、(052)、(180)等晶面以及CH3COONa·3H2O 中(110)、(-402)、(043)等晶面的特征衍射峰同样出现在Na2S2O3·5H2O-CH3COONa·3H2O低共熔物中,且衍射峰位置相吻合。这表明纯物质Na2S2O3·5H2O与CH3COONa·3H2O形成的是共晶型二元体系,其低共熔物的结构是2种纯物质结构的结合。
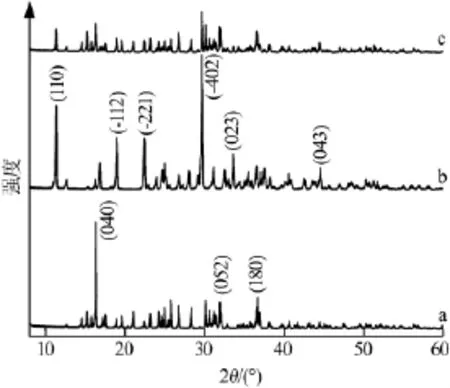
图1 Na2S2O3·5H2O(a)、CH3COONa·3H2O(b)及 Na2S2O3·5H2O-CH3COONa·3H2O(c)的 XRD 谱图
2.1.2 FT-IR分析
通常新相的形成会伴随着物相结构单元间化学键的断裂和重建,因此利用红外分析来判断低共熔物中是否形成新的键型。图2为Na2S2O3·5H2O、CH3COONa·3H2O 以 及 Na2S2O3·5H2O-CH3COONa·3H2O(质量比为72∶28)低共熔物的FT-IR谱图。从图 2a~2b 可以看到,对于 Na2S2O3·5H2O,在 1 648 cm-1和1 136 cm-1处出现的衍射峰分别对应S=O键与S—O 键的伸缩振动;对于 CH3COONa·3H2O,在1 558 cm-1和1 414 cm-1处出现的衍射峰分别对应C=O键和C—O键的伸缩振动。此外,2种纯物质都在3 440 cm-1附近出现由—OH键伸缩振动引起的衍射峰和在1 000 cm-1附近出现的—OH键弯曲振动引起的衍射峰。由图2c可知,Na2S2O3·5H2OCH3COONa·3H2O 的特征峰分别与 Na2S2O3·5H2O、CH3COONa·3H2O的特征峰相符合,这表明低共熔物中没有新类型的键型产生,参与低共熔相形成的化学键型也存在于单一体系中。
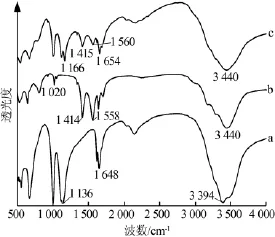
图 2 Na2S2O3·5H2O(a)、CH3COONa·3H2O(b)及 Na2S2O3·5H2O-CH3COONa·3H2O(c)的 FT-IR 光谱图
2.1.3 结构计算
为进一步探究该体系低共熔物的结构,分别对Na2S2O3·5H2O-CH3COONa·3H2O 和 Na2S2O3·5H2OCH3COONa·3H2O分子做了结构优化,结果见图3。由图3可知,O—H…O键普遍存在于Na2S2O3·5H2O分子和CH3COONa·3H2O分子之间,其平均键长为0.179 7 nm,平均键角为162.548°,属于氢键范畴。Na2S2O3·5H2O 分子和 CH3COONa·3H2O 分子中的氧原子与水分子形成氢键,直接或间接的将2种水合盐分子连接,构成了该体系的低共熔物。因此水分子的存在对低共熔物的产生具有重要作用。
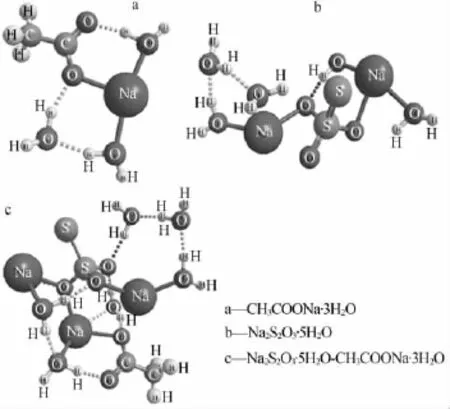
图3 分子结构优化结果(氢键用虚线连接)
2.2 低共熔物的改性
2.2.1 改性剂的选取
Na2S2O3·5H2O-CH3COONa·3H2O 体系低共熔物在放热过程中存在过冷现象,为使其成为有效的储能材料,需要在低共熔物中添加合适的成核剂。本实验选取了 Na2S2O3·5H2O与 CH3COONa·3H2O单独作为相变储能材料时常用的4种成核剂:Na2CO3·10H2O、Na4P2O7·10H2O、Na2HPO4·12H2O 以及 CaSO4·2H2O,利用冷却实验对比选出该低共熔体系的成核剂[10-11]。图4为实验所得步冷曲线。从图4可以看出,添加Na2CO3·10H2O的样品过冷度最小,因此选取Na2CO3·10H2O为低共熔体系成核剂。此外,为使成核剂分散均匀,需添加CMC来增加材料黏度,防止内部沉淀。
2.2.2 改性剂用量的优化
表1为改性剂用量优化实验的均匀设计方案及结果,质量比选取在0~3%内,过冷度由步冷曲线获得。采用多元非线性回归方程来拟合因素与指标之间的关系,利用后退法进行回归计算,建立回归方程:
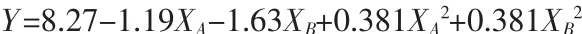
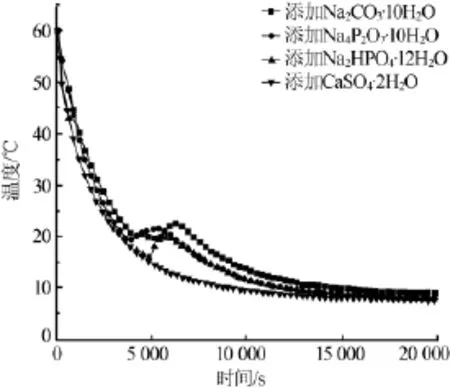
图4 添加不同成核剂后材料的步冷曲线
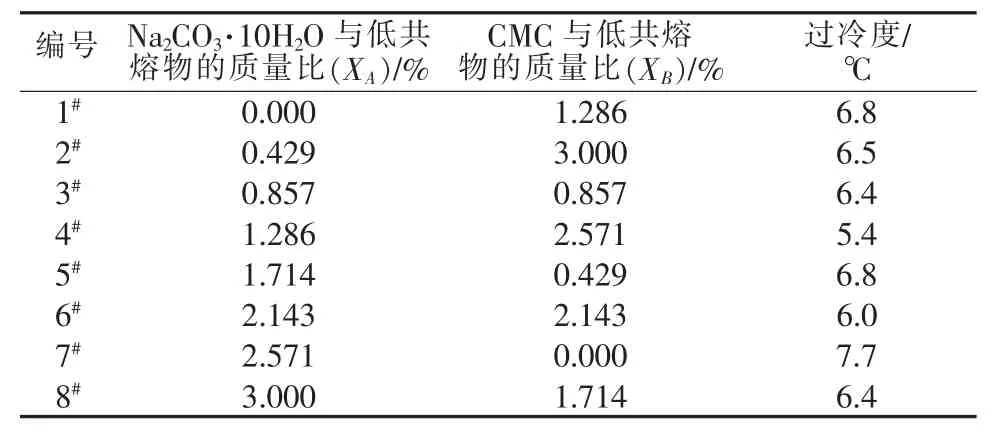
表1 优化实验的均匀设计方案
从Y的相关系数可知,均匀设计结果与二次回归模型吻合较好(复相关系数R=0.968 9),表明该模型回归效果较好。求解该二次回归方程,得到因素A为1.558%、因素B为2.136%时制备的Na2S2O3·5H2OCH3COONa·3H2O低共熔材料的过冷度最小。根据二次回归方程计算的预期目标最小值为4.81℃。优化改性前后的低共熔材料的步冷曲线见图5。由图5可见,未经改性的低共熔物在常温下不结晶,优化改性后的低共熔物过冷度为4.9℃,与优化期望值相符。
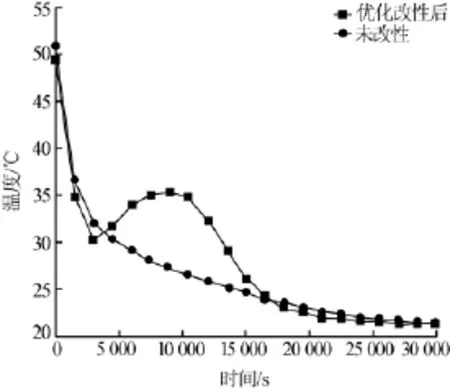
图5 优化改性前后Na2S2O3·5H2O-CH3COONa·3H2O低共熔相变材料的步冷曲线
2.3 热稳定性分析
将优化后的材料做熔化-凝固循环实验,循环50次后,未出现相分离现象。对循环前后的材料做DSC分析,结果见图6。由图6可知,相变温度由循环前的40.13℃变为40.04℃,相变潜热值从189.7 J/g变为184.5 J/g,最大偏差为2.7%。表明该材料有较好的稳定性,可以作为相变储能材料。
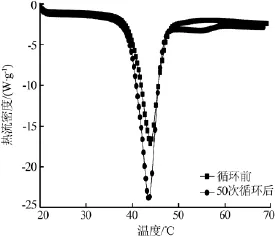
图6 循环50次前后材料的DSC曲线
3 结论
Na2S2O3·5H2O-CH3COONa·3H2O 所形成的是共晶型二元体系,该体系低共熔物的结构基于纯物质Na2S2O3·5H2O 和 CH3COONa·3H2O 的结构, 通过其中的水分子,以O—H…O键直接或间接地结合在一起。为解决该体系低共熔物的过冷问题,选取了Na2CO3·10H2O作为成核剂,CMC作为增稠剂。利用均匀设计优化后确定Na2CO3·10H2O与CMC的最优用量(质量分数)分别为1.558%和2.136%,优化改性后的低共熔材料过冷度为4.9℃,符合优化预期。经过熔化-凝固循环50次后,材料熔化温度稳定在40℃左右,熔化潜热为184.5 J/g。表明该体系低共熔物有作为相变储能材料的潜力,并且其相变温度可以弥补水合盐类相变储能材料在该温度范围内的空缺,可以应用于工业余热回收及太阳能储热等领域。
