胸腺肽辅助治疗糖尿病合并肺结核的临床疗效及安全性评价
2018-11-15汪成琼李娜娜王永梅
汪成琼,李娜娜,王永梅,胡 洋,肖 政,陈 玲
(1.遵义医学院附属医院 呼吸内科,贵州 遵义 563099;2.遵义医学院附属医院循证医学中心暨循证医学教育部网上合作研究中心遵义医学院分中心,贵州 遵义 563099;3.遵义医学院 药学院2014级药学专业本科生,贵州 遵义 563099)
近年来糖尿病并肺结核发病呈现上升趋势,成为当前重大公共卫生问题[1-2]。糖尿病为继发性肺结核的重要发病因素,结核中毒症状及抗痨药物能干扰糖代谢而加重糖尿病,进而加剧免疫功能紊乱,削弱抗感染免疫力,结核易感性增加,形成糖尿病高血糖—免疫功能紊乱—肺结核—糖尿病的恶性循环圈。糖尿病并肺结核治疗难度大,抗结核治疗失败率高,且预后差[2-4],因此如何矫正免疫功能紊乱的恶性循环状态,是成功治疗糖尿病并肺结核的难点和关键点。胸腺肽是由胸腺组织分泌的小分子多肽,可上调非特异性细胞免疫功能而提高抗感染免疫。其衍生制剂包括胸腺肽α1及胸腺五肽等,常被用于细菌或病毒感染性疾病[5-8]。有研究[9-12]报告胸腺肽辅助化疗单纯性及耐药肺结核,能提高菌转阴率,改善病灶吸收及空洞闭合等。但胸腺肽辅助化疗糖尿病并肺结核,能改善临床疗效吗?在研究[13-15]报告胸腺肽辅助化疗糖尿病并肺结核,能提高患者痰菌转阴率并改善临床症状,但纳入研究样本量小,其临床疗效评估不足,因此其疗效依然不清楚。临床实践中,胸腺肽包括胸腺肽α1及胸腺五肽等药物,用药时间差异极大,最佳时间也不清楚。因此,本研究系统评价胸腺肽类药物辅助化疗糖尿病并肺结核相关文献,揭示其临床疗效、安全性及最佳用药时间,为临床合理用药提供证据。
1 资料与方法
依据PRISMA标准实施本研究,纳入研究资料为已发表文献,因此无需伦理学审查。
1.1 检索策略 采用主题词与自由词构建检索式;由两名检索员(汪成琼与李娜娜)独立地计算机检索中英文数据库,辅以手工检索相关专业期刊,根据检索结果修正完善检索策略,尽可能全面搜集相关文献。检索词包括“糖尿病、DM、结核、TB、胸腺肽、胸腺五肽、胸腺素、胸腺多肽、胸腺刺激素、胸腺体液因子、胸腺生成素、胸腺喷丁、PEG-Tα1、diabetes mellitus、diabetes insipidus、DM、tuberculoses、tuberculosis、pulmonary tuberculosis、TB、Koch Disease、Kochs Disease、Koch's Disease、thymosin、thymopentin、thymopoietin pentapeptide、timunox、thymosins、thymalfasin、thymopolypeptides、thymostimulin、thymulin、thymopetidum、thymopeptides、thymopeptide、thymopoietin、thymic humoral factor、prothymosin、thymic polypeptide、thymopoietin polypeptide、thymins、polyethylene glycol thymosin alpha1、PEG-Tα1、active thymus factor、thymustimulin、thymic factor、thymulin、serum thymic factor、thymuline、nonathymulin、thymic serum factor、thymopoietins”;中英文数据库包括中国生物医学文献数据库(CBM)、中国知网(CNKI)、万方(Wanfang)、Web of Science(ISI)、Pubmed、Embase (建库-2017年10月20日)及Cochrane Library临床试验注册数据库(CENTRAL,2017年第10期)。
1.2 纳入与排除标准 纳入标准:①糖尿病合并肺结核(符合糖尿病和肺结核的诊断标准),无严重心、肝、肾疾患,无合并其它免疫功能低下性疾病,近3个月未接受免疫抑制剂治疗;②干预措施为胸腺肽或衍生制剂;试验组:胸腺肽联合化疗组;对照组:单纯化疗组,包括异烟肼、利福平、吡嗪酰胺、乙胺丁醇及链霉素等联合构建的化疗方案;③结局指标包括痰菌转阴、病灶吸收、空洞闭合及药物不良反应;④研究设计为随机对照试验,包括报告“随机”二字的所有研究。排除标准:①重复文献;②无详细数据的成果、会议摘要及普通综述;③无关研究包括非糖尿病并肺结核及非胸腺肽治疗研究;④非随机对照研究;⑤未被CBM收录的刊物;⑥无痰菌转阴、病灶吸收、空洞闭合及药物不良反应指标文献。
1.3 疗效评价指标 依据1982年全国结核病学术会议修订的标准[16]判定疗效:①痰菌转阴:连续2个月痰菌阴性,且不再复阳;②病灶吸收;病变范围以所有X线/CT表现病灶相加后所占肺野数计算;病灶吸收包括完全吸收、显著吸收和吸收;完全吸收:病灶完全吸收;显著吸收:病灶吸收面积≥原病灶1/2;吸收:病灶吸收面积<原病灶1/2;③空洞闭合:空洞闭合或阻塞闭合。采用白细胞或血小板减少、胃肠道反应及肝功能损害等评价药物安全性。
1.4 纳入研究的方法学质量评价 采用Cochrane RCT研究的偏倚风险评估工具(5.1.0版)[17]评价纳入研究方法学质量。评价指标包括:①随机序列的产生方式;②分配方案的隐藏;③盲法实施(对受试者,实施者及结果测评者);④随访是否完整;⑤选择性报道结果;⑥其他偏倚来源评价(试验与对照组间基线是否具有可比性)。
1.5 文献筛选与质量评价 由两名评价员(李娜娜与胡洋)根据纳入、排除标准及质量评价标准,独立筛选及评价文献,筛选与评价中的分歧与第三方(陈玲)讨论解决。
1.6 资料提取 依据PICO原则(P:研究对象;I:干预措施;C:研究对照;O:研究结果)设计资料提取表格,由两名评价员(汪成琼与王永梅)独立提取数据。提取数据包括文献出处、研究地域、社会人口学特征、试验组及对照组病例数,药品名称、剂量、用药时间、疗程及用药路径,治疗时间,痰菌转阴、病灶吸收及空洞闭合等主要结局指标;白细胞或血小板减少、胃肠道反应、肝功能损害、皮疹及关节疼痛等药物不良反应。
1.7 统计分析 采用RevMan 5.3进行Meta分析,二分类变量采用相对危险度(Relative risk,RR)及其95%CI进行描述。采用χ2检验各研究间统计学异质性,如I2<50%为异质性较低或异质性可接受,如I2≥50%则为异质性较高;对临床疗效指标,按照整体低估临床疗效策略,均采用随机效应模型合并指标[18];不能低估不良反应,因此根据异质性高低采用不同的效应模型进行评估,如无统计学异质性或异质性可接受(I2<50%)则采用固定效应模型进行合并,反之则采用随机效应模型合并;纳入超过10个研究,采用漏斗图分析发表偏倚,并判断高估、低估及有无偏倚风险。
2 结果
2.1 文献检索及筛选结果 共检索207条文献记录(见图1),阅读题目排除重复文献,纳入110篇;阅读摘要排除会议摘要、成果、综述,纳入58篇全文;阅读全文排除病例对照、无结果指标研究等,最终纳入符合标准的41个RCT[14-15,19-57]。
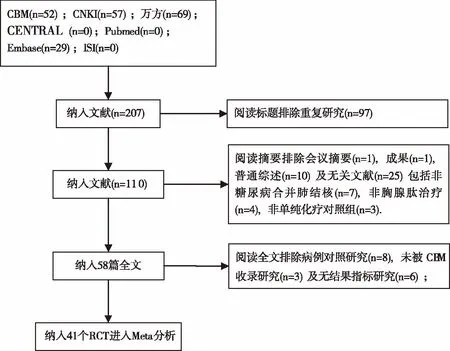
图1 纳入研究检索结果及筛选流程图
2.2 纳入研究基本特征 纳入来自广东、河北及天津等21个省市2000~2017年间发表的41个RCT (见表1)。纳入4 002例糖尿病并肺结核患者,年龄为16~88岁;试验组2 012例;对照组1 990例。胸腺肽类药物包括胸腺肽、胸腺肽α1及胸腺五肽;21个研究[14-15,30,33-37,39-40,42,44-45,49-55,57]报告使用胸腺α1联合化疗,各有10个研究报告使用胸腺肽联合化疗[19-23,25-26,29,43,48]及胸腺五肽联合化疗[24,27-28,31-32,38,41,46-47,58]。胸腺肽α1常用剂量为1.6 mg/次,2次/周,皮下注射3~6月;胸腺肽为10~80 mg/d,1次/d,静脉滴注或肌肉注射治疗1~18月;胸腺五肽为1~2 mg/次,1次/2 d,静脉滴注或肌肉注射1~6月。化疗方案为异烟肼+利福平+吡嗪酰胺+乙胺丁醇(链霉素)强化治疗2~3月,异烟肼+利福平(吡嗪酰胺+乙胺丁醇)巩固治疗4~10月[2-3HRZE(S)/4-10HR(ZE)]。采用痰菌转阴、病灶吸收及空洞闭合等评价临床疗效;采用粒细胞减少、胃肠道反应、肝功能损害等指标评价安全性。
表1纳入研究基本特征

文献出处地区研究对象试验对照男女年龄干预措施试验组药物剂量/疗程,给药方式对照组治疗时间研究指标O1O2O3 卢水英2000[19]广东3530501538~67胸腺肽60mg/qd/9M,ivggt/imHRE,9M9个月O1-史慧敏2002[20]河南 4341642035~76胸腺肽40mg/qd/9M,ivggt3HRZS/9HR9个月O1--向娥2006[21]湖北4640473935~65胸腺肽80mg/qd/6M,ivggt2HRZ/4HR6个月O1O2O3骆欢2009[22]广东4036463042~84胸腺肽100mg/qd/1M,ivggtHRZES 9-12M1个月O1O2O3于晶2009[23]吉林5147762231~65胸腺肽80mg/qd/6M,ivggt2HRZ/4HR6个月O1O2O3刘俊婷2010[24]辽宁4848603634~70胸腺五肽2mg/qod/3M,im2HRZE(S)/4HR3个月O1O2-刘卫民2010[25]新疆88871165935~69胸腺肽40mg/qd/6M,ivggt/im左氧+化疗6个月O1-O3周鸿雁2011[26]云南4242493532~74胸腺肽40mg/qd/9M,-3HRZE/6HRE9个月O1O2O3杜永国2012[27]海南1081081417535~77胸腺五肽1mg/qod/2M,im2HRZE(S)/7HR2个月O1O2-王爱辉2012[28]河北6060685230~72胸腺五肽1mg/qd/2M,ivggt/imHRZES6个月O1O2-徐梯2012[29]浙江4544632660~87胸腺肽15mg/qd/1M,imHRE1个月O1O2O3杨朝晖2012[30]浙江4849653216~69胸腺肽α11.6mg/biw/3M,ih2HRZE/4HR3个月-O2-李娜2013[31]山东4343523442~80胸腺五肽1mg/qod/1M,im2HRZE(S)/7HR1个月O1O2-王爱辉2013[32]河北8080946630~72胸腺五肽1mg/qd/2M,im/ivggtHRZES2个月O1--高香平2014[33]山西4849653216~69胸腺肽α11.6mg,1次/2W,3M,ih2HRZE/4HR3个月-O2-刘纯钢2014[34]湖北38385422-胸腺肽α11.6mg/biw,6M,ih2HRZE/4HR6个月O1O2O3刘建春2014[35]河北4743434742~66胸腺肽α120mg/qd/3M,ih2HRZE/4HR3个月O1O2O3刘鹏霄2014[36]河南4444563220~72胸腺肽α11.6mg/biw/6M,ih2HRZE/4HR6个月O1O2-王典2014[37]河南3030352515~69胸腺肽α11.6mg/biw/3M,ihHRZE3个月-O2-王彦芹2014[38]山东86861046852~77胸腺五肽1mg/qod/1M,im2HRZE(S)/7HR1个月-O2-张汉2014[39]广东4545543616~72胸腺肽α11.6mg/biw/3M,ih2HRZE/4HR3个月-O2-赵坚峰2014[40]浙江4545---胸腺肽α11.6mg/biw/6M,ih2HRZES/4HRZE6个月O1--董璇2015[14]湖北2727302460~75胸腺肽α11.6mg/biw/6M,ih2HRZES/1HRZE/5HRZE6个月O1-O3郭文霞2015[41]河北75757971-胸腺五肽1mg/qd/2M,ivggtHRZES2个月O1--李清旺2015[42]天津5757555920~73胸腺肽α11.6mg/biw/6M,ih2HRZE/4HR6个月-O2-司果2015[43]四川35405025-胸腺肽10mg/qd/6M,im2SHRZE/1HRZE/5HRE6个月O1O2-王玉莲2015[44]黑龙江3535---胸腺肽α16MHRZE6个月-O2-薛峰2015[45]甘肃5050693132~59胸腺肽α11.6mg/biw/3M,ih2HRZE/4HR3个月O1--杨忠2015[46]湖南5454604819~72胸腺五肽1mg/qod/2M,imHRZES2个月O1O2-钟殿海2015[47]黑龙江6161655735~71胸腺五肽1mg/qd/2M,ivggt 3HRZE/6HRE2个月O1--钟焕华2015[48]广东12012012211835~75胸腺肽40mg/qd/4M,po2HRZE/10HR4个月O1--周耀南2015[49]广西5050604020~71胸腺肽α11.6mg/biw/3M,ih2HRZE/4HR3个月-O2-邓雯秋2016[50]四川4242493531~88胸腺肽α11.6mg/biw/3M,ih2HRZE/4HR3个月-O2-李沛军2016[51]青海5555694118~69胸腺肽α11.6mg/biw/3M,ih2HRZE/4HR3个月-O2-刘常路2016[52]天津2525292120~73胸腺肽α11.6mg/biw/6M,ih2HRZE/4HR6个月O1O2-吕月秋2016[53]辽宁3433412621~72胸腺肽α11.6mg/biw/6M,ih2HRZ(E)S/4HR6个月O1O2O3彭晔2016[54]内蒙古3535412946~79胸腺肽α11.6mg/biw/6M,ihHRZE6个月-O2-宋立彬2016[55]辽宁2525302021~65胸腺肽α11.6mg/biw/6M,ih2HRZE/4HR6个月-O2-杨丽2016[56]新疆6564597042~65胸腺五肽1mg/qod/6M,im2HRZE/4HR6个月-O2-朱洪坤2016[57]江苏2626282434~72胸腺肽α11.6mg/biw/6M,ihHRZE6个月-O2-蒋红球2017[15]吉林3131392353~79胸腺肽α11.6mg/biw/3M,ih2HRZE/4HR3个月O1O2O3
qd:1次/d;qod:隔日1次;biw:每周两次;ivggt:静脉滴注;im:肌注;ih:皮下注射;po:口服;O1:痰菌转阴;O2:病灶吸收;O3:空洞闭合;HR:异烟肼+利福平;HRE:异烟肼+利福平+乙胺丁醇;HRZE:异烟肼+利福平+吡嗪酰胺+乙胺丁醇;HRZES:异烟肼+利福平+吡嗪酰胺+乙胺丁醇+链霉素;-:不清楚。
2.3 纳入研究质量评价 纳入41个RCT(见图2),仅15个研究[15,31,33-35,37,38,40-43,48,51,52,57]报告采用随机数字表法产生随机序列;所有研究均未描述分配方案是否隐藏、盲法实施情况;纳入研究均无失访,数据完整,且无选择性报道结果;仅2个研究[20-21]基线不清楚,其余研究基线均具有可比性。
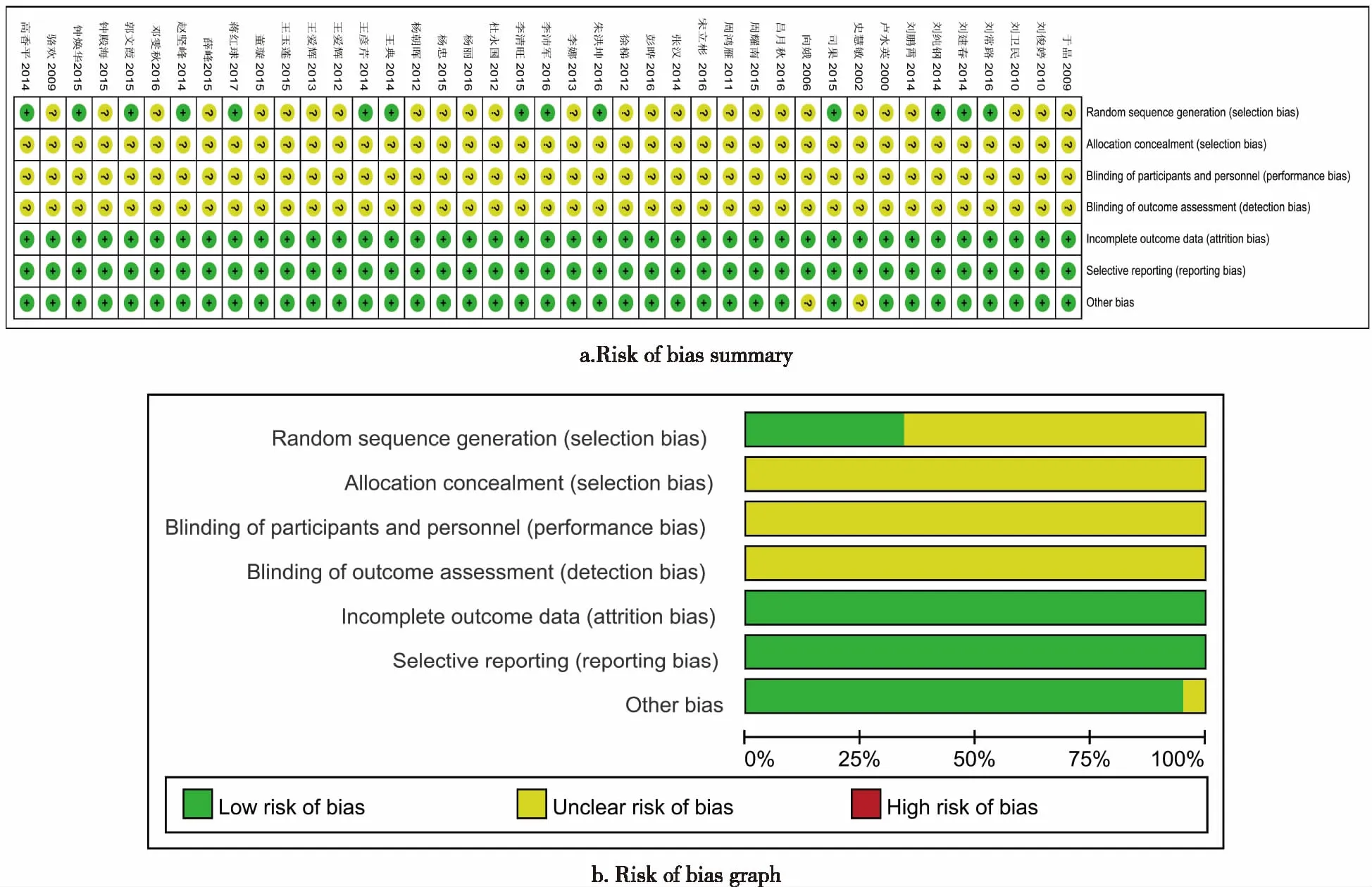
图2 纳入研究偏倚风险评价
2.4 临床疗效评价 参照1982年全国结核病防治会议疗效评定标准,采用痰菌转阴、病灶吸收及空洞闭合评价临床疗效;因治疗时间为临床异质性的主要来源,因此依据不同治疗时间实施亚组分析,探讨不同治疗时间对临床疗效的影响。
2.4.1 痰菌转阴 纳入25个研究[14,15,19-26,28,29,31,
32,34-36,40,41,43,46-48,52,53]2 491例患者报告痰菌转阴,随机效应模型Meta分析结果表明胸腺肽辅助化疗能显著提高患者痰菌转阴率[RR=1.31,95%CI(1.24,1.38),P<0.000 01]。亚组分析结果表明胸腺肽辅助化疗1、2、3、6个月,其痰菌转阴合并效应值分别为1.47,95%CI(1.26,1.72)、1.26,95%CI(1.15,1.37)、1.32,95%CI(1.12,1.57) 和1.33,95%CI(1.22,1.45),在两组间均有统计学差异(见图3)。
2.4.2 病灶吸收 纳入33个研究[15,19,21-24,26-31,
33-39,42-46,48-52,54-57]3 200例患者报告肺部病灶吸收,随机效应模型Meta分析结果表明胸腺肽能显著提高患者肺部病灶吸收[RR=1.25,95%CI (1.18,1.32),P<0.000 01]。亚组分析结果表明胸腺肽辅助化疗1、2、3、6个月,其肺部病灶吸收合并效应量分别为1.36,95%CI(1.14,1.61)、1.39,95%CI(1.15,1.69)、1.26,95%CI(1.18,1.33) 和1.17,95%CI(1.06,1.28),在两组间均有统计学差异(见图4)。

图3 联合化疗与单纯化疗比较痰菌转阴的Meta分析
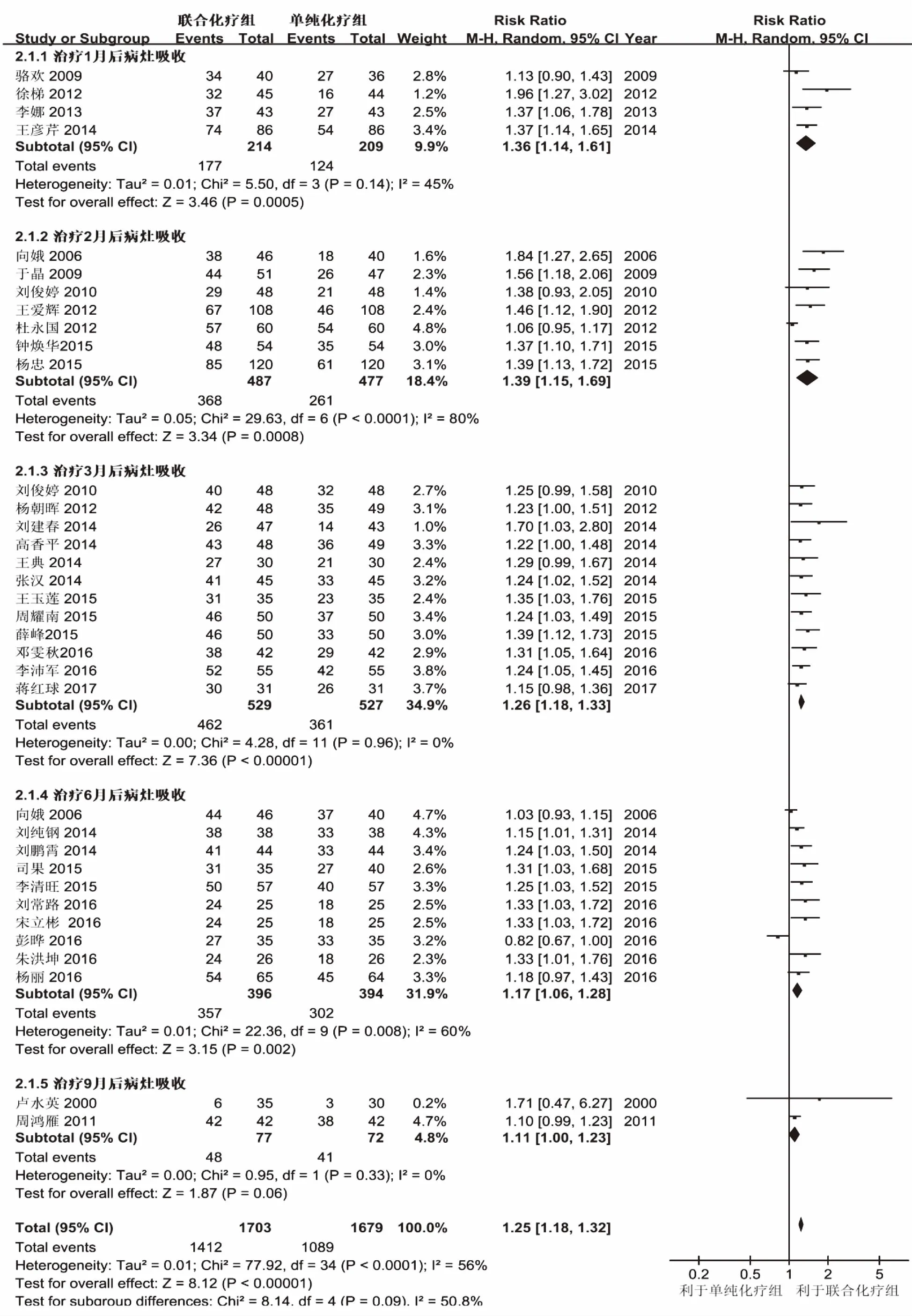
图4 联合化疗与单纯化疗比较病灶吸收的Meta分析
2.4.3 空洞闭合 纳入11个研究[14,15,21-23,25,26,29,
34,35,53]957例患者报告空洞闭合率,随机效应模型Meta分析结果表明胸腺肽能显著改善肺部空洞闭合[RR=1.60,95%CI(1.22,2.10),P=0.000 6]。亚组分析结果表明胸腺肽辅助化疗1和9个月,其肺部病灶吸收合并效应量分别为2.18,95%CI(1.35,3.53)和7.67,95%CI(2.49,23.60),在两组间均有统计学差异(见图5)。

图5 联合化疗与单纯化疗比较空洞闭合的Meta分析
2.5 不良反应 纳入41个研究,9个研究[14,19,21,24,26,27,31,35,43,48,53]报告白细胞减少、血小板减少、肝功能损害、胃肠道反应(恶心、呕吐、腹胀)、皮疹、关节疼痛等不良反应。异质性均可接受(I2≤50%),采用固定效应模型合并胃肠道反应、肝功能损害、皮疹合并效应量,对白细胞减少、血小板减少、关节疼痛采用森林图的方式进行展示完整数据展示。结果显示白细胞减少、血小板减少、胃肠道反应、肝功能损害、皮疹及关节疼痛发生风险在两组间无统计学差异(见图6)。

图6 联合化疗与单纯化疗比较不良反应的Meta分析
2.6 发表偏倚分析 在痰菌转阴、病灶吸收及空洞闭合等Meta分析中,纳入超过10个研究,故采用漏斗图判断发表偏倚(见图7)。结果痰菌转阴漏斗图中有2个研究[23,48]位于倒漏斗左外侧和1个研究[20位于倒漏斗右外侧,提示痰菌转阴有高估有低估;病灶吸收有四个研究[21,26-27,54]位于倒漏斗左外侧,提示病灶吸收被低估;空洞闭合有两个研究[14,23]位于倒漏斗左外侧,提示空洞闭合被低估。
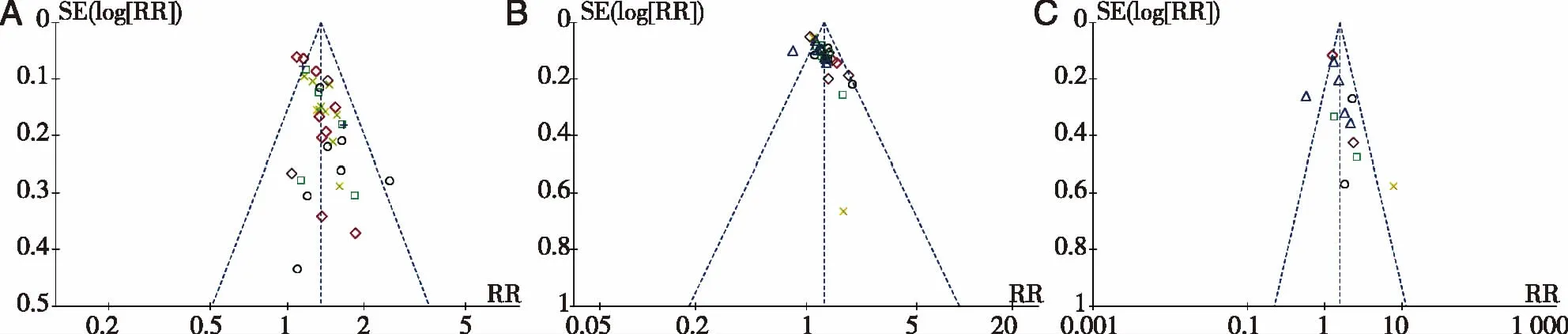
○治疗1月后痰菌转阴;□治疗3月后痰菌转阴;+治疗9月后痰菌转阴:◇治疗2月后痰菌转阴;×治疗6月后痰菌转阴。A.痰菌转阴;B.病灶吸收;C.空洞闭合。图7 发表偏倚分析
3 讨论
本研究纳入国内21个省市2000~2017年间发表的41个RCT[14,15,19-57],4 002例糖尿病并肺结核患者,年龄为16~86岁;干预措施包括胸腺肽α1、胸腺肽及胸腺五肽;胸腺肽α1常用剂量为1.6 mg,2次/周,皮下注射3~6月;胸腺肽为40~80 mg,静脉滴注或肌肉注射2~3月;胸腺五肽为1~2 mg,隔日1次,静脉滴注或肌肉注射1~6月;结果表明不同类型胸腺肽,其用药剂量相对稳定,但用药时间差异较大,存在临床异质性。采用痰菌转阴、肺部病灶吸收、空洞闭合及不良反应评价胸腺肽辅助化疗后的疗效及安全性。
胸腺肽是重要的免疫反应调节剂,广泛应用于辅助治疗各种慢性感染性疾病[13,58-61]。辅助化疗糖尿病并肺结核能否有效提高临床疗效,目前无有力证据予以证实。本研究纳入25个RCT[14,15,19-26,28,29,31,32,34-36,40,41,43,46-48,52-53]2 491例患者评估胸腺肽能否改善痰菌转阴率,Meta分析结果表明胸腺肽辅助化疗能显著提高患者痰菌转阴率,提示胸腺肽能提高结核杆菌清除率,但其治疗时间存在临床异质性,故采用亚组分析揭示不同治疗时间对痰菌转阴率的影响,探索最佳治疗时间。亚组分析结果表明胸腺肽辅助化疗1、2、3及6月后均能提高痰菌转阴率。Meta分析中,纳入研究数量及样本量能满足评价,且采用随机效应模型低估合并值;但大部分研究的方法学偏倚风险不清楚,这削弱了研究结局的可靠性。因此本研究认为胸腺肽辅助化疗可能提高痰菌转阴率。本研究纳入33个RCT[15,19,21-24,26-31,33-39,42-46,48-52,54-57]3 200例患者评价胸腺肽辅助化疗能否改善患者治疗后病灶吸收。结果表明胸腺肽能改善肺部病灶吸收,而进一步亚组分析结果揭示治疗1、2、3及6月均能改善肺部病灶吸收;纳入11个RCT[14,15,21-23,25,26,29,34,35,53]957例患者评估空洞闭合率,表明胸腺肽能提高空洞闭合率;亚组分析结果揭示仅治疗1、9月能提高空洞闭合率。综合研究结果表明胸腺肽能提高痰菌转阴、病灶吸收和空洞闭合率,且仅治疗1个月即可改善上述指标。相关研究报道[62]胸腺肽辅助化疗耐多药肺结核,能显著提高痰菌转阴率,同时改善肺部病灶吸收和空洞闭合;另有余国平等研究[63-64]报告胸腺肽α1辅助治疗老年单纯性肺结核,能显著提高痰菌转阴,以上研究结论间接支持胸腺肽辅助化疗能提高糖尿病并肺结核患者的痰菌转阴率,改善其病灶吸收和空洞闭合。另外,胸腺肽为高成本药品,亚组分析结果揭示仅治疗1月均可能改善痰菌转阴、病灶吸收及空洞闭合,如能证实仅治疗1个月即能显著提高患者临床疗效,这将大大降低治疗成本,但该结论尚需深入研究予以证实。
相关研究表明[61,65-66]胸腺肽辅助化疗晚期肺癌、单纯性肺结核、COPD急性加重期,也未增加不良反应风险。本研究纳入9个RCT[14,21,24,26,27,31,35,43,53]报告药物不良反应,Meta及描述性分析表明白细胞和血小板减少、胃肠道反应、肝损害、皮疹及关节疼痛在胸腺肽联合化疗与单纯化疗间无统计学差异,提示胸腺肽辅助化疗尚未增加药物不良反应风险。但纳入研究数量及样本量小,且纳入大部分研究偏倚风险不清楚,可能导致低估治疗风险,因此该结论尚需高质量证据予以证实。
本研究局限性:①本研究未检索非英及非中文数据库,可能存在潜在的语言偏倚;②纳入大部分研究偏倚风险不清楚,尤其未清楚描述随机分配方法、分配方案隐藏及盲法实施;③本研究纳入胸腺肽、胸腺肽α1及胸腺五肽3种胸腺肽类药物,其疗效可能存在差异,尚需进一步研究予以揭示。
综上表明胸腺肽辅助化疗糖尿病并肺结核可能提高痰菌转阴率,改善病灶吸收及空洞闭合,且未增加血液、胃肠道等不良反应风险。仅治疗1月即可改善痰菌转阴、病灶吸收及空洞闭合,提示其治疗1个月可能为有效治疗时间。然而不同胸腺肽间的疗效差异,其剂量、疗程与疗效的关系依然不清楚,且大部分研究偏倚风险不清楚。因此其疗效差异、安全性、最佳剂量及治疗时间等尚需的大样本规范性研究予以证实。
