锌铝水滑石材料的合成及其电化学性能
2018-10-31赵宇杨玉彬徐冰于越李竹馨迟立萍
赵宇,杨玉彬,徐冰,于越,李竹馨,迟立萍
(大连交通大学 辽宁省新能源电池重点实验室,辽宁 大连 116028)*
0 引言
超级电容器作为新型储能装置,其具有高功率密度、超长寿命、温度范围广、环境友好等特点,一直是国内外电化学和能源领域里的研究热点[1- 2].各种碳材料[3]、金属氧化物及复合氧化物[4- 5]等是主要的电极材料.
近年来,二维材料在化学储能和转换研究中得到了越来越多的关注.这一类材料突出特点表现在高比表面,独特的层状结构,丰富的物理化学性能[3,6].层状双金属氢氧化物(Layered double hydroxides, LDHs),是典型的无机层状材料,由于其金属离子和层间阴离子可以较大范围调变且并不改变主体结构,活性物质在层中晶格的高分散,单层的易于分离和化学修饰,为其成为多功能电化学电极材料提供了可能,也使这一类材料在很多应用领域都得到广泛关注,如催化、吸附、能量储存和转换等[7].
本文以泡沫镍为基体,采用原位水热的方法,在泡沫镍表面生长锌铝水滑石电极材料,并对其进行了电化学性能测试,通过电极材料有序结构的形成提高其电化学活性,同时提供了一种广泛使用的原位有序复合材料的合成方法.
1 材料与方法
1.1 材料制备过程
将泡沫镍在乙醇溶液中浸泡15 min去除油渍,并用去离子水清洗.放入0.1 mol/L的HCl溶液中浸泡15 min后去离子水反复冲洗至中性, 80℃烘干备用.
采用水热反应制备ZnAl-LDHs,硝酸锌0.375 mmol,硝酸铝0.075 mmol,氢氧化钠、碳酸钠加入总量为离子摩尔数的5倍,保持碳酸钠总量为2 mmol,将以上物质溶于36 mL去离子水中,转入50 mL水热釜,加入1.5 mm×1.5 mm预处理后泡沫镍,于80~120℃恒温12 h,反应结束后取出水洗至中性,60℃干燥过夜,样品记为hydro-LDHs-T,T为水热反应温度;与其对比,80℃共沉淀法4 h合成产物标记为co-LDHs.
1.2 材料表征
采用JEOL TEM 2000EX型透射电镜(TEM)和JEOLJEM-6360LV扫描电镜(SEM)进行形貌分析;采用荷兰PAN Analytical公司的X’pert ProSuper型射线衍射仪上进行晶相组成分析(XRD),铜靶线为光源(λ=1.543 2 nm),石墨单色器,管电压为40 kV,管电流为100 mA,晶胞参数的计算采用最小二乘法.样品的红外光谱分析(IR)在TJ270- 30A 型号傅立叶变换红外光谱仪上测定,扫描范围400~4 000 cm-1.
1.3 电化学性能评价
在6 mol/L KOH溶液中,以Pt网电极作为对电极,饱和甘汞电极(SCE)作为参比电极,ZnAl-LDH电极作为工作电极,以电化学工作站CHI 660E对LDHs电极进行测试.循环伏安测试的扫描电压范围为0~0.6 V,恒流充放电测试电压窗口为0~0.55 V.
共沉淀法制备的co-LDHs样品、乙炔黑和PTFE按质量比80∶10∶10的比例充分混合均匀后,担载到泡沫镍上,面积1.5×1.5 cm2,担载量5~8 mg.80℃真空干燥,作为对比用工作电极.
2 结果与讨论
2.1 ZnAl-LDHs的XRD分析
共沉淀产物co-LDHs的XRD测试结果如图1所示.在XRD图谱中2θ=11.64、23.39、34.56、39.15和46.64°等处出现多个衍射峰,对照标准图谱,其分别对应于水滑石结构Zn6Al2(OH)16CO3·4H2O的(003)、(006)、(012)、(015)和(018)晶面的衍射峰,与标准卡(JCPDS No.038- 0486)完全一致,说明共沉淀法合成了目标产物水滑石结构,产物晶体结构为六方晶系,层板间存在六方堆积和菱形堆积两种堆积模式,归属R-3m空间群[8],晶胞参数为a=b=3.076°,c=22.800°,α=β= 90°,γ=120°.由XRD图谱分析可知,产物特征衍射峰峰型尖锐,经计算可知,d003=0.754 nm,d006=0.378 9 nm,d003=2d006,说明层间结晶度和晶相结构良好;(110)晶面的衍射峰为LDHs阳离子层板的特征衍射峰,(113)
晶面的衍射峰为层间水分子的特征衍射峰,两者的存在说明层状结构所具有的较好的对称性.
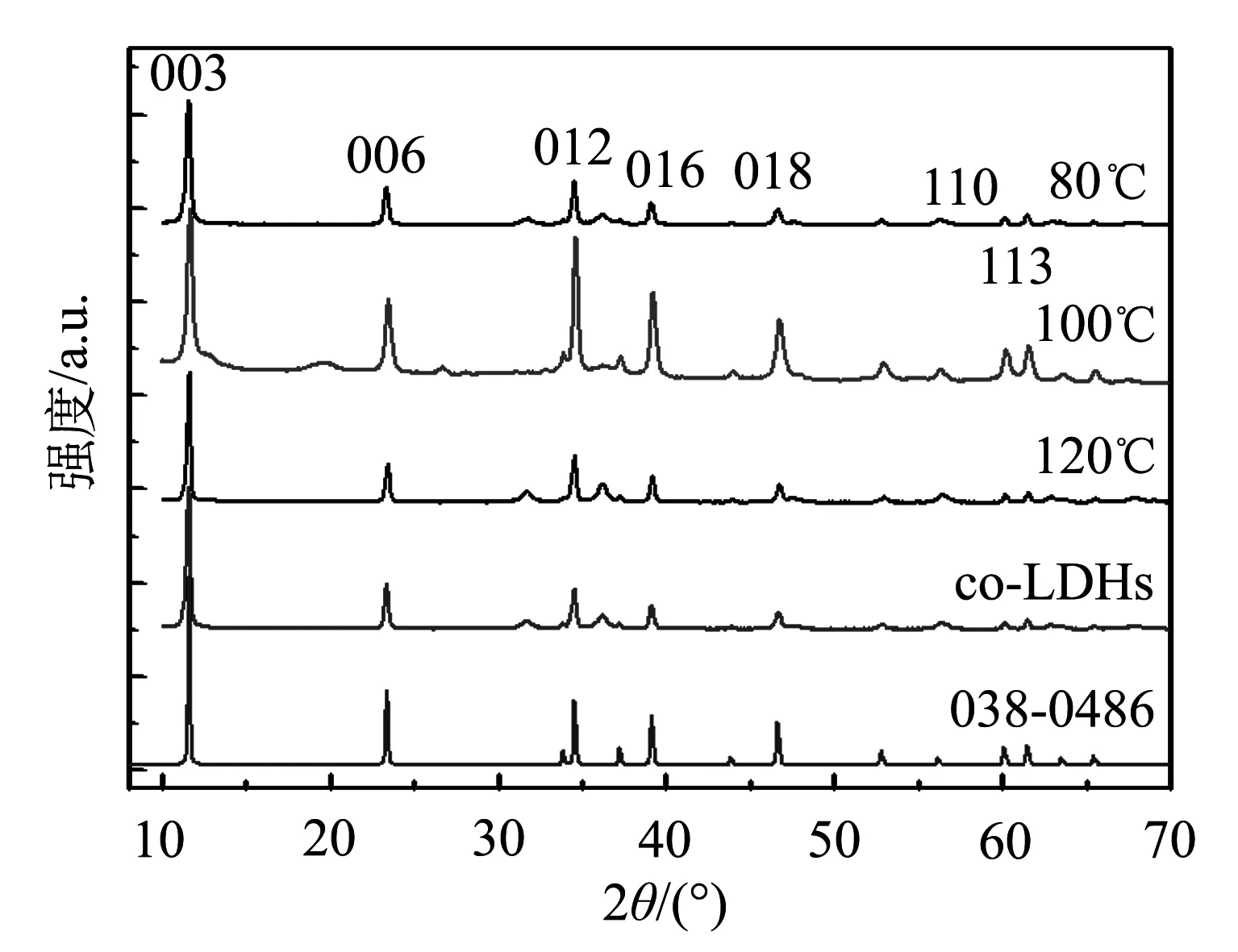
图1 ZnAl-LDHs样品的XRD分析图谱
同时可见,80~120℃水热条件下合成产物的XRD图谱与共沉淀法合成产物的XRD图谱一致,说明水热法同样合成了目标产物水滑石结构;另一方面,随着水热反应温度的升高,产物XRD图谱中各特征晶面衍射峰的峰强度并没有明显增高,说明晶粒的大小没有明显的变化;进一步计算可知80、100、120℃水热条件下d003值分别为0.758 7、0.759 8、0.757 5 nm,与共沉淀产物(d003=0.754 3 nm)基本一致,说明在水热条件下,层间距无明显变化,层间阴离子的状态及其与层板间的结合能都没有明显变化.
2.2 ZnAl-LDH结构和形貌分析
采用SEM对co-LDHs产物进行了形貌分析,结果如图2(a)所示.可以看出产物为相对均匀、形貌不规则的微纳米片状结构,微片的直径约为200~400 nm,片的厚度约为80~100 nm,这种片状结构与文献报道的水滑石的片层状结构相一致,SEM测试分析中可以看出产物无明显团聚,说明分散度较好.

(a)共沉淀(b)80℃

(c)100℃ (d)120℃
图2共沉淀法合成产物及不同水热温度下电极表面SEM图
hydro-LDHs产物微观形貌的SEM分析,如图2(b)~(d)所示.当原位水热反应温度80 ℃时(图2(b))水热产物在泡沫Ni表面呈两种状态分布,靠近泡沫Ni表面的附着层,产物料子多为正六边形薄片状,薄片直径约为500~800 nm,薄片厚度约为50~80 nm,薄片的生长方向多数沿泡沫Ni表面或小角度方向;产物的另一种分布出现在此薄层外部,这一层中粒子较小,为正六边形薄片和更小的不规则微球两种微观状态.其中,六边形薄片的直径约为200~400 nm,厚度约为10~30 nm,微球直径约为10 nm,富集在六边形薄片的表面,这一层分布的粒子相互聚集,形成分散在外层的小团簇,团簇与泡沫Ni表面有一定空隙.很显然,这一层粒子与泡沫Ni本体间结合力较小,容易从其表面脱附.
当原位水热温度逐渐升高至100~120℃时(图2(c), (d)),合成产物在泡沫Ni表面形成的外围团簇附着层明显减少,表面六边形片状附着层更加完整,与泡沫Ni表面的结合更加紧密;120℃产物相对于100℃产物厚度略有增加,直径约为300~500 nm,厚度约为10~30 nm.这说明,随着反应温度的提高,外层吸附力较小的薄片状产物或者从表面剥离,或都通过溶解再结晶过程重新参与了近表面层产物的再生长过程.通过泡沫Ni表面产物的晶体生长形貌分析,并与共沉淀合成产物相比较不难看出,泡沫Ni的存在诱导了水热产物在其表面的有序生长.
同时,这一结果通过TEM分析得到了进一步的证明(图3).如图3(a)所示,共沉淀产物为不规则片状,粒径约为200~400 nm,相互吸附形成小的团簇,而水热产物hydro-LDHs- 120(图3(b))呈现典型的正六边形片状,较小的粒子粒径约为300 nm,较大的粒子粒径可达约1 μm,这一结果与SEM表征相一致;同时,图3(b)可明显观察到六片形薄片状粒子上深度接近中心的缺口,这与图2(d)中观察到的产物片状粒子交叉自组装生长结构是一致的,图3(b)中部分非规则薄片则来自于这种交叉自组装结构在样品在测试过程中从泡沫镍表面剥离、分散过程中所产生.

(a)co-LDHs(b)hydro-LDHs- 120
图3合成产物的TEM图
2.3 合成产物的红外光谱分析
图4为ZnAl-LDHs样品的IR图谱,图中3 443、3 346和3 142 cm-1处的红外吸收峰可分别归属为LDH中Metal-OH的伸缩振动、物理吸附水或结晶水的伸缩振动[9],出现在约1 660 cm-1吸收峰可归属为层间水分子O-H的弯曲振动,1 350~1 550 cm-1处出现的吸收峰归属于O-C-O键的非对称振动,属于单齿碳酸盐基团,1 119 cm-1处出现的吸收峰归属于C-O键的伸缩振动峰,1 069 cm-1处出现的弱吸收峰归属于C-O键的对称振动,400~700 cm-1处出现的吸收峰来自于LDH结构中晶格振动,包括Zn-O、Al-O、Zn-O-Al等[10].从两种合成方法合成产物的红外光谱分析结果可以看出,产物表面官能团无明显差别.

图4 ZnAl-LDHs样品的IR图谱
3 电化学性质分析
为了研究水热合成温度,原位生长技术对ZnAl-LDHs电极电化学性能影响,对电极进行了循环伏安和恒流充放电测试.
采用三电极体系,以ZnAl-LDHs电极为工作电极,Pt网电极为对电极,饱和甘汞电极为参比电极,6 mol/L的KOH溶液为电解质溶液,进行了循环伏安测试.图5(a)将80和120℃原位水热合成电极与共沉淀法合成电极进行了扫描速度为10 mV/s的循环伏安曲线比较.可以看出,co-LDHs电极的CV曲线在约0.38 V(vs SCE)处出现了成对氧化还原峰,这表明电极呈现出典型的赝电容性质.
图5(a)中同时考察了hydro-LDHs电极在制备温度分别为80和120℃条件时产物电化学性能.可以看出,两种温度条件下合成的电极均也同样出现了成对的氧化还原峰,而且原位水热生长电极氧化还原主峰的峰电流响应值增加明显,这是由于原位生长电极表面活性LDHs组份更加规整有序的表面结构,有利于电解质溶液离子在其孔隙内的有效浸润;同时,原位生长的电极不需要加入粘结剂,这样相对于涂覆电极而言,有效减少了死体积,进一步提高了电极材料表面的利用率.
由前所述,ZnAl-LDHs是以Zn、Al两种金属氢氧化物形成的阳离子层状结构主体,电极在充电过程中,Zn(II)和Al(III)将逐步还原为低氧化态.理论分析可知,物种的标准电极电势越负,还原反应越困难.Eθb(Zn(OH)2/Zn)和Eθb(Al(OH)3/Al)分别为-1.199 V和-2.31 V(vs.SHE),因而在充电过程中,Zn(II)会优先还原.大量研究表明,在超级电容器中,Zn基氧化物、复合氧化物等电极材料,其表面氧化还原过程来自于电解质溶液中的阳离子,如K+,在氧化物、复合氧化物等电极结构中插入和脱出过程,所伴随Zn活性物质电子得失[11].
图5(b)为LDHs电极在0.5 A/g电流密度下恒电流充放电曲线和恒电流放电曲线.可以看出,电极的充放电曲线均呈现出明显的充放电平台,与循环伏安曲线明显的氧化还原峰相对应,说明电极材料在所考察的电位范围同表现出良好的法拉第赝电容特性,可逆性较好.hydro-LDHs电极表现出更长的充放电时间,说明其具有更高的比电容.
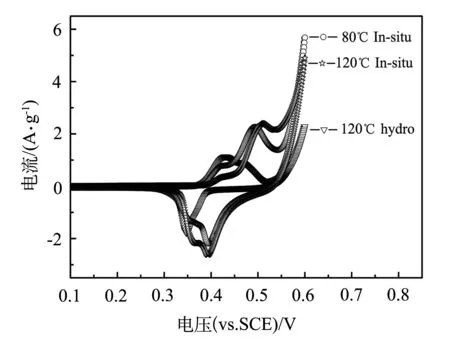
(a)循环伏安曲线
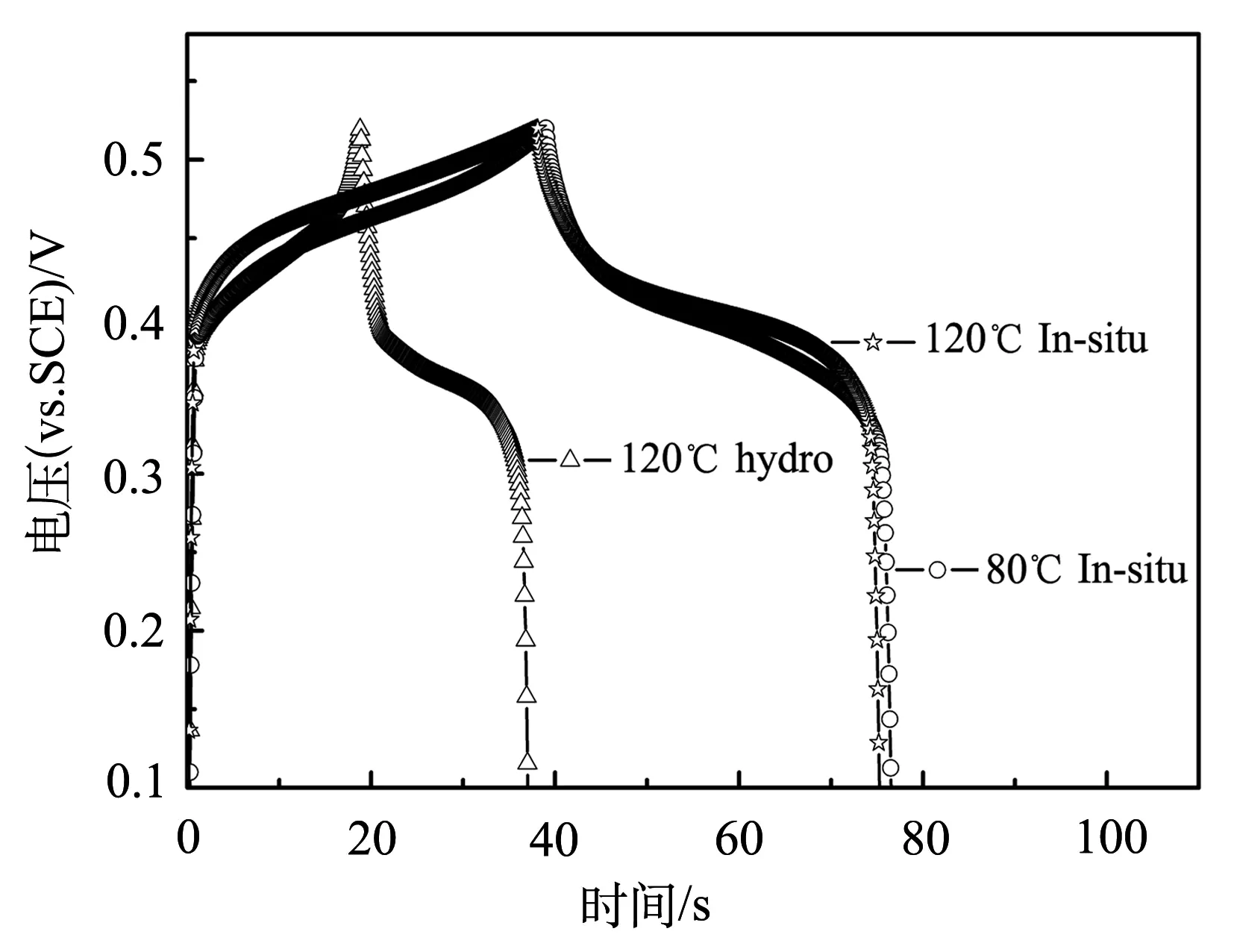
(b)恒电流充放电曲线
通过放电曲线可计算电极的比电容,计算公式如下:
C=I×t/(m×ΔV)
式中,C为电极的比电容,单位为F/g;I为充放电电流,单位为A;t为放电时间,单位为s;ΔV为充放电电压窗口,单位为V;m为电活性材料质量,单位为g.电极的比电容计算结果,在0.5 A/g电流密度下,hydro-ZnAl-LDH- 120表现了最大的比电容为84.9 F/g,比共沉淀产物电极的比电容(34.4 F/g)提高了约2.4倍.
4 结论
以NaOH和Na2CO3为沉淀剂,以多孔泡沫Ni为基体,采用原位水热的方法获得了泡沫Ni表面原位生长的hydro-ZnAl-LDHs活性材料,120℃水热条件下,泡沫Ni表面活性物质主体为靠近泡沫Ni表面方向伸展的六边形薄片,直径约为200~400 nm,厚度约为10~30 nm.电化学性能测试结果,hydro-LDHs电极本体具有一定的电化学活性,并呈典型法拉第赝电容性质,电流密度为0.5 A/g时,原位有序生长ZnAl-LDHs的比电容为84.9 F/g,是共沉淀产物电极比电容的2.4倍.
