回顾性心电门控CT肺动脉成像评估慢性肺栓塞患者右心功能及肺动脉膨胀性的价值
2018-10-30窦瑞雨杨海霞张丽君范占明
窦瑞雨 张 楠 常 星 杨海霞 张丽君 范占明
肺栓塞是最常见的三种急性胸痛相关的心血管疾病之一,约0.1% ~14.1%的急性肺栓塞进展成慢性血栓栓塞性肺动脉高压(chronic thromboembolic pulmonary hypertension,CTEPH)[1]。CTEPH是由于血栓未能完全溶解或反复的再栓塞,引起肺循环阻力升高,并长期在神经、体液等多因素作用下血管痉挛、重构,最终肺动脉压力进行性升高的一类肺血管疾病[2-3]。持续肺循环阻力增高致右心室后负荷增加,最终因右心衰竭死亡,未经治疗的CTEPH患者预后差、致死率高,平均肺动脉压力超过40mmHg(1mmHg=0.133kPa)的患者5年生存率约30%[4-5]。CT肺动脉成像(CTPA)是一种快速、无创、可复的首选诊断肺栓塞的方法,应用心电门控技术提高了图像质量,又获得右心室功能及各级肺动脉膨胀性等参数来评估慢性肺栓塞患者的病程进展及预后[5]。
资料与方法
1.研究对象 收集2017年2月至8月,于我院行CTPA检查202例,筛选出慢性肺栓塞患者(实验组): 40例(男性22例,女性18例),平均年龄(59.45±15.15)岁,正常对照组:33例(男性13例,女性20例),平均年龄(59.97±14.08)岁;体质量指数(body mass index,BMI)。实验组入选标准:已明确诊断肺栓塞(治疗/未治疗),且病程>3个月。排除标准:①碘对比剂过敏;②严重肾功能不全;③急性肺栓塞;④慢性阻塞性肺疾患、先天性心脏病肺动脉高压、特发性肺动脉高压、心脏瓣膜病变、心肌病、心肌梗死及血液、免疫系统疾病等。

图1 心功能分析:AW4.6心功能软件(GE),右心室舒张期心内膜下测绘;图2 右心室收缩期心 内膜下测绘,包含右心室乳头肌、流出道

图3 主肺动脉截面积(MPACSA)测量,三维多角度平行主肺动脉长轴方向得到肺动脉横截面,选取肺动脉瓣上2cm处 A:轴位, B:矢状位, C:CSAmax 821mm2,D:CSAmin 662mm2;图4 LPACSA测 量,选取肺动脉分叉以远1.5cm处 A:轴位, B:矢状位, C:CSAmax 392mm2, D:CSAmin 339mm2
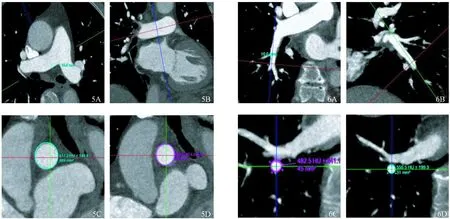
图5 RPACSA测量,选取肺动脉分叉以远1.5cm处 A:轴位, B:冠状位, C:CSAmax 489mm2, D:CSAmin 395mm2;图6 右下肺动脉后基底支CSA测量,选取分支开口以远1cm处 A:斜冠状位, B:斜矢状位, C:CSAmax 45mm2, D:CSAmin 31mm2
2.扫描方法 采用回顾性心电门控技术Revolution CT(GE,美国)轴扫模式,范围主动脉弓上2cm至膈面,患者平静呼吸状态下完成扫描。扫描参数:管电压:(100kV),管电流(150~550mA),探测器宽度16cm,转速0.28s/rot;采集时相:单心动周期(R-R间期)全期曝光,其中75%时相全剂量曝光(余时相1/2剂量曝光)。肘正中静脉注射对比剂(优维显 370),注射流速4mL/s、用量40mL。每隔6%(R-R间期),层厚:0.625mm、层间隔:0.625mm,重建18组图像。
3.数据分析 18组数据传输至后处理工作站(AW4.6,GE)心功能软件,于垂直室间隔短轴位及平行室间隔两腔心层面覆盖整个右心室,勾画右心室(舒张/收缩末期)心内膜,得到右心室EDV、 ESV、EF、SV、CO(右心室乳头肌、流出道包括在右心室容积内)(图1~2)。测量主肺动脉(肺动脉瓣上2cm)、左/右肺动脉(分叉处以远1.5cm)及段级分支(分支开口以远1cm)CSAmax、CSAmin,并计算DPA=(CSAmax-CSAmin)/ CSAmax[6](图3~6)。实验组中选择无栓子存在的段级肺动脉测量截面积,目的是除外栓子对肺动脉膨胀性的影响。考虑到18支段级肺动脉截面积大小存在差异,故仅计算段级肺动脉膨胀性,而CSAmax、CSAmin不计入数据统计。
4.统计学分析 采用SPSS 21.0统计学软件。计量资料以均数±标准差表示,两组间计量资料比较采用独立样本t检验。采用Spearman相关性分析评价各级肺动脉膨胀性与右心室功能参数之间的关系。以P<0.05为差异有统计学意义。
结 果
1.202例完成CTPA检查者中,筛选出慢性肺栓塞40例,正常者33例。上述73例CTPA图像经2名放射科主治医师共同评价图像质量,满足诊断及测量要求。
2.两组年龄、BMI,差异无统计学意义(P>0.05)。慢性肺栓塞患者右心室收缩功能减低为主:两组EDV、SV、CO差异无统计学意义(P>0.05);实验组较对照组右心室ESV增大,EF减低,ESV、EF(86.49±48.60)%vs. (66.84±26.82)%,(52.48±15.21)%vs. (58.77±6.02)%,差异有统计学意义(P<0.05,表1)。

表1 两组基本资料
3.慢性肺栓塞患者近端肺动脉收缩期、舒张期管腔均扩张,实验组MPA(CSAmax、CSAminx)、LPA(CSAmax、CSAminx)高于对照组,差异有统计学意义(P<0.05)。而RPA(CSAmax、CSAminx)差异无统计学意义(P>0.05,表2)。

表2 两组近端肺动脉最大、最小截面积(CSA)比较
4.两组DMPA、DLPA、DRPA:(0.11±0.07)vs. (0.12±0.07),(0.12±0.06)vs. (0.11±0.06), (0.16±0.07)vs. (0.17±0.05)差异均无统计学意义(P>0.05)。DLsPA、DRsPA:实验组低于对照组(0.15±0.07)vs. (0.19±0.08), (0.13±0.07)vs. (0.17±0.04),差异有统计学意义(P<0.05,表3)。

表3 两组各级肺动脉膨胀性(D)比较
注:实验中无栓子的段级肺动脉:LsPA(n=35),RsPA(n=30)
5.根据2016 ESC标准(EF<40%:心力衰竭;40%≤EF<50%:中位数EF值;EF≥50%:EF值正常/保存心功能不全),将实验组细化分为(A组:EF>50%,B组:EF<50%)后,发现B组DLPA、DRPA低于A组,差异有统计学意义(P<0.05),DMPA、DLsPA、DRsPA均差异无统计学意义(P>0.05,表4)。

表4 实验组细化分各级肺动脉膨胀性比较
注:A组:DLsPA(n=21)、DRsPA(n=24),B组:DLsPA(n=13)、DRsPA(n=13)
6.各级肺动脉膨胀性与右心室功能相关性分析发现DLPA、DRPA与RVEF轻度相关(r=0.23p=0.04,r=0.24p=0.04),DMPA、DLsPA、DRsPA与RVEF无相关性(表5)。

表5 各级肺动脉膨胀性与RVEF相关分析结果
讨 论
急性肺栓塞在持续抗凝治疗超过3个月后,仍可能存在部分未溶解的栓子或再次栓塞发生,数个月甚至数年后可进展为慢性肺栓塞性高血压,同时大块栓子和不充分的抗凝治疗增加了CTEPH发生风险[7]。CTEPH早期无或缺乏临床症状、体征,诊断存在严峻挑战,就诊的大部分CTEPH病人已经处于晚期阶段;而晚期CTEPH因长期右心室高后负荷,造成右心室扩张、心肌肥厚,甚至发生缺血性心肌纤维化,最终导致不可逆的右心衰竭或全心力衰竭致死[8-9]。
肺栓塞后肺血管床面积减少,肺循环阻力增加,早期出现近端肺动脉扩张,进而在多种因素共同作用下肺动脉壁僵硬、膨胀性减低,晚期持续肺动脉压力、肺循环阻力增高[10-11]。目前有创性右心导管检查是诊断肺动脉高压的金标准,而未加心电门控CT检查根据肺动脉扩张程度诊断肺动脉高压:主肺动脉内径>3cm或同层面主肺动脉/升主动脉>1提示肺动脉高压存在,但其与肺动脉高压的程度没有相关性[12]。由于肺动脉内径随血管收缩、舒张而变化,同时肺动脉形态不规则且存在血管搏动伪影,因此测量内径值欠精确;并且老年患者因动脉粥样硬化等因素造成升主动脉扩张,主肺动脉/升主动脉内径比可能漏诊一部分肺动脉高压患者。应用心电门控技术可避免血管运动伪影,通过收缩期、舒张期截面积测量更精确反应肺动脉扩张程度。为了降低应用心电门控技术CTPA成像的辐射剂量,本研究中仅在75%采集时相时全剂量曝光(其余时相为半剂量曝光),同时采用低管电压及管电流调制技术,辐射剂量平均约2.44mSv。本研究发现慢性肺栓塞患者主肺动脉、左肺动脉在收缩期、舒张期管腔扩张(截面积增大);而右肺动脉截面积两组间差异无统计学意义,考虑时因为肺栓塞多累及右肺动脉及其分支,而且左肺动脉较短、走行陡直,对压力增高反应更敏感。
Hajime等[6]研究中发现主肺动脉膨胀性与平均肺动脉压力、肺血管阻力呈负相关(r=-0.594、r=-0.659);Revel等[12]研究中发现右肺动脉膨胀性与平均肺动脉压力相关,将肺动脉高压的临界值定为右肺动脉膨胀性低于0.16(敏感性:86%、特异性:96%);实验组中右肺动脉膨胀性低于0.16发生率为50%(20/40),依据上述研究考虑肺动脉高压已经形成,进入CTEPH期。两组近端肺动脉(主肺动脉、左肺动脉、右肺动脉)膨胀性差异无统计学意义,而实验组左、右段级肺动脉膨胀性较对照组减低差异有统计学意义,考虑原因如下:①栓子在移行过程中对小血管内膜损伤较大血管严重,肺动脉重塑是由小血管向大血管进展;②小血管对肺动脉压力升高代偿能力较大血管差。有研究[13]证实肺动脉膨胀性减低出现早于肺动脉压力升高,在静息状态下肺动脉压力正常(仅存在运动后肺动脉压力升高)的患者,肺动脉膨胀性减低已经发生;慢性肺栓塞向CTEPH进展过程中,段级肺动脉血管重塑早于近端肺动脉,甚至早于肺动脉高压形成。急性肺栓塞后肺动脉膨胀性同样减低,溶栓治疗后可恢复正常[14];由此推断慢性肺栓塞段级肺动脉膨胀性减低是早期/潜伏期CTEPH改变。
超声心动图是肺栓塞患者评估右心室功能的首选检查方法,但检出肺动脉栓子(尤其位于段级及其以下肺动脉)能力较低。目前心脏磁共振检查(CMR)是评估右心室功能指标的金标准,但检查时间长并需患者严格屏气状态下扫描,部分患者无法耐受而检查失败[15]。传统无心电门控CTPA检查采用四腔心层面测量舒张期右心室、左心室内径比:RV/LV>1,提示RV增大、右心衰竭,但受限于右心室几何形态复杂(尤其右心室重构后),比值法不能精确反映右心室功能[16];应用心电门控CTPA检查评估右心室功能准确性已经得到证实[17]。慢性肺栓塞患者ESV增加,EDV增大无统计学意义,因此RVEF减低是由于右心室收缩功能减低所致。Dogan等[18]心电门控CTPA研究中将RVEF<47%设定为临床恶性事件发生的最佳预测值(敏感性达到100%,特异性60%);本研究发现慢性肺栓塞组中EF<45%的右心衰竭发生率为25%(10/40),需要及时有效的个体化治疗预防心脏恶性事件发生。
慢性肺栓塞患者右心室后负荷增加,不仅与肺循环阻力相关,而且肺动脉弹性与右心衰竭程度独立相关,同时肺动脉膨胀性又是反映动脉弹性的因素,因此肺动脉膨胀性、右心室功能是评判CTEPH进展程度及预后的重要指标[12, 19]。本研究中仅DLPA、DRPA与RVEF轻度相关,RVEF细化分组后(A组:EF>50%、B组:EF<50%),B组DLPA、DRPA低于A组, 推断出DLPA、DRPA较DMPA、DLsPA、DRsPA对慢性肺栓塞患者右心功能影响更大。根据①DLsPA、DRsPA减低,②DRPA<0.16,③RVEF<45%,将实验组患者分为四组:⑴继发CTEPH风险低:①②③均正常;⑵潜在继发CTEPH:①减低,②③正常;⑶继发CTEPH可能:①②减低,③正常;⑷危重CTEPH:①②③均减低。四组不同进展期慢性肺栓塞患者采取相应个体化治疗方案,有助于改善预后,提高患者生存率。
但是本研究存在一定的局限性:①依据ESC GUIDELINE[9]诊断CTEPH的标准,入组病例无确切肺动脉压力值(右心导管检查),实验组仅根据DRPA<0.16诊断肺动脉高压存在。②不是连续入组病例,没有急性肺栓塞期数据,也无治疗后长期随访,对慢性肺栓塞患者病程分组的准确性需要长期随访证实。③外周小动脉病变同样影响CTEPH病程进展[7],本研究未纳入研究范围。
综上所述,应用心电门控CTPA检查不仅能检出肺栓塞,同时测量各级肺动脉膨胀性、右心室功能等参数对慢性肺栓塞患者早期评估病程进展,对临床治疗策略选择、治疗效果评估和提高患者生存率有潜在价值。
