CYP2C9基因多态性对瓣膜置换术后华法林抗凝效果的影响
2018-10-30高明喜温沁竹
高明喜 施 盛 温沁竹
尽管直接凝血酶和Ⅹa抑制剂的广泛使用,维生素K拮抗剂仍是非瓣膜性心房颤动和人工瓣膜置换术后主要的抗血栓药物,其中华法林治疗可使肝脏产生羧酸化和去羧酸化蛋白失衡而降低机体凝血功能[1]。华法林的维持剂量取决于饮食习惯、合并用药、个体情况等因素,其中VKORC1和细胞色素酶P450(CYP)2C9基因变异可能影响华法林的药效动力学和药代动力学对华法林个体间变异起关键作用[2]。CYP2C9的基因定位于染色体10q24,编码细胞色素P450酶使华法林S-华法林转化为R-对映体,药理学活性增加2.7~3.8倍[3]。亚洲人群中约有10%和6%携带CYP2C9*2 和/或CYP2C9*3等位基因,使华法林治疗的出血不良反应增加(分别增加90%和80%),尤其在抗凝治疗早期和华法林剂量调整期,但目前大部分数据均来源于房颤和单瓣膜置换术患者,联合瓣膜置换术后病例较少(不足10%)。二尖瓣和主动脉瓣置换术后出血和血栓风险均高于房颤、单瓣膜术后患者,同时二尖瓣置换术又高于主动脉瓣置换(32.3%vs. 21.8%),不过严重的出血事件无明显差异[4-5]。也有研究认为不同类型瓣膜置换术后出血风险相当,但主动脉瓣联合二尖瓣置换术后出血和血栓风险均高于单一瓣膜组,因此华法林的用量控制要求更严格[5],而目前为止尚未有研究评价CYP2C9基因多态性与联合瓣膜置换术后出血风险的相关性。为进一步评价CYP2C9基因多态性对联合瓣膜置换术后华法林剂量的影响,本研究选取部分患者进行对比研究,报告如下。
资料和方法
1.一般资料 选择2014年10月至2017年3月,在我院接受瓣膜置换术的患者,入选标准:①年龄18~70岁,性别不限;②择期同时进行主动脉瓣和二尖瓣置换术,术后坚持服用华法林3个月的患者;③了解研究内容,并自愿签署知情同意书。排除标准:①合并急性心肌梗死、严重心律失常、不稳定性心绞痛等疾病;②同时服用阿司匹林、氯吡格雷、糖皮质激素、免疫抑制剂等药物;③需要使用可能影响华法林药代动力学的药物(如胺碘酮、利福平、卡马西平、酮康唑、苯巴比妥等);④合并肝、肾、血液、消化系统疾病,可能影响药物吸收和试验安全性。符合入选标准的患者65例,随机分为自我检测组32例和标准检测组33例。
2. 治疗方法 自我检测组32例和标准检测组分别给予康固全凝血检测仪(CoaguChek XS, Roche Diagnostics GmbH生产)和定期门诊复诊监测INR,自我监测组在手术期完成检测仪的使用和数据记录训练,研究期间每周测量1次,INR超出预定范围则联系研究者进行剂量调整;标准检测组和CYP2C9*1/*1基因型的患者每3~4周返院复查INR。各组患者预测的华法林剂量根据http://www.warfarindosing.org提供的计算方法,首次服药在心外膜电极移除后(术后5~10d),后续剂量根据INR调整,前两周每2~3d测量1次,之后每7~9d直到剂量稳定。根据《华法林抗凝治疗的中国专家共识》[6]将目标INR(TTR)设定为2.5~3.5,术后90d进行最后一次INR测量,计算两组各时点INR处于TTR、低于或超过TTR的百分比。
3. 检测指标 ①人口学资料:术前记录人口学资料,血压>140/90mmHg(1mmHg=0.133kPa)或术前已经接受降压治疗者可确诊高血压;吸烟是指每日抽烟≥1支;正在接受胰岛素、降糖药治疗或空腹血糖>7mmol/L诊断为糖尿病;左心室射血分数由经胸彩色多普勒采用Bernoulli计算。②不良事件: 包括死亡、轻微出血(如鼻出血、结膜下出血、皮下血肿)、严重出血(脑出血、胃肠道出血)、血栓事件(瓣膜血栓、短暂性脑缺血发作、心肌梗死、脑梗死、静脉血栓),研究期间有患者自行填写或研究者检查确诊后记录。③基因型检测:晨起采肘静脉血4mL,EDTA抗凝后储存于-80℃冰箱,采用TaqMan基因型试剂和ABI PRISM 7900HTReal-Time PCR检测VKORC1(c.-1639G>A、rs9923231)、CYP2C9*2(p.Arg144Cys、c.430C> T、rs1799853)和CYP2C9*3(p.Ile359Leu、c.1 075A > C、rs1057910),检测同时设置阳性和阴性对照。
4. 统计学方法 以SPSS 19.0统计学软件进行数据分析。计量资料使用“Kolmogorov-Smirnov”作正态性检验,符合正态分布的数据以均值±标准差描述,组间比较采用单因素方差分析;不符合正态分布的数据以中位数(四分位间距)表示,组间比较采用MannWhithey U检验;计数资料以百分率描述,组间比较采用χ2检验;基因型分布采用χ2检验。以P<0.05为差异有统计学意义。
结 果
1.一般情况 所有患者均顺利完成手术,无死亡、心力衰竭、心源性休克、瓣膜撕裂等严重并发症。CYP2C9*2、CYP2C9*3和VKORC1 -1639G > A等位基因分布见表1,以上各基因型分布均符合Hardy-Weinberg遗传平衡定律。

表1 CYP2C9、VKORC1的基因型分布频率 [n(%)]
2. 不同基因型人口学资料和治疗效果比较 两组年龄、性别、BMI、LVEF、合并疾病、合并用药、INR监测类型、VKORC1-1639G > A比例组间比较,差异均无统计学意义(P>0.05);非CYP2C9*2/3组INR检测次数低于CYP2C9*2/3组(P<0.05),而CYP2C9*2/3组TTR比例、华法林预计剂量及实际剂量均低于非CYP2C9*2/3组(P<0.05);两组轻微出血事件比例组间比较,差异无统计学意义(P>0.05),均未出血严重出血事件和血栓事件,见表2。
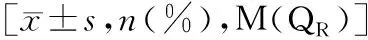
表2 两组人口学及治疗效果比较
3. 两种INR检测方式的疗效比较 两组CYP2C9、VKORC1基因型组间比较差异无统计学意义(P>0.05),TTR、超过TTR比例、低于TTR比例、INR测量次数、华法林预计剂量及实际剂量、轻微出血事件比例组间比较,差异均无统计学意义(P>0.05,表3)。
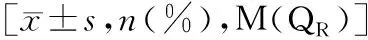
表3 不同INR检测方法的治疗效果比较
讨 论
华法林主要通过抑制肝脏维生素K环氧化物还原酶复合体1(vitamin K epoxide reductase complex subunit 1,VKORC1)而减少氧化型维生素K转变为还原型维生素K(KH2),KH2是维生素K依赖性凝血因子(Ⅱ、Ⅶ、Ⅸ、Ⅹ因子)N末端羧化的辅助因子[7]。华法林治疗效果和安全性高度依赖于用药期间的国际标准化比值(INR),而肝代谢酶的基因多态性对剂量和INR有明确影响,已知主要的CYP2C9基因多态性包括CYP2C9*2外显子3(p.Arg144Cys, c.430C > T, rs1799853)和CYP2C9*3外显子7(p.Ile359Leu, c.1 075A> C, rs1057910)与酶活性下降相关[8]。体外研究发现与CYP2C9*1/*1基因型相比,S-华法林的清除率在CYP2C9*2、CYP2C9*3等位基因下降5.5倍和27倍,而VKORC1野生型和CYP2C9*1/*2基因型的华法林剂量一致。在CYP2C9*2/*2、CYP2C9*2/*3或 CYP2C9*1/*3基因型合并VKORC1野生型的患者中,华法林剂量较CYP2C9*1/*1减少1.7倍,而CYP2C9*3/*3基因型华法林则较CYP2C9*1/*1减少3.5~10倍就可以达到预期INR范围[9]。本研究中最常见的基因型(即CYP2C9*1/*1)仅占52.3%(34/65),显著低于同类研究的报道[3],考虑与抽样误差相关。
本研究中CYP2C9变异基因型患者华法林的预期和实际使用剂量均少于CYP2C9*1/*1型,与国外的流行病学调研结论一致,CYP2C9*2 和/或 *3的人群华法林使用量更低[10],本研究中CYP2C9*2 和/或*3的患者预期和实际华法林用量基本相当,同时均无严重的出血事件,相反,CYP2C9*1/*1型的患者预期和实际华法林用量却有较大差异,可能由于药理学公式计算的中等剂量在非CYP2C9变异的患者准确度较低有关[11]。国际华法林药物遗传学会也曾经报道过剂量计算公式对于低剂量(≤21mg/周)或高剂量(≥49mg/周)准确度更高,对于使用量≤21mg/周的患者,超过50%能准确预测华法林剂量,而临床算法准确率只有33%。本研究中笔者也认为药理学公式对于低剂量华法林的患者准确度更高,但对于CYP2C9基因变异的人群抗凝效果稳定性较差(表现为TTR更窄和INR超过治疗范围的时间更长),表明CYP2C9*2 和/或*3人群华法林剂量更谨慎和INR检测更频繁。
INR可以在门诊或患者家中检测,在欧洲患者自我INR测量越来越流行,本研究中自我检测组和标准监护组的TTR和不良事件无明显差异,国外早期研究也认为两组检测方法对AF和瓣膜置换术后脑卒中、出血事件和死亡无明显影响,但自我检测人群TTR更佳[12],可能由于本研究样本量较少而未能印证上述结果。同时,较少的样本量也无法检测出血事件与CYP2C9变异的相关性。Roth等[13]的病例对照研究则认为瓣膜置换术后约有20%和10%的患者为CYP2C9*2/*3、VKORC1变异,而该人群在华法林治疗初期6个月内出血风险增高。因此笔者认为老年人群每天自我检测INR的治疗效果并不优于标准检测,但对于长期定时返院有困难的患者可以推荐使用。
本研究表明联合瓣膜置换术后3个月,CYP2C9*2 和/或 *3变异基因型患者的华法林剂量和TTR均低于CYP2C9*1/*1型,结果与国外研究基本一致[14],但服药剂量均高于相关研究,可能与联合瓣膜置换术后抗凝强度需求更大有关。本组数据表明国内在瓣膜置换术后TTR的管理有长足进步,但相比发达国家,在华法林长期治疗的管理水平仍有待提高。本研究的不足之处如下:①单中心研究、样本量偏少,代表性较差;②检查数据局限于术后3个月,更长时间的随访可能提供更多的临床数据,尤其是临床预后结果与基因型的相关性;③本研究所有患者均服用华法林,因此研究数据不能外推值其他维生素K拮抗剂。
综上所述,CYP2C9*2和/或*3基因型增加联合瓣膜置换术后3个月华法林抗凝效果的不确定性,但不会增加心血管事件的发生率,同时INR自我检测不能改善TTR达标比例。
